肿瘤相关性贫血(CRA)指肿瘤患者在疾病发展及治疗过程中发生的贫血,是恶性肿瘤常见的伴随疾病之一,患病率达30%~90%[1]。随着化疗的开展,贫血患者比例逐渐增加。高达92.84%的CRA患者未得到任何纠正贫血的治疗[2],CRA管理亟待加强。
2024年中国临床肿瘤学会(CSCO)指南大会于4月26日至27日在济南召开。本次会议基于最新的循证医学证据,更新发布了《肿瘤相关性贫血临床实践指南(2024)》,为CRA的诊断及临床治疗带来了最新的指导意见和策略。【肿瘤资讯】整理相关内容,以供参考。
一、CRA诊断思路
CRA诊断使用血红蛋白(Hb)数值来进行判断:海平面地区,成年男性Hb<120g/L;非妊娠成年女性Hb<110g/L;妊娠成年女性Hb<100g/L。根据NCI、WHO和我国标准,CRA严重程度分级如图1所示。从形态学和网织红细胞数量的角度来看,可以将CRA分为小细胞性贫血、正常细胞性贫血、大细胞性贫血、网织红细胞减少和网织红细胞增多。根据病因学,CRA可分为非化疗相关CRA和化疗相关CRA两大类。非化疗相关CRA主要指肿瘤方面的因素(如失血、溶血、骨髓受侵犯等)引起的贫血;化疗相关CRA为肿瘤治疗方面的因素(如化疗的骨髓抑制作用、肿瘤放射治疗等)引起的贫血。在病因部分新增注释内容:抗体偶联药物(ADC)作为一类新型的肿瘤治疗靶向药物,兼具了传统化疗药物对肿瘤细胞的强大杀伤作用以及抗体药物的精准靶向性。该类药物所携带的有效载荷即细胞毒性药物所产生的骨髓抑制效应,也会造成贫血。最新荟萃分析显示临床试验中ADC药物导致贫血的发生率为33.1%,骨骼放疗也与血液毒性相关(图2)。
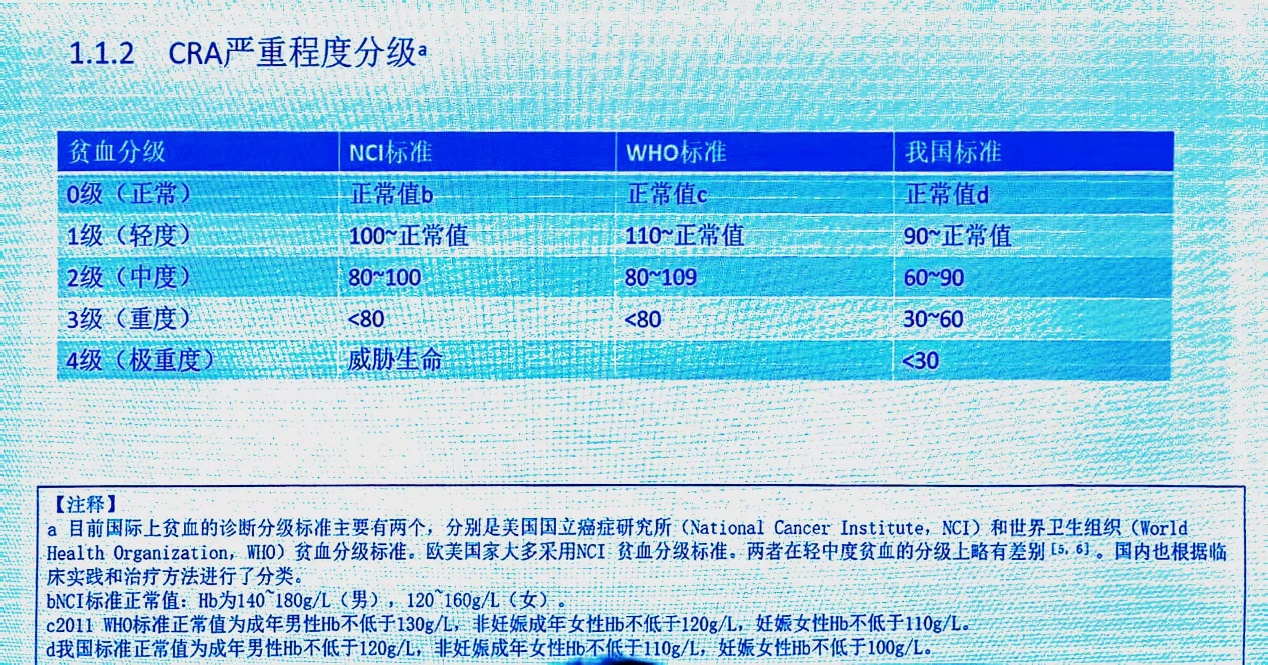
图1. CRA严重程度分级

图2. CRA病因分类
二、CRA病情评估
当Hb<110g/L或低于基线值≥20g/L,应启动CRA评估(2A类证据)。评估的内容包括贫血原因、贫血严重性、症状严重性,详见图3。
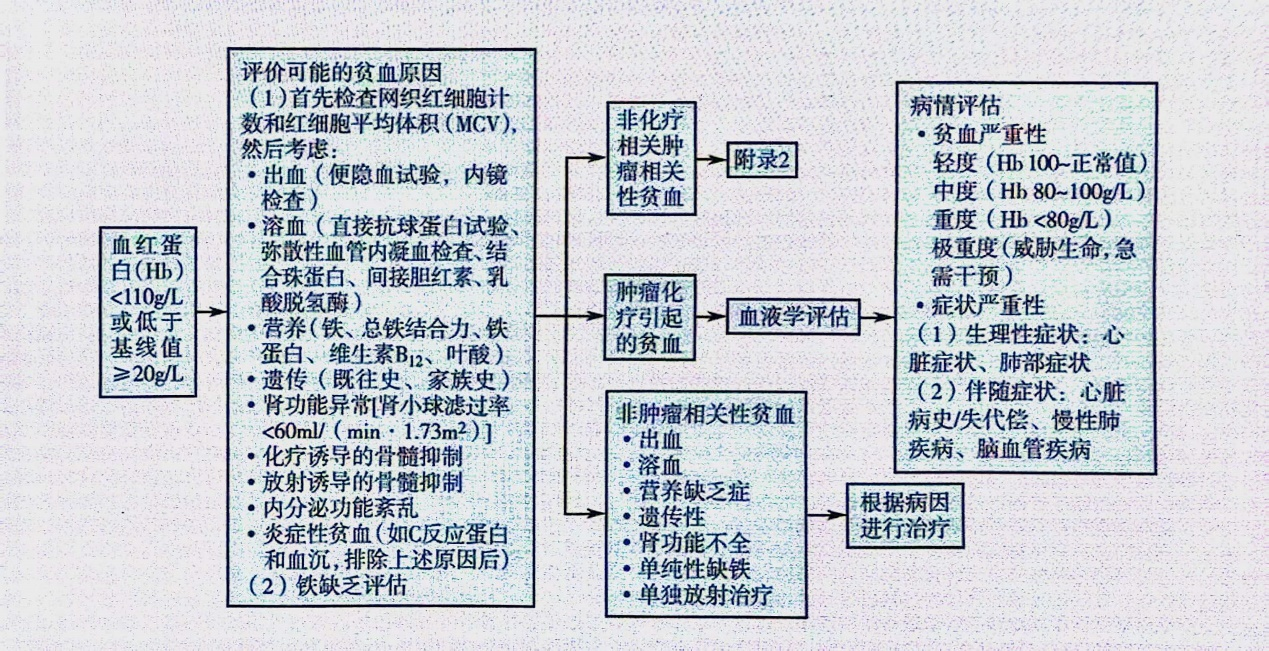
图3. CRA诊断及病情评估
三、CRA治疗原则
非化疗相关CRA
非化疗相关CRA的治疗包括实体瘤、造血系统恶性肿瘤、支持/姑息治疗的恶性肿瘤等的治疗,整体治疗流程如图4。
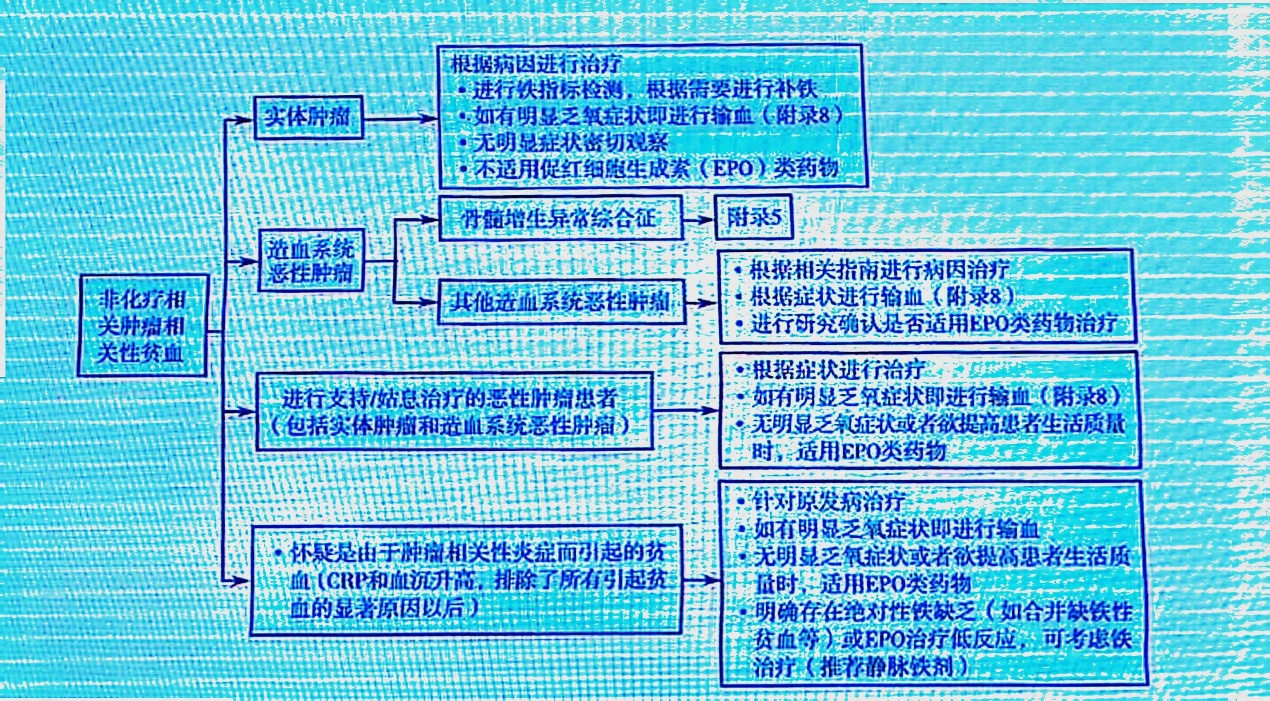
图4. 非化疗相关CRA的治疗
化疗相关CRA
化疗相关CRA根据贫血分层进行输血、EPO类药物、罗沙司他治疗(图5-6)。

图5. 化疗相关CRA治疗原则

图6. 化疗相关CRA的治疗
本处相较于2022年版指南有如下更新:增加“推荐使用罗沙司他治疗(Ⅱ级推荐)”:罗沙司他是一款口服低氧诱导因子脯氨酰羟化酶抑制剂(HIF-PHI)。一项多中心、随机、开放、阳性对照(rhEPO)III期注册研究(FGCL-4592-898),在非髓系恶性肿瘤患者中评价罗沙司他治疗化疗引起贫血的有效性和安全性,研究结果显示罗沙司他与ESA在纠正化疗引起的贫血方面表现出相当的疗效[3]。
四、CRA治疗手段
CRA的治疗方法主要包括输血、EPO、铁剂等,最新版指南新增HIF-PHI(罗沙司他)治疗方式。
4.1 输血治疗
输注全血或红细胞是治疗CRA的主要方式,主要优点是可以迅速升高Hb浓度、可用于EPO治疗无效的患者。尽管输血后Hb浓度迅速升高,但恶性肿瘤的持续存在或具有细胞毒性的化疗药物引起患者的红细胞生成反应依然钝化,Hb很快降至输血前水平,因此治疗过程中Hb的波动较大,维持时间短。
4.2 红细胞生成刺激剂(ESA)治疗
红细胞生成刺激剂(erythropoiesis stimulating agents, ESA)治疗是治疗CRA的最重要方法。EPO是临床上最常用也是研究最多的ESA。EPO治疗的主要优点是符合正常生理、生活质量明显改善、可用于门诊患者以及耐受性好。治疗的主要缺点是大约2/3患者有效,用药2~4周起效。
4.3 罗沙司他治疗
最新版指南基于罗沙司他用于CIA的Ⅱ期及Ⅲ期临床研究结果,新增罗沙司他用于CRA治疗,具体内容如下:
■ 4.3.1罗沙司他起始治疗时机及目标值
本指南中对于罗沙司他治疗化疗相关性贫血的血红蛋白(Hb)初始值和目标值的推荐,主要参考ESA类药物的治疗原则以及罗沙司他说明书。罗沙司他的起始治疗时机为Hb<100g/L,Hb目标值为110-120g/L(图7)。

图7. 罗沙司他起始治疗时机及目标值
■ 4.3.2罗沙司他使用剂量及剂量调整
根据体重选择起始剂量,随后根据当前Hb水平及前4周内Hb变化进行剂量调整。目标是将Hb维持在100-120g/L(图8)。
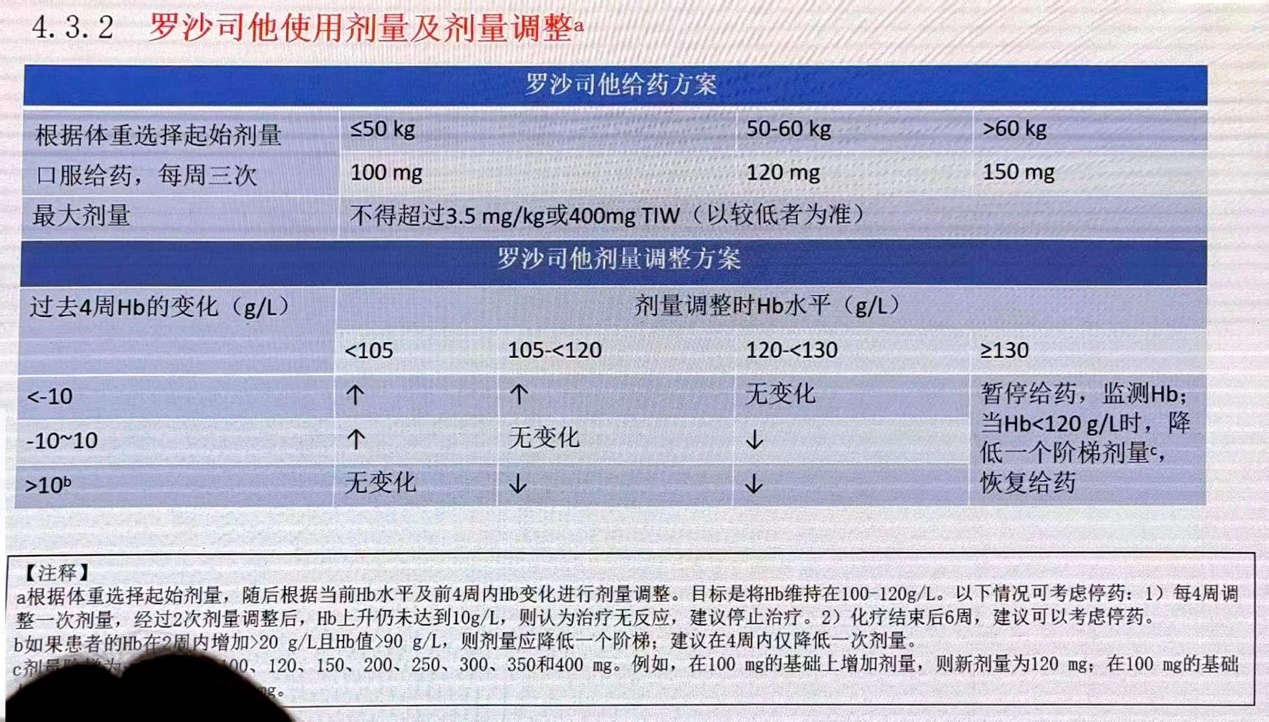
图8. 罗沙司他使用剂量及剂量调整
4.4 化疗相关CRA治疗的获益与风险管理
ESA治疗化疗相关性贫血可有效增加和维持Hb水平,降低红细胞输注率,改善患者生活质量和贫血相关症状,增加患者对化疗的敏感性,但也存在血栓风险和可能的肿瘤进展风险。指南中特别提到,目前尚无证据显示临床使用罗沙司他会刺激肿瘤患者疾病进展或复发(图9)。

图9. 化疗相关CRA治疗的获益与风险管理
4.5 铁剂
根据血清铁、总铁结合力、血清铁蛋白等铁检查可将铁缺乏症分为绝对性铁缺乏、功能性铁缺乏、可能的功能性铁缺乏和非缺铁。对于功能性铁缺乏,新增EPO治疗(2A类)(图10-11)。静脉铁剂使用剂量、途径及注意事项小节增加Ganzoni公式计算铁需求量(图12)。

图10. 铁缺乏治疗

图11. 铁缺乏症判断及治疗选择
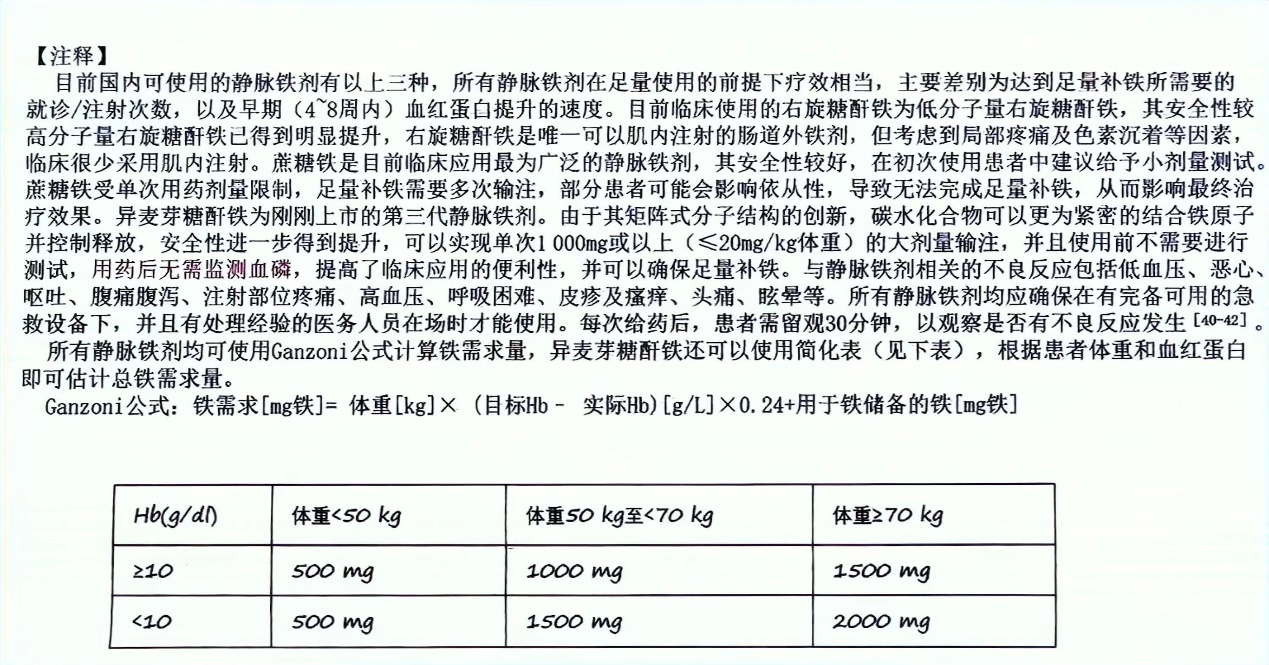
图12. 静脉铁剂使用剂量、途径及注意事项
总结展望
肿瘤相关性贫血(CRA)可发生在肿瘤治疗的任何阶段,与肿瘤类型、分期和治疗方式密切相关,在消化道肿瘤、乳腺癌和肺癌等肿瘤患者中发病率较高。贫血是肿瘤患者预后不良的独立因素之一,并与肿瘤复发密切相关,有研究显示非小细胞肺癌(NSCLC)患者放化疗期间,血红蛋白(Hb)<111g/L会显著缩短OS、LRPFS以及PFS等生存指标[4];贫血还会显著降低肿瘤患者的化疗应答率、影响患者生活质量[5]。纠正贫血对于改善患者的生活质量和提高生存率至关重要。但由于多种因素,目前中国肿瘤患者贫血的治疗率远低于国外[2,6]。为了提升临床医生对CRA的重视,并规范CRA诊疗,CSCO指南工作委员会于2021年首次发布CRA临床实践指南,并于2022年进行首次更新。本次更新主要基于2022年以来最新的循证医学证据,主要更新在于,对化疗相关CRA患者增加了小分子口服药物罗沙司他的治疗推荐。罗沙司他是一款低氧诱导因子脯氨酰羟化酶抑制剂(HIF-PHI),可在氧分压正常情况下,通过抑制脯氨酰羟化酶(PHD)活性稳定低氧诱导因子(HIF)的表达,从而促进EPO表达。除此之外,罗沙司他还上调十二指肠细胞色素B(DcytB)和二价金属转运体1(DMT1)增加肠道对铁的吸收;下调铁调素水平,增加机体可利用铁,从而改善铁代谢紊乱,促进机体红细胞的生成[7,8]。在美国开展的罗沙司他治疗非髓系恶性肿瘤化疗相关性贫血(CIA)的多中心、单臂、开放标签II期临床研究(FGCL-4592-092),结果显示了罗沙司他显著的疗效和可接受的安全性[9]。一项在中国进行的开放标签、非劣效性、多中心、阳性对照(rHuEPO-α)III期研究对罗沙司他治疗非髓系恶性肿瘤患者CIA的疗效与安全性进行了评估[3],结果表明,在主要终点上,罗沙司他组Hb从基线至第9~13周的平均变化相较于rHuEPO-α达到了非劣效性。此外,罗沙司他治疗组中Hb水平升高≥10g/L、≥15g/L和≥20g/L的患者比例高于对照组;在FAS人群的罗沙司他治疗组中,观察到Hb首次升高15g/L和20g/L的中位时间在数值上更短(罗沙司他治疗组42.0和57.0天,rHuEPO-α治疗组52.0和77.0天)。其他关键次要终点上罗沙司他均非劣于rHuEPO-α。探索性终点发现,相较于rHuEPO-α,罗沙司他或许能够降低输血负担,口服药依从性更优。在安全性方面,罗沙司他与rHuEPO-α相当。
针对CRA治疗方案的不断更新与完善为患者提供了更加有效的选择,罗沙司他作为一种新型治疗药物,在纠正贫血、改善生活质量和提高生存率方面具有优势和潜力。未来,我们期待通过更多的研究和临床实践,进一步明确其在CRA治疗中的地位,并为患者带来良好的临床疗效和预后改善。
[1] Knight, Kevin, Sally Wade, and Lodovico Balducci. "Prevalence and outcomes of anemia in cancer: a systematic review of the literature." The American journal of medicine 116.7 (2004): 11-26.
[2] 宋正波, 陆舜, 冯继锋, 等. 中国肿瘤相关性贫血发生率及治疗现状的流行病学调查研究[J]. 中国肿瘤, 2019, 28(9): 718-722.
[3] Lu, S., et al. "LBA96 Roxadustat for chemotherapy-induced anemia in patients with non-myeloid malignancies: A randomized, open-label, active-controlled, phase III study." Annals of Oncology 34 (2023): S1335-S1336.
[4] Topkan E, Selek U, Ozdemir Y, et al. Chemoradiotherapy-induced hemoglobin nadir values and survival in patients with stage III non-small cell lung cancer[J]. Lung Cancer, 2018, 121: 30-36.
[5] Lind M, Vernon C, Cruickshank D, et al. The level of haemoglobin in anaemic cancer patients correlates positively with quality of life[J]. British journal of cancer, 2002, 86(8): 1243-1249.
[6] Ludwig H, Van Belle S, Barrett-Lee P, et al. The European Cancer Anaemia Survey (ECAS): a large, multinational, prospective survey defining the prevalence, incidence, and treatment of anaemia in cancer patients[J]. European journal of cancer, 2004, 40(15): 2293-2306.
[7] 中国医师协会肾脏内科医师分会肾性贫血指南工作组. 中国肾性贫血诊治临床实践指南. 2021, 101(20): 1463-1502.
[8] Li ZL, Tu Y, Liu BC. Treatment of Renal Anemia with Roxadustat: Advantages and Achievement. Kidney Dis (Basel). 2020 Mar;6(2):65-73.
[9] Glaspy J, Gabrail NY, Locantore‐Ford P, et al. Open‐label, Phase 2 study of roxadustat for the treatment of anemia in patients receiving chemotherapy for non‐myeloid malignancies. American J Hematol. 2023;98(5):703-711.
排版编辑:栗子
版权归肿瘤资讯所有。欢迎个人转发分享,其他任何媒体、网站如需转载或引用本网版权所有内容,须获得授权,且在醒目位置处注明“转自:良医汇-肿瘤医生APP”。











 苏公网安备32059002004080号
苏公网安备32059002004080号


