
神经内分泌肿瘤是一类相对少见的肿瘤,胰腺是其常见的发病部位。近年来,胰腺神经内分泌肿瘤(pNET)的发病率明显上升。同时,学界对疾病认识的不断深入也使得pNET的诊疗水平有了显著提升。根治性切除肿瘤是pNETs治疗最重要的环节之一,在药物治疗方面,生物治疗、靶向治疗、核素治疗、化疗及免疫治疗均有所进展,不同药物联合治疗也取得了一定的疗效。生长抑素类似物(SSAs)如长效奥曲肽(LAR),是pNETs的主要治疗药物之一。【肿瘤资讯】特邀代瑞红教授、郑建伟教授、王小波教授、徐焕基教授、郑秋香教授与刘清华教授,分享2例从LAR的治疗中获益的G2级胰腺神经内分泌瘤晚期肝转移病例,供读者交流讨论。
病例一:
长效奥曲肽一、二线治疗G2级晚期胰腺神经内分泌瘤均有效
病例汇报:代瑞红教授 四川大学华西医院
病例点评:
郑建伟教授 福建医科大学附属协和医院
王小波教授 广西医科大学附属肿瘤医院
四川大学华西医院腹部肿瘤医师
四川省肿瘤学会人工智能与大数据专业委员会委员兼任专委会秘书
参与多项临床基金项目
病例介绍
1. 患者基本情况
一般资料:男,48岁。
主诉:中上腹疼痛1+月,进行性加重2天。
病史:1+月前患者进食后中上腹部胀痛,站起时疼痛明显,排便后疼痛缓解。2天前,患者进食油腻食物后疼痛加剧。
查体:ECOG评分1分,浅表淋巴结未扪及肿大,皮肤巩膜无黄染。全腹软,无压痛及反跳痛,未触及明显肿块,肝脾肋下未触及。
既往史、个人史、家族史无特殊。
入院检查:血常规、肝肾功、电解质、凝血常规、大小便常规、肿瘤标志物无明显异常。
2021-08:全腹部增强扫描CT:胰腺钩突区见软组织肿块影,最大截面约3.4×3.2 cm,多系肿瘤性病变(胰腺癌/其它);肝内多发稍低密度结节及肿块影,大者约2.7×2.5 cm,不均匀明显强化,多系转移瘤。
病理活检:于2021-08在全麻下行:左肝肿瘤局部切除活检术。
手术发现:肝脏呈灰红色,肝脏表面满布大小不等白色包块,触之质硬,较大者直径约3.0×3.0 cm,边界不清,胰头处扪及大小约4.0×3.5 cm包块,质硬,边界不清,肝十二指肠韧带、肝胃韧带可触及多发肿大淋巴结,质硬,局部融合,边界不清。
术后病理:<肝脏>神经内分泌肿瘤(G2)。免疫组化:肿瘤细胞CK(+),CgA(+),SSTR2(+),Syn(+),CK20(-),CK7部分(+),Ki67阳性率约8%。
临床诊断:
神经内分泌瘤(G2)伴肝、肝十二指肠韧带、肝胃韧带淋巴结多发转移(cT2N+M1 IV期 非功能性),肝转移分型:3型。
2. 治疗经过
2021-08 在全麻下行:左肝肿瘤局部切除活检术。
一线治疗:
2021-10至2022-07 MDT讨论:患者原发灶、转移灶范围较广,目前无法达到R0切除,Ki67偏低,使用奥曲肽治疗9周期。疗效评价疾病稳定(SD)。
2022-07 复查患者肝脏病灶进展(PD)。
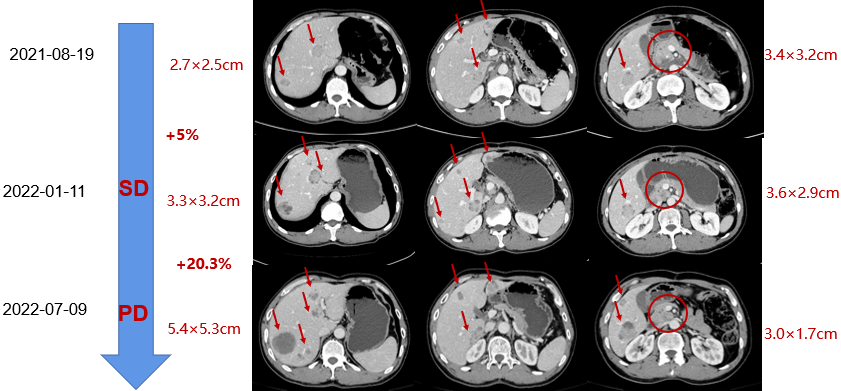
图 1 晚期一线疗效评价
二线治疗:
2022-07 MDT讨论:
(1)没有外科手术指征;
(2)更换内科治疗方案:索凡替尼;
(3)必要时行肝脏动脉化疗栓塞(TACE)。疗效评价疾病缓解(PR)。出现不良反应:继发性高血压(3级),未出现蛋白尿、肾功异常的情况。索凡替尼减量。
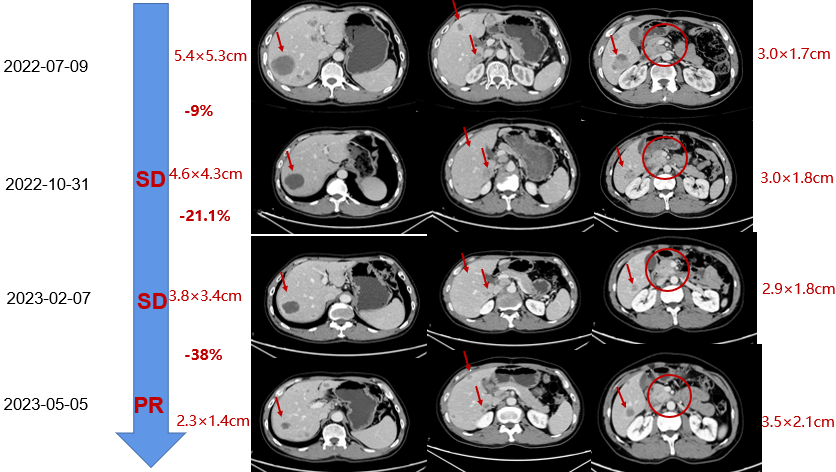
图 2 晚期二线疗效评价
2023-07 MDT讨论:建议手术切除原发灶+转移灶。在全麻下行胰十二指肠切除+左肝肿瘤切除+右肝肿瘤切除+门静脉修补+肠粘连松解术。
术后病理:
(1)胰十二指肠:神经内分泌瘤(NET G2),肿瘤累及十二指肠壁肌层及粘膜下层,查见脉管内癌栓及神经侵犯。免疫组化示肿瘤成分:CK(+),EMA(+),CgA(+),CD56(+),Syn(+),p53(部分+),Ki-67(+,约8%)。标本之胃断端,十二指肠断端,胆总管断端,胰腺断端,未见肿瘤累及。
(2)右肝、左肝:神经内分泌瘤(NET G2),免疫组化示肿瘤成分:CgA(+),CD56(+),Syn(+),Ki-67(+,约10%)。
(3)淋巴结送检“16A2组淋巴结”(3/4)枚,查见肿瘤转移;“12组淋巴结”1枚,“14组淋巴结”4枚,及标本之胰腺周围淋巴结4枚,胃周淋巴结1枚,未见肿瘤转移;“8组淋巴结”为结缔组织,未见肿瘤累及。免疫组化示肿瘤区域淋巴结:CgA(+),CD56(+),Syn(+),Ki-67(+,约10%)。
2023-10 全腹部增强CT:残肝多发不均匀环状强化结节,较大者位于肝右后叶上段,长径约3.8 cm,部分病灶内可见液化坏死,多系转移。
2023-11 患者继续服用索凡替尼,出现消化道出血不能耐受,故暂停索凡替尼治疗。
2023-12患者一般情况欠佳,CPS评分2-3分,予以患者奥曲肽治疗。疗效评价SD。
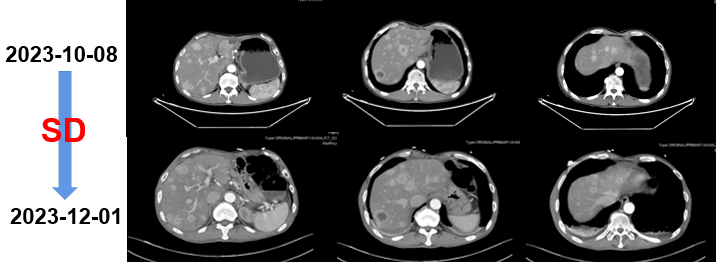
图 3 疗效评价
3. 病例小结
该患者为48岁男性,诊断为神经内分泌瘤(G2)伴肝、肝十二指肠韧带、肝胃韧带淋巴结多发转移(cT2N+M1 IV期 非功能性),肝转移分型:3型。诊疗过程多次行MDT讨论,依次行左肝肿瘤局部切除;一线奥曲肽治疗,无疾病进展生存(PFS) 9个月;二线索凡替尼治疗,PFS 11个月;手术切除原发灶+转移灶,术后3个月肝转移灶复发,继续服用索凡替尼,消化道出血不能耐受,继续奥曲肽治疗至今。
福建医科大学附属协和医院肿瘤内科
内科学(血液)博士
福建省医师协会肿瘤内科分会委员
研究方向:移植免疫、肿瘤免疫
医学博士、博士后、副主任医师、硕士研究生导师
广西医科大学附属肿瘤医院中青年学术骨干
入选广西高等学校千名中青年骨干教师培育计划
中国抗癌协会中西整合胰腺癌专业委员会委员
广西抗癌协会神经内分泌肿瘤专业委员会委员
广西抗癌协会肿瘤分子医学专业委会 委员
主持及参加多项国家级省级课题,第一作者及通讯作者发表论文20篇,其中SCI10篇。
获得中国抗癌协会胰腺癌专业委员会年会(PCCA2022)手术视频大赛“二等奖”
郑建伟教授:神经内分泌肿瘤是一类相对少见的肿瘤,但近年来,发病率明显上升。其中胰腺肿瘤约占12%,非功能性胰腺内分泌瘤由于发现时大多已处于晚期,预后较差。该患初诊时已发生远处转移,Ki67阳性率约8%,生长抑素受体阳性表达SSTR2(+),有奥曲肽治疗指征,治疗后疗效显著,安全可控。另外NETTER-1试验显示,177Lu-Dotatate加长效奥曲肽与单独使用高剂量长效奥曲肽相比,无进展生存期有显著改善。控制肿瘤负荷是治疗关键,一线治疗时肝脏病灶不大时也可考虑射频消融等局部治疗手段。内科治疗效果好的情况下谨慎决定手术相关细节。
王小波教授:此例患者在遵循循证医学证据的规范化治疗的基础上,进行个体化、精准化治疗。诊断为神经内分泌瘤(G2),病理Ki67阳性率约8%,生长抑素受体阳性表达SSTR2(+)。一线、二线规范使用奥曲肽、索凡替尼治疗,术后肝脏复发,不能耐受索凡替尼,继续奥曲肽治疗。肝转移是影响神经内分泌瘤预后的重要因素,该患肝转移较为复杂,可以考虑局部行TACE联合射频消融控制肝内病灶进展。
病例二:
长效奥曲肽联合肝脏局部介入治疗胰腺神经内分泌瘤术后肝转移效果显著
病例汇报:徐焕基教授 四川大学华西医院
病例点评:
郑秋香教授 龙岩市第一医院
刘清华教授 德阳市人民医院
四川大学华西医院腹部肿瘤病房
讲师,硕士生导师
Trends Mol Med、JECCR、Exp Hematol Oncol等杂志审稿人
以第一作者/共一发表SCI论文15篇,其中高被引论文2篇,IF10以上6篇,主持博新计划、国自然青年基金等省部级以上课题4项,累计经费100万。
病例介绍
1. 患者基本情况
一般资料:男,55岁。
主诉:胰腺神经内分泌瘤术后8+年,确诊肝转移4+年。
病史:8+年前(2015-8-14)因“皮肤巩膜黄染伴消瘦”于我院行“胰十二指肠胆囊切除术”,术中见:胰头近十二指肠处4.5 cm囊性包块,术后病理:肿瘤侵及胰腺实质、十二指肠黏膜层及胆总管开口,胰周2/8枚淋巴结阳性。免疫组化:PCK (+),CK56 (+),CgA (+),Syn (+),Insulin (-),glucago (-),gastrin (-),生长抑素 (-),Ki67 (+,最高约5%),支持为胰腺神经内分泌肿瘤(NET,G2)。术后未定期复查。2019-7-15门诊复查CT示肝多发转移瘤,穿刺活检示:肿瘤细胞呈PCK (+),CD56 (弱+),Syn (+),CgA (+),SSTR (+),Ki67阳性率约2%(肿瘤少,不宜分级),支持为神经内分泌肿瘤,多为转移性。
查体:ECOG PS 0分,未见皮肤潮红、皮疹、水肿及手足关节肥大。
既往史:高血压10+年。
入院检查:
实验室检查:血红蛋白 68 g/L、肝功、肾功、凝血、肿标(AFP、CEA、CA199、CA125、烯醇化酶)、输血前全套、大便及尿常规等未见明显异常。
影像检查:2019-07腹部增强CT示:肝脏内可见多发动脉期强化结节影,考虑转移。肠系膜上动脉旁及沿肠系膜多发淋巴结增大。胸部CT未见转移结节。
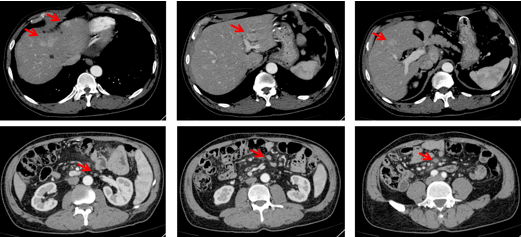
图 4 2019-07腹部增强CT
初步诊断:
胰腺神经内分泌瘤术后(G2 非功能性,pT3N1M0 IIIB)肝脏多发转移(IV期);腹腔淋巴结增大 转移待排;中度贫血(考虑营养吸收不良相关)。
2. 治疗经过:
一线治疗:
2019-08至2020-10共行5次肝脏局部介入治疗(TACE)。
2019-12 奥曲肽微球治疗30 mg 每4周1次。
2022-02复查MRI,疗效评价:SD(肝脏病灶缓慢增大;淋巴结无明显变化)。
2022-08复查上腹部MRI提示:肝脏病灶增多增大,疗效评价:PD,停用奥曲肽微球。
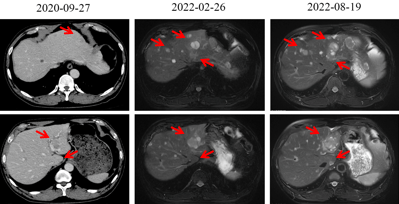
图 5 一线治疗期间复查MRI
二线治疗:
2022-09 索凡替尼口服300 mg qd。
2023-09 复查MRI,肝脏个别结节较前缩小,大部分病灶较前增多增大。疗效评价:SD(缓慢进展)。
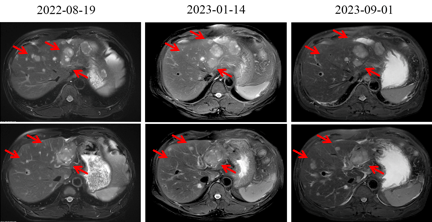
图 6 二线治疗期间复查MRI
2023-09 参加“比较镥【177Lu】氧奥曲肽注射液与长效奥曲肽对无法手术或转移性、进展性、分化良好(G1和G2)、生长抑素受体阳性的胃肠胰神经内分泌瘤患者的安全性和有效性:一项多中心、随机、开放、平行对照临床研究。”经68Ga-DOTATATE PET/CT确认,部分肝转移灶为生长抑素受体阴性,筛选失败。
68Ga-DOTATATE PET/CT:肝实质内见多个稍低密度影,部分病灶摄取信号增高;腹盆腔均未见摄取信号增高,腹部增大淋巴结倾向反应改变。
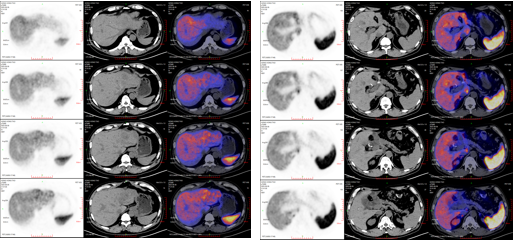
图 7 68Ga-DOTATATE PET/CT
三线治疗:
2024-01 出现消化道出血,依维莫司口服10 mg qd至今。
3. 病例小结:
该患者为55岁男性,诊断为胰腺神经内分泌瘤术后(G2 非功能性,pT3N1M0 IIIB)肝脏多发转移(IV期)。诊疗过程依次行胰腺神经内分泌瘤G2根治术,术后4年发生肝转移;一线奥曲肽治疗,PFS 36个月;二线索凡替尼治疗,PFS 16个月,后出现消化道出血停药;三线依维莫司治疗至今,病情平稳。
龙岩市第一医院肿瘤内科 副主任医师
福建省抗癌协会肿瘤内科第一届青年委员会委员
福建省海峡医药卫生交流协会临床肿瘤学诊疗分会理事
福建省肿瘤防治联盟结直肠癌专委会委员
海医会临床肿瘤分会闽西南罕见靶点学组副组长
海医会临床肿瘤分会小细胞学组委员
闽西南结直肠防治联盟委员
龙岩市医学会肿瘤内科分会秘书
龙岩市抗癌协会理事
医学博士、中西医结合临床博士后、主任医师、教授、硕士生导师、美国梅奥诊所和以色列海法大学访问学者。
世界中医药学会联合会癌症姑息治疗研究专业委员会常务理事
欧美同学会(中国留学人员联谊会)医师协会青年委员会常务委员
国际肝胆胰协会中国分会肝胆胰MDT专业委员会委员
中国民族医药学会肿瘤学分会常务理事
中国医师协会中西医结合医师分会肿瘤病学专业委员会委员
中国抗癌协会肿瘤支持治疗专业委员会第一届青年委员会委员
中华医学会心身医学分会心身肿瘤协作学组委员
中国药理学会表观遗传药理学专业委员会委员
成都市抗癌协会放疗与免疫专业委员会常务委员
德阳市医学会肿瘤病学专业委员会主任委员
郑秋香教授:该患者的总体生存期长,治疗成功。肝转移病灶活检SSTR (+),Ki67阳性率约2%,68Ga-DOTATATE PET/CT确认,部分肝转移灶为生长抑素受体阴性,显示了神经内分泌瘤的异质性。一线长效奥曲肽治疗PFS 36月,治疗过程中肿瘤缓慢增大,必要时可再次行穿刺活检,明确当前患者的病理状态,有的放矢地用药。整体诊疗规范。
刘清华教授:此例患者手术获益最大。最初发现肝转移时可行SSTR PET-CT,对评价肝脏多发转移灶、淋巴结转移情况以及后续治疗均有帮助。患者全身治疗也明显受益,治疗过程中肝转移缓慢进展。虽然患者68Ga-DOTATATE PET/CT显示部分肝转移灶为生长抑素受体阴性,并不代表不能从核素治疗中获益。后续治疗可联合局部治疗,推荐局部放疗,为患者带来更长的生存获益。
总结
全身联合局部系统性治疗,全程管理更好帮助pNET获益最大化
手术切除是局限的胰腺神经内分泌肿瘤唯一根治性的手段。对于能手术切除的患者5年生存率可以达到80%~100%。然而大多数肿瘤会发生远处转移,CSCO神经内分泌肿瘤诊疗指南(2021版)建议如果发生肝转移,建议行全身系统性治疗为主的综合治疗,必要时MDT讨论决定局部治疗的时机。全身治疗目的包括抗肿瘤增殖和控制激素相关症状。胰腺神经内分泌肿瘤标准的内科治疗是生长抑素类似物和a-干扰素。PROMID研究表明生长抑素类似物与安慰剂对比无论对于功能性还是无功能的神经内分泌肿瘤均能延长无疾病进展生存(PFS),分别为14.3个月和6个月;SD可以达到66.7%和37.2%。生长抑素类似物不仅能够减轻症状,还具有抗肿瘤活性,同时也能改善生活质量, 因此生长抑素类似物仍然是神经内分泌肿瘤的重要治疗药物。
此外,研究也指出切除原发肿瘤和肝转移灶行减瘤术的患者可以获得更多的获益。达到R0切除对于有转移的患者有临床获益。对于存在肝转移的神经内分泌肿瘤,手术可以减轻瘤负荷延长生存,此外射频消融、TACE以及对于那些无法行肝肿瘤切除的患者进行肝移植也是一种选择。肽受体放射性核素治疗(PRRT)、分子靶向药物及免疫治疗是未来NET药物治疗的发展方向。
NENs具有高度异质性,诊断困难和复杂,治疗策略的制定需要既遵循指南规范,又要在多学科协作基础下进行个体化选择。NENs治疗方式多样,包括内镜、外科、内科、核素、介入、化疗、中医、姑息治疗和心理治疗,对于如此之多的NEN治疗选择,在进行选择时,应该在患者病情特点的基础上进行个体化的选择,考虑的主要因素:肿瘤部位、是否为功能性、肿瘤分期、生长速度生长抑素受体表达以及患者基础疾病、经济是否可以承担等因素。
[1] CSCO神经内分泌肿瘤诊疗指南(2021版)
[2] Rinke A, Muller HH, Schade-Brittinger C, et al. Placebocontrolled, double-blind, prospective, randomized study on the effect of octreotide LARin the control of tumor growth in patients with metastatic neuroendocrine midgut tumors: a report from the PROMID study group. J Clin Oncol. 2009;27(28):4656-4663.
排版编辑:肿瘤资讯-SY











 苏公网安备32059002004080号
苏公网安备32059002004080号


