2023 WCLC公布了FLAURA-2的主要研究结果,奥希替尼联合化疗较奥希替尼单药一线治疗EGFR敏感突变的晚期NSCLC患者的无进展生存期(PFS)显著延长,而不同基因组突变亚组以及脑转移患者组均获益显著。但该联合治疗仍存在局限性,如毒性发生率增加、静脉给药带来的不便,且缺乏总生存期(OS)获益。因此,奥希替尼联合化疗是否应成为所有晚期EGFR+ NSCLC的一线治疗方案这一问题在学界引发了广泛讨论。
正方观点:奥希替尼+化疗应作为所有晚期EGFR+NSCLC的一线治疗
FLAURA-2试验达到了主要终点,即奥希替尼联合铂类-培美曲塞化疗(osi-chemo)的中位无进展生存期(mPFS)较奥希替尼单药治疗有统计学改善,研究者评估的HR为0. 62。设盲独立中心审查(BICR)评估达到了相同的HR 0.62。Osi-chemo BICR评估的mPFS为29.5个月,绝对延长了8.8个月(INV评估)和9.5个月(BICR评估)。
重要的是,两个关键的预后因素(外显子19缺失/L858R和脑转移[是或否])在两个研究组之间平衡,尽管没有分层。osi-chemo治疗约9个月的mPFS改善迎来了晚期EGFR+ NSCLC一线(1 L)治疗的“第三次工业革命”(mPFS约为30个月),这之前是“第一次工业革命”,一代EGFR TKI成为标准治疗(约10个月mPFS),以及“第二次工业革命”,其中三代EGFR TKI(约20个月mPFS)取代一代EGFR TKI作为1L标准治疗。
目前缺乏FLAURA-2的OS获益不应阻止临床医生采用osi-chemo,因为所有6项1L一代EGFR TKI对比化疗的III期试验(WJTOG3405、NEJ002、EURTAC、OPTIMAL、ENSURE、CONVINCE)均未实现OS获益。同样,开创性的AURA-3试验也没有实现OS获益。尽管如此,AURA-3的mPFS结果影响了亚洲卫生监管机构首次批准4种三代EGFR TKI(lazertinib、aumolertinib、伏美替尼、贝福替尼)治疗EGFR T790M+ NSCLC,因为大型II期研究显示,尽管AURA-3缺乏OS获益,但其ORR和缓解持续时间(DOR)与奥希替尼相似,无需设计相似的关键性试验。 此外,正在中国进行一项“FLAURA-2-like”设计的aumolertinib联合或不联合化疗作为晚期EGFR+ NSCLC的1L治疗的试验(NCT 04923906),以BICR评估的PFS作为主要终点。关注NMPA是否会基于极有可能的mPFS获益批准aumolertinib联合化疗将非常重要。
序贯治疗是osi-化疗的替代方案。迄今为止,唯一发表的osi后3期试验是MARIPOSA-2。 MARIPOSA-2中含EGFR TKI的“四联”方案(lazertinib + amivantamab +铂双药化疗[LACP])的mPFS(8.3个月)在统计学上优于单独化疗(CP)(mPFS 4.2个月)(BICR HR=0.44),但92%的LACP患者发生了3级或以上毒性,77%的患者中断了治疗。22%的LACP患者发生静脉血栓栓塞事件,而CP患者为5%,因此建议在LACP的前4个月进行预防性抗凝治疗。ACP(不含lazertinib)的mPFS(6.2个月)也比CP(HR=0.48)有所改善,但短于Osi-chemo提供的预期9个月mPFS获益。发现不含EGFR TKI的“四元”方案(化疗+抗血管生成剂+免疫检查点抑制剂)的mPFS优于单独CP(4.2个月)(ORIENT-31,mPFS 7.2个月,HR=0.51)。阿替利珠单抗+贝伐珠单抗+化疗(ABCP)在IMpower151(EGFR+亚组)和ATTLAS中均实现了8.5个月的mPFS。然而,只有11%(ORIENT-31)、18%(IMpower151)和9%(ATTLAS)的NSCLC患者在使用三代EGFR TKI后接受治疗。此外,在EGFR/ALK亚组中,IMpower 151 ABCP未实现mPFS相对于BCP(mPFS 8.3个月)的统计学改善(HR=0.86)。由于这些不含EGFR TKI的治疗方案虽然有希望,但都是单一国家试验,只有极少数患者是纯粹的三代EGFR TKI治疗后患者,因此推荐ABCP(或类似组合)作为奥希替尼后治疗还为时过早(图1)。图1显示了序贯治疗可能的“最佳情况”结果,我们认为即使在最佳考虑下,mPFS2也没有达到至少9个月的目标。
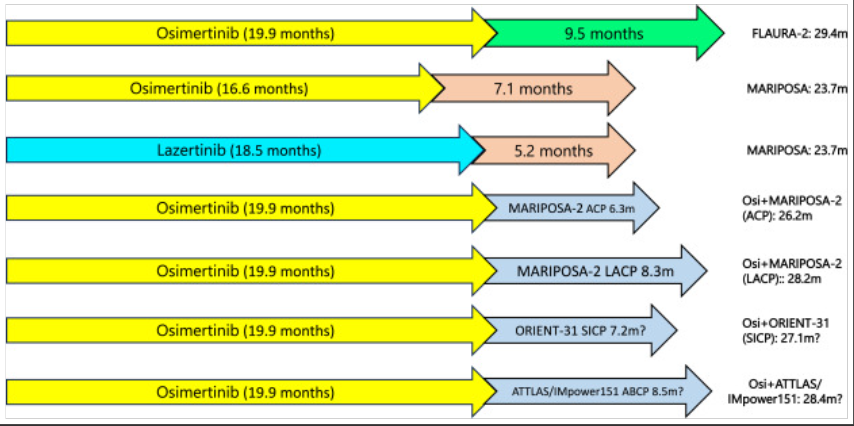
图1.根据报告的EGFR TKI治疗后BICR mPFS,比较osi-chemo和LACP的总mPFS,以及奥希替尼与现有治疗方案的序贯治疗的假想示意图
抗体-药物偶联物(ADC)也在三代EGFR TKI治疗后背景下开发,但目前报告的疗效均至少在三线背景下;奥希替尼治疗后和化疗后,mPFS为5.5(HERTHENA-Lung-019的patritumab deruxtecan [HER3-DXd])至5.8个月(TROPION-Lung-05的datopotamab deruxtecan [Dato-DXd])。有趣的是,Dato-DXd在TROPION-Lung01中具有可操作基因组改变的一小组患者中实现了0.38的HR。在EGFR TKI治疗后和化疗后的相同情况下,Bl-B01D1(双特异性EGFR/HER3 ADC)实现了5.6个月的mPFS。比较三代EGFR TKI治疗后立即使用HER3-DXd与含铂化疗的试验(HERTHENA-Lung02,NCT05338970)正在进行中,结果令人期待。
几乎所有EGFR+NSCLC患者的主要亚组均受益于FLAURA-2(外显子19缺失,L858R,存在基线脑转移)。尽管在基线无脑转移的患者中,使用osi-化疗的mPFS绝对增加了6.6个月,但HR为0.75(95%CI:0.55-1.03)。在奥希替尼基础上添加化疗使颅内缓解率从71%增加至78%,发现累积中枢神经系统进展从23%降低至9%。根据方案设计,在FLAURA-2中,无基线脑转移的患者未定期接受脑成像。因此,考虑到化疗的颅内和颅外效应的额外疗效,不能排除如果定期安排脑成像,在无基线脑转移的患者中可能实现统计学显著的HR获益。相比之下,MARIPOSA试验(对所有患者定期进行脑成像)中,有或无脑转移的患者的HR相同,为0.69,基线脑转移的MARIPOSA患者mPFS从13.0个月改善至18.3个月,而基线脑转移的osi-化疗患者mPFS从13.8个月改善至24.9个月(HR=0.47)。
FLAURA-2中的化疗(包括培美曲塞维持治疗)与奥希替尼同时给药,直至疾病进展和累积毒性成为患者和临床医生的有效关注点。FLAURA-2中的中位化疗周期为16(4+12个维持周期),这与化疗和一代EGFR TKI的另外两项III期试验一致:Tata Memorial Centre试验15个周期(4+11)和NEJ009 20个周期(4+16)。因此,现有数据表明,12个月的化疗可能足以实现FLAURA-2中报告的mPFS获益。重要的是,联合治疗组奥希替尼的平均相对剂量强度为95%,奥希替尼组为98%,表明同时化疗给药不影响奥希替尼的累积给药。此外,联合治疗组奥希替尼总暴露时间和实际暴露时间的中位差异为1.3个月(奥希替尼组为0.3个月),再次表明化疗期间奥希替尼中断的总时间较短。mPFS是否与化疗时间呈正相关是需要从FLAURA-2数据库中解决的一个重要问题。
“无化疗”方案是肿瘤学家和患者的理想目标。MARIPOSA显示lazertinib+amivantamab(LA)的mPFS改善在统计学上优于奥希替尼,HR为0.70,mPFS绝对增加7.1个月,BICR评估的总mPFS为23.7个月。简单交叉比较显示LA的所有三个值(HR、mPFS的绝对增加、总mPFS)在数值上均劣于osi-化疗。此外,LA方案导致75%的患者出现≥3级毒性,83%的患者出现剂量降低,37%的患者出现静脉血栓栓塞事件。重要的是报告lazertinib和amivantamab的平均和中位相对剂量强度,以进一步明确LA的耐受性。虽然amivantamab不是“化疗”,但MARIPOSA在前五周每周静脉注射一次,然后每两周静脉注射一次,需要花费比osi-化疗多50%以上的时间,且需额外管理皮肤毒性。FLAURA-2和MARIPOSA分别报告了osi-化疗(HR=0.7)和LA(HR=0.75)方案的初步PFS2获益,表明即使在osi-化疗的1L背景下使用标准化疗,进展后治疗也是有效的。
联合化疗与EGFR TKI的禁忌源于在NSCLC(INTACT1、INTACT2、TRIBUTE、TALENT) 中的大规模试验中早期缺乏OS改善,并在我们对EGFR突变的了解尚不充分且无法获得下一代EGFR TKI时,由于IMPRESS中EGFR T790M+NSCLC的联合方法对OS的损害而再次加强。随着联合化疗和吉非替尼的阳性OS数据的出现,这种看法开始改变,现在被FLAURA-2打破。
FLAURA-2研究者虽然指出osi-化疗中发现的获益的确切机制尚不清楚,但表明化疗通过具有非选择性抗肿瘤作用和克服肿瘤内异质性补充了奥希替尼的靶向作用。此外,尽管未来对预测性生物标志物的研究可能会进一步细化最有可能从osi-化疗中受益的患者人群,但目前还没有可以可靠地弥补osi-化疗9个月优势的序贯疗法。
反方观点:奥希替尼+化疗不应作为所有晚期EGFR+NSCLC的一线治疗
在用于靶向致敏突变(19号外显子缺失、21号外显子L858R)的各种EGFR-TKI中,奥希替尼仍然是FDA批准的EGFR突变晚期NSCLC的一线治疗标准。但疾病进展仍然不可避免,对于携带L858R的患者,脑转移的发生率高且预后差。之前,第一代EGFR TKI与化疗联合使用,显示出PFS获益,但以毒性为代价,并且在OS方面没有获益。
FLAURA2研究中,尽管奥希替尼联合化疗达到了研究者评估的PFS延长的主要终点,但该联合治疗仍存在相当大的局限性,如毒性发生率增加、静脉给药带来的不便以及是否达到PFS改善与可接受毒性之间平衡的最终目标。
对于FLAURA2,有几个关键问题待回答。第一,在所有患者中,奥希替尼+铂-培美曲塞联合治疗是否优于奥希替尼单药治疗。FLAURA2达到了研究者评估的主要终点PFS,改善了8.8个月。其对照组奥希替尼单药治疗的中位PFS为16.7个月,短于关键III期FLAURA研究的18.9个月。PFS的亚组分析显示,不同人种(亚裔、非亚裔)、EGFR突变亚型(19号外显子缺失,L858R)和中枢神经系统(CNS)转移的疗效一致。然而,奥希替尼+化疗患者的PFS2或OS未观察到获益。两个治疗组的PFS2一致,奥希替尼+铂类-培美曲塞的PFS2仅获益3个月。OS的中期分析(尽管尚不成熟(27%))显示,奥希替尼联合铂类-培美曲塞未显示出优于奥希替尼单药治疗的获益(HR 0.90,0.65-1.24,p=0.5238)。两组的Kaplan-Meier曲线最初继续合并,奥希替尼+铂类-培美曲塞未显示出有利于OS的趋势。因此,增加化疗使PFS延长,但可能最终不会转化为OS获益。
此外,54%的奥希替尼+化疗组患者未接受后续化疗,33%的患者再次接受细胞毒性化疗。表明在奥希替尼联合化疗失败后,可能没有有效的后续治疗选择。在2期研究TROPION-Lung05中,新型药物(如Dato-Dxd,TROP-2 ADC)在标准治疗难治的晚期NSCLC患者中显示出相当适度的活性,EGFR突变亚组的确认客观缓解率(ORR)为43.6%。Patritumab deruxtecan是一种靶向EGFR3(HER3)的ADC,在既往接受过EGFR TKI和铂类化疗的患者中开展的II期研究HERTHENA-Lung 01中显示疗效有限,确认的ORR为29.8%,mPFS为5.5个月。与其同时进行化疗,为什么不将化疗留到第二线或更晚的治疗中呢?
这导致了以下问题:奥希替尼和铂类培美曲塞的毒性特征在临床环境中是否可控。在联合治疗组中,仅77%的患者完成了铂类-培美曲塞的4个周期治疗,联合治疗组中导致治疗中止的任何不良事件均显著较高(48% vs 6%)。在联合治疗组中止治疗的患者中,11%的患者中止了奥希替尼治疗,这是奥希替尼单药治疗(6%)的两倍,此外还有化疗的中止率(铂类17%,培美曲塞43%)。尽管不良事件(AE)的频率和严重程度在诱导期(0-3个月)最高,并在维持期(9个月后)下降,但应注意的是,无论如何停用奥希替尼都是不可接受的。培美曲塞维持治疗难治性病例的标准做法被认为是安全可行的,但与奥希替尼联用会导致严重的毒性,而且每三周一次的就诊也会给患者带来不便。
接下来,问题仍然是化疗是否是奥希替尼的最佳组合伙伴。目前的工作重点是EGFR TKI与化疗靶向药物或抗血管生成药物(包括贝伐珠单抗和雷莫芦单抗)的联合治疗。然而,奥希替尼与抗血管生成药物联合使用的结果相互矛盾。在II期研究WJOG9717L中,奥希替尼+贝伐珠单抗作为一线治疗未能显示PFS改善,III期研究正在进行(NCT 0418060)。最近,奥希替尼+雷莫芦单抗的2期RAMOSE试验的中期分析报告了PFS的改善(24.8 vs 15.6个月,HR=0.55,95%CI:0.32-0.93,p=0.023)。
最近,在全球III期研究MARIPOSA(NCT04487080)中,Amivantamab和lazertinib联合治疗被证明是治疗初治EGFR突变晚期NSCLC患者的另一种前期联合治疗策略。与奥希替尼单药治疗相比,通过盲法独立中心审查,Amivantamab联合lazertinib使PFS延长7.1个月(23.7 vs 16.6个月,HR=0.70,95% CI:0.58-0.85)。PFS的数值短于FLAURA 2(研究者评估的PFS),但应谨慎解释交叉试验比较。在中位随访22个月时,中期OS(25%)显示Kaplan-Meier曲线在12个月时早期分离,并继续支持amivantamab+lazertinib(HR =0.75,95% CI:0.58-0.98,p=0.03)。对这一发现有两种合理的解释。首先,MET相关的耐药机制可以通过添加amivantamab作为一线治疗来直接抑制。其次,保留化疗用于后续治疗可能有助于获得耐药机制的患者,如鳞癌或SCLC的组织学转化。
在等待MARIPOSA的数据和最终OS数据成熟时,amivantamab+lazertinib的毒性管理是增强抗肿瘤活性同时保持缓解持续时间和深度的关键。amivantamab和lazertinib联合治疗会导致抑制EGFR(甲沟炎、皮疹、腹泻)和MET(低白蛋白血症、外周水肿)的AE,以及联合治疗导致的静脉血栓栓塞,治疗期间需要4个月的预防性抗凝治疗。输注相关反应和其他AE的发生率以及静脉给药带来的不便可能通过皮下注射amivantamab而不是静脉给药得到改善。PALOMA-2(NCT05498428)是一项在晚期实体瘤(包括EGFR突变的NSCLC)中皮下给予amivantamab的II期研究。 然而,amivantamab+lazertinib的耐受性仍然是一个障碍,除了频繁的门诊就诊外,任何药物中断(83%)、减量(59%)和停药(35%)的发生率很高。
最后,问题仍然是奥希替尼和化疗是否应考虑用于特定的患者亚组,如脑转移患者。这可能是因为增加化疗并不能在所有患者中克服药物耐受性。脑转移患者的亚组分析显示CNS PFS改善(HR=0. 47,95% CI:0. 33-0.66)。然而,仅根据CNS亚组分析解释和概括数据并将其应用于现实世界的实践需要谨慎。考虑到奥希替尼更好的颅内疗效,对无症状、脑部寡转移患者增加化疗的做法应提出质疑。因此,脑转移瘤的数量和肿瘤负荷也应考虑在内。此外,应通过前瞻性随机对照试验来支持对化疗增强CNS疗效的机制的理解,以支持化疗在接受奥希替尼治疗的脑转移患者中具有累加效应的观点。在此之前,脑转移的立体定向放射治疗仍然是一种可行的选择,因为先前的报告发现了放射治疗与EGFR TKI的协同性。
与其提前给每位患者化疗,不如在TKI初始治疗后,在检测循环肿瘤DNA(ctDNA)的基础上加强治疗?目前,针对高危患者(包括TP53突变和C2D1时ctDNA阳性)联合化疗的不同策略正在进行中。基于第2周期第1天收集的可检测ctDNA,进行奥希替尼单药或与化疗联合的2期研究(NCT04410796),可为特定患者亚组的治疗强化提供答案。
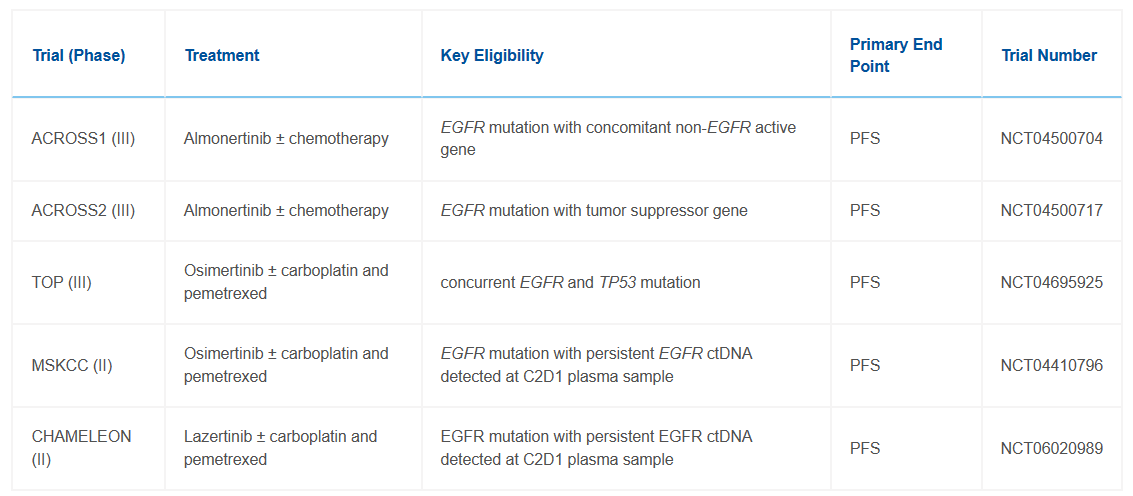
表1.正在进行的针对EGFR突变晚期NSCLC的化疗+第三代EGFR TKI的临床试验
责任编辑:TY
排版编辑:TY
版权声明











 苏公网安备32059002004080号
苏公网安备32059002004080号


