2024年正式拉开序幕,那么,在新年的第一个月内,血液肿瘤领域的各大顶级血液学期刊中有哪些值得重点回顾的研究动态?在此,小编带您一睹为快!
Blood
A phase 2 trial of CD24Fc for prevention of graft-versus-host disease
CD24Fc用于预防移植物抗宿主病(GVHD)的一项2期研究
异基因造血干细胞移植(allo-HSCT)是治疗恶性血液肿瘤的重要手段之一,但移植物抗宿主病(GVHD)是其带来的问题之一,尤其对于无关供者造血干细胞移植(MUD-HSCT)而言,针对该问题,John Magenau教授等开展了一项2期研究,旨在评估CD24Fc融合蛋白(CD24Fc/MK-7110)在预防GVHD方面的价值,将接受MUD-HSCT治疗的恶性血液肿瘤患者随机分配至CD24Fc组和对照组进行治疗,结果显示,在第180天时,CD24Fc组未出现3~4级GVHD的患者比例高达96.2%,要明显高于对照组的73.6%(HR=0.1,95%CI:0.0~0.6; p =0.03). 安全性方面,CD24Fc组无任何患者出现了剂量限制性毒性(DLTs)。该研究表明,CD24Fc能有效预防MUD-HSCT治疗后的GVHD发生。
The Lancet Haematology
Oral decitabine–cedazuridine versus intravenous decitabine for myelodysplastic syndromes and chronic myelomonocytic leukaemia (ASCERTAIN): a registrational, randomised, crossover, pharmacokinetics, phase 3 study
口服地西他滨-西达尿苷(Cedazuridine) vs 静脉地西他滨在骨髓增生异常综合征(MDS)和慢性粒单核细胞白血病(CMML)治疗中的应用:(ASCERTAIN):一项注册、随机、交叉、药代动力学、3 期研究
该研究最终入组了133例MDS或CMML患者,随机1:1分配至口服地西他滨+西达尿苷(含地西他滨35mg和cedazuridine 100mg,连续口服5天)或静脉地西他滨20mg/m2治疗。主要终点是第1和第2周期口服地西他滨-西达尿苷与静脉注射地西他滨5天内的总暴露量。中位随访时间为966天。结果显示:①口服地西他滨-西达尿苷与静脉注射地西他滨总暴露的比例为98.93%,表明基于AUC曲线下面积的药代动力学暴露相当。②安全性方面,口服地西他滨-西达尿苷和静脉注射地西他滨的安全性相似。最常见的3级或更严重不良事件包括血小板减少症(61%)、中性粒细胞减少症(57%)和贫血(50%) 。第 1~2 周期中,口服地西他滨-西达尿苷组的严重不良事件发生率为31%,而静脉注射地西他滨组则为18%, 有5例与治疗相关的死亡;2例被认为与口服治疗有关(败血症和肺炎),3例被认为与静脉治疗有关[败血症休克(n=2)和肺炎(n=1)]。
该研究表明,口服地西他滨-西达尿苷的药理学及药效学与静脉注射地西他滨相当。结果支持使用口服地西他滨-西达尿苷可作为静脉注射地西他滨的安全有效替代品,用于治疗MDS或CMML。
Haematologiga
Carfilzomib, thalidomide, and dexamethasone is safe and effective in relapsed and/or refractory multiple myeloma: final report of the single arm, multicenter phase II ALLG MM018/AMN002 study.
卡非佐米+沙利度胺及地塞米松在复发或难治多发性骨髓瘤(RRMM)的治疗中是安全有效的:ALLG MM018/AMN002研究II期结果
Slavisa Ninkovic教授等近期在Haematologica杂志上更新了ALLG MM018/AMN002研究的II期结果,入组了93例复发或难治多发性骨髓瘤(RRMM)患者并接受卡非佐米[20mg/m2,静脉d1~d2; 56mg/m2(年龄≧75则36mg/m2),d8开始]+沙利度胺100mg/天口服+地塞米松40mg/周(年龄≧75岁则改为20mg)。主要研究终点为无进展生存(PFS);次要终点为总体缓解率(ORR)、总体生存(OS)、缓解持续时间(DOR)和安全性。
中位随访26.4个月,结果显示:该联合方案(KTd)能使RRMM患者的中位PFS达到22.3个月,2年PFS为46.3%,中位OS尚未达到,2年OS为73.8%,ORR达88%,≧非常好的部分缓解(VGPR)率为73%。安全性方面,KTd方案未出现新的毒副反应,耐受性良好。
Leukemia
Real-world analysis of teclistamab in 123 RRMM patients from Germany
Teclistamab在123例复发或难治多发性骨髓瘤(RRMM)治疗中的真实世界分析
Teclistamab是一类BCMA/CD3的双特异性抗体,在既往MAJESTEC-1研究中显示出对于RRMM患者具有不俗的疗效。C. Riedhammer教授等开展了一项研究并分析了真实世界中Teclistamab治疗RRMM的疗效,中位随访5.5个月,结果显示:总体缓解率(ORR)为59.3%,中位无进展生存(PFS)为8.7个月,亚组分析发现,伴有髓外病变、ISS 3期和既往接受过ide-cel治疗的RRMM患者, Teclistamab疗效明显更差,ORR依次为37%、37%和33%,中位PFS则依次为 2.1个月、1.3个月和1.8个月。具体详见下图。
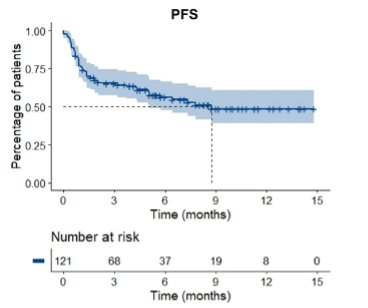
Teclistamab治疗RRMM患者的整体PFS
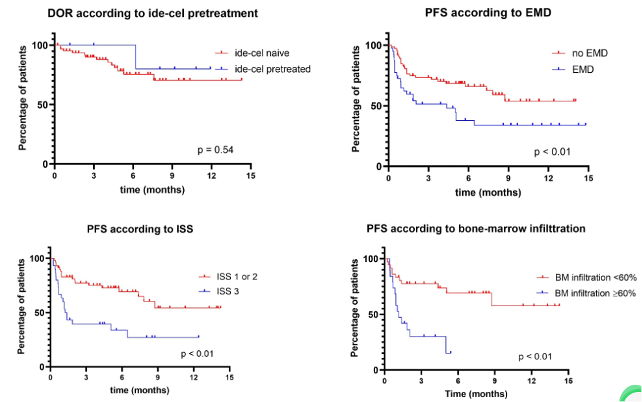
髓外病变、ISS分期3及既往接受过ide-cel治疗是影响 Teclistamab疗效的不利因素
1. https://ashpublications.org/blood/article-abstract/143/1/21/497727/A-phase-2-trial-of-CD24Fc-for-prevention-of-graft?redirectedFrom=fulltext
2. https://www.thelancet.com/journals/lanhae/article/PIIS2352-3026(23)00338-1/abstract
3. https://haematologica.org/article/view/haematol.2023.284238
4. https://www.nature.com/articles/s41375-024-02154-5
排版编辑:Amiee











 苏公网安备32059002004080号
苏公网安备32059002004080号


