近年来,免疫治疗的临床应用彻底改变了晚期非小细胞肺癌(NSCLCL)的治疗格局,国内免疫治疗药物百花齐放,免疫治疗获得广泛运用。为了进一步改善患者预后,提高免疫治疗的用药规范,以保证患者最大化获益,是当前关注的重点。CSCO免疫治疗专家委员会牵头领域内临床药学专家,齐力打造《CSCO-“拯救生命的另一半”肺癌免疫治疗持续用药规范化白皮书》,全方位展现我国肺癌免疫治疗持续用药的真实状况,发现临床实践中尚未被解决的问题,进一步推动临床治疗规范化,使更多临床工作者正确认识、掌握并规范化使用免疫治疗手段。
本期由上海交通大学附属胸科医院晋悦萍教授带来一例晚期肺鳞癌的病例分享:患者给予替雷利珠单抗治疗2周期后首次疗效评估为SD(疾病稳定),坚持治疗至4周期后,疗效评估虽仍然是SD但却观察到肿瘤缩小,故继续原方案治疗。坚持至7周期时肿瘤明显缩小,疗效评估部分缓解(PR),后坚持替雷利珠单抗维持治疗至今,患者PFS 13个月,持续PR,且未出现免疫相关不良反应。【肿瘤资讯】特别邀请上海交通大学附属胸科医院李子明教授进行病例点评,深入探讨免疫治疗疗效评估的时机与坚持治疗的临床意义。
病例介绍
病例分享:
现任上海交通大学附属胸科医院 肿瘤科住院医师
毕业于上海交通大学医学院 肿瘤学博士
主要研究方向:肺癌的内科治疗,包括化疗、免疫治疗、靶向治疗等
共参与发表SCI论文3篇,其中作为共一在Journal of Thoracic Oncology杂志上发表高质量文章;2019年ASCO大会壁报交流
基本信息:
患者:男性,70岁
主诉:确诊右肺鳞癌1年余,入院治疗
既往史:糖尿病
就诊经历:
2022年7月,患者开始咳嗽,伴咳痰,少量痰血丝,就诊我院。
2022年10月13日,PET-CT检查显示,右肺上叶空洞型病变,考虑恶性肿瘤性病变;右侧第2、3侧肋局部骨质缺损,部分FDG代谢增高,考虑恶性肿瘤性病变直接侵犯可能。
2022年10月21日,B超下肺穿刺活检,病理显示低分化鳞状细胞癌。
免疫组化:CD56(-)、P40(+)、NapsinA(-)、CK(+)、TTF-1(-)、KI-67(80%+),ALK(-)抗ALK(D5F3)兔单克隆抗体,PD-L1肿瘤细胞(80%+)22C3抗体。
基因检测结果显示:CDKN2A exon c.203_204insT,TP53 exon c.725G>T, NF1 exon c.2283del,KDR exon c.455G>T,MTOR exon c.484G>T, NOTCH1 exon c.1860C>A。
ECOG评分: 1分。
诊断结果:
右肺鳞癌(c-T4N0M0,IIIA期)
治疗经过及疗效评估:
2022年11月1日,因患者PD-L1表达≥80%,因此选择一线给予免疫单药治疗:替雷利珠单抗200mg。
2022年11月22日,2周期治疗后,12月9日行胸部CT影像学检查,疗效评估:SD。
2023年1月10日,第4周期治疗后,2月2日行胸部CT影像学检查,疗效评估为SD,但已观察到肿瘤开始缩小。
2023年3月17日,第7周期治疗后,4月7日行胸部CT影像学检查,疗效评估PR。
2023年7月19日,第12周期治疗后,行胸部CT影像学检查,疗效评估:PR。
2023年8月11日,第13周期治疗后,9月5日行胸部CT影像学检查疗效评估持续PR。目前患者仍使用替雷利珠单抗200mg方案维持治疗中,至今用药18周期,疗效评估持续PR,PFS为13个月,且身体状况良好,未发生免疫相关不良反应。
影像资料:
2022.10.13基线状态胸部CT
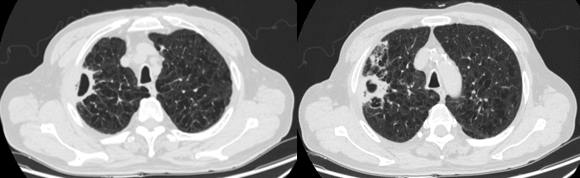
2022.12.09,治疗2周期后复查,疗效评估:SD
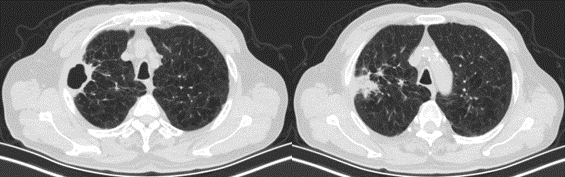
2023.2.01,治疗4周期后复查,疗效评估:SD
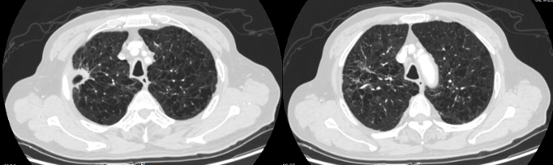
2023.4.07,治疗7周期后复查,疗效评估:PR
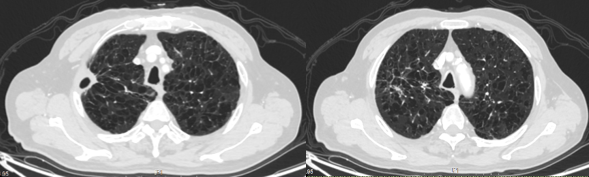
2023.7.09,治疗12周期,疗效评估:PR
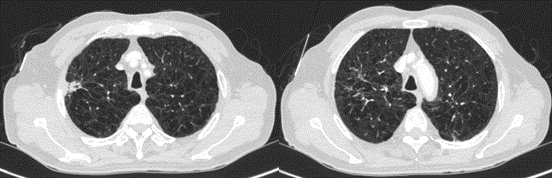
2023.9.05,治疗13周期,疗效评估:PR

病例小结
患者初治为右肺鳞癌(c-T4N0M0,IIIA期),驱动基因阴性。患者PD-L1表达≥80%,结合CSCO指南推荐及患者具体情况,一线给予替雷利珠单抗治疗。2周期后,首次疗效评估为SD;坚持治疗至4周期后,虽然疗效评估仍为SD,但通过影像学检查已明显观察到肿瘤开始缩小。患者继续坚持治疗至7个周期后再次评估,肿瘤持续缩小,疗效评估PR。后续使用替雷利珠单抗维持治疗至13周期时,疗效评估持续PR,肿瘤病灶进一步缩小。截止目前,患者共接受替雷利珠单抗治疗18个周期,PFS达13个月,身体状况良好,且未出现免疫相关不良反应。

治疗流程图
专家点评
上海交通大学附属胸科医院
上海市胸科医院肺部肿瘤临床医学中心 副主任
中华医学会肿瘤学分会青委委员
中国临床肿瘤学会(CSCO)青委委员
中国抗癌协会肺癌专业委员会青委委员兼内科学组秘书
美国纽约叶史瓦大学爱因斯坦医学院访问学者(2014.8-2015.9)
主要研究方向为肺癌多学科综合治疗的基础与临床研究,擅长肺癌的微创肿瘤消融术
获得:上海市青年拔尖人才、上海市浦江人才、上海市人才发展基金资助。
作为第一/共同第一作者发表SCI论著收录于:Nature Communications、PNAS、JTO、Chest等杂志 承担国家自然科学基金面上项目、青年项目等多项课题
近年来,免疫治疗的出现为肺癌治疗带来了革命性的变化,显著改善了驱动基因阴性肺癌患者的预后,特别是晚期肺癌患者的生存期得到持续提升。随着越来越多的免疫治疗药物及适应症纳入医保,免疫治疗得以广泛运用。为了进一步提升患者获益,推进免疫规范化治疗观念及行为是当前临床工作的重中之重。国家卫健委发布的《原发性肺癌诊疗指南》指出,免疫治疗在没有出现疾病进展及不可耐受的不良反应时,应当使用2年1。然而一项纳入43家医院共计28,670位患者的真实世界数据提示,我国肺癌免疫治疗平均时长仅约4个周期,远低于临床研究中的理论免疫治疗时长和指南,这明我国肺癌真实世界中免疫治疗普遍存在治疗时间不足的问题,而过短的治疗时长将大幅降低免疫治疗获益,也会潜在影响患者生存预后。
准确评估,优化决策:掌握起效特征,推进免疫治疗规范化
免疫治疗为无驱动基因突变的肺癌患者提供了更多治疗选择,然而何时进行疗效评估,如何准确判断免疫治疗是否起效,是免疫治疗过程中经常遇到的问题。
从作用机制的角度来分析,免疫治疗是通过激活自身免疫系统,重新激活肿瘤特异性T细胞来识别、杀伤肿瘤细胞,这一过程包括抗原呈递、T细胞活化、增殖、迁移等多个环节,需要较多时间2-3。所以在临床中会观察到,免疫治疗的延迟反应导致NSCLC免疫治疗起效/缓解时间存在较大个体差异。研究显示,部分患者的靶病灶在免疫治疗后3-6个月才获得缓解4,因此如果某个患者早期效果不明显,贸然停药是不可取的,或许免疫治疗需要一定时间来起效。
近期发表的RATIONALE-304研究肿瘤缓解特征探索性分析结果显示,替雷利珠单抗联合化疗组应答者的中位TTR为7.9周(约2个月),其中约50%的应答者在首次疗效评估(2周期)时获得缓解,而另外50%的患者则是在4周期治疗后陆续达到PR。这一发现也提示如果按照化疗、靶向治疗等的评估时间,在2~3个周期时即进行疗效评估并作出方案调整,则可能有一半的患者会因此错过免疫治疗获益的机会。
因此当首次疗效评估为SD时,应当继续坚持免疫治疗至4周期后,再判断患者是否达到PR,避免过早更改治疗方案,让患者错失获益机会。所以《CSCO-“拯救生命的另一半”肺癌免疫治疗持续用药规范化白皮书》中专家组进行如下倡议:对于首次疗效评估为SD的患者推荐继续治疗,4周期导入治疗后再评估才能更准确判断患者免疫治疗是否获益,应充分了解免疫反应的个体化差异,提前终止免疫治疗潜在影响患者免疫治疗的获益。
持之以恒,疗效更佳:坚持免疫长期治疗,助力晚期NSCLC患者更深获益
免疫巩固治疗对于患者预后的改善也非常重要。对此,替雷利珠单抗的RATIONALE-304研究5为临床治疗提供了更多证据支持,肿瘤缓解特征探索性分析结果显示,对于初始治疗获得缓解的患者,巩固治疗至缓解后5周期将会达到最大缓解。其中,75%的患者在获得首次缓解后,通过巩固治疗会使肿瘤进一步退缩至最大肿瘤缓解;50%的患者肿瘤进一步退缩比例≥15%;20.8%的患者肿瘤进一步退缩比例≥30%,首次缓解到最大肿瘤缓解的中位时间为3.6个月,且肿瘤缓解程度更深的患者可以获得相对更长的PFS。从该项探索性分析可以发现,已经达到缓解的患者,通过持续进行替雷利珠单抗免疫治疗可以推动肿瘤的进一步退缩,将有望转化为更好的生存获益。此外,既往临床研究也显示,免疫治疗维持使用2年,约有70%患者在免疫治疗结束后能够继续存活3年,提示免疫维持治疗为患者带来了长生存获益6,7。
因此,《CSCO-“拯救生命的另一半”肺癌免疫治疗持续用药规范化白皮书》也指出:患者出现首次缓解后,继续进行5周期巩固治疗,有望达到最大深度的缓解。对于疾病控制良好的晚期NSCLC患者,患者应继续免疫治疗至疾病进展或出现不可耐受的毒性,条件满足的情况下建议治疗至2年,在持续进行免疫治疗的过程中,患者的获益有望进一步提升。
综上所述,患者在首次疗效评估为SD后,应该完善相关检查和评估、耐心等待起效;起效后也应继续坚持用药至少5个周期,让药物深度发挥作用;在有明确缓解后,还需要坚持免疫治疗,进一步维持治疗效果、防止肿瘤“死灰复燃”。期待在未来,以替雷利珠单抗代表的免疫治疗能在肺癌领域不断突破,持续拓展治疗边界,为更多患者带来新的治疗选择和生存获益!目前肺癌的免疫治疗正向着全面规范化不断推进,改变肺癌的治疗策略,相信最终可以使越来越多的肺癌患者获益。
[1] 原发性肺癌诊疗指南.
[2] Chen, Daniel S., and Ira Mellman. immunity 39.1 (2013): 1-10.
[3] Paz-Ares, Luis, et al. New England journal of medicine 379.21 (2018): 2040-2051.
[4] Osorio, Juan C., et al. Journal of Clinical Oncology 37.36 (2019): 3546.
[5] Lu S. et al. CSCO 2022.
[6] M.C. Garassino,et al 2022 ESMO
[7] Silvia Novelloo, et al.2022 ESMO
排版编辑:肿瘤资讯-IRIS











 苏公网安备32059002004080号
苏公网安备32059002004080号


