通过对2023.10.16-2023.10.31期间发表的乳腺癌领域最新文献进行检索和梳理,本期“乳腺癌新文联播“主要介绍了CDK4/6抑制剂应用原理、ESMO中内分泌治疗相关进展等内容,接下来让我们一起来了解这些最新文献吧!
卵巢组织中细胞周期蛋白依赖性激酶 (CDK) 4/6 的作用及其外源性抑制可能产生的影响
The Role of Cyclin-Dependent Kinases (CDK) 4/6 in the Ovarian Tissue and the Possible Effects of Their Exogenous Inhibition1
PMID: 37894292 [Cancers (Basel); IF=6.126; Q1]
细胞周期蛋白依赖性激酶(CDK)4/6抑制剂联合内分泌治疗是HR+/HER2-晚期乳腺癌患者的标准治疗方法。近期,这种联合疗法也开始作为早期辅助治疗手段,用于治疗(新)辅助化疗后疾病复发风险较高的HR+/HER2-疾病患者。尽管 CDK4/6抑制剂目前已用于临床实践,但有关其潜在性腺毒性的数据仍然有限。因此,绝经前患者担心使用该疗法可能会导致卵巢早衰和不孕症,因此很难在充分知情的情况下做出治疗决策。颗粒细胞和积层细胞的细胞周期进展是卵巢功能的关键过程,尤其是确保卵泡正常生长和获得能力的关键过程。由于CDK4/6抑制剂的药理特性,可能会对育龄妇女的卵巢功能和生育能力产生潜在的负面影响。本综述旨在总结细胞周期蛋白D-CDK4和CDK6复合物在卵巢中的作用,以及CDK4/6抑制对卵巢生理过程的潜在影响。
Imlunestrant联合或不联合依维莫司或阿培利司治疗ER+、HER2-晚期乳腺癌(aBC):Ia/b期EMBER研究结果
Imlunestrant with or without everolimus or alpelisib, in ER+, HER2- advanced breast cancer (aBC): Results from the phase Ia/b EMBER study
ESMO 383MO
背景
Imlunestrant 是一种正在研究的新一代口服SERD,旨在持续抑制ER靶点,包括ESR1突变的BC。在首次人体1a/b期EMBER研究中,imlunestrant作为单药治疗(Jhaveri ASCO 2022)或与阿贝西利联用(Jhaveri SABCS 2022)显示出良好的安全性、药代动力学(PK)和临床获益率。我们展示了imlunestrant与依维莫司或阿培利司的首次临床数据,以及EMBER研究(NCT04188548)中imlunestrant单药治疗的最新数据。
方法
患者(pts)在1a期(升级)或1b期(扩展)单独接受imlunestrant治疗,或在1b期与依维莫司或阿培利司一起接受治疗。1b期的主要资格条件包括:ER+、HER2- aBC、既往对内分泌治疗(ET)敏感、既往治疗次数≤2次以及PIK3CA突变(仅阿培利司治疗组)。1b期治疗组的分配由研究人员决定。男性和绝经前女性接受GnRH激动剂治疗。关键终点包括RP2D、安全性、PK以及根据RECIST v1.1的ORR(完全应答 [CR] 加部分应答 [PR])和 CBR(CR 或 PR,或疾病稳定≥24 周)。
结果
截至2022年10月6日,114名患者接受了imlunestrant单药治疗,42名患者接受了imlunestrant+依维莫司治疗,21名患者接受了imlunestrant+阿培利司治疗。各组合队列的基线特征相似;46%的患者有内脏疾病,46%的患者基线时有ESR1突变。联合用药队列中既往接受过aBC治疗的中位数为:1(范围 1-2);包括既往接受过ET(100%)、CDK4/6i(100%)、氟维司群(35%)和化疗(17%)。未发现心脏或眼部毒性。安全性和初步疗效见表。
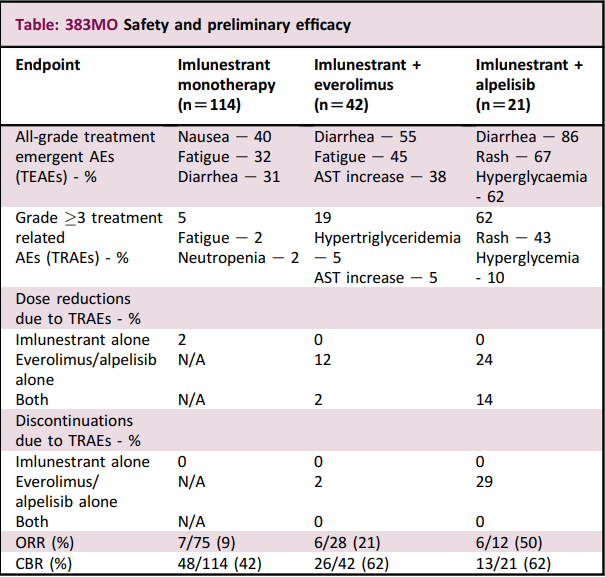
结论
Imlunestrant单独使用或与依维莫司或阿培利司联合使用,对预先接受治疗的ER+、HER-2 aBC患者具有显著疗效。其毒性与已知的阿培利司和依维莫司的安全性一致。临床试验注册号:NCT04188548。
针对HR+/HER2-早期乳腺癌(EBC)患者(pts)的瑞波西利(RIB)+非甾体芳香化酶抑制剂(NSAI)III期NATALEE研究中各主要亚组的无侵袭性疾病生存期(iDFS)
Invasive disease–free survival (iDFS) across key subgroups from the phase III NATALEE study of ribociclib (RIB) + a nonsteroidal aromatase inhibitor (NSAI) in patients (pts) with HR+/HER2- early breast cancer (EBC)
ESMO LBA23
背景
NATALEE试验表明,在有复发风险的II期或III期HR+/HER2- EBC患者中,RIB+NSAI与单用NSAI 相比具有统计学意义的iDFS益处(Slamon D等,ASCO 2023。口头演讲LBA500)。评估临床相关亚组的iDFS结果对于了解特定患者的治疗(tx)获益非常重要。在此,我们对参加NATALEE的患者进行了iDFS的预设探索性亚组分析。
方法
HR+/HER2-EBC患者按1:1随机分配到RIB治疗3年(400 mg/d,连用3周/停药1周)+非甾体芳香化酶抑制剂治疗≥5年(来曲唑2.5 mg/d或阿那曲唑1 mg/d)或单用非甾体芳香化酶抑制剂治疗。绝经前的女性和男性每28天接受一次戈舍瑞林治疗。NATALEE纳入了解剖学分期为IIA期(N0需要其他危险因素或N1[1-3个腋窝淋巴结])的患者,以及所有根据 AJCC 癌症分期手册(第 8 版)分期为 IIB 期或 III 期的患者。iDFS分析根据解剖分期、绝经状态、结节状态、年龄和Ki-67评分(局部检测)进行。这项预设分析不具备统计学意义。
结果
本分析共纳入了5101例患者(数据截止日期:2023年1月11日;两组患者的iDFS随访中位数均为27.7个月)。总体而言,在所有临床相关亚组中,RIB+NSAI与单用NSAI相比,iDFS的获益是一致的(见表),而这与在整个试验人群中观察到的获益也是一致的。
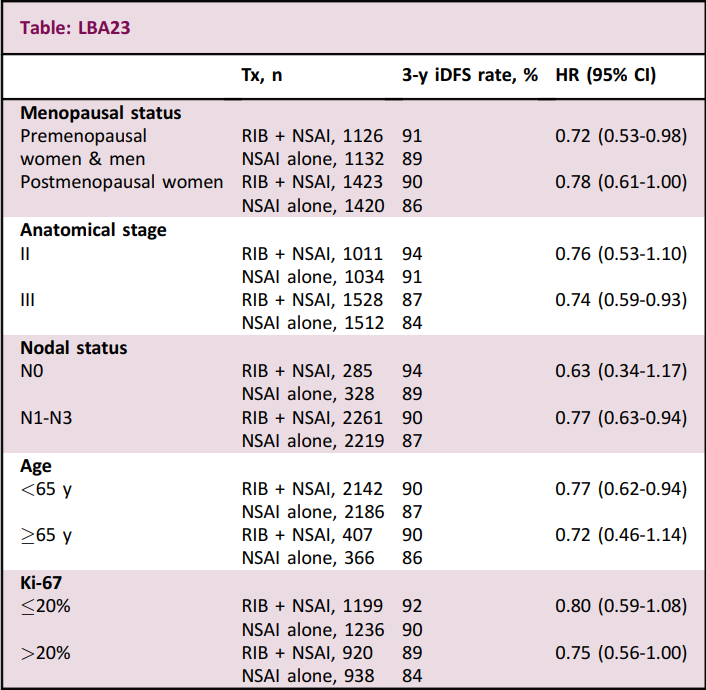
结论
RIB+NSAI的iDFS获益与NATALEE意向治疗(ITT)人群的获益基本一致,不受任何特定亚组的影响。这些结果进一步支持将RIB+NSAI作为HR+/HER2- EBC患者的新治疗选择。临床试验注册号:NCT03701334。
接受一线细胞周期蛋白依赖性激酶(CDK)4/6抑制剂治疗的ER阳性HER2阴性转移性乳腺癌患者药物性肝损伤的预测因素
Predictive factors for drug-induced liver injury in patients with ER-positive HER2-negative metastatic breast cancer treated with first-line cyclin-dependent kinase 4/6 inhibitors
ESMO 473P
背景
内分泌治疗(ET)和CDK4/6抑制剂(CDKi)联合治疗ER+HER2阴性转移性乳腺癌与13%的药物性肝损伤(DILI)有关。在之前的一项研究(Vega 等人,ESMO Breast 2023)中,我们在472例接受治疗的患者(pts)中发现了26例 DILI(5.5%),定义为 AST/ALT 升高≥G2。在此,我们进行了一项病例对照研究,以评估与 DILI 相关的临床因素。
方法
病例对照研究包括 i) 随机挑选并回顾性分析的89例无DILI的患者(对照组)和 ii) 26例先前报告的DILI患者。对15个潜在的预测因素进行了单独或联合评估。基线肝脏脂肪变性基于计算机断层扫描报告。为了研究与DILI的关系,采用Logistic回归法计算了几率比(OR)。
结果
115 例患者的主要特征见表。在单变量分析中,没有一个基线风险因素单独与 DILI 有统计学关联,脂肪变性和 AST/ALT 基线升高的结果最好(P<0.15)。然而,合并脂肪变性和绝经前状态(9人,7.8%)会使风险显著增加至 66.7% vs 19% (20/105)(OR=8.6,95% CI 2.1-43.6;P=0.004)。心血管风险因素、联合应用ET或肝转移等其他变量均不能预测DILI的发生。
结论
在我们的病例对照系列中,绝经前状态和脂肪变性是CDKi相关DILI的最强预测因素。我们的研究结果表明,卵巢因子抑制导致的新陈代谢变化与CDKi共同诱发了潜在脂肪变性患者的DILI。需要进行前瞻性研究来验证这些发现。
胚系BRCA1/2致病变异(gBRCA1/2 PV)会影响接受细胞周期蛋白依赖性激酶4/6抑制剂(CDK 4/6i)加内分泌治疗(ET)的激素(HR)阳性HER2阴性转移性乳腺癌(MBC)患者(pts)的预后: BREAK研究
Germline BRCA1/2 pathogenetic variants (gBRCA1/2 PV) affect outcome of hormone (HR)-positive HER2-negative metastatic breast cancer (MBC) patients (pts) treated with cyclin-dependent kinase 4/6 inhibitor (CDK 4/6i) plus endocrine therapy (ET): The BREAK study
ESMO 478P
背景
DNA修复基因的胚系致病变异(PV)对Luminal型MBC患者的影响在现有证据下存在矛盾,但CDK 4/6i加ET是标准的治疗方法。
方法
在这项回顾性多中心研究中,纳入了2017年1月1日至2021年12月31日期间检测出gBRCA1/2基因并接受CDK 4/6i加ET治疗的HR+ HER2- MBC患者。目的是根据gBRCA1/2状态(PV与野生型[wt]/意义不确定变异[VUS])评估结局(主要/次要终点:无进展生存期[PFS]/总生存期[OS]),采用K-M方法估算。采用Cox模型评估基线变量与结果之间的相关性。
结果
13个中心的249名患者被纳入研究:40例(16.1%)患者携带gBRCA1/2 PV(31例携带gBRCA2 PV),20例(8.0%)患者携带VUS BRCA1/2,189例(75.9%)患者为wt BRCA1/2。基线特征为:中位年龄52岁(范围:26-83岁);男性2.8%(N=7;有3个gBRCA2 PV);绝经前46.6%(N=116);内脏转移78%(N=194);ECOG PS 0分80%(N=199);一线 CDK4/6i加芳香化酶抑制剂(AI)53%(N=132);CDK4/6i加ET前进行化疗(CT)16.5%(N=41)。两组患者在ECOG PS≥1(32.5% vs. 17.7%;p=0.032)和既往CT(32.5% vs. 13.4%;p= 0.003)方面存在差异。中位随访时间为37.5个月(95%CI 31.4 - 43.5),gBRCA1/2 PV和wt患者的mPFS分别为10.7个月 vs. 26.7个月(p< 0.001)。同样,gBRCA1/2 PV患者的生存期也较短(40.1个月 vs. 69.0个月;p=0.013)。根据 ECOG PS状态和既往使用CT治疗MBC的情况调整生存率后,证实gBRCA1/2 PV患者的预后更差(PFS HR,1.61;95%CI:1.09-2.44;p=0.017;OS HR,1.72;95%CI:1.01 - 2.94;p= 0.047)。在 gBRCA1/2 PV患者中,CDK4/6i进展后接受PARP抑制剂和CT治疗的患者分别占15.6%(5人)和62.5%(20人;8人接受了铂类治疗)。
结论
这些数据表明,gBRCA1/2 PV是接受CDK4/6i 加ET治疗的HR+ HER2- MBC患者的一个负面预后因素。这一亚组患者非常需要不同的治疗策略。
1、Scavone G, Ottonello S, Blondeaux E, et al. The Role of Cyclin-Dependent Kinases (CDK) 4/6 in the Ovarian Tissue and the Possible Effects of Their Exogenous Inhibition. Cancers (Basel). 2023;15(20):4923. Published 2023 Oct 10.
排版编辑:肿瘤资讯-momo











 苏公网安备32059002004080号
苏公网安备32059002004080号


