胃癌被认为是一种与年龄相关的疾病,在英国,新发病例多为75岁以上。目前,与癌症治疗相关的指导多是基于对健康、年轻患者进行的试验。从历史上看,老年人在临床试验中的代表性一直不足,临床试验通常被限制在75岁以下。随着年龄的增长发生生理变化,包括器官功能下降、药代动力学和药效学变异,以及功能状态受损,所以针对老年或体力评分差的患者的治疗决策应采取更加个性化的方法。本期分享的这例老年晚期胃癌患者,采用免疫联合靶向联合抗血管治疗模式获得了令人满意的治疗效果,为患者带来良好生存获益和生活质量。
吉林大学第一医院肿瘤中心
中国细胞生物治疗协会青年委员
中国吴阶平基金会营养学部青年委员
国家自然基金面上项目第2负责人2项
省科技厅项目第1负责人1项
省科技厅科技发展计划第1参与人1项
吉林省省级产业创新专项第2参与人1项
病例介绍
一般资料
患者,男性,76岁,因“胃胀、反酸半年”就诊,胃镜见胃窦占位性病变,病理为低分化腺癌。PET-CT见胃窦壁、胃角及胃小弯侧壁厚伴代谢增高,考虑胃癌,肝内多发高代谢,考虑肝转移,肝门区、胃周、胰腺上方、肠系膜间隙淋巴结转移,左侧骨转移。患者存在胃胀、胃痛、嗳气、返酸,进食后腹痛加重,伴乏力,每日白天卧床时间在50%左右,无发热,饮食较前明显减少,睡眠尚可,二便基本正常,近半年体重下降10kg。
既往史:既往体健,母系家属肺癌病史,吸烟指数600支年。否认过敏史。
病例特点:患者老年男性,以腹部症状为主症起病。ECOG评分3分,胃镜、PET-CT提示患者为胃癌晚期,伴全身多发转移癌。
检查资料
查体: 生命征平稳,ECOG评分3分, 神志清楚,未触及肿大浅表淋巴结,心肺查体无特殊。腹部:腹平坦,未见腹壁静脉曲张及蠕动波,腹软,左上腹轻压痛,无反跳痛,无肌紧张,肝脾肋下未触及,无液波震颤,未触及包块,移动性浊音阴性,肝脾肾区无叩击痛,肠鸣音正常,未闻及血管杂音。
辅助检查:
【初诊2022年9月】
胃镜病理:病理:低分化腺癌,CK+,CK7+,部分CK20-,CEA-,villin+,P53+,Ki67 60%,Syn+,CD56-,CD45+,Ecad+,CgA-,CK5/6-,P63-,Her2 2+,PDl1 CPS=2(Dako 22c3)。
基因检测(2022年9月20日):CCNE1基因扩增,ERBB2基因扩增,检出肿瘤突变负荷(TMB)为TMB-H,13.44Muts/Mb;检出微卫星不稳定性(MSI)为MSS。
肿瘤标志物(2022年9月6日):细胞角蛋白19片段130.91ng/ml;癌胚抗原 76.3ng/ml;糖链抗原125 318.77 U/ml;神经元特异性烯醇化酶129.34ng/ml。
PET-CT(2022年9月6日):1)胃窦壁、胃角及胃小弯侧壁厚伴代谢增高,考虑胃癌;2)肝内多发高代谢,考虑肝转移;3)肝门区、胃周、胰腺上方、肠系膜间隙淋巴结转移;4)左侧坐骨转移。
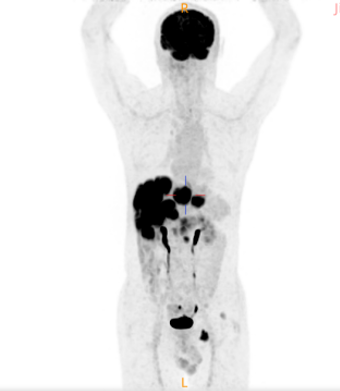
 图1.2022年9月影像学辅助检查
图1.2022年9月影像学辅助检查
【首次复查2022年11月】疗效评估为疾病稳定(SD)
肿瘤标志物:癌胚抗原8.19ng/ml。
颈部软组织多排CT平扫:1)左侧咽隐窝变浅;2)左侧胸锁乳突肌较对侧饱满;3)左侧颈静脉起始部扩张,上述所见,请结合临床必要时进一步检查。
肺部多排CT平扫:1)考虑支气管炎;双肺散在慢性炎症;2)右肺中叶钙化灶;左肺下叶磨玻璃样影,建议复查;3)双肺散在限局性肺气肿;4)双侧胸膜限局性增厚并钙化;5)纵隔淋巴结略肿大并钙化;6)胸主动脉及冠状动脉硬化。
上腹部、下腹部、盆腔多排CT平扫+三期增强:检查所见:肝影不大,表面光滑,各叶比例协调,肝门肝裂不宽,肝内见多个团块状低密度影,其内见斑片状高密度影,边缘模糊,大小约0.8cm×1.2cm~7.0cm×5.9cm,增强扫描后未见明显强化。肝内见类圆形低密度影,大小约0.5~1.7cm,增强扫描未见强化,肝内胆管未见扩张。右肾见点状钙化影,大小约0.2cm,右肾见类圆形低密度影,大小约0.8cm,未见强化。肝门区及胃小弯侧见增大淋巴结,大小约0.6~0.9cm。左侧坐骨见斑片状高密度影。
检查结论:1)胃窦壁及胃小弯侧壁改变,考虑胃癌,请结合镜检结果;2)考虑肝多发转移治疗后改变,未见明显强化,建议复查;3)肝囊肿;4)右肾囊肿;右肾小结石;5)前列腺增生伴钙化;6)腹腔内淋巴结略增大;7)左侧坐骨改变,请结合临床。
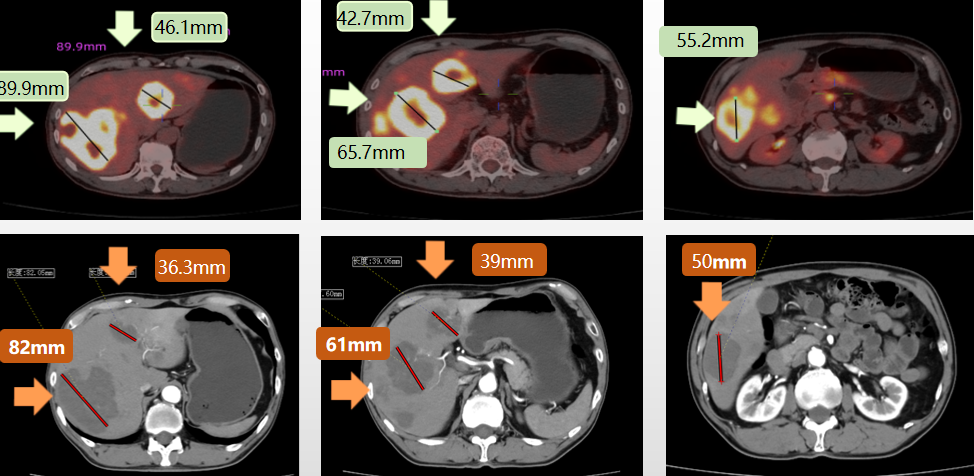 图2. 2022年11月首次复查
图2. 2022年11月首次复查
【第二次复查,2023年2月】疗效评估为部分缓解(PR)
肿瘤标志物:正常。
颈部软组织多排CT平扫(神经组):1)左侧咽隐窝变浅;2)左侧胸锁乳突肌较对侧饱满;3)左侧颈静脉起始部扩张,对比2022年11月17前片未见明显改变。
肺部多排CT平扫:1)考虑支气管炎;双肺散在炎症;2)右肺中叶钙化灶;左肺下叶磨玻璃样影,不除外炎性,较2022年11月17前片相仿,建议复查;3)双肺散在限局性肺气肿;4)双侧胸膜限局性增厚并钙化;5)纵隔淋巴结并钙化;6)胸主动脉及冠状动脉硬化。
上腹部、下腹部、盆腔多排CT平扫+三期增强:检查所见:肝影不大,表面光滑,各叶比倒协调,肝门肝裂不宽,肝内见多个团块状低密度影,其内见斑片状高密度影,边缘模糊,大小约0.8×0.6cm~6.7×5.6cm增强扫描后未见明显强化。肝内见类圆形低密度影,大小约0.5~1.7cm,增强扫描未见强化,肝内胆管未见扩张。右肾见点状钙化影,大小约0.2cm,右肾见类圆形低密度影,大小约0.8cm,未见强化。肝门区及胃小弯侧见增大淋巴结,大小约0.6~0.9cm。左侧坐骨见斑片状高密度影。
检查结论:1)考虑胃窦及胃小弯胃癌,对比2022年11月17日前片未见明显变化,请结合镜检结果;2)肝脏多发囊肿;肝脏多发转移治疗后改变,部分病灶较前片体积略减小,建议复查;3)不除外胆囊炎症,请结合病史;4)双肾微小囊肿;右侧肾盏小结石;5)前列腺增生伴钙化;6)腹腔内胃大弯旁淋巴结肿大;7)右侧骶骨翼骨岛;左侧坐骨片状高密度影,对比前片未见明显变化,请结合临床。
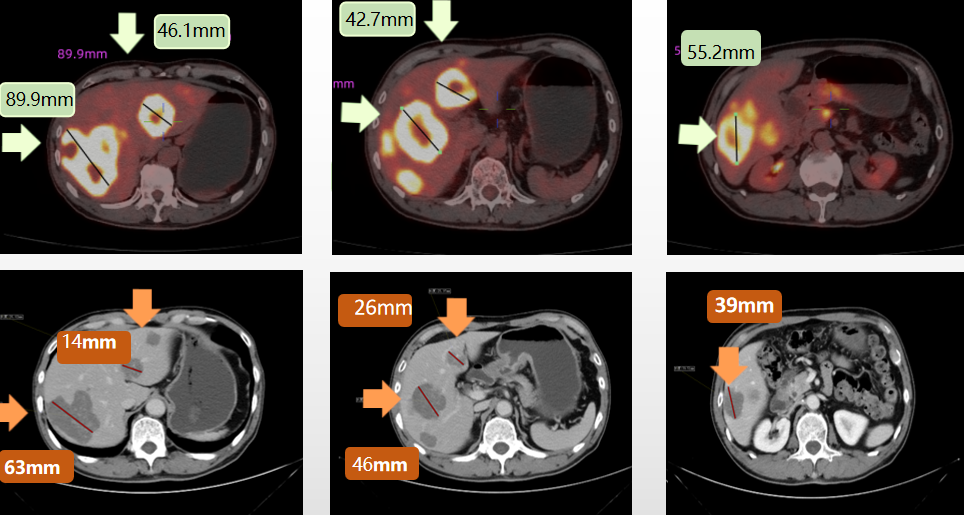 图3. 2023年2月第二次复查
图3. 2023年2月第二次复查
【第三次复查,2023年4月】疗效评估为持续PR
肿瘤标志物:正常。
颈部软组织多排CT平扫:左侧胸锁乳突肌较对侧饱满,对比2023年2月15日前片未见明显变化。
肺部多排CT平扫:1)考虑支气管炎;右主支气管及右肺上叶支气管少许痰液潴留,双肺少许炎症;2)左肺下叶磨玻璃样影,较2023年2月15日前片相仿,请结合临床注意复查;3)右肺中叶钙化灶;双肺散在限局性肺气肿;4)双侧胸膜限局性增厚并钙化;5)纵隔淋巴结并钙化;6)胸主动脉及冠状动脉硬化。
上腹部、下腹部、盆腔多排CT平扫+三期增强:肝影不大,表面光滑,各叶比例协调,肝门肝裂不宽,肝内见多个团块状低密度影,其内见斑片状高密度影,边缘模糊,大小约0.8×0.6cm~6.7×5.6cm,增强扫描后未见明显强化。肝内见类圆形低密度影,大小约0.5~1.7cm,增强扫描未见强化,肝内胆管未见扩张。双肾上腺、左肾大小形态及密度未见异常改变,右肾见点状钙化影,大小约0.2cm,右肾见类圆形低密度影,大小约0.8cm,未见强化。双侧督主输尿管未见扩张,膀胱充盈不佳,腔内未见异常密度影,前列腺体积增大,其内见结节状钙化影。腹腔内未见游离气体及液体影。胃窦壁及胃小弯侧壁增厚,增强扫描早轻度强化。肝位间隙可见结节状稍高密度影,其内可就见点状钙化影,动脉期可见轻度强化。左侧坐骨见斑片状高密度影。
检查结论:1)考虑胃窦及胃小弯胃癌,对比2023年2月15日前片未见明显变化,请结合镜检结果;2)肝脏多发囊肿;肝脏多发转移治疗后改变,部分病灶较前片体积略缩小,建议复查;3)不除外胆囊炎症,请结合病史;4)双肾微小囊肿:右侧肾盏小结石;5)前列腺增生伴钙化;6)肝胃间隙淋巴结肿大并钙化,较前片相仿;7)右侧骶骨翼骨岛;左侧坐骨片状高密度影,对比前片未见明显变化,请结合临床。
诊断:
胃低分化腺癌Ⅳ期(TxN+M1),腹腔淋巴结转移癌,肝转移癌,骨转移癌。
治疗
患者高龄,75岁以上,ECOG评分3分,且强烈抗拒化疗,2022年9月开始,给予卡度尼利单抗+呋喹替尼+曲妥珠单抗治疗18周期。
治疗结果、随访及转归
1)疗效:2疗程后患者腹胀、腹痛、返酸缓解,ECOG评分1分。肿瘤缩小明显,疗效评估为SD,4疗程后至今疗效评估为PR、持续PR。
2)不良反应:乏力 CTCAE 1级。
总结
免疫治疗+靶向治疗+抗血管治疗老年晚期胃癌耐受性良好,安全性良好,卡度尼利单抗作为全球首款以PD-1、CTLA-4为基础的双特异性抗体,在真实世界治疗中取得出色成绩,疗效显著且安全可控。
经验与讨论:
目前,文献中有关老年晚期胃癌患者的数据是有限的,有时还相互矛盾,文献检索中,老年患者的确可以从姑息治疗中获益,但往往需要采取个性化治疗。
PD-1抑制剂联合化疗是晚期胃癌的首选治疗[1],但对于PD-L1低表达的患者,PD-1抑制剂获益有限,AK104-201 Ⅱ期研究结果证明卡度尼利单抗全人群高效缓解,ORR达68.2%,PD-L1 CPS<5人群中位OS为17.28个月,PD-L1 CPS≥5人群中位OS达20.24个月,III期临床试验AK104 302中,在PD-L1 CPS < 5的人群卡度尼利联合化疗显著降低全人群的死亡风险。表明卡度尼利单抗联合化疗在PD-L1低表达的人群中仍能获得与高表达人群类似的生存期[2]。异常血管生成和免疫逃避是胃癌进展的重要因素,两者协同促进肿瘤的发生发展,已有多项研究证明肿瘤血管正常化可以提高免疫检查点抑制剂治疗的疗效,反之免疫刺激的增强也进一步促进血管正常化;KEYNOTE-811研究证实针对HER2阳性的胃癌患者,免疫联合靶向联合化疗给患者带来更深、更久的缓解[3]。
本例为老年患者,患病时ECOG评分3分,且拒绝化疗,初始治疗给予卡度尼利单抗联合呋喹替尼治疗,患者耐受良好,症状缓解明显,体力恢复,肿瘤缩小,基因检测结果回报后,在此基础加用曲妥珠单抗治疗,患者肿瘤进一步缩小并持续缓解,副作用为CTCAE 1级的乏力,目前已治疗14个月,仍持续缓解中。对于老年体力评分差的晚期胃癌患者,卡度尼利单抗联合呋喹替尼治疗耐受、疗效良好,对于合并HER2扩增的患者,联合曲妥珠单抗可为患者带来更好的缓解。
专家点评
吉林大学第一医院肿瘤中心
头颈部肿瘤内科负责人
中国医药教育协会头颈肿瘤专业委员会委员
中国抗癌协会中西医整合食管癌专业委员会常委
中国医药教育协会肿瘤化学治疗专业委员会委员
中国抗癌协会科普专业委员会委员
中国医药生物技术协会医药生物技术临床应用专业委员会委员
吉林省抗癌协会肺癌专业委员会常委
吉林省营养师协会肿瘤分会常委
北京肿瘤防治研究会肺癌分委会委员
吉林省生命关怀协会肿瘤舒缓治疗专业委员会肿瘤营养学组委员
吉林省生物治疗学会理事
吉林省健康科普专家
长春市医学会医疗事故技术鉴定专家
晚期胃癌患者的一线治疗仍以化疗为基石。目前,在免疫检查点抑制剂对比化疗的临床试验中,亚组分析均不支持ECOG评分2分或以上的患者存在总生存获益。对于75岁以上的高龄患者的数据非常有限。CheckMate 649、ORIENT-16等研究奠定了PD-1抑制剂在晚期胃癌一线治疗中的地位[4,5],但对于CPS评分偏低的患者,生存获益有限。卡度尼利单抗是抗PD-1和抗CTLA-4的双特异性抗体,在Ⅱ期研究中卡度尼利单抗显示了良好的耐受性,而且PD-L1低表达人群获得了与高表达人群类似的总生存(OS)[2]。VEGFR抑制剂在抑制肿瘤的血管生成中起到至关重要的作用。呋喹替尼是一种高选择性、强效的口服血管内皮生长因子受体(VEGFR)-1、2及3抑制剂,其激酶选择性更高,脱靶毒性低、耐受性好。FRUTIGA研究中[6],呋喹替尼联合紫杉醇与紫杉醇单药相比明显延长了二线晚期胃癌患者的无进展生存(PFS),也陆续有REGONIVO、LEAP005、UMIN000025947、NCT04067986、CAMILLA等一系列研究证明PD-1抑制剂联合抗血管治疗具有良好的安全性及疗效[7-11],而HER2扩增阳性更是为患者增加了曲妥珠单抗靶向治疗的可行性。
本例患者初始采用“卡度尼利单抗+呋喹替尼”的去化疗模式,显示了安全性良好,而且肿瘤缩小,患者体力恢复,在此基础上加用曲妥珠单抗治疗,达到了更深的缓解。以上提示对于高龄或体力评分差的HER2阳性的晚期胃癌患者,卡度尼利单抗联合呋喹替尼和曲妥珠单抗可能是一个安全有效的选择。这份报告为晚期高龄或体能评分差的胃癌患者提供了重要的治疗经验。
[1] 中国临床肿瘤学会(CSCO)胃癌诊疗指南,2023版.
[2] Jiafu Ji, et al.A phase Ib/II, multicenter, open-label study of AK104, a PD-1/CTLA-4 bispecific antibody, combined with chemotherapy (chemo) as first-line therapy for advanced gastric (G) or gastroesophageal junction (GEJ) cancer.2022ASCO-GI,Abstract 308.
[3] Yelena Y, Akihito K, Patricio Y et al. The KEYNOTE-811 trial of dual PD-1 and HER2 blockade in HER2-positive gastric cancer[J]. Nature. 2021 Dec;600(7890):727-730.
[4] Shitara K, Ajani JA, Moehler M, et al. Nivolumab plus chemotherapy or ipilimumab in gastro-oesophageal cancer. Nature. 2022;603(7903):942-948.
[5] J.Xu,H.Jiang,Y.Pan,et al.Sintilimab plus chemotherapy(chemo)versus chemo as first-line treatment for advanced gastric or gastroesophageal junction(G/GEJ)adenocarcinoma(ORIENT-16):First results of a randomized,double-blind,phase III study.2021ESMO,LBA53.
[6] Xu RH, et al. Cancer Communications. 2022;1–4.
[7] Fukuoka S, Hara H, Takahashi N, et al. Regorafenib plus Nivolumab in patients with advanced gastric (GC) or colorectal cancer (CRC): an open-label, dose-finding, and dose-expansion phase 1b trial (REGONIVO, EPOC1603). ASCO, 2019, abstract 2522.
[8] Carlos Gomez-Roca, et al. LEAP-005: A phase II multicohort study of lenvatinib plus pembrolizumab in patients with previously treated selected solid tumors—Results from the colorectal cancer cohort. 2021 ASCO GI Abstract 94.
[9] Nakajima TE, Kadowaki S, Minashi K, et al. Multicenter Phase I/II Study of Nivolumab Combined with Paclitaxel Plus Ramucirumab as Second-line Treatment in Patients with Advanced Gastric Cancer. Clin Cancer Res. 2021;27(4):1029-1036.
[10] Xiao L, et al. Camrelizumab combined with apatinib in the treatment of patients with advanced gastric cancer and colorectal cancer: One-arm exploratory clinical trial.2020 ESMO Abstract 442P.
[11] Saeed A, et al. Cabozantinib (cabo) combined with durvalumab (durva) in gastroesophageal(GE) cancer and other gastrointestinal (GI) malignancies: Preliminary phaseIb CAMILLA study results. 2020 ASCO Abstract 4563.
排版编辑:肿瘤资讯-Wendy











 苏公网安备32059002004080号
苏公网安备32059002004080号


