
肝内胆管癌(intrahepatic cholangiocarcinoma,ICC)是肝脏第二大原发恶性肿瘤(约占原发性肝癌的10%~15%),且发病率不断上升[1]。由于起病隐匿、侵袭性强、发展迅速,多数患者初诊时已处于中晚期,失去了根治性手术机会[2]。对于无法手术的晚期ICC患者,吉西他滨联合铂类的化疗策略是一线标准治疗,但应答率不高,总体而言患者预后不佳[3]。以免疫检查点抑制剂为代表的免疫治疗时代的到来,为恶性肿瘤包括胆道系统恶性肿瘤治疗展现了令人鼓舞的前景。其中,以免疫检查点抑制剂为基础的联合化疗和(或)靶向治疗已经在胆道系统恶性肿瘤治疗中显现良好的效果[4]。本期由烟台毓璜顶医院肝胆外科黄庆先医生为大家分享并解读一则病例,该病例为“替雷利珠单抗+安罗替尼”一线治疗IVB期ICC的真实案例,经治疗患者肿瘤明显缩小,达到部分缓解(PR),目前(截至2023-06-20)患者无进展生存期(PFS)已达30个月。
专家介绍
烟台毓璜顶医院
肝胆外科 医学博士 主任医师 硕士研究生导师
青岛大学医学院硕士研究生导师
山东省中西医结合学会肝胆胰分会副主任委员
山东省医师协会肝胆胰腔镜微创医师分会委员
中国医师协会胰腺疾病委员会微无创专业学组委员
中国医师协会腹膜后疾病委员会委员
中国成人教育协会医学继续教育专业委员会理事
国家肿瘤微创产业联盟普通外科专业委员会委员
烟台市抗癌协会肝胆胰肿瘤分会副主任委员
病例详情
01基本信息
患者男性,63岁。
主诉:检查发现肝功异常1天。
现病史:患者1天前体检发现肝功能异常,伴皮肤、巩膜轻微发黄,无腹痛、腹胀、恶心、呕吐等不适,无消瘦、发热等表现。为求进一步诊治特来我院,以“肝功能异常待查”收住入院。
既往史、个人史、家族史:均无特殊。
体格检查:东部肿瘤协作组(ECOG)体能状态评分:0分,全身皮肤巩膜轻度黄染。
02辅助检查
入院(2020-10-09)实验室检查:
肝功能:TBIL:102umol/L,DBIL:57umol/L,IBIL:44umol/L,AST:180U/L,ALT:372U/L。
肿瘤标志物:SCCA:7.5ng/mL,CEA:11.11ng/mL,CA19-9:255u/mL,CA12-5:408u/mL。
2020-10-09增强磁共振(MRI)+磁共振胰胆管成像(MRCP)示:肝内胆管细胞癌侵犯胆囊、肝门部胆管、肝右叶、尾状叶,瘤灶最大径约6.7cm×5.6cm;肝内胆管扩张明显。
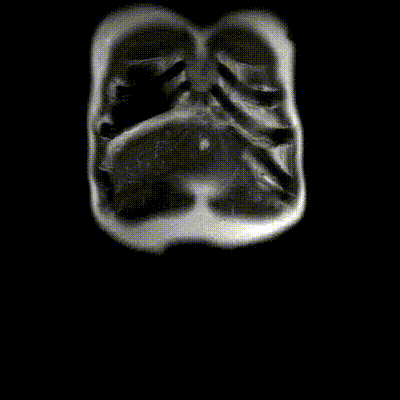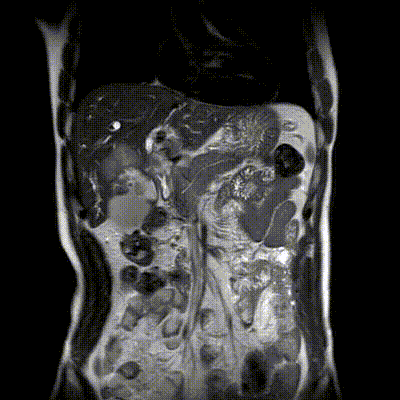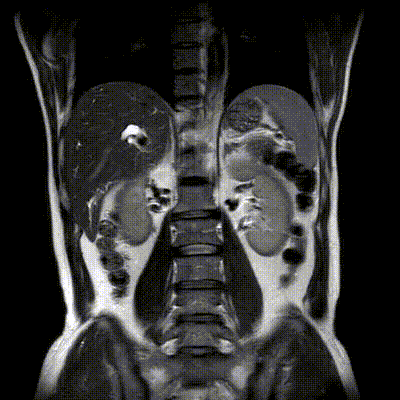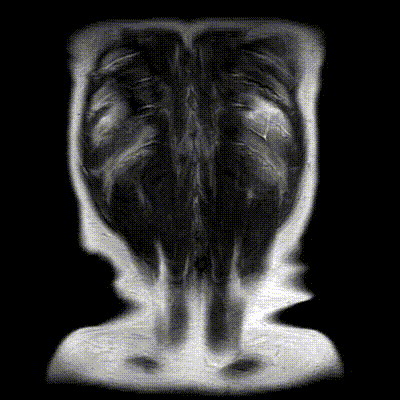
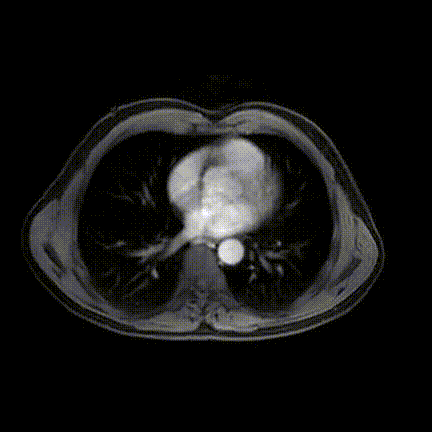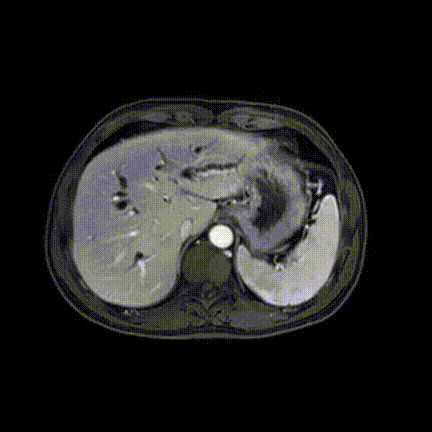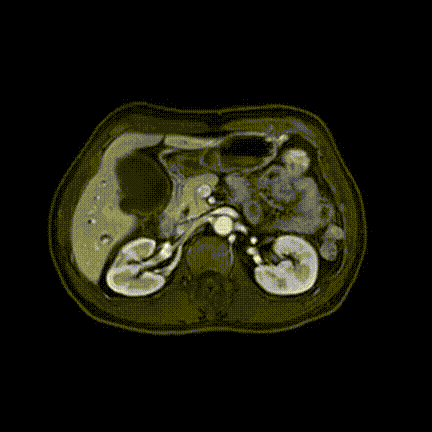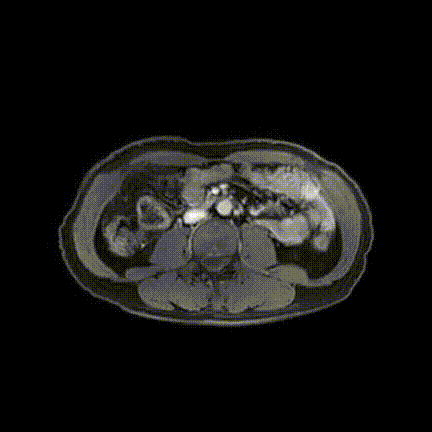 2020-10-09增强MRI+MRCP影像
2020-10-09增强MRI+MRCP影像
03临床诊断
肝内胆管细胞癌伴肝内转移(IVB期);
梗阻性黄疸。
04治疗经过
考虑患者存在梗阻性黄疸、肝内胆管扩张明显,排除禁忌后于2020-10-14行经皮肝穿刺胆道引流术(PTCD)+肝穿刺活检术,操作过程顺利,病理化验结果示:腺癌考虑胆管来源。
上述病理结果证实为胆道系统肿瘤,结合其它临床资料,认为该患者转移性肝内胆管癌诊断明确,无手术切除指征,拟定下一步治疗方案为:行胆管内支架植入术以减黄+一线靶免联合系统治疗。
于2020-10-27行胆管内支架植入术,操作过程顺利。
于2020-12-10启动靶免治疗,具体用药方案为:安罗替尼12mg po qd,连续用药2周后休1周,每3周为一个疗程 + 替雷利珠单抗200mg ivgtt q3w。
靶免治疗3个月后(2021-03-07)实验室检查:
肝功能:TBIL:20umol/L,DBIL:5umol/L,IBIL:15umol/L,AST:21U/L,ALT:20U/L。
肿瘤标志物:SCCA:1.1ng/mL,CEA:6.54ng/mL,CA19-9:39u/mL,CA12-5:12U/mL。
2021-03-07行肝胆增强CT检查示:瘤灶较前缩小,肝内胆管无明显扩张。
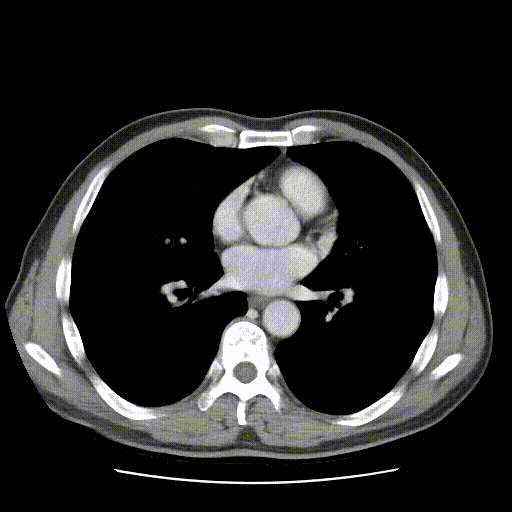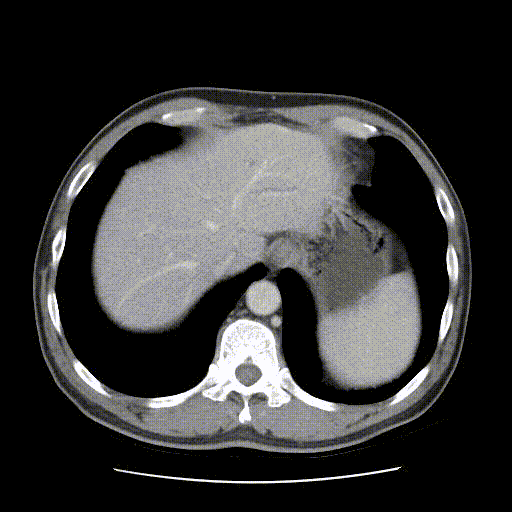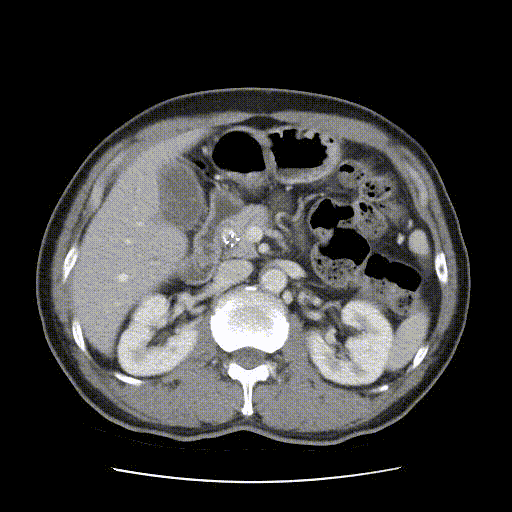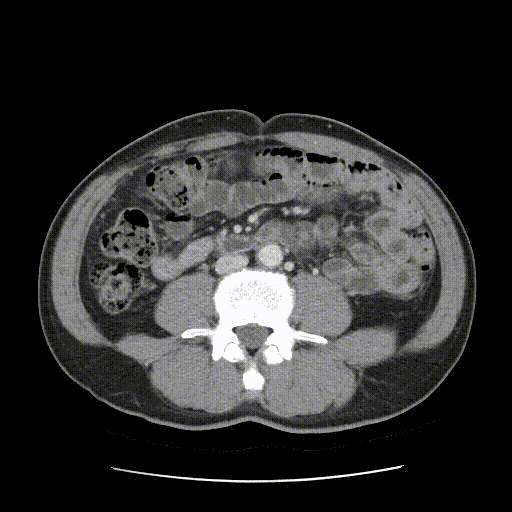 靶免治疗3个月后(2021-03-07)肝胆增强CT影像
靶免治疗3个月后(2021-03-07)肝胆增强CT影像
靶免治疗7个月后(2021-07-26)实验室检查:
肝功能:TBIL:10.7umol/L,DBIL:1.9umol/L,IBIL:8.8umol/L,AST:23U/L,ALT:19U/L。
肿瘤标志物:SCCA:1.0ng/mL,CEA:3.84ng/mL,CA19-9:10.9u/mL,CA12-5:7.42U/mL。
2021-07-26行肝胆增强MRI示:瘤灶明显缩小,最大径约2.3cm×1.6cm。
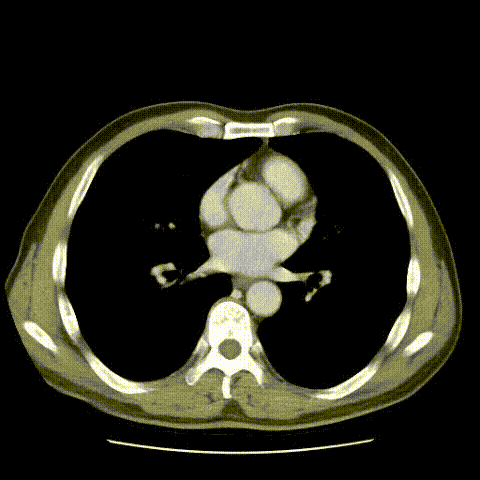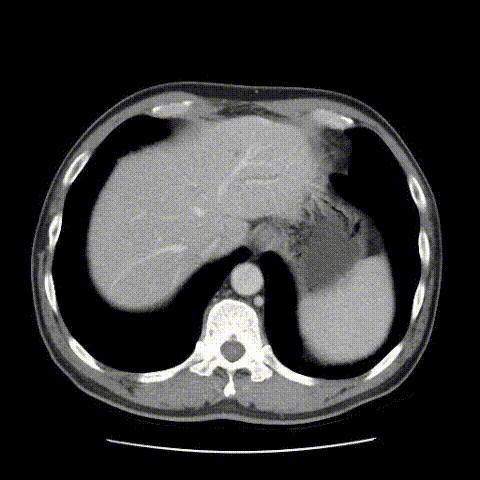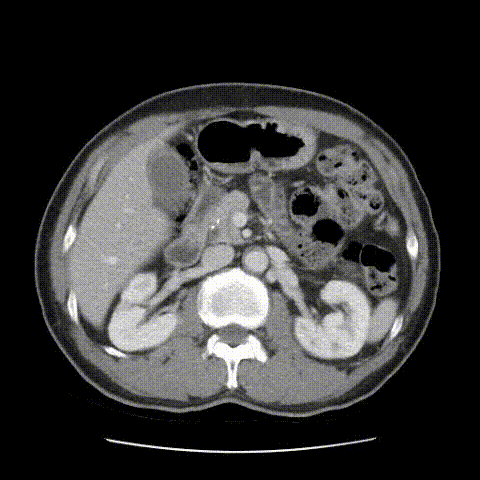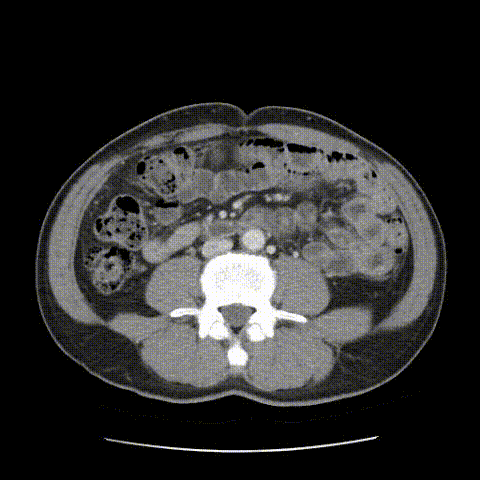
靶免治疗7个月后(2021-07-26)肝胆增强MRI影像
最近一次(靶免治疗30个月后,2023-06-20)实验室检查:
肝功能:TBIL:7.7umol/L,DBIL:1.4umol/L,IBIL:6.3umol/L,AST:17U/L,ALT:17U/L。
肿瘤标志物:CEA:2.95ng/mL,CA19-9:15.49u/mL,CA12-5:17.7U/mL。
2023-06-20肝胆增强MRI示:胆管支架引流术后,瘤灶进一步缩小至约2.1cm×1.0cm大小,边缘轻度强化。
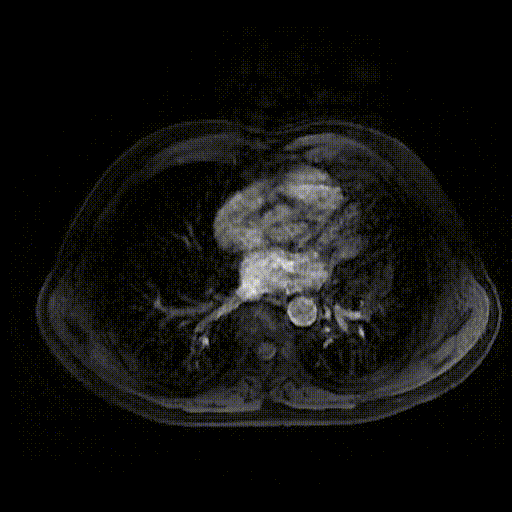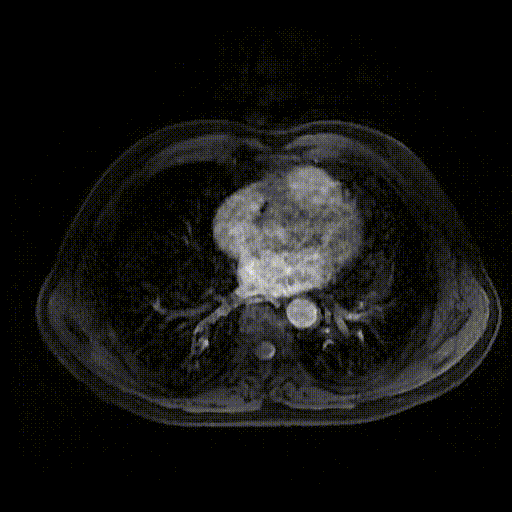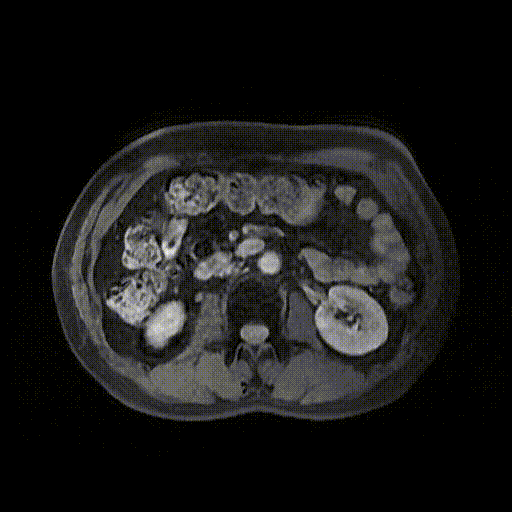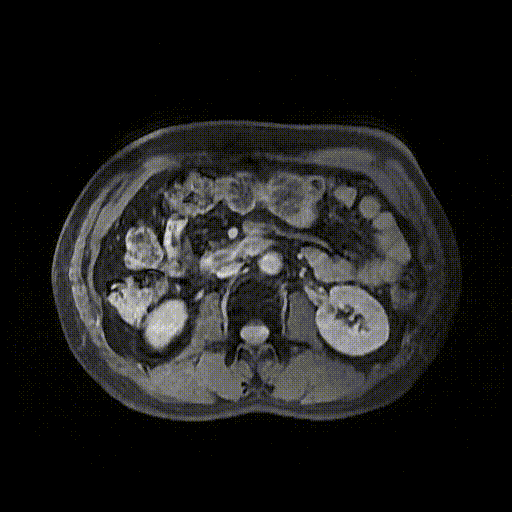 靶免治疗30个月后(2023-06-20)肝胆增强MRI影像
靶免治疗30个月后(2023-06-20)肝胆增强MRI影像
经靶免联合治疗,目前患者一般情况可,肝功能已恢复正常,肿瘤标志物水平维持在较低水平,影像学检查见瘤灶逐渐缩小,已达PR。且长期治疗过程中,患者耐受性良好,目前仍在服药随访中,期待后续更长期的获益。
疗效评估:“替雷利珠单抗+安罗替尼”一线治疗IVB期ICC实现PR,目前(截至2023-06-20)患者PFS已达30个月。
不良反应:整个治疗期间未出现任何治疗相关不良反应,药物安全性和患者耐受度良好。
病例总结
ICC是起源于肝内胆管上皮的恶性肿瘤,绝大多数为腺癌,在我国呈相对高发且发病率近年来呈现上升趋势[3]。由于发病隐匿、恶性程度高,大多数患者(>65%)初诊时病灶已不可切除[3]。对于此类晚期ICC患者,以吉西他滨为基础的化疗是一线治疗方案,但一直以来其疗效不尽如人意[4]。研究发现,高达70%的ICC患者至少有一个可用于靶向治疗的分子突变靶点,如FGFR2融合、KRAS、BRAF、EGFR、IDH突变[1]; 72.2%的ICC患者肿瘤前缘细胞表达 PD- L1,而且PD-L1阳性者存活率下降60%[5];在ICC的治疗中,抗血管生成靶向药物可与免疫治疗产生协同作用[2]等。以上这些研究为小分子抗血管生成靶向药物和PD-1/PD-L1免疫检查点抑制剂在ICC患者中的应用提供了有力的支持。
事实上,以免疫检查点抑制剂为基础的联合化疗和(或)靶向治疗已经在胆道系统恶性肿瘤治疗中显现良好的效果[4]。一项采用GEMOX联合多纳非尼和替雷利珠单抗一线治疗局部晚期或转移性胆道系统恶性肿瘤的前瞻性单中心探索性研究显示: 6个月总生存期(OS)率高达90.9%,转化治疗成功率约23.1%;且整个研究期间,≥3级治疗相关不良事件发生率(TRAEs)为53.8%,未观察到5级TRAE和非预期不良事件[6]。另一项采用替雷利珠单抗联合仑伐替尼和GEMOX治疗潜在可切除的局部晚期胆道系统恶性肿瘤的单臂、开放标签、II期研究结果表明:客观缓解率(ORR)可达56%,转化治疗成功率高达84%,约52%的患者实现了R0切除,其中1例(4%)患者达到pCR,且所有患者术后均未发生严重并发症[7]。以上研究数据充分体现了替雷利珠单抗在中晚期胆道系统恶性肿瘤治疗中的重要价值,在临床上已成为晚期胆道恶性肿瘤患者治疗的优选。
基于上述研究证据,对于本例IVB期ICC患者,在积极治疗梗阻性黄疸的基础上,我们采取了“替雷利珠单抗免疫治疗+安罗替尼靶向药物治疗”的方案,经治疗,患者黄疸消退、肝功能恢复正常、瘤灶明显缩小,影像评估达到PR,目前患者PFS已达30个月。在长期靶免联合治疗的过程中,患者未发生任何严重不良反应,耐受性良好,充分彰显了该方案治疗的良好安全性。目前患者仍在继续采用该靶免方案治疗,期待后续见证更长期的生存获益。本例患者的治疗策略对晚期ICC的一线系统治疗具有一定的借鉴意义,希望替雷利珠单抗能够助力更多晚期ICC患者收获更长期的生存期和更好的生活质量。
[1]喻彦熹, 吴忠均, 唐伟,等. 肝内胆管癌国际临床实践指南和共识的诊疗建议比较[J]. 中华外科杂志, 2023, 61(4):297-304.
[2]中国抗癌协会肝癌专业委员会胆管癌协作组. 原发性肝癌诊疗指南之肝内胆管癌诊疗中国专家共识(2022版)[J]. 中华消化外科杂志,2022,21(10):1269-1301.
[3]赵海涛, 杨旭. 肝内胆管癌转化治疗[J]. 中国实用外科杂志, 2020, 40(6):732-737.
[4]施国明, 裴晏梓, 陆品相, 等. 胆道系统恶性肿瘤免疫检查点抑制剂治疗[J].临床肝胆病杂志, 2022, 38(5):998-1001.
[5]张荷月,金添强,戴朝六,等.肝内胆管细胞癌免疫治疗和靶向治疗研究现状[J].中国肿瘤临床, 2019, 46(13):694-699.
[6]Lu Wang, et al. Efficacy and safety of sintilimab combined nab-paclitaxel and gemcitabine as first-line treatment for metastatic pancreatic ductal adenocarcinoma (PDAC): A retrospective analysis,2022 ESMO World GI ,p-110.
[7]Huikai Li, et al. A single-arm, open-label, Phase II study of tislelizumab combined with lenvatinib and GEMOX regimen for conversion therapy of potentially resectable locally advanced biliary tract cancers.2022 ESMO 65P.
排版编辑:肿瘤资讯-小编











 苏公网安备32059002004080号
苏公网安备32059002004080号


