▎药明康德内容团队编辑
结直肠癌(CRC)是全球最常见的癌症之一。和其他癌症相比,CRC的独特之处在于肠道内共生的菌群成为了肿瘤微环境的重要组成部分,它的失调对于癌症的发展、进展和治疗有着重要影响。近日,《自然》子刊Nature Reviews Clinical Oncology发布了一篇综述,系统性地回顾总结了肠道菌群与CRC之间的关系,以及它们对癌症治疗的重要意义。

人类肠道菌群是一个由细菌、真菌、病毒、古生物和寄生虫等微生物所构成的复杂生态系统,其细胞数量甚至超过人体细胞的数量,因此肠道菌群表现出比人类基因组更大的遗传多样性。从新生儿开始,微生物便开始定居在我们的胃肠道中,并随着宿主的成长和发育共同进化。肠道菌群易受生活方式变化的影响(如饮食、吸烟和运动),故而有着显著的个体差异性。
肠道菌群的稳态被认为有益于人体健康,反之,其失调可能会对宿主健康造成威胁,并导致包括CRC在内多种疾病的发生。研究表明,肠道菌群在CRC的发展过程中变得失调,是肿瘤发生过程中的重要因素,此外,它还可以改变人体对癌症治疗的反应,比如化疗和免疫检查点抑制剂(ICIs)治疗。想要精确地实现个体化肠道菌群调控,在癌症治疗过程中获得临床益处、并将不良事件的风险降到最低,我们需要深入理解对肠道微生物与CRC之间的关联及其背后的机制。
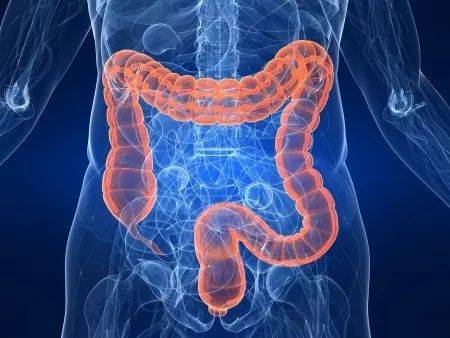
肠道微生物与CRC的关系
1.“有益”和“有害”菌群之间的平衡
这篇综述指出,肠道菌群失调(不论是细菌微生物失调或是非细菌类微生物失调)促进了CRC的发生和进展。在机制研究中,肠道菌群失调被认为是结直肠癌发生的早期事件,一些特定的“核心菌群”在其中起着关键性作用,不过它们是单独起作用或与其他微生物协同作用来加速CRC的进展目前尚不清楚。
有益肠道菌群的减少也同样值得关注,这些有益的菌群可以与癌症病原性菌群形成共排斥网络,研究表明病原性共生物和益生菌之间很可能存在竞争性或对抗性的相互作用,菌群失调破坏了促癌的病原性共生物和抗肿瘤益生菌之间的平衡,这可能对癌症病理发生有潜在的影响,同时也为开发基于肠道微生物的癌症疗法和生物标志物提供了可能性。此外,肠道中的微生物还可能会定植在肿瘤组织中,而且能在转移后的病灶中持久存在——这可能会对癌症的进展和转移产生影响。
图片来源:123RF
2.其他“小众”菌群的失调对CRC的影响
在肠道微生物中,细菌的丰度占绝对优势,其序列占肠道微生物序列的93%,因此大多数针对CRC中肠道微生物失调的研究都集中于细菌。然而,有研究发现,CRC癌症患者和健康患者相比,其他肠道微生物(包括病毒、真菌和古菌)的组成发生了改变,提示它们也可能与CRC病程相关。
进一步的研究发现,病毒和细菌之间的协同作用可能参与了CRC的发展。此外,部分真菌物种在CRC癌前病变(如结肠息肉和腺瘤)患者中存在肠道真菌失衡的现象,暗示了真菌可能参与早期阶段CRC的发生。近年的研究发现,古菌——这种常年生活在极端环境中的微生物也居住在胃肠道中,而且能从肠道细菌的发酵产物中获取能量。部分核心古菌种的水平在CRC发生过程中逐渐增加,并且和已知的致病性菌种呈正相关、与益生菌却存在着拮抗关系,这些发现提示古菌也构成了CRC患者体内失调的微生物网络的一部分。
对于一些无法利用现有微生物培养手段进行体外培养、或是没有可用的高质量参考基因组的“未知“肠道微生物,测序和计算技术的进步使得我们不依赖于体外培养就能揭示这些神秘微生物的特征,其中一些微生物被认为可能是结直肠癌的潜在生物标志物。此外,单细胞技术、微流体技术的进步有望为大规模地研究单个微生物提供技术支持,使得科学家们绘制人类和小鼠肠道微生物组的单细胞图谱成为可能,从而更精确地揭示这些以往被认为是“未知”的生物在CRC发生过程中所扮演的角色。
图片来源:123RF
总的来说,越来越多的证据表明,非细菌微生物在CRC的发病过程中发生了改变,但当前我们对于这些“小众”微生物在CRC发生、发展过程中的直接和间接作用仍不甚了解,亟需更多的研究来填补这一研究空白。随着单细胞技术和其他新兴技术的涌现,相信它们会进一步刷新我们对于CRC相关肠道微生物的理解。
微生物菌群失调与CRC肿瘤发生之间是否存在因果关系目前仍无定论。在小鼠模型中,植入CRC患者的粪便菌群,可以增强结肠细胞的增殖并加速致癌物诱导的结肠肿瘤的发生,如果植入其他已知的CRC致病菌群也有此效果。不仅如此,肠道菌群还可以与某些环境因素——如高脂饮食和吸烟,共同作用来加速CRC的发展。
肠道微生物促进CRC发展的潜在分子机制非常多样化。在这篇综述中,作者把这些机制大致分为以下几类:由基因毒性介导的遗传变异、致癌信号级联传导、炎症、促使免疫逃逸的发生、微生物-宿主间的共代谢以及营养组分所介导的变化。

图片来源:123RF
4.肠道微生物与宿主遗传学/表观遗传学之间的相互作用
既往研究揭示,宿主遗传/表观遗传特征与肠道菌群之间存在着双向交互作用。环境因素往往被认为是影响健康个体肠道菌群的主要因素,除此之外,宿主体内与癌症相关的遗传/表观遗传变异实际上与特定肠道微生物的富集或耗竭紧密相关。另一方面,肠道菌群也会影响宿主的遗传/表观遗传修饰——有研究表明肠道菌群组分的变化影响了p53、BRAF等关键癌症基因的活性,特别是在这些基因发生突变的情况下。
综合动物模型研究的结果,作者认为肠道微生物能够放大致癌因子的下游效应,促进CRC的发展。但这一结论需要进一步的验证,以判断癌基因变异和肠道菌群在CRC患者中的相互作用的临床相关性。
肠道菌群在CRC防治中的作用
治病不如防病。早在上世纪80年代,科学家们就发现,一些菌株可以抑制啮齿动物中由致癌物诱导的CRC肿瘤发生,为使用益生菌来预防CRC提供了最初的概念验证。在一些早期临床试验中,接受益生菌制剂的CRC患者显示出疾病复发风险的降低。不过,这些肠道益生菌并不直接定植在肠道黏膜,而是通过它们的代谢产物,以及与病原体的相互作用来保护肠道屏障功能,从而降低CRC发病风险。
依据现有研究成果,作者指出,肠道菌群可能通过以下机制来预防CRC的发生,同时影响治疗效果:
①肠道菌群丰富多样的代谢产物和细胞壁成分对肿瘤生长和存活起着抑制作用;
②肠道菌群可以抑制宿主炎症水平;
③肠道菌群失调的逆转可以抵消促癌病原体的致癌效应从而遏制CRC发生;
④增强宿主的先天性和适应性免疫反应;
⑤调节化学药物在结直肠癌化学预防中的效果;
⑥参与调控化疗药物的生物利用率和患者对化疗的反应、以及化疗耐药性的发生;此外还能通过免疫调节增强化疗药物的抗肿瘤活性;
⑦减少化疗相关的毒性。
肠道菌群影响着免疫检查点抑制剂的治疗效果
靶向性免疫检查点抑制剂(ICIs)已经彻底变革了多种癌症的治疗方式。然而,对于CRC患者来说,ICIs的治疗效果大多不佳,临床前和临床研究已经证实肠道菌群在ICIs治疗应答中起着不可或缺的作用。
肠道菌群拥有丰富的抗原库,这些抗原分子可以被宿主先天免疫细胞识别,从而诱发针对性的免疫反应。其中,肠道菌群-效应细胞、肠道菌群-CRC肿瘤细胞之间的信号crosstalk显得尤为重要。鉴于肠道菌群在癌症发展和机体免疫中不可忽视的作用,研究人员已尝试通过调节患者肠道菌群,来改善ICIs治疗CRC患者的效果,具体的干预方式包括粪便移植、益生菌等相关活菌制剂和益生元摄入,此外,也有研究人员利用基因工程手段改造益生菌以适应实际应用需要。
图片来源:123RF
调节肠道菌群失衡不仅可以提高免疫检查点抑制剂的疗效,还可能减少副作用的发生率。由于肠道微生物组在不同的人群中有显著的差异,所以基于肠道微生物的治疗干预在效果上也可能因人而异。理解这种差异性有助于设计更有效的个体化治疗,并减少因免疫治疗和化疗带来的不良反应。尽管这些问题需要进一步研究,但毋庸置疑,肠道微生物在癌症免疫治疗中拥有巨大潜力。
肠道菌群作为肿瘤生物标志物
有证据表明,CRC的早期诊断和优良的临床结局相关,如果能找到早期CRC或是癌前病变的生物标志物,实现CRC的早诊早治,对于改善患者预后有着重要意义。鉴于肠道菌群失衡通常是CRC肿瘤发生的早期事件,许多研究已对粪便微生物组进行了测试和数据挖掘,以期找到可用于诊断的生物标志物。
肠道微生物群与CRC发病机制中的代谢物密切相关,既往研究探索了综合肠道微生物和其代谢特征的生物标志物组合的诊断能力,另一些研究则将宿主特征(粪便免疫化学测试结果、遗传学和表观遗传学特征)和环境(肠道微生物群)的互补风险因素整合到一种检测方法中,以提高CRC检测方法的准确性。这些多靶点的检测策略在临床上究竟效果如何,还需要进行多队列、独立验证研究来加以确认。

图片来源:123RF
肠道微生物群作为生物标志物的意义不仅仅是诊断,特定的肠道微生物组成及其代谢产物被发现可能对CRC患者的全身治疗反应具有预测价值——肠道微生物可以作为CRC的预后标志物。一些研究已证实特定肠道细菌物种和ICIs治疗应答之间的关联,但综合来看,这一类研究的结果并不完全一致,它们并没有显示出单一微生物与患者对ICI的应答之间的一致关联。对此,作者认为这类研究结果的不一致性可能是因为与免疫检查点抑制剂的有效性相关的微生物代谢物来源于肠道微生物群中的不同成员,而这些成员的组成有着极强的个体差异性。因此,对肠道微生物的功能进行分析是确定ICI应答的预测标记物的可行方法。
结语
近年来,人们对于肠道菌群在CRC的发病机制、诊断、预防和治疗方面有了更深入的认识,但这些发现只是冰山一角,关于肠道菌群还有太多未解之谜等待探索。
随着新兴的第三代测序技术和单细胞微生物测序技术的发展,科学家们有望对菌株级别的微生物进行基因组分析,并且通过de novo基因组组装来解读未知的微生物基因组,这将增进我们对于肠道微生物多样性的全面认识。此外,对于肠道微生物的异质性认识,也将从菌株组成的异质性拓展到空间异质性(spatial heterogeneity),届时我们将得以窥见肿瘤内微生物的差异分布以及其与肿瘤内不同细胞类型(包括肿瘤细胞、免疫细胞和成纤维细胞)的相互作用,并从中找到CRC预防或治疗的新的分子靶点。
总言之,微生物对于CRC的临床意义已经得到了充分验证,如果能找适当的干预方法来实现肠道菌群的精准调控,基于肠道菌群的疗法在防止或延缓CRC的发生、增强化疗或免疫疗法的疗效、开发更精确的早期诊断工具和指导治疗决策等多个领域拥有非常广阔的前景。
参考资料:
[1] Wong, Chi Chun, and Jun Yu. “Gut microbiota in colorectal cancer development and therapy.” Nature reviews. Clinical oncology, 10.1038/s41571-023-00766-x. 11 May. 2023, doi:10.1038/s41571-023-00766-x
免责声明本文仅供专业人士参看,文中内容仅代表药明康德立场与观点,不代表肿瘤资讯平台意见,且肿瘤资讯并不承担任何连带责任。若有任何侵权问题,请联系删除。
排版编辑:肿瘤资讯-Kate











 苏公网安备32059002004080号
苏公网安备32059002004080号


