2020年美国临床肿瘤学年会(ASCO)在线科学大会发布了帕博利珠单抗联合含铂化疗一线治疗转移性非鳞非小细胞肺癌(NSCLC)的Ⅲ期临床研究KEYNOTE-189的最终分析结果[1]。
KEYNOTE-189是一项全球多中心、随机、双盲的Ⅲ期临床研究,旨在评估帕博利珠单抗联合培美曲塞与铂类化疗治疗转移性非鳞NSCLC患者的疗效。入组616例患者为未治的经病理证实转移非鳞状NSCLC,EGFR/ALK阴性。患者被随机(2∶1)分为两组,每3周给予培美曲塞/铂类+帕博利珠单抗(200mg,i.v)或安慰剂共4个周期,然后给予培美曲塞+帕博利珠单抗(200mg,i.v,q3w)或安慰剂维持治疗共31个周期。其中,安慰剂联合组疾病进展患者可以转到帕博利珠单抗单药治疗。研究终点:双主要终点为总生存期(OS)和无进展生存期(PFS),次要终点为客观缓解率(ORR)、缓解持续时间(DOR)和安全性。
该研究结果不但改变了Ⅳ期非鳞NSCLC的临床实践,而且在肿瘤免疫治疗的研究和临床实践的发展史上,KEYNOTE-189具有重大意义,且占有重要的地位。
自2018年4月16日美国癌症研究学会(AACR)年会及《新英格兰医学杂志》同步首次发布KEYNOTE-189中位随访10.5个月的研究结果[2]; 2019年ASCO又发布中位随访23.1个月的中期分析结果[3],到2020年5月29日,ASCO正式发布KEYNOTE-189中位随访31.0个月的最终分析结果[1]。以OS和PFS为双终点,ORR,DOR,治疗安全性为为次要终点,PFS2为探索性终点的KEYNOTE-189研究为我们验证了免疫联合化疗一线治疗带来的OS和PFS的持久改善,验证了无论PD-L1表达情况,OS和PFS均有获益。
本篇文章回顾KEYNOTE-189上述3次数据发布的结果,展现并剖析该研究为非鳞NSCLC治疗带来的富有改变临床实践意义的结果,并从中感悟KEYNOTE-189研究设计与执行的科学与稳健,以及该研究所体现的那种不懈追求以寻找答案的精神。
数据“稳”-核心结果皆可重复呈现
KEYNOTE-189完整的统计学分析计划要求开展两次中期分析,一次终期分析。三次分析结果在OS和PFS的双重主要终点,以及次要终点指标的分析结果都验证了稳定的生存获益。



图片引用自KEYNOTE-189三次分析结果在OS和PFS的双重主要终点,以及次要终点指标数据[1, 2, 3]
化疗组的中位OS和中位PFS:中位OS在10.6~11.3个月之间,中位PFS为4.9个月[1, 2, 3];
2019年ASCO发布和2020年ASCO发布的结果显示帕博利珠联合化疗组的中位OS为22.0个月,死亡风险降低44%,24个月的OS率分别为45.5%(化疗组29.9%)和45.7%(化疗组27.3%)[1, 3];
三次分析结果帕博利珠联合化疗组的中位PFS在8.8~9.0个月区间内;疾病进展或死亡风险降低区间在48%~52%[1, 2, 3];
2019年ASCO发布和2020年ASCO发布结果显示24个月的PFS率分别为20.5%(化疗组1.5%和22.0%(化疗组3.4%)[1, 3];
三次分析结果帕博利珠联合化疗组的ORR分别为47.6%、48.0%和48.3%,对比化疗组的18.9%、19.4%和19.9%[1, 2, 3];
三次分析结果帕博利珠联合化疗组的3~5级治疗相关不良反应分别为67.2%、 71.9%和72.1%,对比化疗组的65.8%、66.8%和66.8%[1, 2, 3];
免疫一线治疗早用可能改善生存获益?
“研究结果显示[i],70岁或70岁以上人群的中位OS和2两年OS率与整体人群的相当,但在ECOG PS评分2分的人群中,中位OS和2两年OS率都要低于整体人群的水平[4]”,同济医科大学附属上海市肺科医院肿瘤内科主任周彩存教授曾指出:“免疫治疗的疗效受患者的基础免疫功能状态的影响;患者状态好的时候,用免疫治疗效果好,而接受二线或后线治疗的患者往往 ECOG 评分较高、肿瘤负荷大、免疫功能差,因此,PD-1 单抗的治疗效果可能就差了”。
另外,周彩存教授指出:“一线治疗的PFS,加上二线治疗的PFS称为PFS2。从一线治疗开始,到二线治疗发生疾病进展或因任何原因的死亡,这段时间称之为 PFS2;这个指标可以反映一线治疗对后续二线治疗的影响,也就反映了用药的顺序怎样更好”。在2019 ASCO大会上公布的 KEYNOTE-189的PFS2分析数据[3],让这个理论首次在一个Ⅲ期临床研究中得到了验证。
帕博利珠单抗联合化疗组的中位PFS2是17个月,化疗组是9个月(中位随访时间18.8个月)[3];该数据结果显示,帕博利珠单抗应该用于一线治疗方案中,以给PD-L1表达阳性和阴性的转移性非鳞状NSCLC患者带来最大化的获益可能[3]。
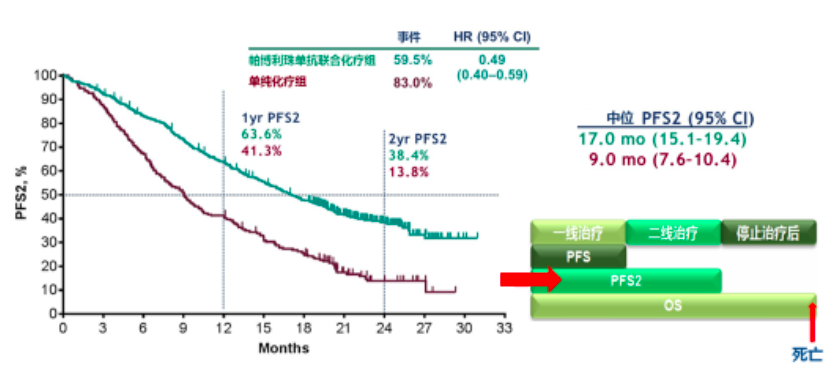
图片引用自KEYNOTE-189 2019年ASCO公布的结果中PFS2的数据[3]
此次2020年ASCO公布的结果也再次验证了该结论。在针对不同PD-L1分层人群中,无论PD-L1表达情况,免疫一线治疗的PFS2结果都要优于化疗一线治疗[1]。
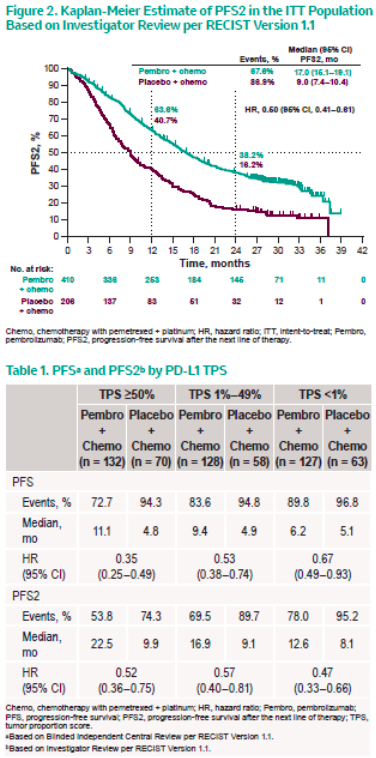
图片引用自KEYNOTE-189 2020年ASCO公布的结果中PFS2的数据[1]
无论PD-L1表达阳性或阴性都有OS获益
在KEYNOTE-189研究首次于2018年AACR大会上公布时,帕博利珠单抗联合化疗方案针对不同PD-L1表达人群都显示了OS和PFS的获益,但是PD-L1表达阴性患者的中位OS的HR值略高于PD-L1表达阳性的患者[2]。
在临床实践中,针对PD-L1表达阴性的非鳞NSCLC患者是否采用帕博利珠单抗联合培美曲塞和含铂化疗方案也曾一度有些许质疑。
2019年ASCO公布的KEYNOTE-189研究随访23.1个月的OS、PFS和PFS2数据结果显示免疫联合化疗一线治疗为PD-L1表达阴性患者带来的生存获益与PD-L1表达阳性患者相当[3];2020年ASCO公布的结果[1]再次验证了这个结论。

图片引用自KEYNOTE-189 2020年ASCO公布的数据[1]
KEYNOTE-189将指导临床实践
KEYNOTE-189研究所展现的是唯有依靠科学严谨的态度,脚踏实地的研究风格,循序渐进的研发策略才有可能获取最高级别循证医学证据,才有可能让临床医生在给予患者施治的临床实践中更有信心和安全感。这KEYNOTE-189研究带给我们的启示。
近日,在中国临床肿瘤学会(CSCO)发布的2020版《CSCO非小细胞肺癌诊疗指南》中,基于KEYNOTE-189研究结果的1A类证据,帕博利珠单抗联合培美曲塞和铂类化疗一线治疗非鳞NSCLC获得了专家Ⅰ级推荐,也是在此版指南中唯一一个Ⅰ级推荐给该类患者的免疫治疗[5]。
任何临床诊疗指南都是为了规范诊疗实践。KEYNOTE-189及其所研究的治疗方案被中国权威指南推荐意味着KEYNOTE-189将正式从仅在医学大会上或医学媒体上看到、听到的一个临床研究变为在真实世界中具有规范临床实践意义的治疗方案之一。
上海交通大学附属胸科医院呼吸科韩宝惠教授指出:“指南更新给了临床医生用药提供了学术指导,但是在临床实践中更多的是看国家是否批准了药物治疗适应证。如果国家批准,那医生会根据病人的情况来灵活的掌握。我们建议临床医生在用药上,尤其是免疫治疗药物的临床应用,要规范,必须以国家规定的适应证为准绳。根据获批适应证和指南推荐来指导临床实践对临床医生和患者是一种双重保障。”
KEYNOTE-189临床研究虽然已划上句号,但仍然有尚无答案却仍值得探究的问题:
在2020年ASCO公布的结果中,帕博利珠单抗联合化疗组仍有45.7%的患者在24个月存活1。这些患者3年、4年甚至5年的生存率是多少?
2020年ASCO公布的结果显示,56例完成了35个周期帕博利珠单抗治疗的患者的ORR达到85.7%,包括4例肿瘤完全缓解,44例部分缓解和8例稳定患者[1]。
2019年ASCO公布的KEYNOTE-001[ii]五年随访研究结果显示,接受帕博利珠单抗单药治疗两年或两年以上的初治患者(n=14)的五年生存率达78.6%[6]。所以免疫治疗的疗程应该是多久?疗程与长期生存有无关联?有哪些因素可预测长期生存?能否找到长期生存的预测因子?
……
希望在明年的ASCO,我们还能看到KEYNOTE-189的身影。
帕博利珠单抗注射液简明处方资料
【适应证】
黑色素瘤
帕博利珠单抗适用于经一线治疗失败的不可切除或转移性黑色素瘤的治疗。
非小细胞肺癌
帕博利珠单抗适用于由国家药品监督管理局批准的检测评估为PD-L1肿瘤比例分数(TPS)≥1%的表皮生长因子受体(EGFR)基因突变阴性和间变性淋巴瘤激酶(ALK)阴性的局部晚期或转移性非小细胞肺癌一线单药治疗。
帕博利珠单抗联合培美曲塞和铂类化疗适用于表皮生长因子受体(EGFR)基因突变阴性和间变性淋巴瘤激酶(ALK)阴性的转移性非鳞状非小细胞肺癌(NSCLC)的一线治疗。
帕博利珠单抗联合卡铂和紫杉醇适用于转移性鳞状非小细胞肺癌(NSCLC)患者的一线治疗。
食管癌
帕博利珠单抗单药用于通过充分验证的检测评估肿瘤表达PD-L1(综合阳性评分(CPS)≥10)的、既往一线全身治疗失败的、局部晚期或转移性食管鳞状细胞癌(ESCC)患者的治疗。
【用法用量】
本品须在有肿瘤治疗经验医生的指导下用药。帕博利珠单抗通过静脉注射给药,每3周一次,每次持续至少30分钟。
用于治疗非小细胞肺癌和食管癌时的患者选择
对于以下患者,应根据其PD-L1阳性表达状态,选择使用帕博利珠单抗单药治疗:
一线局部晚期或转移性非小细胞肺癌,PD-L1表达由国家药品监督管理局批准的检测评估。
二线局部晚期或转移性食管鳞状细胞癌,PD-L1表达经充分验证的检测评估。
推荐剂量
黑色素瘤:2 mg/kg
非小细胞肺癌或食管癌:200 mg固定剂量
帕博利珠单抗联合化疗给药时,应首先给予帕博利珠单抗。另请参见化疗药物联合给药的处方信息。
患者应使用帕博利珠单抗治疗至疾病进展或发生不可接受的毒性。
已观察到接受帕博利珠单抗治疗肿瘤的非典型反应(例如,治疗最初几个月内肿瘤出现暂时增大或出现新的小病灶,随后肿瘤缩小)。
在对KEYNOTE-001中黑色素瘤患者的回顾性分析中,7%的患者发生假性进展,其中大部分(> 60%)患者发生在治疗的前3个月内。
如果患者临床症状稳定,即使有疾病进展的初步证据,但基于总体临床获益的判断,可考虑继续应用本品治疗,直至证实疾病进展。
根据个体患者的安全性和耐受性,可能需要暂停给药或停药。不建议增加或减少剂量。有关免疫相关性不良反应管理的详细指南,请参见【注意事项】。
【禁忌症】
对本说明书【成份】项下的活性成份和辅料过敏者禁用。
【注意事项】
免疫相关不良反应
接受帕博利珠单抗治疗的患者中发生过免疫相关不良反应,包括重度和死亡病例。帕博利珠单抗治疗期间发生的大多数免疫相关不良反应是可逆的,并且可通过中断帕博利珠单抗、皮质类固醇治疗和/或支持治疗来处理。帕博利珠单抗末次给药后也会发生免疫相关不良反应。免疫相关不良反应可同时发生在多个器官系统。
对于疑似免疫相关不良反应,应进行充分的评估以确定病因或排除其他病因。根据不良反应的严重程度,应暂时停用帕博利珠单抗,并应用皮质类固醇治疗。当免疫相关的不良反应改善至≤1级时,需至少一个月的时间逐步减少皮质类固醇的用量直至停药。基于有限的临床研究数据,发生皮质类固醇无法控制的免疫相关不良反应时可以考虑使用其他全身性免疫抑制剂。
如果不良反应保持在≤1级,且皮质类固醇剂量已降至每天≤10mg泼尼松或等效剂量,则可在最后一次帕博利珠单抗给药后12周内重新开始帕博利珠单抗治疗。
除了可用激素替代疗法控制的内分泌疾病外(参见【用法用量】项下剂量调整部分和【不良反应】),对于任何复发性3级免疫相关不良反应以及任何4级免疫相关不良反应,应永久停用帕博利珠单抗。
免疫相关性肺炎
接受帕博利珠单抗治疗的患者中有肺炎报告(参见【不良反应】)。应对患者肺炎的相关体征和症状进行监测。疑似肺炎的病例应采用影像学检查进行确认并排除其他可能病因。
对于≥2级肺炎患者应给予皮质类固醇治疗(初始剂量为1-2 mg/kg/天泼尼松或等效剂量,之后逐渐减少剂量)。出现2级肺炎的患者暂停使用帕博利珠单抗,出现3级、4级或复发性2级肺炎的患者应永久停用帕博利珠单抗(参见【用法用量】)。
免疫相关性结肠炎
在接受帕博利珠单抗治疗的患者中有结肠炎报告(参见【不良反应】)。应对患者结肠炎的相关体征和症状进行监测,并排除其他可能病因。对于≥2级结肠炎给予皮质类固醇(初始剂量为1-2 mg/kg/天泼尼松或等效剂量,之后逐渐减少剂量),发生2级或3级结肠炎的患者应暂停使用帕博利珠单抗,发生4级结肠炎的患者应永久停用帕博利珠单抗(参见【用法用量】)。应考虑胃肠穿孔的潜在风险。
免疫相关性肝炎
在接受帕博利珠单抗治疗的患者中有肝炎报告(参见【不良反应】)。应监测患者的肝功能变化[治疗开始时、治疗期间(定期)以及基于临床评估具有指征时]和肝炎症状,排除其它病因。给予皮质类固醇治疗[初始剂量为0.5-1 mg/kg/天(针对2级肝炎)和1-2 mg/kg/天(针对≥3级肝炎)泼尼松或等效剂量,之后逐渐减少剂量],并根据肝酶升高的严重程度决定是暂时停药还是永久停药(参见【用法用量】)。
免疫相关性肾炎
在接受帕博利珠单抗治疗的患者中有肾炎报告(参见【不良反应】)。应监测患者的肾功能变化,排除肾功能损伤的其他病因。对于≥2级肾炎给予皮质类固醇(初始剂量为1-2 mg/kg/天泼尼松或等效剂量,之后逐渐减少剂量)。根据肌酐升高的严重程度,2级肾炎患者应暂停使用帕博利珠单抗,3级或4级肾炎患者应永久停用帕博利珠单抗(参见【用法用量】)。
免疫相关性内分泌疾病
帕博利珠单抗治疗可发生重度内分泌疾病,包括肾上腺功能不全、垂体炎、1型糖尿病、糖尿病酮症酸中毒、甲状腺功能减退症和甲状腺功能亢进。发生免疫相关内分泌疾病时,可能需要长期使用激素替代治疗。
免疫相关性皮肤不良反应
在接受帕博利珠单抗治疗的患者中有免疫相关重度皮肤不良反应报告(参见【不良反应】)。应监测患者的重度皮肤不良反应,并应排除其他病因。根据不良反应的严重程度,暂停或永久停用帕博利珠单抗,并应给予皮质类固醇(参见【用法用量】)。
接受帕博利珠单抗治疗的患者中报告了SJS或TEN(参见【不良反应】)。对于SJS或TEN体征或症状,应暂停使用帕博利珠单抗,并将患者转诊给专科机构进行评估和治疗。如果患者确诊SJS或TEN,应永久停用帕博利珠单抗(参见【用法用量】)。
对于既往使用其他免疫刺激性抗癌药治疗时发生过严重或危及生命的皮肤不良反应的患者,应谨慎考虑使用帕博利珠单抗。
其他免疫相关性不良反应
在临床试验或上市后使用中报告了以下其他有临床意义的免疫相关不良反应:葡萄膜炎、关节炎、肌炎、心肌炎、胰腺炎、格林巴利(Guillain-Barré)综合征、肌无力综合征、溶血、贫血、结节病和脑炎(参见【用法用量】和【不良反应】)。
应根据不良反应的严重程度,暂停使用帕博利珠单抗,并给予皮质类固醇治疗。如果不良反应保持在≤1级,并且皮质类固醇剂量已降至每天≤10mg泼尼松或相当剂量,则可以在最后一剂帕博利珠单抗给药后12周内重新开始帕博利珠单抗治疗。对于任何复发性3级免疫相关不良反应以及任何4级免疫相关不良反应,必须永久停用帕博利珠单抗治疗。
异基因造血干细胞移植(HSCT)的并发症
异基因HSCT后使用帕博利珠单抗治疗
在既往接受过异基因HSCT的患者中,在使用帕博利珠单抗治疗后有发生急性移植物抗宿主病(GVHD),包括致命性GVHD的报道。移植手术后出现GVHD的患者,在使用帕博利珠单抗治疗后可能会增加GVHD风险。对于进行过异基因HSCT的患者,应考虑帕博利珠单抗治疗的获益与可能的GVHD风险。
多发性骨髓瘤
对于多发性骨髓瘤患者,在沙利度胺类似物和地塞米松的基础上加用帕博利珠单抗治疗后,死亡率增加。
输液相关反应
在接受帕博利珠单抗治疗的患者中有重度的输液相关反应报告,包括超敏和过敏反应(参见【不良反应】)。对于重度的输液反应,必须停止输液并永久停用帕博利珠单抗(参见【用法用量】)。出现轻度或中度输液反应的患者在密切监测下可继续接受帕博利珠单抗治疗;可考虑用解热镇痛类抗炎药和抗组胺药预防。
疾病特异性预防措施
使用帕博利珠单抗一线治疗NSCLC患者
一般而言,帕博利珠单抗联合治疗观察到的不良反应频率高于帕博利珠单抗单药治疗或单独化疗,反映了联合治疗中这些药物各自的作用(参见【用法用量】和【不良反应】)。尚无法直接进行帕博利珠单抗联合化疗与帕博利珠单抗单药治疗的比较。
来自≥75岁患者的有效性和安全性数据有限。对于≥75岁患者,在仔细评估个体潜在的获益/风险后,应谨慎使用帕博利珠单抗联合治疗(参见【临床试验】)。
临床试验排除的患者
在重度肾功能不全和中度至重度肝功能不全患者中信息有限。在仔细考虑潜在增加的风险后,可以对这些患者使用帕博利珠单抗治疗,但需要进行必要的医疗管理。
胚胎毒性
基于其作用机理,在妊娠期间使用本品可能会对胎儿造成伤害。动物模型通过诱导母体对胎儿组织的免疫耐受将PD-1/PD-L1信号传导途径与维持妊娠联系起来。如果在妊娠期间应用了这一药物,应向患者告知对胎儿的潜在危害。建议育龄女性在帕博利珠单抗治疗期间采用高效避孕方法,并在最后一次帕博利珠单抗用药后4个月内持续避孕。
配伍禁忌
在没有进行配伍性研究的情况下,本品不得与其他医药产品混合。本品不应与其它医药产品经相同的静脉通道合并输注。
对驾驶和操作机器能力的影响
帕博利珠单抗可能对驾驶和操作机器的能力有轻微影响。有帕博利珠单抗给药后出现疲劳的报告。
【不良反应】
安全性特征总结
帕博利珠单抗最常发生免疫相关不良反应。其中大部分(包括重度反应)会在给予适当的药物治疗或停用帕博利珠单抗后缓解。
临床研究中,已在6,342例晚期黑色素瘤、已切除的III期黑色素瘤(辅助治疗)、非小细胞肺癌、经典霍奇金淋巴瘤、尿路上皮癌、头颈部鳞状细胞癌或食管癌患者中评价了帕博利珠单抗4个剂量(2 mg/kg每3周一次,200 mg每3周一次,或10 mg/kg每2周1次或每3周一次)单药治疗的安全性。下文及表2中所列的不良反应的发生频率是基于所有报告的药物不良反应,由申办方评估,不论研究者判断其是否与研究药物相关。该患者群体中,中位观察时间为7.1个月(范围:1天至37个月)。最常见的帕博利珠单抗不良反应是:疲劳(31.2%)和恶心(20.3%)。单药治疗所报告的大多数不良反应的严重程度为1级或2级。最严重的不良反应为免疫相关不良反应和重度输液相关反应(参见【注意事项】)。
在临床研究中,已在791例每3周接受200mg、2 mg/kg或10 mg/kg 帕博利珠单抗的NSCLC患者中评价了帕博利珠单抗联合化疗的安全性。下文以及表所列的联合治疗中不良反应的发生率是基于所有报告的药物不良反应确定的,与研究者评估的因果关系无关。在该患者人群中,最常见的不良反应是恶心(49%)、贫血(48%),疲劳(38%)、便秘(34%)、腹泻(31%)、中性粒细胞减少症(29%)和食欲减退(28%)。帕博利珠单抗联合治疗的3-5级不良反应发生率为67%,单独化疗的3-5级不良反应发生率为66%。
不良反应汇总表
下表列出了帕博利珠单抗在临床研究中以单药治疗或与化疗联合治疗中观察到的或上市后使用报告的不良反应。已知的单独使用帕博利珠单抗或化学疗法发生的不良反应可能在这些药物联合治疗期间发生,即使这些反应未在联合治疗的临床试验中报道。按照系统器官分类和发生频率列出这些反应。发生频率定义如下:十分常见(≥1/10),常见(≥ 1/100至< 1/10),偶见(≥ 1/1,000至< 1/100),罕见(≥ 1/10,000至< 1/1,000),十分罕见(< 1/10,000),以及未知(无法从已获得的数据估算发生频率)。每个发生频率分组内,不良反应按严重程度从高到低依次排列。
表 用帕博利珠单抗治疗的患者的不良反应



其他不良反应请参阅完整产品说明书
中国患者临床试验经验
已在临床研究(KEYNOTE-151、KEYNOTE-032、KEYNOTE-042和KEYNOTE-181)中,共计335例黑色素瘤、非小细胞肺癌或食管癌中国患者中评价了帕博利珠单抗3个剂量(2 mg/kg每3周一次,200 mg每3周一次,或10 mg/kg每3周一次)单药治疗的安全性。中国患者的总体安全性特征与全球人群一致,报告不良反应发生率与全球人群相似,中国人群中未发现新的安全性问题。单药治疗所报告的大多数不良反应的严重程度为1级或2级。最严重的不良反应为免疫相关不良反应和重度输液相关反应(参见【注意事项】)。
KEYNOTE-407研究中,在65例转移性鳞状非小细胞肺癌中国患者中,评价了帕博利珠单抗200mg联合卡铂和紫杉醇的安全性。总体上,帕博利珠单抗联合卡铂/紫杉醇治疗中国患者的安全性与已知的卡铂/紫杉醇的安全性和帕博利珠单抗单药治疗的安全性基本一致,同时也与全球患者人群中观察到的安全性总体一致。未发现新的安全性问题。
联合用药最常报告的不良事件通常与化疗相关。并且,免疫介导的不良事件的发生率与帕博利珠单抗单药治疗肺癌患者的发生率基本一致;这些不良事件的发生率并未因帕博利珠单抗联合化疗而增加。
【药物相互作用】
帕博利珠单抗尚未进行正式药代动力学药物相互作用研究。由于帕博利珠单抗通过分解代谢从血液循环中清除,预计不会发生代谢性药物-药物相互作用。
在使用本品之前应避免使用全身性皮质类固醇或免疫抑制剂,因为这些药物可能会影响本品的药效学活性及疗效。但在本品开始给药后,可使用全身性皮质类固醇或其他免疫制剂治疗免疫介导性不良反应(参见【注意事项】)。
【特殊人群】
育龄期妇女: 育龄妇女在接受帕博利珠单抗治疗期间,以及最后一次帕博利珠单抗给药后至少4个月内应采取有效避孕措施。
妊娠期: 尚无孕妇使用帕博利珠单抗的相关信息。通过保持母体对胎仔的免疫耐受来维持妊娠是PD-1/PD-L1通路的主要功能之一。阻断妊娠啮齿类动物模型的PD-L1信号通路可破坏母体对胎仔的耐受性,导致胎仔丢失增加。妊娠期间给予帕博利珠单抗有潜在的风险,包括流产或死胎的比例增加。已知人免疫球蛋白G4(IgG4)能够穿过胎盘屏障;因此,作为一种IgG4,帕博利珠单抗可能从母体传播给发育中的胎儿。除非孕妇的临床疾病需要使用帕博利珠单抗进行治疗,妊娠期间不得使用帕博利珠单抗。
哺乳期: 尚不清楚本品是否在人乳汁分泌。由于许多抗体可在人乳汁中分泌,不能排除本品对新生儿/婴儿的风险。应权衡哺乳对胎儿的获益以及本品治疗对女性患者的获益,再决定是停止哺乳,还是停止帕博利珠单抗治疗。
生育力:尚无关于帕博利珠单抗对于生育力潜在影响的临床数据。
儿童患者: 帕博利珠单抗在儿童患者(<18岁)中的安全性和有效性尚不明确。
老年患者: 老年(≥65岁)与年轻患者(<65岁)在安全性或有效性上未出现总体的差异。无需在这一人群中进行剂量调整。
肾功能不全: 轻度或中度肾功能不全患者无需剂量调整。帕博利珠单抗尚未在重度肾功能不全患者中进行研究(参见【注意事项】和【药代动力学】)。
肝功能不全: 轻度肝功能受损患者无需剂量调整。帕博利珠单抗尚未在中度或重度肝功能不全患者中进行研究(参见【注意事项】和【药代动力学】)。
其他特殊人群: 在群体药代动力学分析中评估了各种协变量对帕博利珠单抗药代动力学的影响。以下因素对于帕博利珠单抗的清除无临床重要影响:年龄(范围15-94岁)、性别、种族、轻度或中度肾功能受损、轻度肝功能受损和肿瘤负荷。体重和清除率的关系支持按体重给药和固定剂量给药均会导致适当且相似的暴露量。
处方前请参考完整版说明书
*本资料仅供医疗卫生专业人士作学术参考,而非针对一般公众,亦非广告用途。医疗卫生专业人士作出的任何与治疗有关的决定应根据患者的具体情况并应参照国家药品监督管理局批准的药品说明书。
*资料仅代表个人观点,仅作学术交流之用,请勿分发或转发
*本文由默沙东提供支持
*内审编号:08-2021-CN-LAM-00075
[i] Checkmate-153(ClinicalTrials.gov,NCT2066636)是一项Ⅲb/Ⅳ期在美国和加拿大社区开展的旨在评估纳武利尤单抗用于经治晚期NSCLC的治疗的安全性。研究入组了1426例(556例年龄在70岁或以上;128例为ECOG PS评分2分)至少接受过一种系统治疗的晚期非小细胞肺癌患者。患者接受3 mg/kg纳武利尤单抗剂量,每2周接受一次,直至毒性不可耐受,疾病进展,或患者要求退出。主要研究终点是3~5级治疗相关的不良反应。
[ii] KEYNOTE-001(ClinicalTrials.gov,NCT01295827)是一项Ib期的多中心、开放标签、多队列研究,评估帕博利珠单抗用于多种晚期癌症,其中包括了550例初治或经治晚期非小细胞肺癌患者。患者以2 mg/kg或10 mg/kg剂量每3周接受一次帕博利珠单抗剂量,或者以10 mg/kg 剂量每2周接受一次帕博利珠单抗,直至毒性不可耐受或疾病进展。主要研究终点是 ORR,次要终点包括 PFS、OS 和 DOR。
[1] Rodriguez-Abreu D et al., Final analysis of KEYNOTE-189: Pemetrexed-platinum chemotherapy (chemo) with or without pembrolizumab (pembro) in patients (pts) with previously untreated metastatic nonsquamous non-small cell lung cancer (NSCLC). 2020 ASCO, Abstract #9582
[2] Ghandi L et al., Pembrolizumab plus Chemotherapy in Metastatic Non–Small-Cell Lung Cancer, N Engl J Med 2018;378:2078-92.
[3] Shirish M. Gadgeel, et al. KEYNOTE-189: Updated OS and progression after the next line of therapy (PFS2) with pembrolizumab (pembro) plus chemo with pemetrexed and platinum vs placebo plus chemo for metastatic nonsquamous NSCLC. 2019 ASCO, Abstract #9013.
[4] David R Spigel et al., Safety, Efficacy, and Patient-Reported Health-Related Quality of Life and Symptom Burden with Nivolumab in Patients with Advanced Non-Small Cell Lung Cancer, Including Patients Aged 70 Years or Older or with Poor Performance Status (CheckMate 153), J Thorac Oncol 2019 Sep;14(9):1633
[5] 中国临床肿瘤学会,《CSCO非小细胞肺癌诊疗指南(2020)》
[6] Garon E.B., Five-Year Overall Survival for Patients With Advanced Non-Small-Cell Llung Cancer Treated With Pembrolizumab: Results From the Phase I KEYNOTE-001 Study. JCO.com, June 2nd, 2019
排版编辑:DD











 苏公网安备32059002004080号
苏公网安备32059002004080号


