PD-1免疫检查点抑制剂帕博利珠单抗于2019年在国内获批的三个(单药或联合化疗)一线治疗EGFR/ALK野生型转移性鳞状和/或非鳞非小细胞肺癌(NSCLC)的适应证,使免疫治疗成为此部分人群一线治疗的“中流砥柱”,也必将改变我国晚期NSCLC治疗的临床实践。然而免疫治疗的浪潮并未止步于晚期肺癌。
KEYNOTE-799研究结果公布:PD-1联合同步放化疗初显威力
在2020年美国临床肿瘤学会(ASCO)的在线科学大会上,帕博利珠单抗联合同步放化疗(CCRT)治疗不可切除的Ⅲ期(ⅢA-ⅢC)非小细胞肺癌的Ⅱ期临床研究KEYNOTE-799结果公布。该研究包含了两个队列: 队列A(112例)入组了鳞状或非鳞状NSCLC患者,并接受卡铂和紫杉醇的联合化疗方案;而队列B(73例)仅入组了非鳞NSCLC患者,并接受培美曲塞联合顺铂的化疗方案。

图1、KEYNOTE-799研究设计[1]
结果显示,经过至少15周的随访,帕博利珠单抗联合CCRT在队列A和队列B(53例)的客观缓解率(ORR)分别为67.0%(90%CI,58.9-74.3)和56.6%(90%CI,44.4-68.2),完全缓解(CR)率分别为2.7%和3.8%。
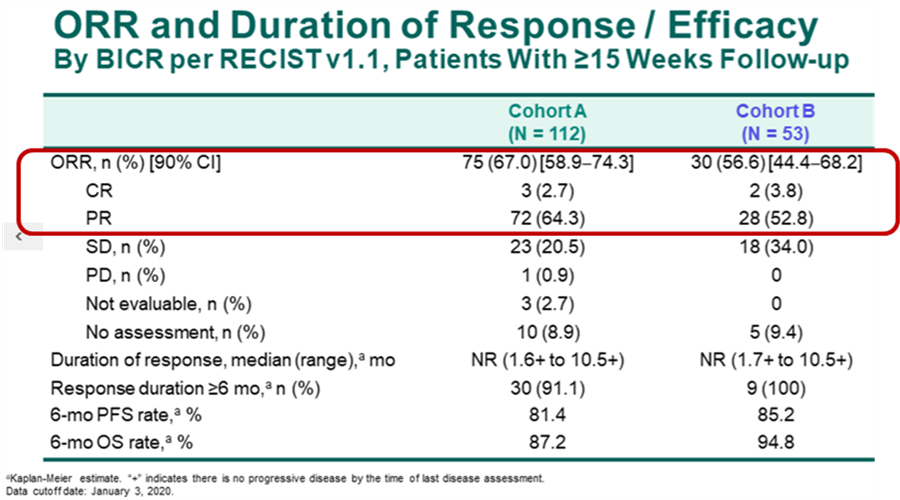
图2、KEYNOTE-799研究中两个队列的ORR和DoR [1]
免疫作为CCRT之后的巩固治疗
免疫联合放射治疗一直被认为会产生协同作用。从机理上来讲,放射治疗后会促进肿瘤特异性抗原的释放,免疫抑制剂的药物也更容易识别这些抗原,起到更好的疗效;另外,放疗会造成肿瘤微环境的改变,减少其中的免疫抑制因素,使“冷肿瘤”变成“热肿瘤”,从而提高免疫治疗疗效。
2017年和2018年《新英格兰医学杂志》两次发表了Ⅲ期临床研究PACIFIC的研究结果[1、2]首次为免疫联合放化疗带来了高级别循证医学证据。PACIFIC研究验证了在根治性CCRT后未出现进展的Ⅲ期不可切除NSCLC,PD-L1免疫检查点抑制剂度伐利尤单抗用于巩固治疗可带来显著的无进展生存期(PFS)和总生存期(OS)获益。
免疫巩固治疗组和对照组的各项终点指标对比如下[3]:
中位PFS分别为17.2个月 vs 5.6个月(HR 0.51;95%CI 0.41-0.63);
12个月和18个月的PFS率,两组分别为55.7% vs 34.4%和49.5% vs 26.7%;
中位OS分别为NR和28.7个月(HR 0.68;95%CI:0.469-0.997;P=0.00251);
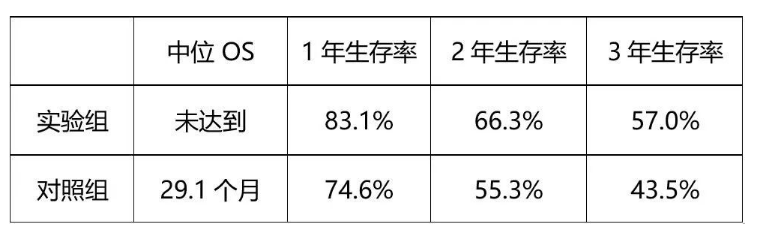
12个月和24个月的OS率,两组分别为83.1% vs 75.3%和66.3% vs 55.6%。
在2019年ASCO年会上,PACIFIC研究3年随访结果公布, 并于Journal of Thoracic Oncology正式发表。结果显示,免疫巩固治疗组的中位OS仍未达到,3年总生存率为57.0%。
表1、PACIFIC研究的3年随访OS数据[4]
另外一项针对PD-1单抗的,研究设计非常类似PACIFIC的Ⅱ期研究也获得了阳性结果。
LUN14-179是由美国Hoosier癌症研究网络协作组自发开展的关于帕博利珠单抗治疗Ⅲ期不可切除NSCLC的Ⅱ期单臂临床研究。研究入组了在完成紫杉醇卡铂、依托泊苷顺铂或培美曲塞顺铂联合59-66.6Gy的同步放化疗后未进展(包括SD、PR、CR)的患者,4-8周后接受帕博利珠单抗(200 mg,I.V,q3w)治疗直至12个月[7]。主要研究终点为至疾病转移或死亡的时间。次要研究终点包括PFS、OS和毒性。
2018年ASCO年会上首次公布的研究结果显示,无论是中位TDDM(至出现转移或死亡事件的时间)、PFS,还是12个月及18个月的无疾病进展率,与PACIFIC研究中的治疗结果都非常相似。
在2018年的世界肺癌大会(WCLC)上,LUN 14-179研究也进一步更新了数据,中位随访时间18.6个月,并纳入了总生存数据。
表2、LUN14-179研究和PACIFIC研究数据汇总

免疫同步放化疗的安全性
在PACIFIC或LUN14-179研究中, 免疫治疗分别在根治性CCRT结束后的1-42天和28-56后开始,其中的一个重要原因是为了规避放射性肺炎和免疫性肺炎叠加所带来的5级以上的治疗相关性肺炎。
另外一项研究纳武利尤单抗联合CCRT治疗ⅢA/ⅢB期NSCLC的Ⅱ期临床研究(ETOP NICOLAS)以放疗后6个月内观察到的3级或3级以上肺炎事件发生率为研究主要终点。该研究入组82例患者,中位随访13.4个月的结果显示,联合治疗最常见的不良事件是贫血、疲劳和肺炎,但未观察到预料之外的不良事件或毒性增加现象。前21例完成放化疗治疗后患者在3个月的随访结束时未观察到≥3级肺炎[5]。
PACIFIC研究的亚组分析显示,在同步化疗后的14天之内开始免疫治疗的患者相比在14-42之后开始免疫治疗的患者,能获得更显著的OS获益[4]。
表3、PACIFIC研究中显示免疫治疗越早开始OS获益越大[4]

免疫治疗能否与放化疗同步开始以取得最大的疗效,而同时又把免疫联合放化疗的不良反应控制在可接受范围内?
KEYNOTE-799研究的主要终点是每个队列的3级或3级以上肺炎发生率小于或等于10%,而结果显示:
队列A中的9例患者(8.0%; 90%CI, 4.3%–13.6%)出现3级以上肺炎,包括4例5级治疗相关的肺炎;
队列B有4例 (5.5%; 90%CI, 1.9%–12.1%),没有5级治疗相关的肺炎;
队列A和队列B分别有72例(64.3%)和30例(41.1%)出现3级以上治疗相关的不良反应。因此,研究者认为所观察到的不良反应与CCRT和免疫单药治疗的毒副作用一致,3级以上肺炎的发生率在预期之中[1]。

图4、KEYNOTE-799研究中队列A和队列B的不良反应[1]
基于KEYNOTE-799研究令人鼓舞的ORR结果, KEYLYNK-012的3期临床研究(NCT04380636)已启动[6], 评估不可切除的Ⅲ期NSCLC患者在经过帕博利珠单抗联合CCRT治疗后,以帕博利珠单抗(治疗组A)或帕博利珠单抗联合PARP抑制剂奥拉帕利(治疗组B)作为维持治疗的疗效和安全性, 并对比同步放化疗后以度伐利尤单抗为巩固治疗(对照组C)的疗效和安全性。
研究假设为治疗组A和B的OS和PFS要显著优于对照组C,即免疫联合放化疗,并以免疫或免疫联合PARP抑制剂为巩固治疗的模式要优于PACIFIC研究建立的不可切除的Ⅲ期NSCLC的标准模式。
[1] Jabbour SK,et al.Phase Ⅱ study of pembrolizumab (pembro) plus platinum doublet chemo- therapy and radiotherapy as first-line therapy for unresectable,locally advanced stage Ⅲ NSCLC:KEYNOTE-799.2020 ASCO,Abstract #9008.
[2] Antonia SJ,et al.Durvalumab after Chemoradiotherapy in Stage Ⅲ Non–Small-Cell Lung Cancer.N Engl J Med,2017;377:1919-29.
[3] Antonia SJ,et al.Overall Survival with Durvalumab after Chemoradiotherapy in Stage Ⅲ NSCLC.N Engl J Med,2018;379:2342-2350.
[4] Gray JE,et al.Three-year Overall Survival with Durvalumab after Chemoradiotherpay in Stage Ⅲ NSCLC—Update from PACIFIC.Journal of Thoracic Oncology,2020,15(2):288-293.
[5] Peters S,et al.Safety evaluation of nivolumab added concurrently to radiotherapy in a standard first line chemo-RT regimen in unresectable locally advanced NSCLC:The ETOP NICOLAS phase Ⅱ trial.Lung Cancer,2019,133:83-87.
[6] www.clinicaltrials.gov
[7] Durm G et al., Consolidation Pembrolizumab Following CCRT for Unresectable Stage III NSCLC: LUN14-179, 2018 WCLC Abstract
排版编辑:DD











 苏公网安备32059002004080号
苏公网安备32059002004080号


