2020年5月29日,肿瘤界年度盛会美国临床肿瘤学会(ASCO)年会大幕开启,受新冠疫情影响,本届年会首次以线上形式开展。随着精准医疗时代的到来,基因检测使得乳腺癌的诊疗过程更加精细化与个体化。本次ASCO年会上公布了多项FoundationOne®CDx 基因检测用于筛选免疫治疗获益人群,发现潜在治疗靶点和耐药机制的研究,卓显了规范而全面的基因检测在乳腺癌治疗中的重要意义。【肿瘤资讯】特邀复旦大学附属肿瘤医院张剑教授带来精彩解析与点评。

复旦大学附属肿瘤医院肿瘤内科 行政副主任
复旦大学附属肿瘤医院一期临床研究中心 医疗主任
上海市“医苑新星”杰青人才获得者
上海市肿瘤化疗质控中心秘书
中国抗癌协会乳腺癌专业委员会委员
CSCO乳腺癌专家委员会委员
CSCO肿瘤支持与康复治疗专家委员会常务委员
CSCO青年专家委员会委员
中国研究型医院协会乳腺专业委员会青委会副主任委员
国家抗肿瘤药物临床应用监测青年专家委员会副主任委员
乳腺癌整合防治全国专家委员会青委会副主任委员
上海市抗癌协会肿瘤药学专业委员会副主任委员
国家食品药品监督管理总局CDE首批化药临床兼职审评员
JCO中文版(泌尿男生殖系统肿瘤专刊)编委
通过FoundationOne®CDx测算的TMB筛选IO获益人群,推进TNBC免疫治疗
【摘要1013】Association of tumor mutational burden (TMB) and clinical outcomes with pembrolizumab (pembro) versus chemotherapy (chemo) in patients with metastatic triple-negative breast cancer (mTNBC) from KEYNOTE 119
KEYNOTE-119是一项对比帕博利珠单抗和单药化疗二、三线治疗转移性三阴性乳腺癌(mTNBC)的随机Ⅲ期研究。之前公布的KEYNOTE-119研究结果显示,两组的总生存(OS)无显著差异,但PD-L1表达越高,帕博利珠单抗的治疗效果越好。研究者又进一步对另一个肿瘤免疫治疗生物标志物——肿瘤突变负荷(TMB)与疗效的关系进行了探索性分析。
601例mTNBC患者按1:1比例随机接受帕博利珠单抗200mg Q3W或卡培他滨、艾立布林、吉西他滨或长春瑞滨中任一种药物化疗。使用FoundationOne®CDx测算TMB。TMB阈值为10 muts/Mb。
253/601例患者(42.1%)的TMB数据可用(两组分别是132例和121例)。结果显示,帕博利珠单抗治疗组中,TMB和客观缓解率(ORR)及OS具有相关性,而化疗组中TMB和结局不相关。TMB≥10 muts/Mb的患者中,帕博利珠单抗疗效优于化疗,两组的ORR分别是14.3%和8.3%,OS风险比(HR)为0.58;而TMB<10 muts/Mb的患者中,两组疗效类似,ORR分别为12.7%和12.8%,OS HR 0.81。所有患者中有26例(约10%)为TMB≥10 muts/Mb。
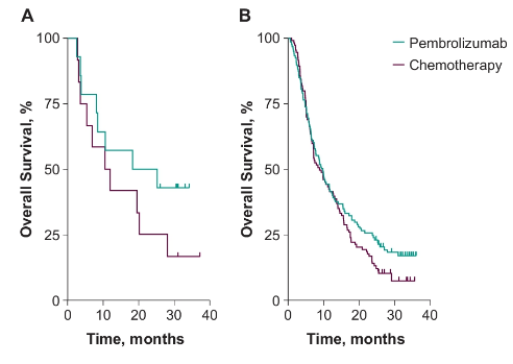
图1. TMB≥10 muts/Mb和TMB<10 muts/Mb的患者中帕博利珠单抗组与化疗组的OS
表2.TMB亚组和临床疗效的关系
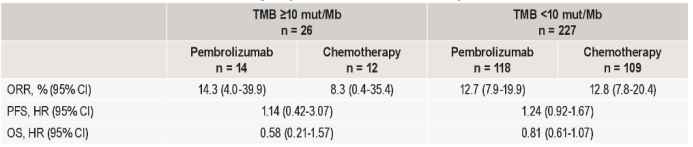
因此,对于mTNBC患者来说,TMB的检测至关重要。TMB和帕博利珠单抗的临床获益之间具有潜在的正相关性。对于TMB≥10 muts/Mb的患者来说,帕博利珠单抗比化疗具有ORR和OS获益增加趋势,可能是更好的二、三线治疗选择。
破译抗细胞周期药物耐药机制,FoundationOne®CDx发掘获得性耐药基因
【摘要1053】Acquired RB1 mutations in estrogen receptor-positive (ER+) clinically advanced and metastatic breast cancer (MBC)
近来发现雌激素受体阳性转移性乳腺癌(ER+ MBC)患者在使用哌柏西利等细胞周期抑制剂药物后出现了RB1基因突变,因此,研究者将未经治疗与治疗后的ER+ MBC患者的活检组织进行了比较,以确定RB1等在耐药中的作用。
研究共纳入了15例未经治疗的原发性乳腺癌患者(PBx)和36例治疗后转移性乳腺癌患者(MBx),使用FoundationOne®CDx进行杂交捕获NGS分析肿瘤组织的基因组变异。
在MBx(经治转移性乳腺癌)组中,和激素治疗获得性耐药相关的ESR1基因(47% vs 0%)和PIK3CA基因(47% vs 20%)突变频率高于PBx(未经治疗的原发性乳腺癌)组。此外,MBx组的RB1基因突变比PBx组更常见(11% vs 0%)。BRCA1基因改变只见于MBx组。两组的潜在治疗靶点包括ERBB2,FGFR1和NF1基因突变。
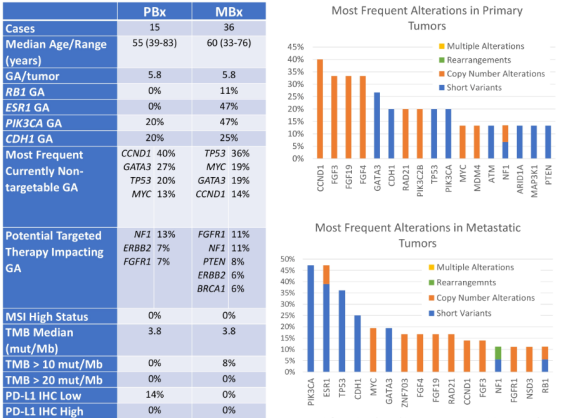
图2. PBx组与MBx组基因突变特点
研究证实了治疗后RB1突变的增加与哌柏西利等抗细胞周期药物暴露相关。
获知亚洲MBC人群基因全景,高效寻找治疗靶点
【摘要3561】Molecular profiling of metastatic breast cancer (MBC) and target-based therapeutic matching in an Asian tertiary phase I oncology unit
MBC体细胞突变图谱可发现潜在治疗靶点,推动相关临床试验。一项研究回顾了115例亚洲MBC患者的NGS检测和治疗结果。
采用Ion Ampliseq Cancer(IAC)V2 扩增子技术(50个基因的panel,43%)或FMI的FoundationOne®CDx(FM1)杂交捕获技术(324个基因的panel,57%)对肿瘤组织进行基因检测,并入组相应的治疗试验。
73例患者接受治疗,其中24/73例(33%)患者根据检测结果进行了靶向治疗,并显示出令人鼓舞的中位无进展生存(mPFS,24周)和临床获益率(PR/CR/SD≥12周,53%)。两个NGS平台的匹配率分别为IAC 28% vs FM1 38%。潜在匹配靶向治疗的突变通路包括PIK3CA/AKT/PTEN(52%)、DNA损伤反应(DRR)(15%)和FGFR(11%)通路。NGS平台比较显示,对比IAC,FM1匹配较未匹配患者改善mPFS(FM1:30 vs 19周,HR = 0.7;IAC:10 vs 11周,HR = 1.2)。
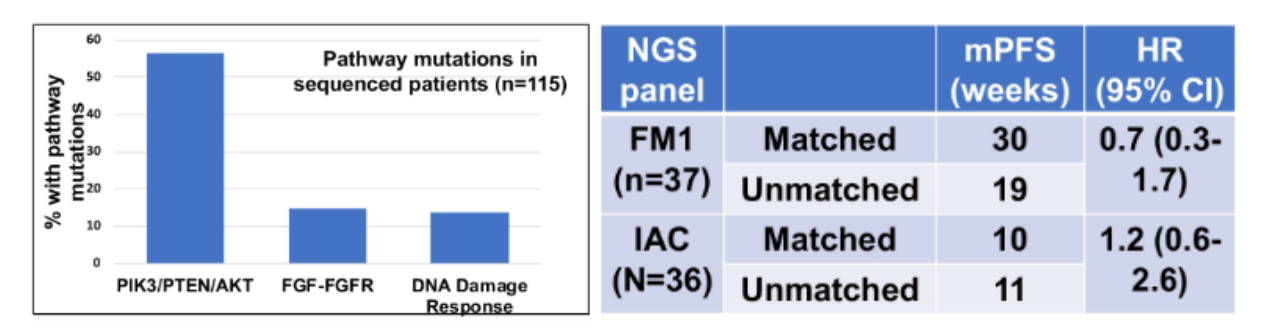
图3.潜在匹配靶向治疗的突变通路(左)和FM1 vs IAC平台的mPFS(右)
研究证实更全面的基因检测(FoundationOne®CDx)为MBC患者带来了更大获益。
今年ASCO年会公布了多项涉及基因检测及疗效评价的研究。KEYNOTE-119是转移性三阴性乳腺癌领域颇受关注的一项随机、对照研究(摘要1013)。既往结果提示,帕博利珠单抗较化疗并未显著改善患者预后,即使是CPS≥1和CPS≥10的患者;但随着CPS评分cutoff值的升高,效应值有增高的趋势。因此研究者进一步分析了TMB与疗效的关系。研究使用FoundationOne®CDx测算TMB,结果提示,帕博利珠单抗组TMB≥10 muts/Mb的患者生存获益明显优于TMB较低的患者,而该差异并未在化疗组中呈现。可见对于基因检测TMB≥10 muts/Mb的患者,使用免疫治疗较化疗具有延长生存获益的趋势,而基因检测对于三阴性乳腺癌的免疫治疗具有一定的提示作用。
众所周知,乳腺癌内分泌治疗无论单药抑或联合靶向治疗均存在耐药性问题,且常为继发性耐药。在摘要1053这项FoundationOne®CDx探索耐药基因的研究中,有以下几个方面值得关注:首先,转移灶组的RB1基因突变增加,达11%,而原发灶组基本为0%,差异较大,提示我们不能忽略在内分泌治疗过程中获得性RB1突变的现象;第二,TMB在两组中的差异不大,但在转移灶组中有8%的患者TMB>10 muts/Mb,结合第一项研究,当TMB≥10 muts/Mb时,可尝试免疫治疗;第三,基因检测有助于发现潜在治疗靶点,如本研究中的ERBB2,FGFR1和NF1基因突变。因此,基因检测,尤其是多基因大Panel在探索精准治疗方向上的作用至关重要。
摘要3561是一项典型的Ⅰ期伞型研究,其中大部分患者接受FoundationOne®CDx检测,少部分接受IAC检测。研究结果显示,通过检测可match相应靶点治疗的患者为33%;而match或unmatch患者的PFS无统计学差异。目前,针对PTEN/PI3K/AKT/mTOR通路靶点的药物越来越多,可通过抑制通路靶点增加治疗疗效,因此应对该通路给予特殊关注;研究中PI3K/PTEN/AKT通路match患者较unmatch患者的PFS绝对值更长,但可能因样本量原因并不具统计学差异。此外,该研究对比了FoundationOne®CDx和IAC对预测患者疗效的作用,结果发现通过FoundationOne®CDx检测人群中,match较unmatch患者获益更大,而通过IAC检测人群中未发现该特点。因此也提示,FoundationOne®CDx可能是作为筛选患者进入合适研究的重要方式。
排版编辑:肿瘤资讯-Frank











 苏公网安备32059002004080号
苏公网安备32059002004080号


