早期乳腺癌的辅助治疗是在根治性手术基础上以治愈为目的的系统治疗。既往,辅助治疗决策多依赖于肿瘤分期、脉管侵犯(LVI)和肿瘤的分子分型等因素。多基因检测(Multigene profiling assays)目前被认为具有辅助临床决策的重要作用,可更有利于平衡辅助治疗所带来的疗效与不利,在避免过度治疗或有害治疗方面具有较好的价值,患者可因此得到生存和生活质量的获益。21世纪初开始至今,多基因检测在早期乳腺癌中应用蓬勃发展,包括21基因(Oncotype Dx®),70基因(Mammaprint®),50基因(PAM50®)等。这些多基因检测均起源于欧美人群,且在中国人群中的多基因检测研究较少,目前国内尚不做常规推荐应用。
乳腺癌复发风险28基因检测(RecurIndex®),自2003年起历经近20年的研究,是当前唯一一个基于亚洲人群肿瘤样本的可用于临床的多基因检测工具,并通过一定规模的临床验证。
从基因模型到基因-临床模型的探索
通过多基因表达谱分析可预测临床预后
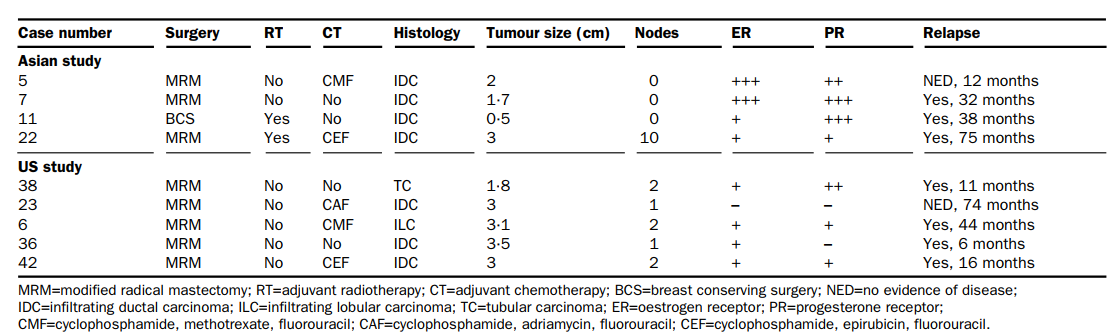
2003年,Cheng带领团队,应用基因芯片技术,分析基因表达与临床相关性。研究者发现,入组的89例华人患者的基因表达与淋巴结转移状态以及临床复发转移存在相关性(图1)。图1显示,37例患者中18例临床高风险(≥10个淋巴结转移),19例临床低风险(淋巴结阴性,年龄>40岁,肿瘤大小<2 cm),结合基因表达分析,发现仅4例患者的临床风险与基因预测不一致(3例临床低危/基因高危, 1例临床高危/基因低危)。结合实际临床结局,这4例患者中有3例最终出现复发转移(表1),而依靠临床信息仅能发现其中1例,而结合基因表达分析则可以找出另外高危的两例患者,提示基因表达分析可以辅助临床信息进一步区分高风险人群。同样的结果也可见于临床复发转移分析,针对其余淋巴结转移1-3个的52例患者(34例未复发,18例复发)进行分析,指出基因表达分析能精准区分出有复发与未复发人群(图2),可以作为乳腺癌患者预后预测的指标。此研究开发了与淋巴结状态和复发相关的基因表达预测模型,90%的预测准确度,为后期开发亚洲人专属基因检测奠定理论基础。
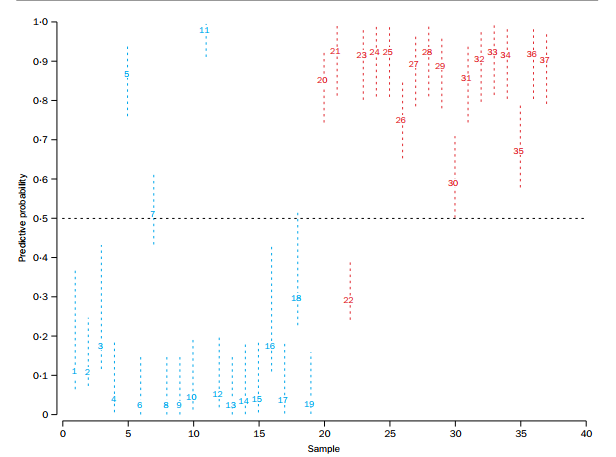
图1. 基因表达与淋巴结转移存在相关性,基因数据以预测概率0.5为阈值。蓝线:临床低风险;红线:临床高风险
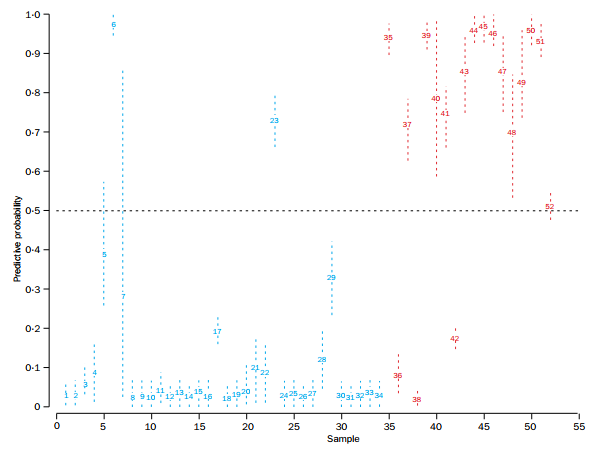
图2.基因表达与3年临床复发转移存在相关性,基因数据以预测概率0.5为阈值。蓝线:未复发;红线:有复发
表 1. 不一致病例的临床资料
初解 基因-临床模型 可预测临床预后
在2004年,研究者首次表明基因表达结合患者临床信息模型的可行性,通过分类树模型,分析基因组与临床信息对复发的影响力,发现除了相关基因组,淋巴结转移状态对预测预后影响也较大,进一步提示基因-临床模型较单独基因表达模型或者临床信息模型更为准确(图3),相关研究成果发表于PNAS。
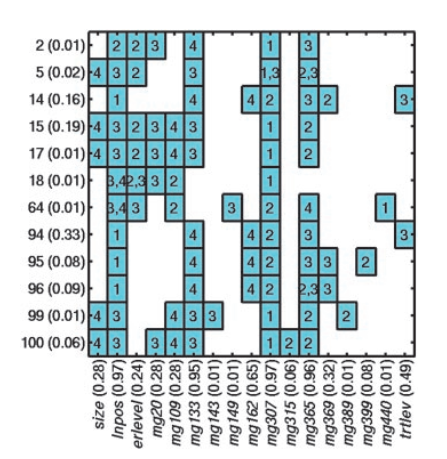
图3. 基因-临床预测模型中的预测变量
精简基因数(258基因-34基因-28基因)
2006年,研究者Cheng等利用94例未做PMRT患者的样本(27 LRR,67 non LRR),对基因模型进一步优化(图4),首先筛选出258基因组(图5),再进一步筛选出最相关的34基因组,可区分出高风险和低风险组(表2)。低风险组的3年局部区域复发(LRR)控制率91%;高风险组的LRR控制率低于40%,检测准确度为75% ~ 78%(图6)。
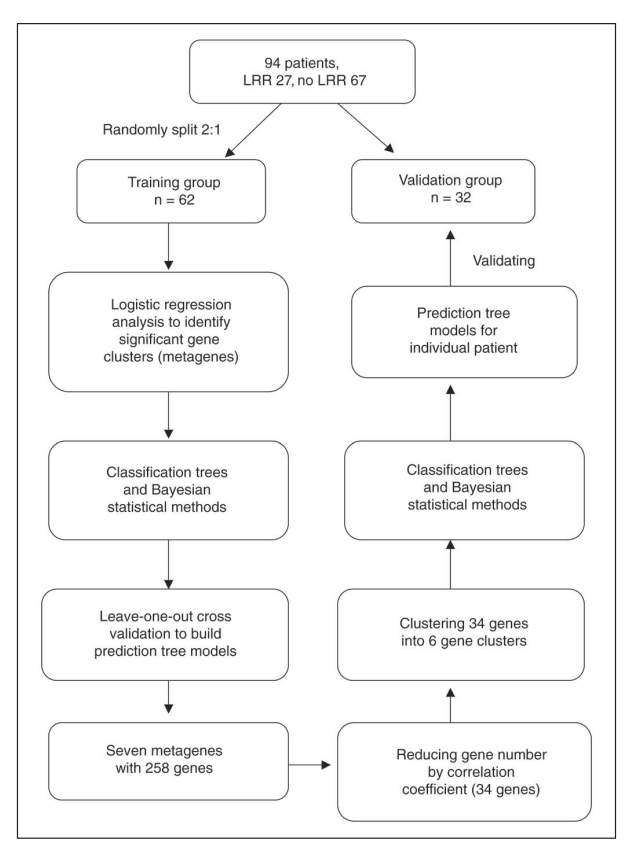
图 4. 研究路线
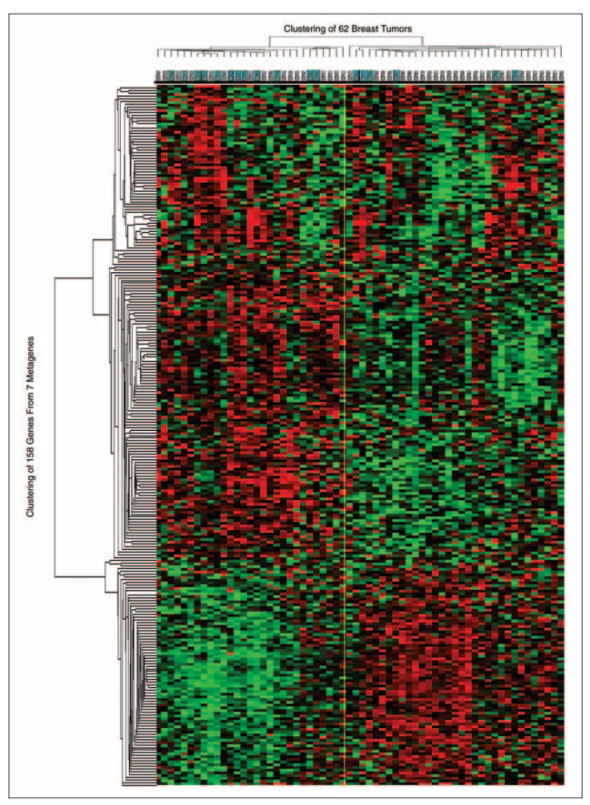
图 5. 258基因在训练组表现(两组分别为局部复发率为41.4%(12/29)和18.2%(6/33)。局部复发患者树状图顶部呈蓝色)
表 2. 258基因对比34基因与3年LR的相关性
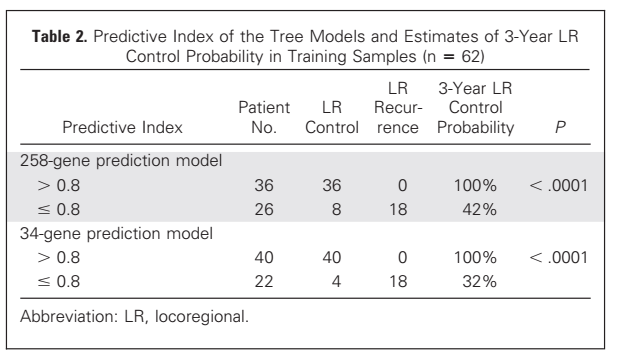
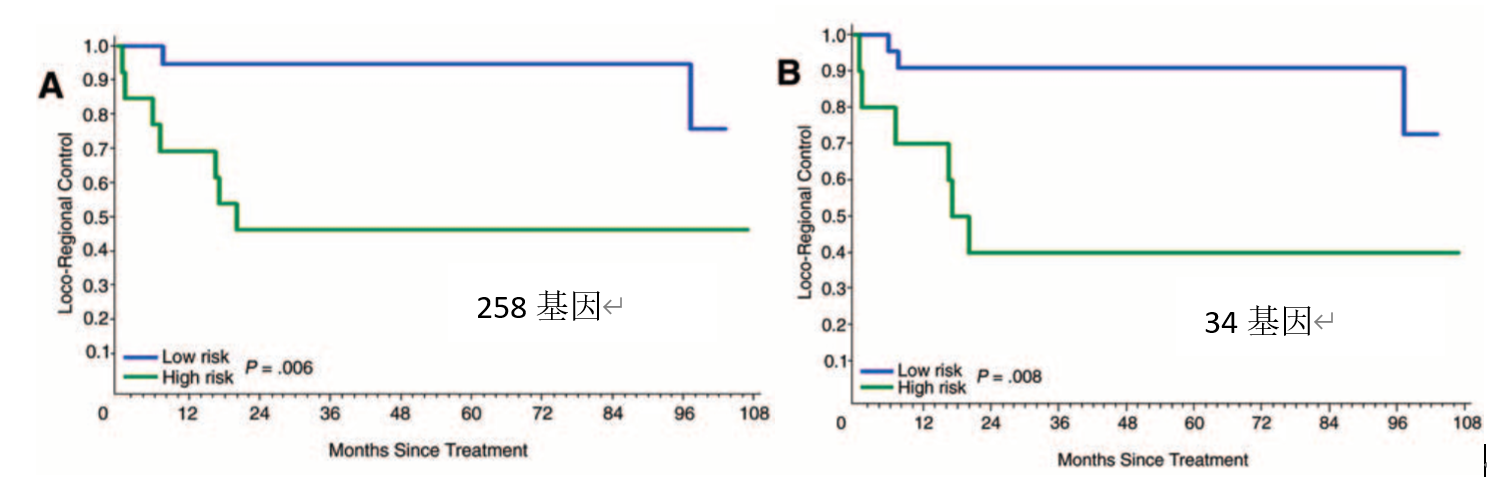
图6. 258基因与34基因区分高低风险
随后34基因组模型在2016年后续的验证中将所需的基因数减少到核心的18个基因(图7),准确率提升至93%,也获得了更好的预测灵敏度和特异性(图8)。该18个核心基因包括BLM, TCF3, PIM1, RCHY1, PTI1, DDX39, BUB1B, STIL, TPX2, CCNB1, MMP15, CCR1, NFATC2IP, TRPV6, OBSL1, C16ORF7, DTX2和ENSA基因。其中RCHY1, PTI1, ENSA和TRPV6与肿瘤生物特性和疾病预后良好有关,而其它14个基因与预后较差有关,且DDX39, BUB1B, STIL, TPX2和CCNB1与调控细胞增殖有关。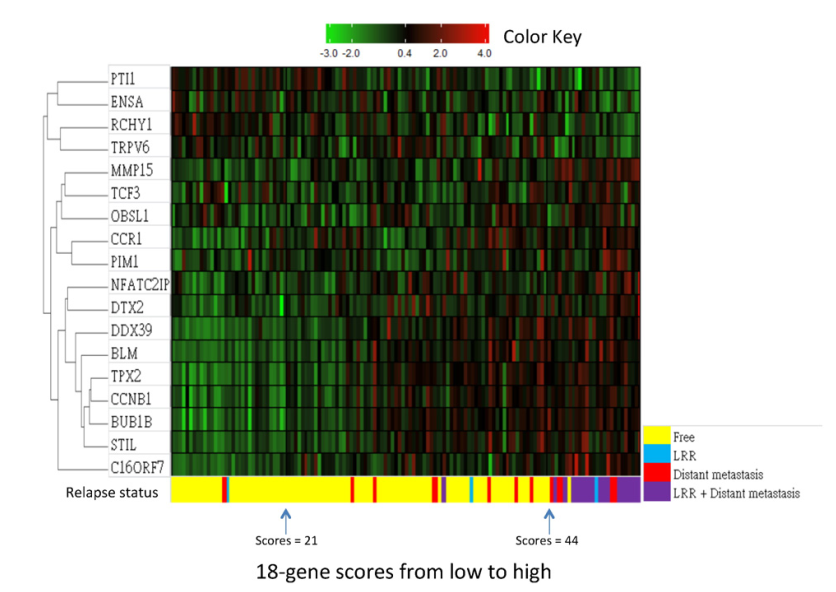
图 7. 核心18基因表达热图分析(135例患者)
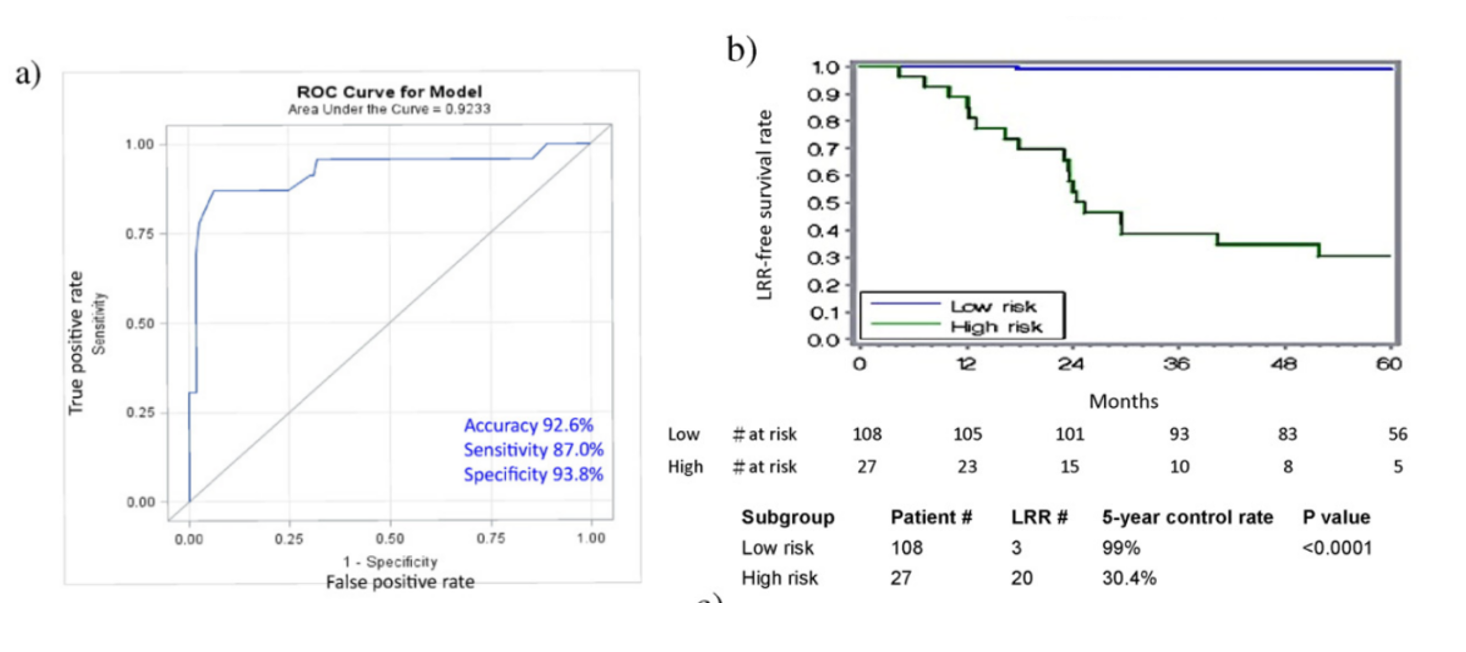
图8. 28基因可以区分局部区域复发高低风险:a. ROC曲线;b.高低风险组别患者的无局部区域复发生存曲线
乳腺癌复发风险28基因检测(RecurIndex®)模型确立
虽然基因表达分析可用于预测乳腺癌患者的临床预后,但是临床病理因素也对预后判断具有不可忽视的作用,且之前已证实,综合运用基因与临床信息,可更准确地区分出高危和低危复发患者。因此2019年在Int J Radiation Oncol Biol Phys上发表可预测局部复发和任意复发的基因-临床模型,LGM-CM4(RI-LR)28个基因结合CM4(年龄、ER状态、脉管癌栓(LVI)和淋巴结分期)模型可以用于预测乳腺癌的局部复发,DGM-CM6(RI-DR)28基因结合CM6(年龄、ER状态、脉管癌栓(LVI)、淋巴结分期、肿瘤大小、肿瘤分级)模型,可用于预测乳腺癌的任何形式复发(图9)。
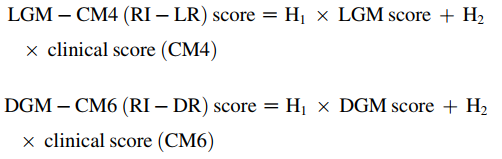
图9.基因-临床模型
本研究中验证了388例T1-3, N1-2浸润性乳腺癌患者,结果显示RI-LR可以很好的区分局部区域复发风险(图10)。低风险组10年LRFI 100%,高风险组10年LRFI 93.0%,有显著差异(P = 0.0146)。
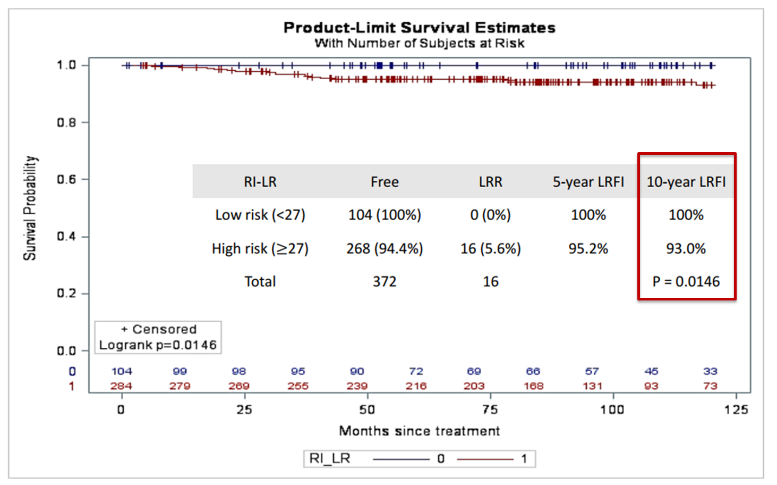
图10. RI-LR 区分局部区域复发风险
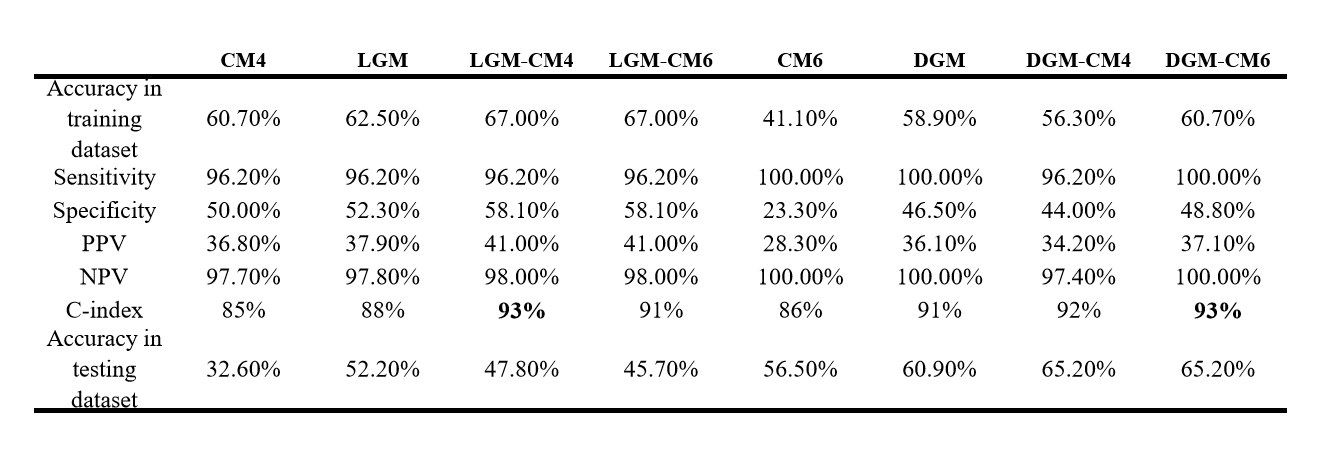
针对不同的模型进行比对分析,结果显示LGM-CM4与DGM-CM6模型(即目前使用的28基因检测)相较于其他单基因表达模型或者单临床信息模型,在复发风险的预测能力上,有最好的一致性指数(concordance index, C-index),并且有更高特异性和敏感性,阴性预测率也达到98%以上(表3)。
表 3. 不同模型比较
28基因从局部区域复发风险预测到远处转移风险预测应用探索
28基因的研发,起源于对局部区域复发风险探索,自2003年起始,分别在Lancet,PNAS,JCO等杂志发表相关研究。28基因检测作为亚洲乳腺癌的预后指标,不仅可以针对预测局部复发,同时也可预测远处转移风险,并进行了研究验证。
在预测远处转移方面,通过683例患者的内部验证和410例外部数据验证。内部验证患者多数为N0与N1期患者(75.3%),65.6%为ER/PR+肿瘤,89.2%的患者接受辅助化疗。28基因可以在不同亚型、不同分期乳腺癌患者中,鉴别5年远处转移风险具有高准确性,整体而言低风险组的5年无远处转移率在96.9%,而高风险组为82.1%(图11)。
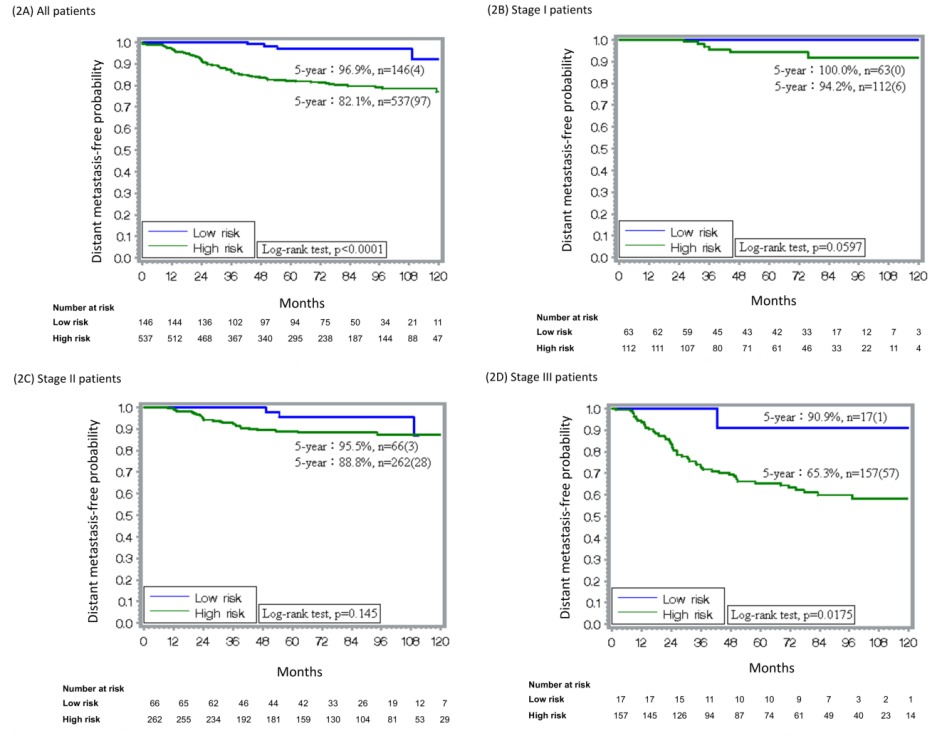
图11. 区分远处转移高低风险
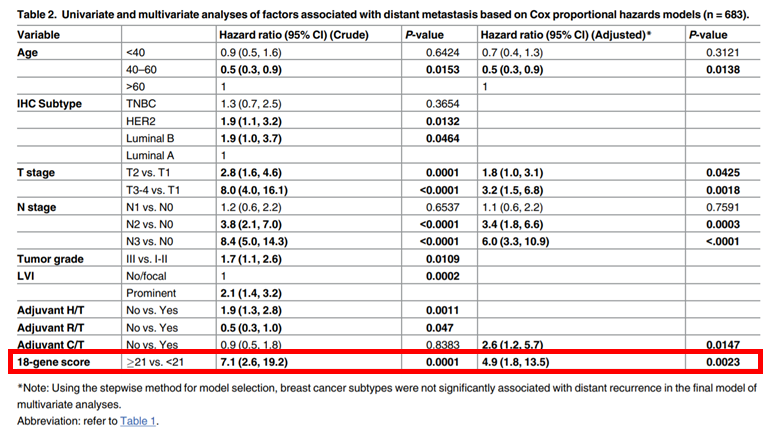
28基因预测远处转移风险的表现,进行单变量分析时,结果显示,相比于低风险组,高风险组有7倍的风险会发生远处转移(HR = 7.1)。加入其他临床因子的多变量分析显示,28基因可以独立预测远处转移风险,相比于低风险组,高风险组有近5倍的风险会远处转移(HR = 4.9)(表4)。
表 4 28基因独立预测远处转移风险
而在410例外部验证患者中,新加坡国家癌症中心提供83例乳腺癌患者样本进行盲测验证(图12)。17例(20.5%)被判断为低风险,五年内仅有1例发生远处转移,5年无远处转移率(DMFP)为94.1%;66例被分为高风险的患者5年无远处转移率(DMFP)为75.5%。乳腺癌基因芯片数据库GEO(GSE20685)的验证中,纳入150例临床为Ⅰ-Ⅱ期、ER/PR+及HER2-的患者。根据28基因结果判定是低风险的67例患者,仅有4例发生远处转移,5年无远处转移率(DMFP)为97.0%。
从内部数据验证到外部数据验证,均证实28基因检测,除了局部区域复发风险以外,还可以预测远处转移风险。
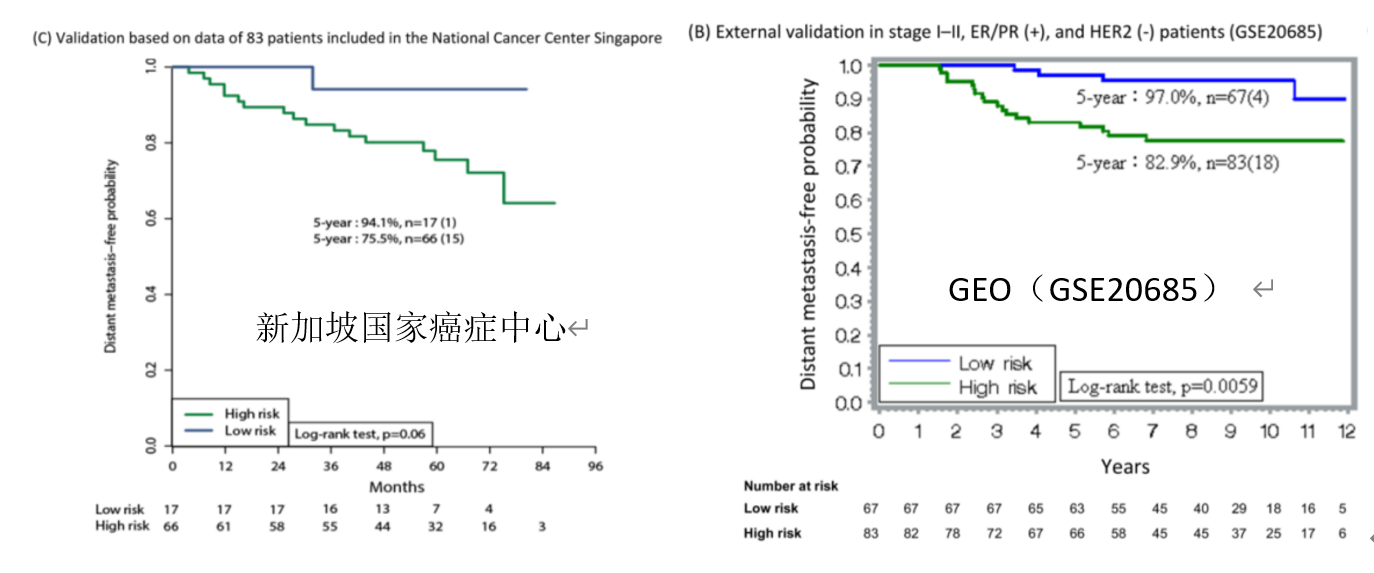
图 12 新加坡国家癌症中心&GEO(GSE20685)验证28基因可预测远处转移风险
总结
自2003年起始,经过近20年的研发,基因筛选自258基因,到28基因;多基因表达分析,到基因联合临床信息表达分析;局部区域复发风险预测,到远处转移风险预测,乳腺癌28基因检测最终通过一定规模验证确立了模型(RI-LR;RI-DR),检测的敏感性分别高达(96.2%,100%),可以帮助乳腺癌患者评估远处转移及局部复发风险,为临床术后辅助化疗及放疗提供参考,实现乳腺癌治疗领域上的个体化诊疗,真实解答临床疑虑。
1. Huang E, Cheng S H, Dressman H, et al. Gene expression predictors of breast cancer outcomes[J]. The Lancet, 2003, 361(9369): 1590-1596.
2. Pittman J, Huang E, Dressman H, et al. Integrated modeling of clinical and gene expression information for personalized prediction of disease outcomes[J]. Proceedings of the National Academy of Sciences, 2004, 101(22): 8431-8436.
3. Cheng S H, Horng C F, Clarke J L, et al. Prognostic index score and clinical prediction model of local regional recurrence after mastectomy in breast cancer patients[J]. International Journal of Radiation Oncology* Biology* Physics, 2006, 64(5): 1401-1409.
4. Cheng S H, Horng C F, West M, et al. Genomic prediction of locoregional recurrence after mastectomy in breast cancer[J]. Journal of Clinical Oncology, 2006, 24(28): 4594-4602.
5. Cheng S H, Horng C F, Huang T T, et al. An eighteen-gene classifier predicts locoregional recurrence in post-mastectomy breast cancer patients[J]. EBioMedicine, 2016, 5: 74-81.
6. Cheng S H C, Huang T T, Cheng Y H, et al. Validation of the 18-gene classifier as a prognostic biomarker of distant metastasis in breast cancer[J]. PloS one, 2017, 12(9).
7. Huang T T, Chen A C H, Lu T P, et al. Clinical-genomic models of node-positive breast cancer: training, testing, and validation[J]. International Journal of Radiation Oncology* Biology* Physics, 2019, 105(3): 637-648.
排版编辑:肿瘤资讯-Cole











 苏公网安备32059002004080号
苏公网安备32059002004080号


