近年来,程序性细胞死亡蛋白1(PD-1)或其配体(PD-L1)检查点抑制剂已改变了非小细胞肺癌(NSCLC)的治疗全景。ASCO、ESMO等国际会议上将免疫治疗列为会议的重要议题,NCCN指南中也已经明确了PD-L1检测对免疫治疗药物的价值,这些均充分表明PD-L1检测是当前预测免疫治疗疗效的一个重要生物标志物。尽管PD-L1表达在免疫治疗中起着重要作用,但其表达相关影响因素尚不清楚。随着NGS等基因检测技术的发展,对PD-L1表达相关因子的深入研究有助于阐明免疫治疗的原发反应或抵抗机制。【肿瘤资讯】有幸邀请到河北医科大学第四医院的刘月平教授,带来两篇基于NGS检测探索NSCLC中PD-L1表达相关的临床病理和基因组因素的文献分享,现整理如下,以飨读者。

河北医科大学第四医院暨河北省肿瘤医院病理科及病理教研室主任 学术带头人
中华医学会病理学分会青年委员会副主任委员
中国医师协会病理科医师分会青年委员会副主任委员
中国抗癌协会肿瘤病理专委会乳腺学组副组长
中国临床肿瘤学会(CSCO)肿瘤病理专家委员会常委
中国抗癌协会肿瘤标志专委会及肿瘤病理专委会常委
河北省医学会病理学分会及河北省医师协会病理科分会候任主任委员
非鳞状NSCLC中PD-L1表达相关的临床病理和基因组因素
研究背景
PD-1/PD-L1免疫检查点抑制剂的问世提高了转移性NSCLC患者的生存率,但仅有部分患者能够受益于此,免疫治疗疗效的生物标志物应用仍存在很大局限。PD-L1表达的肿瘤比例评分(TPS)定义为通过免疫组化染色的PD-L1阳性肿瘤细胞的百分比,其为NSCLC免疫治疗疗效临床可用的主要预测因子。尽管PD-L1表达在免疫治疗中发挥重要作用,但其表达相关影响因素尚不清楚。在多种肿瘤中,PD-L1表达可被外源性因子如γ干扰素或内源性因子刺激,内源性因子包括哺乳动物雷帕霉素靶蛋白(mTOR)和丝裂原激活蛋白激酶(MAPK)途径的激活,以及CD274基因的转录调节。CD274基因位于染色体9p24.1并编码PD-L1蛋白。在NSCLC中,KRAS、EGFR和ALK的激活突变以及PTEN的缺失突变会影响PD-L1的表达水平,NSCLC中CD274的扩增可能与PD-L1表达增加有关,而STK11突变与PD-L1表达减少和免疫治疗疗效降低有关。对PD-L1表达相关因子的深入研究有助于阐明免疫治疗的原发反应或抵抗机制。本研究试图分析与非鳞状NSCLC中PD-L1表达相关的临床病理和基因组因素。
研究方法
临床病理资料收集来自所有进行PD-L1评估并通过丹娜法伯癌症研究所的OncoPanel靶向NGS检测的非鳞状NSCLC患者。比较三组不同PD-L1表达的基因突变和基因及染色体臂的拷贝数变异情况。通过OncoKB数据库注释为原癌基因的改变来筛选基因突变。在多重比较校正后,Q值<0.25是显著的。显著的基因改变在一组接受免疫治疗的患者中作为预测因子进行检测。
临床病理特征与PD-L1表达的关系
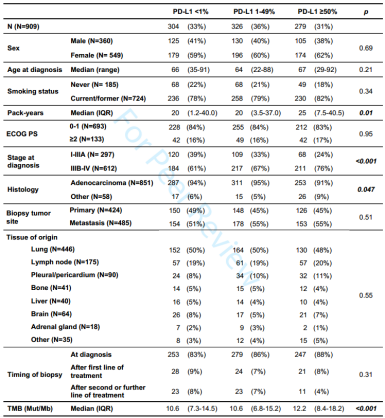
该研究共有909例非鳞状NSCLC癌患者进行了PD-L1检测,并分为以下三组:PD-L1阴性组,TPS<1% (N=304,33%),PD-L1低表达组,TPS为1%~49% (N=326,36%),PD-L1高表达组,TPS≥50% (N=279,31%)(表1)。与PD-L1低表达组和阴性组相比,PD-L1高表达组在晚期诊断时更为常见 (ⅢB~Ⅳ期:分别为76% vs. 67% vs. 61%;P<0.001),并且烟草暴露量更大 (中位吸烟指数:分别为25 vs. 20 vs. 20;P=0.01)(表1)。在组织学亚型方面:具有非腺癌组织学的非鳞状肿瘤与PD-L1高表达组相关(非腺癌分别为9% vs. 5% vs. 6%; P=0.04),多形性癌在PD-L1高表达组也更多(分别为3% vs. 1% vs. 0%; P=0.006)。
表1. 不同PD-L1表达组的患者特征
基因突变特征与PD-L1表达的关系
PD-L1高表达组的中位TMB明显高于PD-L1低表达组和阴性组 (中位分别为:12.2 mut/Mb vs. 10.6 mut/Mb vs. 10.6 mut/Mb; P<0.001)。与PD-L1高表达组相比,PD-L1阴性组与STK11 (19% vs. 6%; P<0.001)、EGFR (22% vs. 11%; P<0.001)、CTNNB1 (4% vs. 0.4%; P<0.001)、APC (5% vs. 1%; P=0.005)、SMARCA4 (9% vs. 4%; P=0.007) 和RB1 (4% vs. 1%; P=0.018) 的突变有关。而与PD-L1阴性组相比,PD-L1高表达组与TP53 (48% vs. 33%; P=0.009)、EP300 (3% vs. 0.3%; P=0.01)、MET (7% vs. 2%; P=0.01) 和CDKN2A (9% vs. 3%; P=0.02) 的突变相关,经过多重比较校正后,这些基因无显著性 (图1A和图1B)。
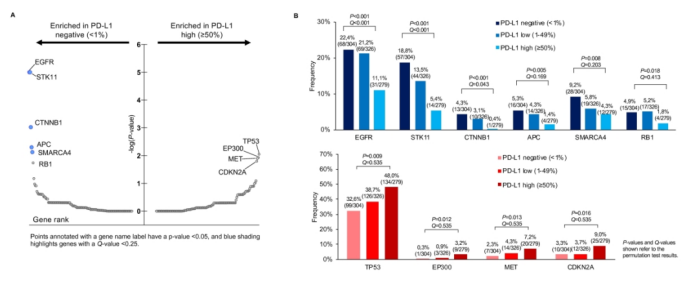
图1. (A)与PD-L1表达水平相关的致癌基因突变;(B)癌基因突变频率与PD-L1<1%(上排)和PD-L1≥50%(下排)显著相关
基因拷贝数变异与PD-L1表达的关系
由于拷贝数变异(CNV)评估仅限于低肿瘤纯度的样本,因此排除了肿瘤含量<20%的病例,剩余909例病例中的873例(96%)可进行CNV分析。与PD-L1高表达组相比,PD-L1阴性组分别与CD274(28% vs.6%;Q<0.001)、PDD1LG2(28% vs.6%;Q<0.001)和JAK2(27% vs.7%;Q<0.001)的拷贝数丢失有关(图2)。PD-L1阴性组还与9p24.1染色体位点缺失(定义为CD274、PDCD1LG2和JAK2共缺失)显著相关(分别为25%vs.6%;P<0.001)。与PD-L1阴性组相比,PD-L1高表达组的基因拷贝数增加最显著的为CD274 (11% vs. 3%;Q=0.01)、PDCD1LG2 (11% vs. 3%;Q=0.01)和JAK2 (9% vs. 3%;Q=0.05)。此外,PD-L1高表达组NSCLC更常检测到9p24.1染色体位点的拷贝数增加 (定义为CD274、PDCD1LG2和JAK2的共增加) (分别为9% vs. 3%;P=0.004)。
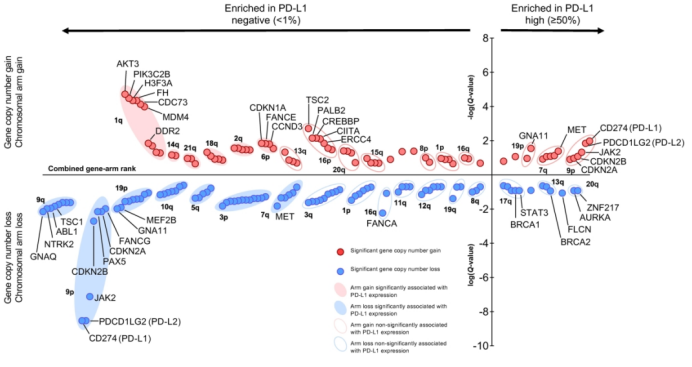
图2. 与PD-L1表达水平相关的染色体臂和基因拷贝数变异
染色体臂拷贝数变异与PD-L1表达的关系
446例样本(49%)的数据可用于此分析。与PD-L1高表达组相比,PD-L1的缺失与染色体臂9q (24% vs. 10%; Q=0.04)、9p (23% vs. 10.1%; Q=0.05)、6q (22% vs. 10%; Q=0.07)和19p (26% vs. 13%; Q=0.07)的丢失以及1q的增加 (46% vs. 21%; Q<0.001)有关。
基因拷贝数变异对免疫治疗疗效的影响
在一个包含486例非鳞状NSCLC患者的队列中,本研究评估了与PD-L1表达相关的基因组改变的预测价值。与无CD274拷贝数丢失的患者相比,存在CD274拷贝数丢失的患者的客观缓解率显著降低(ORR: 9% vs. 23%;P=0.006),并且中位无进展生存期显著缩 (mPFS: 2.0 vs. 3.3个月,HR=1.52;P=0.002),而中位总生存(mOS)却无差异(图3)。类似的结果也见于NSCLCs的9p24.1缺失和染色体臂9p缺失。
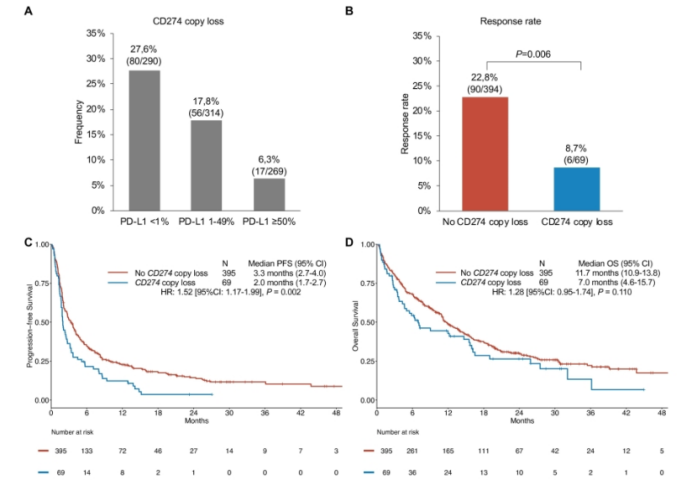
图3. CD274拷贝数丢失的频率及对疗效的影响
研究结果与讨论
PD-L1在NSCLC中的表达具有高度的变异性,但对不同PD-L1表达水平相关因素的了解非常有限。该研究采用了一种全面、公正的方法,来分析与不同PD-L1表达水平相关的临床因素和基因组改变,包括基因突变和CNV。该研究发现,PD-L1的高表达与烟草暴露、诊断晚期、TMB升高和CD274基因座9p24.1的获得有关。而PD-L1阴性与EGFR、STK11、CTNNB1、APC和SMARCA4突变有关,与CD274、PDCD1LG2和JAK2基因拷贝丢失、9p24.1位点丢失、9p染色体臂丢失和1q染色体臂增加有关。
既往报道过CD274的扩增(≥6个基因拷贝)发生在0.6%的肺腺癌中,而在另一项研究中,在5.7%(N=5/94)的NSCLC中发现染色体位点9p24.1的扩增(≥3个拷贝)。在本研究中,CD274和9p24.1的拷贝数增加率分别为6%和5%,这两种改变都与PD-L1的高表达有关。同样,PD-L1阴性与CD274拷贝数丢失(18%)和9p24.1丢失(16%)显著相关。该研究发现CD274拷贝数丢失与NSCLC免疫治疗的疗效降低相关,若能在更大的研究中得到证实,其可能是一个基因组生物标志物,可用于识别那些不太可能从PD-1抑制中获益的患者。
以上研究发现PD-L1的表达与明确的临床病理和基因组特征有关。进一步研究肿瘤基因型与PD-L1免疫表型之间的关联机制是非常有必要的。这些发现将有助于设计策略来提高NSCLC免疫治疗的疗效。而且还需要更大规模的研究将免疫治疗疗效与不常见的NSCLC基因型(如CTNNB1和APC突变、CD274缺失等)相关联,来确定它们作为免疫检查点抑制剂的预测性生物标志物的相关性。
此外,随着精准医学的快速发展,NSCLC的基因表达谱逐渐清晰,越来越多的医疗机构可以提供小Panel的高通量测序。那么,基于NGS的小Panel检测能够揭示患者的哪些信息?下面这篇文献通过收集大量数据,探讨了肺癌分子突变特征与PD-L1表达的关系。
基于NGS检测探索NSCLC中的分子突变特征及其与PD-L1表达的关系
背景
NGS是近年来快速发展的高通量测序技术,可用于检测多种形式的DNA变异,包括点突变、小片段插入缺失、基因重组和拷贝数变异。它可以同时分析多个基因突变,定量检测基因突变率,为临床医生提供全面信息。随着免疫治疗的研究进展,基因突变与PD-L1之间的关系已成为目前研究的热点。因此,该研究在NSCLC患者中采用了15个基因panel的NGS检测,以探索其分子变异特征及其与PD-L1表达的关系。
方法与结果
该研究收集了经15基因panel NGS检测的1017例患者,并且分析其临床病理特点。比较不同的组织病理学改变特点。结果发现在1017例中,640例FFPE样本中至少有一个基因突变,其中600例检测了PD-L1(22C3),其余40例因肿瘤含量不足而未检测PD-L1。在600例肺癌中,248例(41.33%)患者TPS<1%,255例(42.50%)患者TPS为1%~49%和97例(16.17%)TPS≥50%。PD-L1(22C3)的TPS评分结果在EGFR、ALK、BRAF和MET基因突变上有显著性差异(P<0.05)。EGFR突变在TPS<1%(58.87%)中更为常见,ALK突变在TPS(1%~49%)中更为常见(9.80%),BRAF和MET突变在TPS≥50%(7.22%和22.68%)中更为常见(图4)。全面了解肺癌患者基因突变的特点及其在相应病理类型中的潜在临床意义,可以为肺癌的临床治疗提供更多的信息。
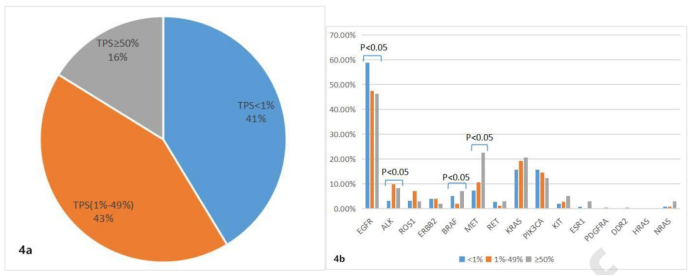
图4. (A)突变基因患者PD-L1的表达;(B)不同突变基因患者PD-L1的表达
讨论
该研究结果表明,PD-L1在至少一个基因突变的患者中有一定的表达率,并且在EGFR、ALK、BRAF和MET中有显著差异。研究者推测生物标志物和PD-L1的结合可以最大限度地提高患者分层的预测准确性。但需要更多的数据来证实这一点。总之,PD-L1联合NGS的小panel检测可以为患者提供更多有用的临床病理信息,从而使患者获得优化的治疗方案。
[1] Lamberti, Giuseppe et al. Clinicopathological and genomic correlates of Programmed Cell Death Ligand 1 (PD-L1) expression in nonsquamous non-small cell lung cancer. Annals of Oncology 2020 Mar 11. [Epub ahead of print]
[2] Liu J, Liu Y, Molecular diagnostic characteristics based on the next generation sequencing in lung cancer and its relationship with the expression of PD-L1, Pathology Research and Practice (2019), doi: https://doi.org/10.1016/j.prp.2019.152797
排版编辑:肿瘤资讯-frank














 苏公网安备32059002004080号
苏公网安备32059002004080号


