
CDK4/6抑制剂等靶向药物的问世,推动了HR+/HER2-晚期乳腺癌进入内分泌治疗+时代。相比于单纯内分泌治疗,CDK4/6抑制剂联合内分泌治疗,不仅可以显著延长PFS和OS,且对于合并内脏转移的患者而言,也带来了更为有效的治疗策略。本文分享1例绝经前首诊Ⅳ期HR+/HER2-乳腺癌患者,因有症状的内脏转移采用联合化疗方案首次治疗,进展后接受CDK4/6抑制剂哌柏西利(palbociclib)+AI+卵巢功能抑制获得治疗,并有效控制肝转移灶的案例。

天津医科大学肿瘤医院主治医师、医学博士
中国女医师协会乳腺专业青委会副主任委员
中国女医师协会会员
中国抗癌协会会员
一般情况
患者女性,45岁,未绝经,因主诉“发现右乳肿物1年半”就诊我院。2年前因宫颈癌前病变行宫颈锥切术,否认输血史。无高血压、冠心病、糖尿病甲亢病史;无肝炎、结核病史。无外伤史、无食物、药物过敏史。姑姑患子宫内膜癌,姨妈患肺癌,否认其他家族遗传性疾病。
现病史
患者于1年半前查体发现右乳肿物,伴乳腺疼痛,乳头无溢液,无皮肤红肿,无发热。未行任何治疗,近日自觉肿物增长迅速,遂就诊于我院。乳腺B超示:右乳多发肿物--考虑多灶性乳腺癌(BI-RADS5),双乳导管扩张伴多发弱回声,考虑乳头状瘤,右腋下多发淋巴结转移,右锁上肿大淋巴结,肝左叶实性肿物转移瘤,门诊以“右乳肿物”收入我院。查体:右乳可及多发肿物,最大位于内上象限,大小约为4.0cm×3.5cm×3.0cm肿物,肿物中心距乳头距离为2cm,质硬,界欠清楚,活动差,尚定,与皮肤粘连。右乳头下方局部皮肤红肿,隆起于表皮,范围约1.0cm×1.0cm,局部破溃。右腋下可及肿大淋巴结,最大约1.5cm×1.0cm,质韧,界欠清楚,活动差。右锁上可及肿大淋巴结,最大约2.5cm×2.0cm,质韧,界欠清楚,活动差,左侧腋下及锁骨上未及肿大淋巴结。
影像学检查
①乳腺B超示:右乳多发肿物,最大范围位于内上边缘3.9cm×3.4cm×2.6cm。右腋下多发淋巴结转移(1.5cm×1.0cm),右锁上肿大淋巴结(最大1.0cm×0.5cm)。肝左叶实性肿物,考虑转移瘤(5.3cm×2.8m)。②胸部CT示:肝左叶内侧段稍低密度肿物,肝左叶小低密度结节。部分椎体及肋骨骨质密度不均匀。③肝脏强化MRI示:肝左叶占位性病变,大小约5.0cm×3.1cm×2.6cm。ECT未见明显骨转移影像。
病理
右乳腺肿物穿刺病理示:(右乳腺粗针穿刺标本)浸润性癌。(右腋下粗针穿刺标本)低分化腺癌;ER 80%、PR 90%、HER-2 1+、KI-67 20-40%、P53 2%、CK5/6<1%、EGFR<1%、AR 70%。(肝脏粗针穿刺标本)低分化腺癌、ER 80%、PR 10%、HER-2 1+,免疫组织支持来自乳腺。分子分型:Luminal B型。
首次治疗
考虑患者肿瘤负荷大,瘤体已经超过5公分,且伴有肝转移,决定先行化疗。于2018-12-28至2019-1-14行第一、二周期TE方案解救化疗。复查超声示:右乳癌(右乳几乎各个象限可见多发低回声区,最大范围位于内上边缘3.0cm×3.0cm×2.0cm),较前减小,右腋下多发淋巴结转移(1.2cm×1.0cm),右锁上肿大淋巴结(最大1.0cm×0.5cm),肝左叶实性肿物一转移瘤(5.0cm×2.0m),较前略减小。2019-2-10行第三周期解救化疗方案同前。复查肝脏核磁:肝左叶肿物较前稍增大(5.2cm×3.3cm×2.5cm)。复查肝脏超声:右乳癌(右乳几乎各个象限可见多发低回声区,最大范围位于内上边缘4.0cm×2.8cm×2.1cm),较前增大,右腋下多发淋巴结转移(1.2cm×1.1cm)。肝左叶实性肿物,转移瘤(6.2cm×3.2cm)较前增大。
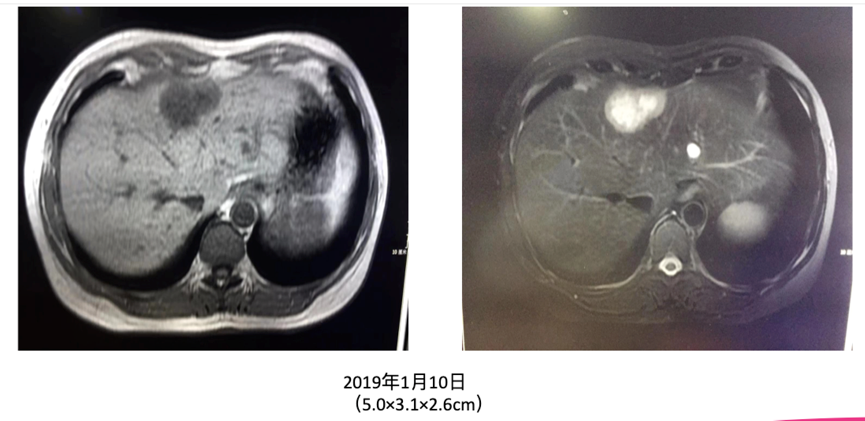
图1. 患者一线化疗期间肝脏MRI检查
进展后再次治疗
2019-3-5开始更改为哌柏西利125mg,qd,连续三周休1周联合来曲唑2.5mg,qd戈舍瑞林3.6mg,IH,Q28d治疗。期间每两周复查血常规,无四度骨髓抑制,均正常周期服药。两周期后复查超声:右乳多灶性乳腺癌化疗后,符合治疗后改变(BI-RADS:6;最大病灶2.9cm×3.7cm×2.0cm);右腋下多发转移性肿大淋巴结(1.1cm×0.7cm),较前测量有所缩小;右锁上肿大淋巴结(最大0.5cm×0.4cm),较前有所缩小;肝左叶实性肿物,考虑转移瘤(4.1cm×2.1cm),较前测量缩小。
于2019-5-5至2019-6-5继续原方案治疗两周期。复査肝脏MRI:肝左叶肿物较前缩小(3.3cm×2.1cm)。胸部CT:双肺部分小结节较前缩小,密度浅淡;肝左叶内侧段肿物较前缩小。拒绝行超声检査。
于2019-7-5至2019-8-5继续原方案治疗两周期,肝核磁检查造影剂过敏,行肝脏CT:肝左叶肿物较前缩小(2.8cm×1.8cm)。乳腺超声:右乳多灶性乳腺癌化疗后,符合治疗后改变(BI-RADS:6;最大2.0cm×2.5cm×1.0cm),右腋下多发转移性肿大淋巴结(1.0cm×0.5cm),较前测量有所缩小。右锁上肿大淋巴结。肝左叶实性肿物一,考虑转移瘤(2.5cm×2.4cm),较前测量缩小。2019-12-31行肝脏CT:肝左叶肿物较前略有缩小(2.6cm×1.6cm)。乳腺超声:原发灶未见明显变化(2.0cm×1.1cm),稳定状态12周。
表1. 患者的治疗历程及影像学评估总结
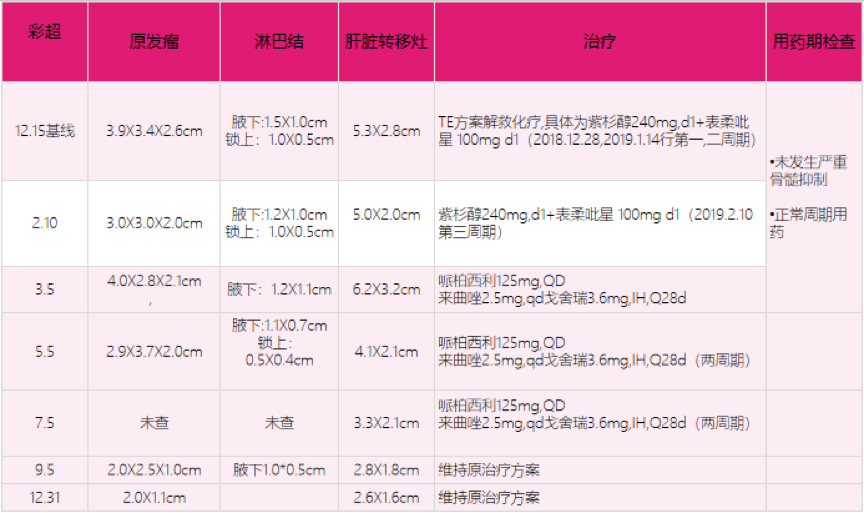
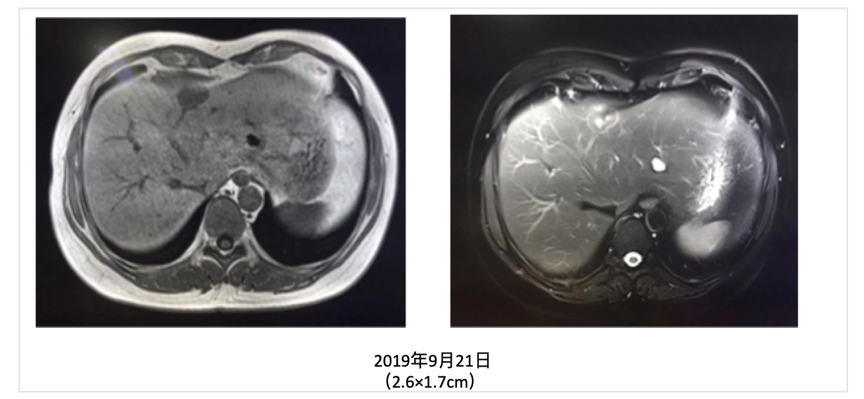
图2. 患者哌柏西利联合来曲唑治疗期间肝脏MRI检查
总结
患者女性,45岁,未绝经,因主诉“发现右乳肿物1年半”就诊。患者为首诊Ⅳ期乳腺癌,合并双肺和肝脏转移。右乳肿物穿刺为低分化腺癌ER 80%、PR 90%、HER-2 1+;肝转移灶穿刺病理符合转移性乳腺癌,分子分型一致。临床诊断为HR+/HER2-晚期乳腺癌,合并肝脏、肺多发转移。一线接受TE方案化疗,两个周期化疗后,肿瘤略微缩小;三个周期化疗后,原发灶及肝转移均进展,评价为PD。之后接受哌柏西利联合AI和卵巢功能抑制治疗,治疗2个周期后评估,肿瘤缩小,疗效评价为PR。治疗4周期后,肿瘤继续缩小,目前患者仍在持续治疗中,并定期复查。
专家点评

天津医科大学肿瘤医院院长助理
中国天津乳腺癌防治研究中心常务副主任
天津医科大学肿瘤医院乳腺肿瘤三科科主任
九三学社中央委员会医药卫生专门委员会副主任
九三学社天津市委员会委员
国家科学技术奖评审专家
中华医学会肿瘤学分会委员
中国抗癌协会乳腺癌专业委员会副主任委员
中国医师协会乳腺癌专家委员会副主任委员
中国宋庆龄基金会肿瘤医疗及产学研联盟副理事长
中国女医师协会乳腺疾病研究中心副主任
中华医学会肿瘤学分会恶性肿瘤早诊早治学组副组长
天津市医学会肿瘤学分会副主任委员
美国临床肿瘤学会会员
美国血液学会会员
美国癌症研究协会会员
这是一例首诊晚期的HR+/HER2-(Luminal B型)乳腺癌。由于患者出现有症状的内脏转移,病情快速进展,为了能让患者的肿瘤迅速缩小、症状迅速缓解,故采取TE的解救化疗方案。患者在接受一线ET方案化疗3周期后,疗效有限,最佳疗效为SD,疾病很快出现进展。对于一线化疗进展的患者,且既往未接受过内分泌治疗,患者后续的治疗策略可以根据一线内分泌治疗方案来进行选择。
我们知道,对绝经前HR+/HER2-晚期乳腺癌患者进行卵巢功能抑制后,CDK4/6抑制剂联合AI或他莫昔芬能够获得很好的疗效,那么CDK4/6抑制剂联合内分泌治疗与化疗相比是否会有更好的优势呢?在2019年ASCO年会上,Young PEARL研究的结果为此带来答案。PK结果显示,CDK4/6抑制剂联合内分泌治疗为患者带来了远超化疗的PFS:CDK4/6抑制剂哌柏西利联合依西美坦获得了20.1个月的中位PFS结果,而对照组卡培他滨单药组仅有14.4个月的PFS。考虑到哌柏西利联合内分泌治疗比化疗带来的获益更大,因而,对于激素受体阳性的Luminal型患者而言,如果有内分泌治疗的机会,就应该毫不犹豫地采用内分泌治疗作为晚期一线治疗。
目前指南推荐的一线内分泌治疗方案包括靶向治疗联合内分泌治疗或内分泌单药(他莫昔芬、AI或氟维司群)治疗。考虑到患者此时疾病负荷较重,需要及时缓解症状并控制肿瘤,因此,靶向治疗联合内分泌治疗可能是更为合理的选择,如CDK4/6抑制剂联合内分泌治疗治疗。哌柏西利是全球最早上市的CDK4/6抑制剂,也是唯一一个在中国上市的CDK4/6抑制剂。既往多项研究证实了哌柏西利的疗效和安全性。在随机Ⅲ期研究PALOMA-2中,研究人员评估了哌柏西利与来曲唑联用作为ER+/HER2-晚期或转移性乳腺癌患者初始内分泌治疗的疗效和安全性。入组患者随机2:1分配至哌柏西利联合来曲唑组与安慰剂联合来曲唑组。根据PALOMA-2研究最新公布的数据,哌柏西利联合来曲唑组与安慰剂联合来曲唑组患者的中位PFS分别为27.6个月和14.5个月(HR 0.563,95%CI 0.461~0.687,P<0.0001),其中约31.5%的患者为初治Ⅳ期[1]。此外,PALOMA-2研究中,对内脏转移亚组进行分析显示,两组患者PFS分别为19.3个月和12.3个月(HR 0.62,95%CI 0.47~0.81,P<0.0005)。既往未使用过内分泌治疗且伴有内脏转移的亚组中,两组中位PFS分别为23.7个月和13.9个月(HR 0.55,95%CI 0.36~0.85,P<0.0005)。肝转移和肺转移患者均能从哌柏西利联合治疗中获得显著的PFS获益。这例患者合并肝、肺转移,接受哌柏西利联合来曲唑治疗后,病灶明显缩小,目前仍在持续治疗和获益中。值得注意的是,患者为绝经前女性,指南建议同时联合卵巢功能抑制,药物卵巢功能抑制是较为常用的手段,可选方案包括戈舍瑞林、亮丙瑞林,也可以考虑行卵巢手术切除,随后遵循绝经后患者内分泌治疗指南。
CDK4/6抑制剂的问世,推动HR+/HER2- 晚期乳腺癌进入靶向联合内分泌治疗时代。值得一提的是,2018年8月,首个CDK4/6抑制剂哌柏西利获得NMPA批准,正式进入中国。其上市,对于中国乳腺癌治疗而言,是非常重要的新起点,开辟了重要的时代。随着哌柏西利的上市,HR+/HER2晚期乳腺癌的治疗格局已经发生变化。临床研究和真实世界研究均证实哌柏西利联合内分泌疗效确切,不良反应可耐受,可作为优选。
[1] Rugo H S,Finn R S,Diéras V et al. Palbociclib plus letrozole as first-line therapy in estrogen receptor-positive/human epidermal growth factor receptor 2-negative advanced breast cancer with extended follow-up.[J] .Breast Cancer Res. Treat., 2019,















 苏公网安备32059002004080号
苏公网安备32059002004080号


