
2018年7月31日,CDK4/6抑制剂哌柏西利(palbociclib)被国家药品监督管理局(NMPA)正式批准上市,联合内分泌药物用于HR阳性/HER2阴性局部晚期或转移性乳腺患者的治疗。本文就一例初诊Ⅳ期HR+/HER2-转移性乳腺癌患者,一线治疗选择CDK4/6抑制剂哌柏西利联合来曲唑,患者不但获得较好的临床获益,而且作为老年患者,内分泌治疗期间不良反应可控,并获得较好的生活质量。

北京大学深圳医院肿瘤内科副主任医师
广东省医师协会乳腺专业委员会青年委员
深圳市抗癌协会化疗专业委员会常委兼秘书
深圳市抗癌协会临床试验委员会委员
中国肿瘤防治联盟深圳市乳腺癌专业委员会副主任委员
深圳市医师协会乳腺专科医师分会常务理事
深圳市医学会乳腺病专业委员会委员
深圳市医学会腹部肿瘤MDT专委会委员
基本病史
患者68岁,老年绝经女性。于2018年10月25日因“发现左乳肿物2年余,明显增大伴全身骨痛2月”就诊。乳腺彩超检查及乳腺肿物穿刺活检病理提示乳腺癌。完善相关影像学检查提示双肺转移瘤、多发骨转移瘤。
既往高血压病史30余年,糖尿病史30余年,现胰岛素+口降糖药控制,血糖控制尚可。2018年8月曾因“心肌梗塞”行“冠状动脉支架置入术”。
辅助检查
乳腺超声(2018年10月25日,本院):左侧乳腺2点方位可见一低回声团块,非平行生长,形状为不规则形,大小约32 mm × 19 mm × 17 mm,边缘不完整、呈蟹足状改变。左侧腋窝可见多个低回声结节,较大者约23 mm × 12 mm,呈类圆形,边界清楚,皮质回声欠均匀。超声诊断:左侧乳腺内实质性占位病变,BI-RADS 4类,左侧腋窝淋巴结肿大,淋巴结转移可能。
乳腺肿物穿刺病理(2018年10月30日):左乳肿物穿刺组织,浸润性癌,部分为非特殊型浸润性癌,部分为浸润性微乳头状癌,待手术后标本,进一步评价。
免疫组化(均设立了阳性及阴性对照):ER(强+,>90%);PR(中等至强+,> 90%);HER2(阴性);Ki-67(阳性率20%);P63(-);E-cad(胞膜+);MUC-1(微乳头外缘+)。
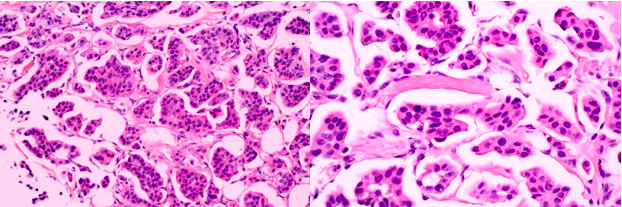
图1 “左乳肿物”穿刺组织病理切片
胸部CT示:①两肺多发结节,考虑转移瘤。②左肺上叶纤维索条左乳外上象限肿块,③左腋窝多发淋巴结。④冠脉PCI术后。
ECT全身骨显像检査(图2)提示:多发性骨盐代谢异常活跃灶,结合病史,多考虑为骨转移瘤影像。
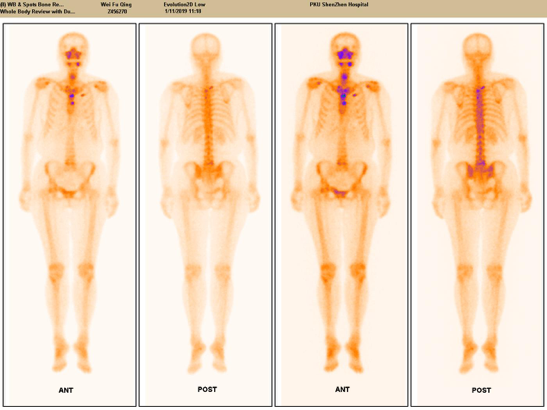
图2 ECT全身骨显像
诊断:①左侧乳浸润性导管癌 双肺转移、多发骨转移 Ⅳ期cT2N2M1 LuminalB型 ②冠脉支架置入术后 ③高血压病Ⅲ级 极高危组 ④2型糖尿病
病例特点及治疗经过
患者为绝经后老年女性,绝经后激素受体阳性、HER2阴性,伴内脏转移晚期乳腺癌,骨转移疼痛明显,无内脏危象,伴有高血压、冠心病、糖尿病等内科疾病。患者一线治疗考虑内分泌治疗优先,予以CDK4/6抑制剂哌柏西利+来曲唑,患者治疗第1个月骨痛开始缓解,3个月时骨痛完全缓解。用药3个月和6个月,乳腺MR评价PR,肺部结节有所缩小,疗效评价为SD,服药期间白细胞减少CTCAE 1-2级,在哌柏西利用药间歇期,白细胞自行恢复正常。目前患者生活如往常,每月在门诊复查一次血常规及肝肾功能。
2018年11月开始口服CDK4/6抑制剂哌柏西利+来曲唑。
2019年1月(治疗后3个月第1次疗效评价):患者骨痛缓解。复查CT双肺转移灶和乳腺病灶缩小,部分骨转移灶消失,部分病灶提示局部骨密度增加,骨质破坏修复。维持治疗。乳腺MR显示病灶PR。
2019年4月(治疗后半年第2次疗效评价):患者未诉骨痛。乳腺MR提示PR。自认为半年来放射性检测过多,拒绝行胸部CT检查。计划第3次疗效评价时(2019年8月)复查。
2019年9月(治疗后第3次疗效评价):患者未诉骨痛。乳腺MR提示PR,继续好转维持原方案治疗。
基线及疗效评估
CT评估

图3. 2018年10月26日治疗前(直径约5.6 mm)

图4. 2019年1月8日治疗后(直径约3.9 mm)
MR评估
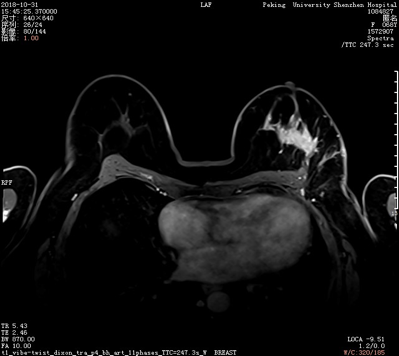
图5. 2018年10月治疗前(大小约26 mm × 20 mm × 25 mm)

图6.2019月年1月治疗后(大小约16 mm × 28 mm × 22 mm,病灶较前缩小)
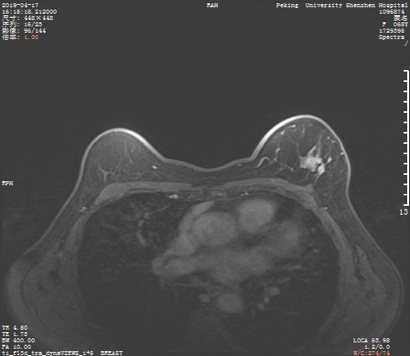
图7.2019年4月治疗后(大小约18 mm × 12 mm × 22 mm,病灶较前缩小)
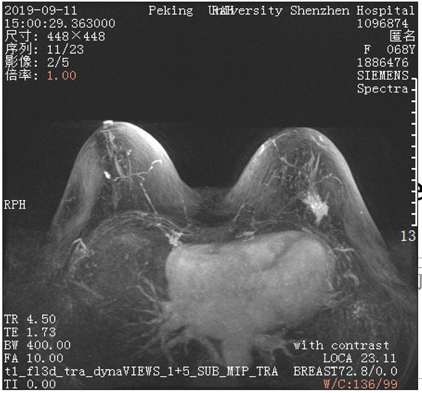
图8.2019年9月治疗后(大小约13 mm × 12 mm × 22 mm,病灶较前缩小)
专家点评

北京大学深圳医院肿瘤科主任、学科带头人
国家肿瘤临床研究中心深圳分中心负责人
深圳市医学会肿瘤专业委员会主任委员
深圳市抗癌协会化疗专业委员会主任委员
深圳市健康管理协会 MDT专委会主任委员
深圳市肿瘤多学科防诊治联盟联盟主席
深圳市医师协会肿瘤医师分会副会长
深圳市精准医学协会副理事长
1. 晚期乳腺癌一线治疗原则
本例患者发现乳腺包块2年余,包块增大伴有骨痛症状2月。虽然初诊时已经晚期乳腺癌,结合免疫组化提示ER、PR强阳性,HER2阴性,Ki-67 30%肿瘤细胞增殖指数并不算太高。总体疾病进展相对缓慢,无内脏危象。根据NCCN 2019 V1版乳腺癌指南和《中国临床肿瘤学会(CSCO)乳腺癌诊疗指南》2019版,对于晚期Luminal B型HER2阴性乳腺癌,现有国内外共识一致推荐内分泌治疗可以作为HR+/HER2-的标准治疗[1],尤其是符合以下特点的患者:①肿瘤进展相对缓慢;②无内脏危象的患者;③既往未曾接受内分泌治疗或内分泌有一定敏感性。综合来看,本例患者一线治疗优选内分泌治疗。
2. 内分泌+的时代治疗的考虑
在Ⅱ期PALOMA-1研究中,来曲唑联合CDK4/6抑制剂哌柏西利组的中位PFS是20.2个月,对照组是10.2个月,联合治疗组延长了10个月的无进展生存期。根据Ⅱ期研究获得的良好临床疗效,2015年2月美国FDA批准了CDK4/6抑制剂哌柏西利联合来曲唑一线治疗ER+/HER2-绝经后晚期乳腺癌患者的适应证[2]。随后进行的PALOMA-2研究是一项全球性、随机双盲安慰剂对照Ⅲ期临床研究[3],该研究纳入666例绝经后既往未接受针对复发或转移性肿瘤进行系统性治疗的晚期乳腺癌患者,按2:1随机分配至哌柏西利联合来曲唑组、安慰剂联合来曲唑组。Ⅲ期研究中,中位PFS为27.6个月(95% CI 22.4 ~ 30.3),而与之相比来曲唑+安慰剂组仅为14.5个月(95% CI,12.3 ~ 17.1), (HR = 0.56;95% CI;0.46 ~ 0.69;P < 0.000001),降低疾病进展的风险达到44%。这是第一个证实CDK4/6抑制剂能够延长患者生存期的Ⅲ期临床研究,也是第一个把HR阳性晚期乳腺癌患者的中位PFS延长到超过2年的Ⅲ期临床研究。
本例患者选择哌柏西利+来曲唑,第一个月骨痛症状开始缓解,3个月后病灶疗效评价达到PR。且该患者为肺转移患者,根据PALOMA-2研究对肺转移亚组的分析,哌柏西利联合来曲唑较来曲唑能够显著延长肺转移亚组患者的PFS,两组中位PFS分别为22.2个月和13.6个月(HR 0.59;95% CI 0.41 ~ 0.83;P < 0.01)。患者的诊疗历程让临床在真实世界重复了PALOMA-2研究的结果,在这位患者的临床实践中获得到预期的结果。
3. CDK4/6抑制剂哌柏西利不良反应可控
既往研究显示,哌柏西利的主要不良反应是骨髓抑制,但哌柏西利主要是诱导骨髓细胞静滞而非骨髓细胞衰老。诱导的中性粒细胞减少症可逆,而化疗则不可逆。特别是在停药后,中性粒细胞前体能够恢复,但对乳腺癌细胞的生长抑制仍持续一段时间。Ⅲ期PALOMA-2研究显示CDK4/6抑制剂哌柏西利+来曲唑较安慰剂+来曲唑最常见的3/4级不良反应为中性粒细胞减少(66.4% vs 1.4%)、白细胞减少(24.5% vs 0)、 感染(6.5% vs 3.2%)以及贫血(5.4% vs 1.8%),未见其他不良反应有特殊报告,安全性可控,因为不良反应停药的比例较低。
该患者年龄68岁,年龄相对较大。2019年ESMO年会报道了一项来自美国和加拿大的真实世界研究POLARIS[4],对老年患者接受CDK4/6抑制剂哌柏西利联合内分泌治疗的功能状态进行分析。研究通过功能状态量表(G8)、每日生活活跃情况(ADL)进行评分,评估哌柏西利联合内分泌治疗是否会影响老年HR+/HER2-晚期乳腺癌患者的生活质量。研究结果显示,入组的282例老年患者,经过6个月的治疗,量表评分较基线状态能够维持,高年患者功能并未受损,生活质量能够保障。
该患者CDK4/6抑制剂哌柏西利+来曲唑服用期间,白细胞减少CTCAE 1-2级,未特殊处理,在哌柏西利用药间歇期,白细胞自行恢复正常。目前患者生活如往常,每月在门诊复查血常规及肝肾功能,基本生活并未受到影响。
4. 总结
该病例遵循各项指南与规范结合临床实践合理诊疗给患者带来了切实的临床获益,值得临床制定激素受体阳性、HER2阴性晚期乳腺癌的治疗策略时进行借鉴。尤其是对转移性乳腺癌患者的解救治疗时,CDK4/6抑制剂联合内分泌治疗能够给患者带来更好的生存获益,提高生存质量。
1.中国临床肿瘤学会指南工作委员会. 中国临床肿瘤学会(CSCO)乳腺癌诊疗指南2019.
2.Finn R S, Crown J P, Lang I, et al. The cyclin-dependent kinase 4/6 inhibitor Palbociclib in combination with letrozole versus letrozole alone as first-line treatment of oestrogen receptor-positive, HER2-negative, advanced breast cancer (PALOMA-1/TRIO-18): a randomised phase 2 study[J]. Lancet Oncol, 2015, 16(1):25-35.
3. Finn R S, Martin M, Rago H S, et al. Palbociclib and Letrozole in Advanced Breast Cancer.[J]. New Engl J Med, 2016, 375(20):1925.
4. Meghan S, Karuturi, Joanne L, et al. Measures of Functional Status in Adults Aged ≥70 Years With Advanced Breast Cancer Receiving Palbociclib Combination Therapy in POLARIS. 2019 ESMO. Abr 365P.












 苏公网安备32059002004080号
苏公网安备32059002004080号


