结直肠癌是我国最常见的恶性肿瘤之一,发病率逐年上升。目前医学家普遍认为,结直肠癌不仅是单一专科的疾病,而是一组疾病症群,涉及到多个学科,因此,多学科协作(MDT)模式正逐渐成为结直肠癌治疗的标准模式。中华结直肠癌MDT联盟单位之一的中山大学附属第六医院已将MDT常态化和标准化,每周二下午进行MDT讨论与学习,力求为患者制定规范化、个体化的综合诊疗方案。2019年7月2日,中山大学附属第六医院成功举办了一场结直肠癌网络MDT直播会,并联合“肿瘤资讯”公众号进行同步线上直播。

此次MDT直播会由中山大学附属第六医院副院长吴小剑教授担任主持,并作为肿瘤外科代表参与讨论。吴教授在会议开场介绍了与会专家:肿瘤内科主任邓艳红教授,放疗科主任郑坚教授,放射与影像科学教研室主任孟晓春教授,介入科主任张波教授,超声科主任刘广健教授,泌尿外科主任王德娟教授。

此次直播会共讨论了6个病例。首先由各主管医生汇报病例情况,然后由专家对患者进行问诊、触诊,并围绕影像诊断、病理诊断、手术、化疗、放疗、靶向治疗以及免疫治疗等问题展开讨论,专业的同时不忘人文关怀,现场氛围热烈。现将病例详情与MDT团队专家意见整理如下,以飨读者。

【病例一】
男性,20岁。诊断:右睾丸横纹肌肉瘤术后复发(腹膜后、右髂窝)。
2017-10-16
2017-10-16CT外院:考虑右侧睾丸胚胎性横纹肌肉瘤并腹膜后多发淋巴结转移,病变与右侧腰大肌、下腔静脉、腹主动脉分界不清,肠系膜根部血管受压前移。
治疗:右侧睾丸及肿瘤根治性切除术。
术后病理:“右侧睾丸及肿瘤”恶性肿瘤,免疫组化:MyoD1+,Myogenin+,Myoglobin少数+,Vim+,Des+,Ki—67约40%,MSA+,CD30-,CAM5.2-,SMA-,CD117-,CK-。结合HE切片组织形态及免疫组化标记结果支持为胚胎性横纹肌肉瘤。
2017-11-23
2017-11-16外院CT:考虑右侧睾丸胚胎性横纹肌肉瘤后腹膜后多发转移,右下腹邻近肠管、右肾静脉、下腔静脉及腹主动脉部分层面受累。
治疗:剖腹探查+双侧后腹膜淋巴结清扫术。建议患者化疗,患者未予化疗,自行外院口服中药治疗。
术后病理:①“左侧腹膜后淋巴结”送诊淋巴结15枚,4枚见肿瘤转移;②“右侧腹膜后淋巴结”送诊淋巴结4枚,2枚见肿瘤转移;③“部分腔静脉及残余肿瘤组织”送诊组织内见肿瘤残留;④“腹主动脉与腔静脉淋巴结”送诊淋巴结2枚,未见肿瘤转移,内见癌结节2枚;⑤“后腹膜淋巴结”送诊融合淋巴结1枚,内见肿瘤转移。
2017-11-29
CT:对比2017-11-16片,原腹膜后可见多发结节、团块影大部分消失,考虑术后改变,腹腔少量积液,腹腔引流管留置,右侧腹腔脂肪间隙模糊,考虑术后改变或腹膜炎,请结合临床;膀胱少量积气。
2018-3-8
我院CT: 考虑右侧睾丸胚胎性横纹肌肉瘤并右下腹、腹膜后多发转移,右下腹邻近肠管、腹直肌、双侧腰大肌、右侧输尿管中上段受累,右肾静脉及下腔静脉部分层面受累,并右肾积水、右肾功能减低,腹腔少量积液。
治疗:CAV/IE方案化疗 8程(2018-3~2018-9);疗效评价:PR。
病理检查:梭形细胞肿瘤,结合外院免疫组化结果,考虑为胚胎性横纹肌肉瘤,淋巴结20余枚,多枚见肿瘤转移。
2018-5
右侧睾丸胚胎性横纹肌肉瘤并右髂窝区(腰大肌前方)、腹膜后大血管旁多发转移,范围较2018-3-18外院CT片明显缩小局限,血供较前减少。
2018-7
中山大学肿瘤防治中心儿童肿瘤科MDT会诊建议:化疗后复查,手术+放疗。
2018-9
我院MDT,手术处理;2018-9 PET-CT。
2018-11
2018-11-21在全身麻醉(气管插管)下“腹腔镜下右侧盆腔淋巴清扫术+腹腔粘连松解术+腹腔引流术+输尿管镜下右侧输尿管支架管置换术”。
术后病理:①(右侧髂外动静脉间淋巴结)淋巴结1枚,未见肿瘤(0/1)。②(右侧闭孔淋巴结)淋巴结2枚,未见肿瘤(0/2)。③(右侧髂外淋巴结)淋巴结3枚,1枚见肿瘤转移(1/3),另见纤维组织内见肿瘤浸润。
2018-12
外院:肺结核;抗结核治疗2月,痰转阴。
2019-3
CT:“右侧睾丸胚胎性横纹肌肉瘤”行右侧睾丸切除术后改变;腰3椎体水平腹膜后新发肿物,考虑为转移瘤;右侧髂血管旁新发囊性病灶,考虑淋巴囊肿可能性大;可疑腹膜种植转移,较前好转;盆腔少量积液,较前相仿;
PET-CT “右侧睾丸胚胎性横纹肌肉瘤综合治疗后”,对比本院2018-09-18日PET-CT:左侧睾丸前上方代谢活跃结节,性质待定,请结合临床。腹主动脉旁(左肾静脉-髂血管分叉水平)多个代谢活跃肿大淋巴结,考虑转移。
2019-3MDT:呼吸科,结核维持治疗;外科,化疗后可行清扫;放疗:最后可以做辅助放疗。
讨论目的
1. 腹膜后淋巴结是否能清扫?
2. 2018-11手术后病理:(右髂外区域)纤维组织内见肿瘤浸润,影像学或手术具体在哪里?
3. 2019-6 CT腹股沟淋巴结转移的几率?是否需要穿刺活检?2019-3 PET-CT的左侧睾丸上方病灶性质?
4. 术后放疗的范围?
MDT团队专家建议
患者接受过多次治疗,目前化疗的敏感性较好,肿瘤缩小比较明显;腹腔内淋巴结转移主要集中于腹主动脉和腔静脉之间;腹股沟两侧的淋巴结转移,其中右侧多发性淋巴结转移较为明确。腹腔内及腹股沟淋巴结尽量清扫,并留放疗标志,以便后续更准确的进行放疗。最后,根据治疗情况及病理结果,考虑相关化疗方案。手术前由呼吸科进行肺结核的相关风险评估。
【病例二】
男性,64岁。主诉:确诊回肠癌腹腔转移8月余,化疗后2周。
目前诊断
①回肠低分化腺癌腹腔转移;②肠梗阻;③败血症;④左侧颈内静脉、锁骨下静脉、头臂静脉血栓形成并闭塞;⑤右侧锁骨下静脉、头臂静脉狭窄;⑥肺结核。
现病史
2018-09-26于外院行剖腹探查+腹腔粘连松解+部分回肠切除肠腔成型+空肠M-A管放置肠管排列+回肠造口术(无外院手术记录);
术后病理:回肠可见低分化腺癌浸润,癌组织浸润肠壁全层及浆膜外脂肪,可见脉管癌栓及神经束膜侵犯,肠系膜可见癌浸润,淋巴结(1/1),腹壁肿物、腹腔结节及大网膜见癌浸润。
免疫组化:部分回肠肠壁全层见低分化腺癌,符合原发,CK、CEA、CK20、CDX-2及VILLIN(+)、CK7及HER2(-),KI67约50%(+)。
2018-10-17行FOLFOX化疗方案第1程(患者出现输液港感染,上肢静脉血栓形成);
2018-11-09至2018-12-13行“爱必妥”双周化疗方案第1-3程,同时予拜瑞妥抗凝治疗;
2018-12-31至2019-03-31行“爱必妥+FOLFOX”化疗方案第1-6程;
2019-04-13至2019-05-14行“爱必妥”单药化疗方案第1-3程,同时予拜瑞妥抗凝治疗。
实验室检查
血常规:RBC. 2.350*10E12/L, HGB 66.000 g/L, PLT 78.000*10E9/L, NEUR. 0.830 , WBC. 、NEU正常;
CRP 149.36 mg/L,.PCT 1.730 ng/mL, ESR 35 mm/h;
BNP 1495.2 pg/mL,心梗标志物、心酶四项正常;
肝肾功能:CHE 1779.48 U/L,RBP 10.90 mg/L, ALb 31.32 g/L, TBIL 24.70 umol/L, DBIL1 10.50 umol/L,转氨酶、肾功能正常。
影像学检查
全腹部增强CT:“小肠部分切除+左下腹造口术后”改变,盆腔小肠、乙状结肠及直肠肠壁增厚,较前稍进展,部分粘连;腹盆腔多发结节、腹膜、直肠系膜广泛增厚,系膜内淋巴结肿大,较前相仿;左下腹造口邻近肠管内导管末端处散在积气较前吸收好转;腹盆腔积液较前增多。
胸部平扫CT:①左肺上叶下舌段新发片絮状模糊影,考虑炎症;②双侧胸腔积液并邻近肺组织局部含气不全,较前进展;③双肺尖及右肺下叶后基底段继发性肺结核(纤维增殖为主),合并左肺上叶结核球形成,结核球空洞现未见显示,右肺下叶纤维增殖灶较前增多;其他基本同前。
讨论目的
请各位老师指导下一步治疗方案:继续化疗?外科手术?其他?
MDT团队专家建议
患者为老年男性,肿瘤波及范围较广,同时合并胸腹水及肺部感染,PS评分与营养状态均较差,且既往接受过药物治疗,因此不适合行系统性化疗,但无其他潜在治疗方法。若患者家属强烈要求,可进行基因检测,根据情况考虑靶向治疗药物。主要是进行减症治疗,改善患者生活质量。
男,53岁。主诉:确诊乙状结肠癌,姑息治疗半年余。
入院诊断
①乙状结肠癌肝转移乙状结肠切除术后;② mFOLFOX6+西妥昔单抗化疗后;③乙肝小三阳。
现病史
患者既往因“便血伴腹痛2月余”于我院就诊,行相关检查后诊断为“①乙状结肠癌;②肝脏多发转移”。完善相关检查后于2018-11-28行“腹腔镜下乙状结肠癌根治术+腹腔引流术”,手术病理分期:T3N1M1。
免疫组化:Ki-67约70%肿瘤细胞(+),MLH1(+),MSH2(+),MSH6(+),PMS2(+),CDX2(+),HER2(-),CK7(-),CK20(-),Braf(-)。
术后于2018-12-23行术后第一次mFOLFOX6方案化疗。
结合患者肿瘤基因检测KRAS基因野生型情况,于2019-1-12开始第二次mFOLFOX6方案化疗+西妥昔单抗靶向治疗,共行5次化疗(西妥昔单抗治疗4次);
2019-3-16复查提示肝转移瘤增多增大。建议患者改行二线方案化疗+靶向治疗。
患者拒绝治疗,返当地行中医药治疗。
本次入院复查CT提示,肝转移瘤进一步增多增大。近期体重下降约3公斤。
2018-12-3手术病理结果
①(乙状结肠肿瘤切除标本)中分化腺癌,伴坏死,Ⅱ级,浸润肠壁全层(T3),脉管内见癌栓,神经束未见癌浸润,两切缘均未见癌累及,另见淋巴结3枚,1枚见癌转移(1/3)。免疫组化:Ki-67约70%肿瘤细胞(+),MLH1(+),MSH2(+),MSH6(+),PMS2(+),CDX2(+),HER2(-),CK7(-),CK20(-),Braf(-)。②(肠系膜淋巴结)淋巴结11枚,2枚见癌转移(2/11)。
基因检测结果
该例标本的KRAS基因第2、3、4号外显子状态为野生型。
该例标本的BRAF基因第600号密码子状态为野生型。
该例标本的PIK3CA基因第9和20号外显子状态为野生型
目前诊断
①肝多发转移瘤;②肺多发转移瘤;③乙状结肠癌姑息治疗后;④乙肝小三阳
讨论目的
请各位老师指导调整治疗方案。
MDT团队专家建议
现阶段先行全身化疗,创造局部处理的机会;重新进行RAS基因检测,确认是否可继续使用爱必妥;并建议强烈三药化疗方案联合靶向治疗。
【病例四】
男,68岁。主诉:反复便血7月余,发现肛管黑色素瘤1月。
现病史
7月前无明显诱因出现便后滴血,呈鲜红色,伴血块,大便表面覆着黏液,成形, 4-5次/天,伴椭圆形肿物脱出,可自行回纳,以“痔疮”治疗后无明显好转;
1月前(5-29)行肛管肿物切除术,病理提示肛管恶性黑色素瘤;
中山大学肿瘤防治中心:会诊病理提示恶性黑色素瘤。BRAF基因突变检测(不分型)阴性。MDM2基因扩增检测:阴性。
专科查体
左侧卧位,肛周未见肿物突出,未见痔核突出,3点钟方向肛周可见一大小约2*2不规则黑色痣斑;直肠指检,肛门可容2指,直肠空虚,截石位2点钟方向距离肛门1cm可及黏膜粗糙增厚,未扪及包块,无压痛,指套未见血染。
入院诊断
肛管黑色素瘤术后。
入院后检查
血常规、生化、凝血、肿瘤相关标志物未见明显异常;
直肠彩超:截石位10-2点钟位置可探及肛管黏膜增厚,最厚处约6mm,上下范围约29mm,形态不规则,边界不清,内部呈均匀低回声,病变局部肛门内外括约肌回声尚连续清晰,周围未见明显异常肿大淋巴结。肛管黏膜增厚并血供丰富,意义待定。
PET-CT:肛管及中下段直肠代谢稍活跃,请结合临床。甲状腺左叶结节,代谢异常活跃,建议进一步检查除外甲状腺癌。其他无显著异常。
讨论目的
1. 是否需要进一步手术治疗,具体术式:局部扩大切除?Mile’s术?
2. 是否需要放疗/化疗?能否使用PD-1靶向治疗?
MDT团队专家建议
患者68岁老年患者,基层较为完整,外科治疗建议行局部扩大切除。黑色素瘤是一种恶性行为较高、很容易发生血行转移的恶性肿瘤,常见转移部位为肺、脑、骨和肝。既往使用化疗药物进行术后预防的效果不尽人意;PD-1治疗用于黑色素瘤的效果较好且具有适应证,但针对黏膜型黑色素瘤,使用PD-1辅助治疗的证据并不充分。综合考虑,内科建议术后使用PD-1进行靶向治疗。放疗科建议,术后全身治疗,待稳定病情且有必要时,再行局部治疗。
【病例五】
男,54岁。
现病史:患者2017年10月因“排黏液血便4月”于我院就诊。
肠镜:距离肛缘9cm见2/3圈肿物;
活检病理:中分化腺癌,免疫组化微卫星稳定型,HER2-;
金域基因:RAS、BRAF、PIK3CA野生型,仅TP53突变;
血CEA: 1252ng/mL。
影像学检查
胸腹盆增强CT及盆腔MR:中段直肠癌,骶2/3前方MRF(+),T3cN2M1;肝内多发转移瘤(最大径64mm);双肺未见异常。
肝脏MR:全肝见多个(>10个)异常信号灶,直径11-64mm,最大位于S2。
胸腹盆增强CT (基线:2017-10):
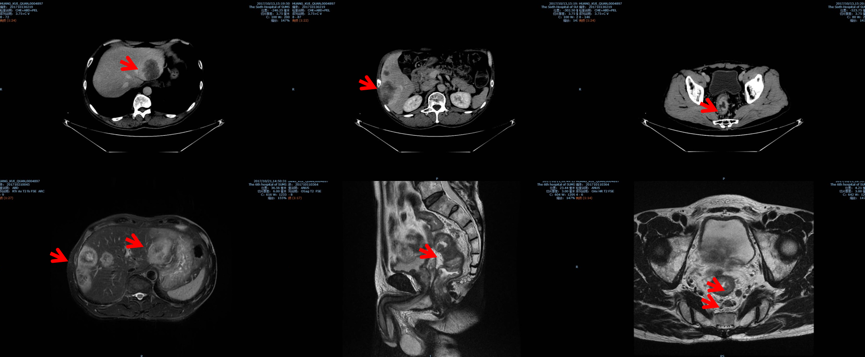
转化治疗 (2017-10至2018-02)
诊断:直肠癌同时性肝转移 cT3N2M1,IVa期;
治疗过程:mFOLFOXIRI×3程;爱必妥+mFOLFOXIRI×5程
不良反应:II度疲乏、II度口腔溃疡、II度粒细胞减少
4程后疗效评估(2017-12-23):PR
肝脏病灶显著缩小、减少,大部分显示不清;最大位于S6,最大径21mm
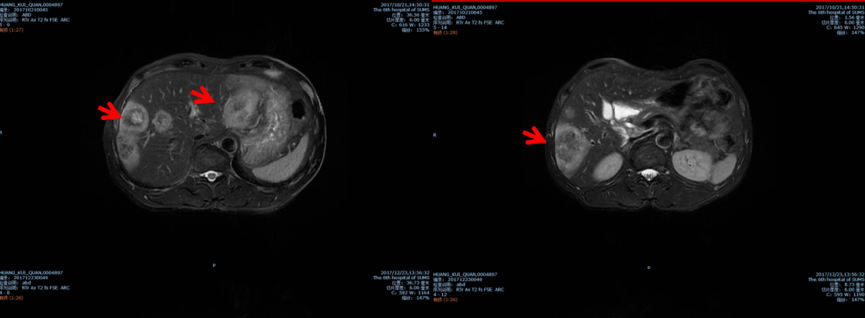
8程治疗后疗效评估(2018-3-2):PR
胸腹盆CT:直肠癌,局部病灶较前明显缩小;再分期cT3bN1;原肝内转移瘤明显缩小、减少。
超声造影:肝內多发转移瘤,约7个,最大位于S2(最大径20mm)
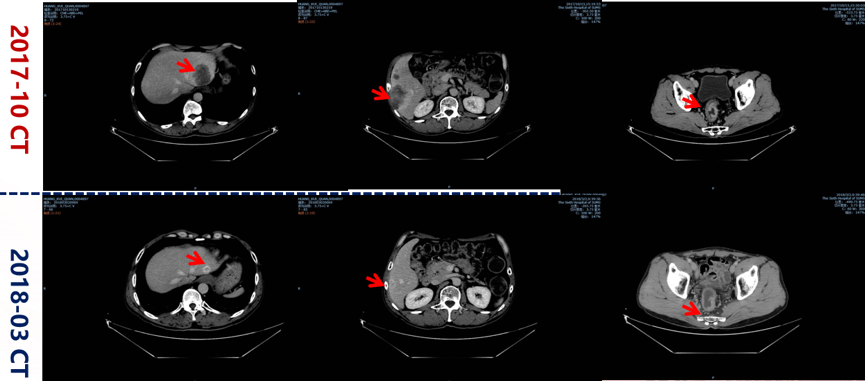
手术治疗
治疗过程:2018-3-5 腹腔镜下直肠癌根治术;2018-3-13 超声引导肝转移瘤微波消融(7个病灶);
术后病理:肠壁黏膜层、黏膜下层、固有肌层见腺癌残留,TRG2级,淋巴结(0/20),脉管-,神经束-;
术后化疗前:CEA:8.95ng/mL;金域ctDNA阴性;2018-04上腹部MR:肝内多发消融灶,未见肿瘤残余。
术后治疗一 (2018-04至2018-05)
mFOLFOX×4程;II度疲乏、II度外周神经毒性;2018-6-1 CT、MR均未见肿瘤残余,但CEA逐渐升高,8.95→12ng/mL。
术后治疗二 (2018-06至2018-12)
爱必妥+FOLFIRI×12程;2018-9-20超声引导肝S6病灶(6mm)微波消融;II度疲乏、III度粒细胞下降;2018-12-18CT、MR均未见肿瘤残余;此过程CEA波动于8-12ng/mL。
术后治疗三 (2018-12至今)
希罗达×3程;2019-3-17 上腹部MR发现肝S5新发结节;2019-3-21 超声引导肝S5病灶(9mm)微波消融;因疲乏明显,其后定期观察,未予全身化疗。
目前复查 2019-05
上腹部MR、PET/CT:2019-05-22 肝内多发消融灶未见血供(超声造影所见一致);2019-05-28 肝S5、以及近胆囊窝共2个病灶;胰头后方肿大淋巴结,转移待排。
上腹部MR:2019-06-25 肝S5、5/6新发2个结节(超声造影所见一致);CEA 50ng/mL。
讨论目的
1. 请影像科老师指导患者肿瘤范围评估(有无肝外转移灶)。
2. 肝脏病灶局部处理时机。
3. 下一步全身治疗方案。
MDT团队专家建议
由于患者病情变化较快,有无肝外转移灶需在复查CT后再做判断。建议先行局部消融,例如肝门区病灶等无法处理的病灶可根据实际情况进行放疗。建议消融过程中进行活检,明确基因状态,根据基因状态以及局部处理的效果,进行综合判断,后续可能会选择使用较为强烈的全身化疗方案。
【病例六】
女,71岁。主诉:大便次数增多半年余。
患者半年前开始出现排便次数增多,每天6-7次,大便稀烂,伴有里急后重感,无腹胀腹痛、恶心呕吐等,未予重视。上述症状逐渐加重,3天前至外院行肠镜检查提示:直肠距肛门约10cm可见半环形肿块,表面溃烂、渗血,呈菜花状,肠腔狭窄,内镜不能通过;活检提示:正常直肠黏膜。现患者为求进一步诊治入住我科。
心电图:Ⅰ度房室传导阻滞。
胸腹盆CT:直肠癌,CT分期:T4aN+M1,EMVI(+);肝S5转移瘤,S4可疑小转移瘤;左肺可疑转移瘤。
盆腔MR:上段直肠癌,MR分期:T4aN2b,EMVI(+)。
上腹部MR结果未回报。
肠镜:距肛门10cm直肠肿物,肠腔狭窄内镜不能通过,活检,结果未回报。
大便潜血:阳性。
肿瘤标志物:CEA 21.03ng/mL; CA19-9 60.37U/mL。
其余检验结果未见明显异常。
主要诊断
上段直肠癌并肝肺转移(cT4aN2M1b, ⅣB期)(?)。
讨论目的
请各位专家指导下一步诊治。
MDT团队专家建议
这是一例非常经典的局部晚期结直肠癌合并肝多发转移可疑肺转移的患者。CEA 21.03ng/mL,CA19-9 60.37U/mL,基于整体的肿瘤分布,局部较远端更为严重,目前无梗阻、出血等需要外科紧急干预的情况,有不全梗阻。建议先做一个横结肠造口,行高强度的三药化疗方案,创造完全切除的机会,再根据化疗效果和患者情况进行局部处理。具体的可选治疗方案,可与患者家属充分沟通后进行选择。该患者肺大泡较多,有些位于胸膜下,因此需叮嘱患者避免剧烈咳嗽,否则容易引发气胸。

会议最后,吴小剑教授进行会议总结:此次MDT直播会共讨论了6个病例,各病例均有其代表性与特殊性。通过本次会议,进一步加强了学科间的临床学术交流,同时保持了结直肠癌治疗的科学性与一致性,这也是进行MDT的目的与意义所在。在规范化诊疗的道路上,结直肠肿瘤的医生将不忘初心,砥砺前行。
扫描以下二维码观看精彩回放:












 苏公网安备32059002004080号
苏公网安备32059002004080号


