
CDK4/6抑制剂哌柏西利(palbociclib)联合内分泌药物用于HR+/HER2-局部晚期或转移性乳腺患者的治疗。CDK4/6抑制剂的出现,成为了晚期乳腺癌一线内分泌治疗的首要选择。现分享一例CDK4/6抑制剂联合治疗的病例。

中国人民解放军总医院第一医学中心肿瘤内科
基本病史
患者女性,43岁,月经规律。2016年12月主因“左侧乳腺癌术后8年,确诊双侧卵巢转移、骨转移7天”来诊。
既往治疗史
患者于2008年8月就诊于当地医院,行左侧乳腺癌局部扩大切除加腋窝淋巴结清扫+前哨淋巴结活检术,病理示:左侧浸润性导管癌(invasive ductal carcinoma,IDC ),SBRⅡ级,大小为1.2cm×1.2cm×1.0cm,侵犯神经,周围乳腺组织局灶可见导管内癌改变。(左侧前哨)淋巴结见转移1/2枚,(左侧腋窝组织)淋巴结未见转移癌0/13枚。免疫组化示:ER (-)、PR (+)、HER2 (1+)、Ki-67 (+,<5%)。结合患者病史和手术,明确诊断为:左乳腺浸润性导管癌术后pT1N1M0 ⅡA期。
2008年9月术后行6周期AC方案化疗,具体用药为:吡柔比星100mg静滴,第1天,环磷酰胺 1000 mg,静滴,第1天。化疗结束后于2009年2月行乳腺第1-2野50Gy/25F,第3野10Gy/5F放疗。并于2009年至2014年口服三苯氧胺治疗5年。患者治疗及随诊期间定期复查,未见明显复发或转移征象。
复发转移
患者2016年11月因腹部不适行超声检查,提示:附件区实性包块,建议进一步明确。盆腔MRI(增强)示:双侧附件区占位性病变,考虑恶性肿瘤可能性大,子宫腺肌病,宫颈那氏囊肿,盆腔积液。后患者就诊于我院,腹部超声示:①双侧卵巢增大,卵巢恶性肿瘤转移癌待除外;②右上腹大网膜增厚;③子宫膀胱陷凹脏层腹膜增厚;④子宫腺肌病声像图改变;⑤肝右后叶上段可疑偏低回声结节,非均匀性脂肪肝⑥盆腔积液。PET-CT示:左侧乳腺术后,术区及左腋窝未见明确异常高代谢灶,右侧乳腺区轻度代谢小结节。双侧附件区(图1)不均匀团块影,考虑恶性病变可能性大,SUVmax5.4。右耻骨、骶骨右侧、胸10、12椎体、右侧第2肋、胸骨柄、左侧第5后肋及左肩胛骨多发异常高代谢灶,SUV max5.8,以上均考虑转移性病变。
后患者行超声引导下右侧卵巢穿刺活检,病理回报:纤维组织内见腺癌组织浸润,符合乳腺癌浸润性导管癌转移。免疫组化示:ER(+75%)、PR(+75%)、HER2(1+)、Ki-67(+5-10%)。结合病史诊断为:左乳腺浸润性癌术后(pT1N1M0ⅡA期→rT1N1M1 Ⅳ期)双侧卵巢转移,多发骨转移。无病生存期(disease-free survival,DFS)为8年2个月。
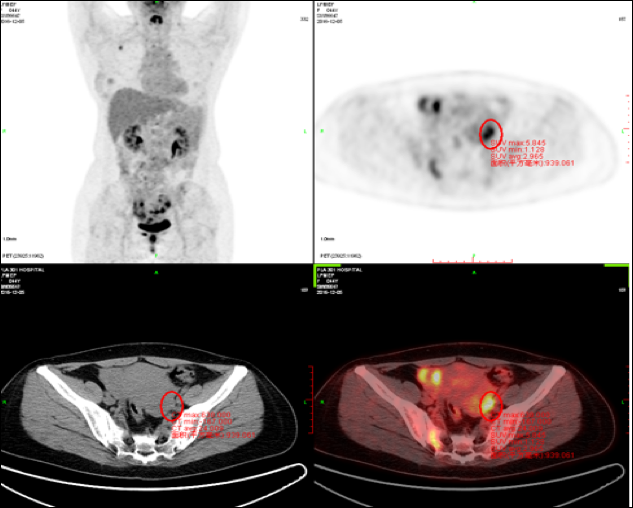
图1 患者PET-CT双附件显影区
患者为HR+/HER2-(1+)的晚期乳腺癌患者,无内脏危象,一线首选内分泌治疗。患者复发转移时未绝经,于2016年12月起行戈舍瑞林(OFS)+来曲唑+CDK4/6抑制剂哌柏西利治疗,具体方案为:醋酸戈舍瑞林缓释植入剂 3.6mg 皮下注射,q28天;来曲唑 2.5mg 口服 1/日;哌柏西利125mg 1/日,d1-21,q28天。患者服药后3个月(2017年3月)复查PET-CT示:双侧附件软组织影,代谢较前降低。多处骨骼成骨改变,部分代谢基本消失,部分代谢降低。综合疗效评价为部分缓解(partial response,PR)。后患者每三个月复查行PET-CT,2017年9月PET-CT示:双侧附件区原代谢增高影消失,右第2肋病变,代谢同前相仿,视野内多发骨骼高密度结节,无代谢。综合疗效评价完全缓解(complete response,CR),持续维持起始剂量治疗至今,未剂量调整。至目前治疗已28个月。不良反应方面:患者服药第一周期和第二周期出现白细胞Ⅰ度抑制,无其他不良反应出现,治疗期间未调整给药剂量。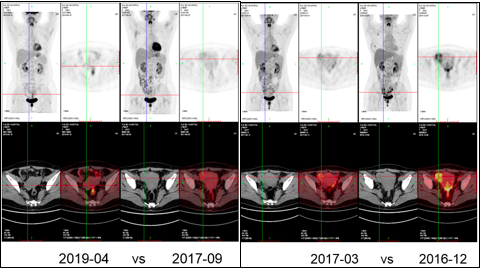
图2 患者一线内分泌治疗期间PET-CT
总结
患者女性,绝经前,保乳术后8年出现卵巢、骨转移,经卵巢穿刺活检,病理符合乳腺癌浸润性导管癌转移。免疫组化示:ER(+75%)、PR(+75%)、HER2(1+)、Ki-67(+ 5%~10%),无内脏危象,根据Paloma1/2研究结果并与患者充分沟通,给予哌柏西利联合内分泌一线治疗方案。一线治疗行戈舍瑞林+来曲唑+CDK4/6抑制剂哌柏西利治疗至今,最佳疗效为CR。不良反应耐受,未调整给药剂量。
大咖点评

中国人民解放军总医院肿瘤内科主任医师 副教授、肿瘤学博士、研究生导师
北京乳腺病防治学会免疫治疗学会常委、姑息治疗委员会常委、内科治疗委员会委员
中国抗癌协会康复会学术指导委员会副主委
北京中西医慢病防治委员会秘书长
中国抗癌协会临床化疗委员会青年委员会常务委员
中国医药教育委员会乳腺病专业委员会常务委员
中华乳腺病杂志等多家学术刊物编委和审稿专家
患者中年女性,绝经前。左乳腺浸润性癌术后8年,双侧卵巢转移,多发骨转移。根据患者年龄、身体状况和既往治疗等情况,结合《美国NCCN2019 V1乳腺癌指南》、《中国晚期乳腺癌临床诊疗专家共识》和《中国临床肿瘤学会(CSCO)乳腺癌诊疗指南》2019版及多种国内外指南,患者的治疗目前来看是较为合适且有效的。
1.首诊乳腺癌手术及术后治疗规范合理
回顾患者初次的手术,以及术后结合患者病理、淋巴结转移及免疫组化激素受体的表达,术后化疗、放疗、内分泌序贯治疗规范合理使得患者术后DFS长达8年2个月。但需要明确的是任何的手术及术后治疗并不能保证乳腺癌一定不复发,只能通过治疗降低未来复发或转移的机会和可能,这点需要在临床工作中充分和患者沟通,使其明确知晓。
2.复发后一线选择哌柏西利联合内分泌治疗,给患者带来切实获益
在晚期解救性治疗方面,对于晚期复发转移的乳腺癌患者,国内外共识一致推荐内分泌治疗可以作为HR+/HER2–的一线标准治疗[1],但需满足以下几点:①初始治疗或复发转移后病理证实为激素受体阳性,并尽量于治疗前对复发或转移部位进行活检,评估ER、PR、HER2的状态;②肿瘤缓慢进展;③无内脏危象的患者。对于晚期内分泌治疗方案的选择,需考虑与患者既往的治疗方案、复发/转移的疾病负荷选择治疗方案。内分泌治疗相对于化疗来说,虽然起效慢,但是持续时间长,治疗较为舒适,不需要住院和输液治疗,仅需口服或/和一月一次的肌肉注射,能够使得患者治疗依从性大大提高。
3. CDK4/6抑制剂联合内分泌治疗成为HR+/HER2–晚期乳腺癌一线治疗的首要选择,希望哌柏西利(爱博新)早日进入医保,惠及更多患者
CDK4/6抑制剂的出现,正迅速改变HR+/HER2-晚期乳腺癌的治疗格局。哌柏西利于2015年2月经FDA批准成为乳腺癌一线治疗靶向用药,成为全球首个上市的CDK4/6抑制剂。关于其获批主要是基于以下临床试验[2-4]:①PALOMA-1研究比较了来曲唑联合或不联合CDK4/6抑制剂哌柏西利在HR +/HER2-绝经后不适合手术的转移或局部复发乳腺癌患者一线治疗中的作用。正是基于Ⅱ期PALOMA-1研究显著将无进展生存期(progression-free survival,PFS)由10.2个月提高到20.2个月;②其后的Ⅲ期研究PALOMA-2研究结果再次证实了上述结论。③PALOMA-3研究是对于既往内分泌治疗进展(包括AI或TAM),包括正在辅助内分泌治疗或停止辅助治疗12个月以内进展,或是复发转移阶段内分泌治疗中进展的患者哌柏西利联合氟维司群,较氟维司群改善PFS(9.2个月 vs 3.8个月),OS可延长6.9个月,虽然未达到统计学意义,但是在既往内分泌治疗敏感的亚组中,OS显著延长10个月,差异具有统计学意义,给HR+/HER2-晚期乳腺癌的治疗带来跨时代的意义。临床结合卫生经济学进行考虑,若患者经济能够承受,则推荐患者一线选择内分泌治疗联合CDK4/6抑制剂。未来,期待哌柏西利可以早日进入医保,给更多HR+/HER2-晚期乳腺癌患者带来获益。
结合患者卵巢转移穿刺的病理结果,一线治疗首选内分泌治疗,采用CDK4/6抑制剂联合OFS+AI的治疗是合适的,至目前已达28个月。
4. CDK4/6抑制剂不良反应的管控
对于PALOMA系列研究中1、2、3研究合并分析发现主要出现的不良反应依次是中性粒细胞减少、白细胞减少等。中性粒细胞减少症是剂量调整的主要原因,且主要发生于前2个月,其后发生率逐渐下降,无剂量累积效应。目前研究认为[5-6],哌柏西利所引起的中性粒细胞减少是使细胞周期停滞,但增殖的中性粒细胞前体会予以保留。在临床试验当中,哌柏西利3/4度骨髓抑制发生率超过50%,但出现中性粒细胞减少性发热的患者较少,患者乏力症状不明显。在血液学毒性监测方面,在治疗时的第1和第2个周期第1天、第15天监测血常规和血生化,如果第15天出现3级中性粒细胞减少症,就需要在第22天重复监测。若监测发现4级中性粒细胞减少症,就必须在下一个治疗周期下调一个治疗剂量(125mg至100mg,或100mg调整至75mg)。但若白细胞总数高于2.0×109/L,或中性粒细胞高于1.0×109/L,则无需进行剂量调整,下周期还可按照原剂量继续用药。目前看来,血液学毒性可以通过剂量调整有效的管理,无需预防性使用集落刺激因子治疗。
在非血液学毒性监测方面,不良反应2级及以下不需要进行剂量的调整。如出现3级及以上非血液学毒性(如感染、腹泻、恶心等症状),若对症处理后仍然持续,就需要暂停给药直至症状缓解。如果认为对患者的安全无风险,则建议以下一个较低的剂量重新开始治疗。既往PALOMA-2研究中,根据剂量调整方案减量的患者PFS与未减量患者无显著差异,因而不需要过分顾虑降低药量是否会降低疗效。综上所述,其不良反应是可防、可控,药物是安全且有效的。
该病例遵循各项指南与规范结合临床实践合理诊疗给患者带来了切实的临床获益,对我们很有启发,值得借鉴和学习。特别是在转移的乳腺癌患者解救治疗中,内分泌治疗中CDK4/6抑制剂作为内分泌治疗的新秀正逐渐走到舞台中央,如何为患者带来更好的临床获益,是我们需要讨论的永恒的话题。
1.中国抗癌协会乳腺癌专业委员会. 中国抗癌协会乳腺癌诊治指南与规范(2007版)[J]. 中国癌症杂志, 2007, 19(5):410-428.
2.Finn RS, Crown JP, Lang I, et al. The cyclin-dependent kinase 4/6 inhibitor palbociclib in combination with letrozole versus letrozole alone as first-line treatment of oestrogen receptor-positive, HER2-negative, advanced breast cancer (PALOMA-1/TRIO-18): a randomised phase 2 study[J]. Lancet Oncol. 2015;16:25-35.
3.Finn RS, Crown J, Lang I, et al. Overall survival results from the randomized phase II study of palbociclib (P) in combination with letrozole (L) vs letrozole alone for frontline treatment of ER+/HER2– advanced breast cancer (PALOMA-1; TRIO-18) [J]. J Clin Oncol. 2017;35(15 suppl):abstr 1001.
4.Cristofanilli M, Turner NC, Bondarenko I, et al. Fulvestrant plus palbociclib versus fulvestrant plus placebo for treatment of hormone-receptor-positive, HER2-negative metastatic breast cancer that progressed on previous endocrine therapy (PALOMA-3): final analysis of the multicentre, double-blind, phase 3 randomised controlled trial[J]. Lancet Oncol. 2016;17:425-39.
5.Diéras Véronique, Rugo H S , Patrick S , et al. Long-term Pooled Safety Analysis of Palbociclib in Combination With Endocrine Therapy for HR+/HER2- Advanced Breast Cancer[J]. JNCI: Journal of the National Cancer Institute, 2018.
6.Turner NC, Ro J, Andre F, et al. Palbociclib in hormone-receptor-positive advanced breast cancer[J]. N Engl J Med. 2015;373:209-19.
点击下图即可关注“CDK4/6i学院”专栏:












 苏公网安备32059002004080号
苏公网安备32059002004080号


