
第37例
乳腺癌是女性发病率第一位的肿瘤,目前经过综合治疗后,早期乳腺癌5年生存率有较大的提高,但仍有30%~40%的患者会发生复发转移。HER2+的乳腺癌占所有乳腺癌的20%~25%,这类患者的预后较差,5年生存率仅为46%。HER2+乳腺癌中有50%的患者为HR+。因此,HR+/HER2+的乳腺癌患者约占总体人群的10%。目前HR+/HER2+型晚期乳腺癌治疗方案尚无统一标准,此类患者的治疗方案强调个体化治疗,以使用化疗、靶向治疗、内分泌治疗等多种模式综合治疗为主,本文通过回顾一个HR+/ HER2+ 型乳腺癌患者持续内分泌治疗联合抗HER2治疗长期获益的病例,介绍目前有关该类患者的临床治疗思路。

南方医院肿瘤科主任
广东省医学教育协会肿瘤学专业委员会主任委员
广东省医学会肿瘤内科分会副主任委员
广东省医师协会肿瘤科医师分会副主任委员
广东省抗癌协会靶向与个体化治疗专业委员会常委
广东省药理学会肿瘤药理专业委员会常委
广东省抗癌协会化疗专业委员会委员
中国抗癌协会肿瘤靶向治疗专业委员会委员
中国抗癌协会大肠癌专业委员会内科学组委员

南方医科大学南方医院肿瘤科
2009年中南大学湘雅医院肿瘤学博士毕业
2011—2012美国迈阿密大学访问学者
广东省临床医学会肿瘤专业委员会委员
主持国家自然科学基金1项,发表SCI论文数篇
病史简介
患者女性,现年64岁,发病年龄53岁。2008年2月,患者于我院行“右乳癌改良根治术”。术后病理:(右)乳浸润性导管癌;乳头、四侧切缘、基底切缘未见癌浸润;淋巴结未见癌转移(0/18)。免疫组化:ER(+++),PR(-),HER2(++)(未行FISH检测),EGFR(++),VEGF(+++)。入院诊断:右乳癌改良根治术后(pT2N0M0,IIA期,ER+/PR-/HER2不确定)。
辅助治疗
术后行CAF方案辅助化疗6周期,口服来曲唑2年。
第一次复发
2015年1月,患者于当地医院进行胸部CT检查提示:左肺门(67mm×42mm×40mm)及两肺占位(右下肺32mm×30mm),后至我院胸外科行气管镜下两侧肺肿物活检。病理示:考虑乳腺癌肺转移。免疫组化:CK(+) 、CK5/6(-)、 P63(-) 、TTF-1(-)、 CK7(-) 、Ki-67(+,50%) 、SPA(-) 、CK14(-) 、CEA(+) 、NapsinA(-) 、GCDFP15(-) 、ER(+) PR(-) HER2(3+)。全身骨ECT:第3胸椎、左侧第6肋根浓聚影,考虑骨转移灶可能性大。考虑患者乳腺癌多发转移(rT2N0M1,Ⅳ期),无手术指征。
DFS:7年。
第一次复发后治疗及评价
2015年1月,患者行8周期TXH方案(多西他赛+卡培他滨+曲妥珠单抗)化疗,予伊班膦酸护骨治疗(每4周期1次)。2015年4月复查CT,疗效评价PR。2015年6月、2015年8月复查CT,疗效评价为持续PR。
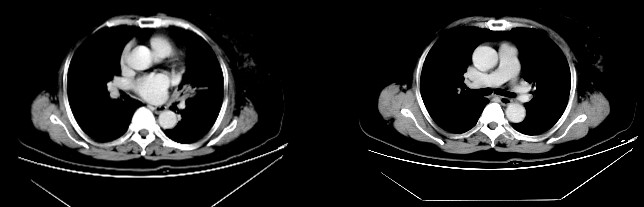
胸部CT(2015年4月)
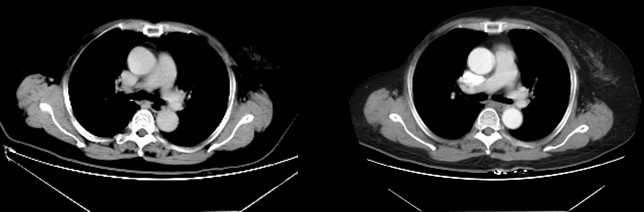
胸部CT(左图,2015年6月;右图,2015年8月)
2015年8月起予“曲妥珠单抗+卡培他滨”维持化疗共7周期,患者出院后卡培他滨单药维持治疗。
第二次进展
2017年3月,患者外院复查胸部CT提示:右肺上叶及右肺中叶多发新发小结节;左肺下舌段病灶变实;左肺下叶结节部分较前增大。
PFS1:26个月 (2015年1月至2017年3月)。
2017年4月,于我院复查骨扫描提示:颅底骨、颈椎上段、双侧锁骨胸骨端、第2和第3腰椎新发浓聚影,考虑新发骨转移灶可能性大。复查CT提示:左肺上叶下舌段支气管旁近肺门处软组织影较前增大;右肺上叶及左肺下叶内基底段新发结节影,考虑为转移瘤。
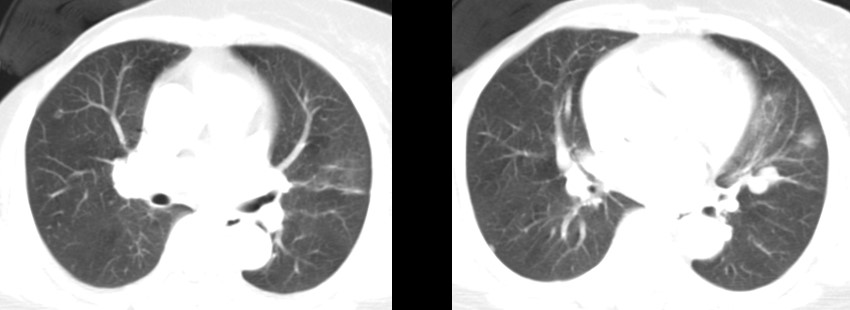
第二次进展后治疗及评价
2017年4月26日起予TCH方案(多西他赛+卡铂+曲妥珠单抗)姑息化疗6周期。其间复查CT提示病情稳定,疗效评价SD。2017年9月起予曲妥珠单抗+阿那曲唑维持治疗。2018年1月复查CT示双肺转移较前增大,病情进展。
PFS2:10个月(2017年3月至2018年1月)。
第三次进展
2018年1月,复查CT示双肺转移较前增大,病情进展。2018年2月1日开始予曲妥珠单抗+多柔比星脂质体化疗共8周期。其间复查CT疗效评估:PR。
2018年8月开始予HX方案(曲妥珠单抗+卡培他滨)维持化疗。
PFS3:超过13个月(2018年1月至今)。
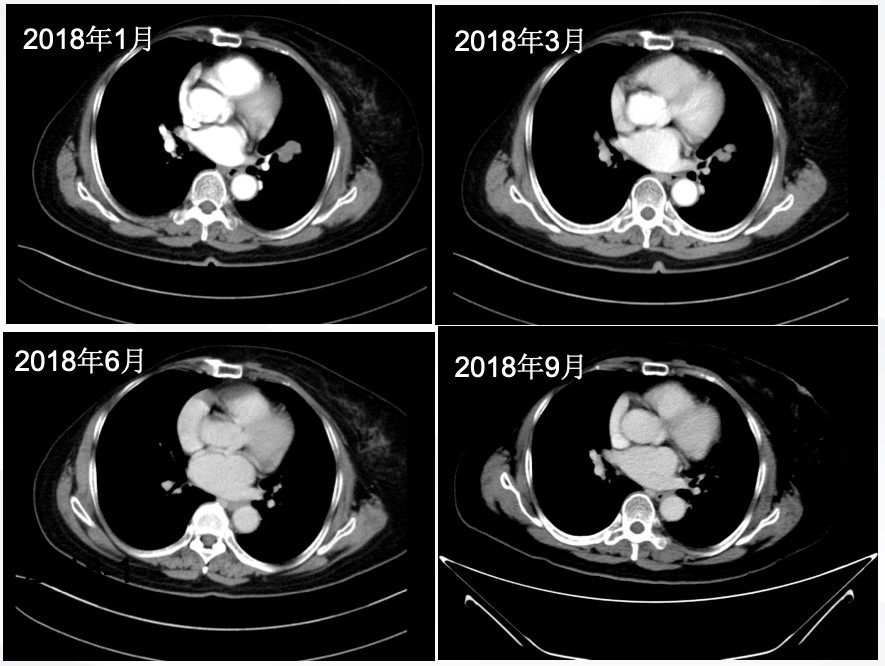
胸部CT
总结
患者中年女性,发病年龄53岁。2008年1月行“右乳癌改良根治术”,术后诊断:右乳癌改良根治术后(pT2N0M0,IIA期,ER+/PR-/HER2不确定)。术后行CAF方案辅助化疗6周期,口服来曲唑2年后停药。2015年1月当地医院胸部CT提示:左肺门(67mm×42mm×40mm)及两肺占位(右下肺32mm×30mm)。后行气管镜下两侧肺肿物活检,病理示:考虑乳腺癌肺转移。免疫组化: ER(+), PR(-),HER2(+++)。全身骨ECT:第3胸椎、左侧第6肋根浓聚影,考虑骨转移灶可能性大。DFS:7年。一线治疗予8周期TXH方案(多西他赛+卡培他滨+曲妥珠单抗)化疗后“曲妥珠单抗+卡培他滨”维持化疗共7周期,后卡培他滨口服维持治疗,并联合伊班膦酸护骨治疗。2017年3月至2017年4月复查胸部CT及骨ECT提示PD,PFS1为26个月。二线治疗予TCH方案姑息化疗6周期。其间复查CT提示病情稳定,疗效评价SD。2017年9月起予曲妥珠单抗+阿那曲唑维持治疗。2018年1月复查CT示双肺转移较前增大,病情进展,PFS2为10个月。三线治疗予曲妥珠单抗+多柔比星脂质体化疗共8周期。其间复查CT疗效评估:PR。2018年8月开始予HX方案(曲妥珠单抗+卡培他滨)维持化疗至今,PFS3超过13个月。

患者治疗历程图
点评专家

任职于国家癌症中心、中国医学科学院肿瘤医院
承担了3项“国家自然科学基金”,1项“863” 课题
获得中国抗癌协会科技奖一等奖、华夏医学科技奖一等奖、中华医学科技奖三等奖、北京市科学技术奖二等奖
中国抗癌协会乳腺癌专业委员会副秘书长
北京乳腺病防治学会国际医疗专业委员会主任委员
中国老年学会肿瘤专业委员会常委
中国医药教育协会乳腺疾病专业委员会常委
北京乳腺病防治学会内科专业委员会常委
点评
患者为中老年女性,既往“右乳改良根治术”病理提示为ⅡA期乳腺癌。回顾之前的治疗,由于药物可及性和患者的依从性,在治疗的全程管理方面,治疗理念基本正确,但从实施情况看,还是有一些值得推敲之处。
HER2+乳腺癌侵袭性强、复发率高,预后不良。临床实践中无论是术后辅助还是晚期解救治疗,抗HER2治疗都有着举足轻重的地位,应该贯穿始终。曲妥珠单抗(trastuzumab)是目前应用最主要、最广泛的抗HER2靶向药物,该药的问世和广泛使用显著改变了HER2阳性乳腺癌的结局。
该患者改良根治术的手术病理提示HER2(++),术后并没有重视HER2的确认检测,错失了乳腺癌辅助治疗中重要的抗HER2治疗这一环节,未能尽早开始术后靶向治疗,在一定程度上未达到可能治愈的最佳治疗,但就当时的年代和药物可及性来说,也是可以理解的。包括HERA研究在内的多项临床研究已经反复证实曲妥珠单抗用于HER2阳性早期的乳腺癌术后辅助治疗,能够显著提高HER2阳性早期乳腺癌的治愈机会,显著降低复发和病死风险。该患者未进行术后的抗HER2靶向治疗,在一定程度上,未获得可能的获益。另外,术后内分泌治疗时间也仅为2年,未达到最佳的治疗时程,这些都可能是造成之后复发转移的原因。
患者出现复发和远处转移后病理检查明确提示HER2(+++),在晚期治疗中采用曲妥珠单抗联合化疗,并在之后进展后选择继续曲妥珠单抗改变化疗方案的曲妥珠单抗的跨线治疗,符合国际和我国的指南。但遗憾的是,在一线治疗取得较好的肿瘤缓解的情况下,没有持续抗HER2治疗,在一定程度上,削弱了前面治疗的疗效,没有达到更长的PFS。目前国际上HER2阳性晚期乳腺癌标准一线治疗方案为帕妥珠单抗、曲妥珠单抗双靶联合多西他赛。2012年获得美国食品药品监督管理局(FDA)批准用于晚期乳腺癌的药物帕妥珠单抗,已获得中国国家药品监督管理局(NMPA)批准上市。
回顾该患者三线的治疗,后线的内分泌治疗联合曲妥珠单抗的治疗是一个亮点。 在晚期患者的治疗中,抗HER2靶向治疗全程使用,联合化疗或内分泌治疗,都可以成为ER+/HER2+患者的选择。化疗和内分泌治疗的交替使用,一方面保证患者的疗效,同时也可患者获得“化疗假期”和较好的生活质量,充分体现了目前晚期乳腺癌的治疗理念,即在控制肿瘤的前提下,提高患者的生活质量,把肿瘤变成“慢性病”。
此病例充分警示,对于HER2阳性乳腺癌往往比HER2阴性肿瘤更具攻击性,早期乳腺癌复发的可能性为HER2阴性肿瘤的2~5倍,即使很小的肿瘤也可能复发转移。该病例基于指南规范,同时又基于临床现实合理调整,患者获得较长时间的生存获益,强调了尽早抗HER2治疗必要性和重要性。











 苏公网安备32059002004080号
苏公网安备32059002004080号


