近年来,免疫治疗研究在全球范围内开展得如火如荼,包括胃癌在内的多项临床研究均取得了令人瞩目的结果。由于具有高特异性和不良反应低等优势,免疫治疗有望开启恶性肿瘤“无化疗”(chemo-free)新时代。本文就肿瘤免疫治疗的作用机制、近期胃癌免疫治疗研究结果解读以及胃癌免疫治疗的未来方向做一综述。

四川大学华西医院肿瘤科(腹部)主任
信号转导及分子靶向治疗研究室主任
中国生物医学工程学会肿瘤分子靶向治疗专委会主任委员
中国生物医学工程学会肿瘤靶向治疗技术分会副理事长
中国老年医学会肿瘤分会副会长
中国医师协会结直肠肿瘤内科治疗专委会副主任委员
中国抗癌协会整合肿瘤分会常委、生物治疗专委会委员
胃癌是严重威胁人类健康与生存的消化道恶性肿瘤之一,我国胃癌发病率高,疾病分期晚,治疗手段有限,化疗和靶向治疗的效果不理想,治疗需求远未被满足。免疫治疗因其独特的作用机制,为这类患者带来了新的希望。
肿瘤免疫治疗作用机制
机体免疫系统可以识别并清除肿瘤微环境中的肿瘤细胞。然而,肿瘤细胞可以通过不同的作用途径,使机体免疫系统受到抑制,不能有效杀伤肿瘤细胞,从而使得肿瘤细胞在抗肿瘤免疫应答过程中幸免,以实现促进肿瘤增殖的目的,即所谓的免疫逃逸。肿瘤免疫治疗是通过重新启动机体免疫系统,恢复机体正常的抗肿瘤免疫反应,从而控制与清除肿瘤的治疗方法。PD-1/PD-L1免疫检查点抑制剂通过阻断PD-1与PD-L1的结合,解除免疫抑制,防止肿瘤逃逸,激活T细胞,发挥肿瘤杀伤功能。目前,免疫检查点抑制剂已在包括黑色素瘤、非小细胞肺癌、肾癌以及胃癌等多种瘤种的治疗中展示出了一定的抗肿瘤活性,开启了恶性肿瘤治疗的新模式。
免疫治疗胃癌领域研究现状
目前国内外批准的靶向PD-1/PD-L1通路的免疫检查点抑制剂一共有7种,其中美国FDA批准上市的有6种,分别为PD-1单抗纳武利尤单抗、帕博利珠单抗和cemiplimab,PD-L1单抗atezolizumab、avelumab和durvalumab。中国获批的有纳武利尤单抗和帕博利珠单抗,以及2个国产PD-1单抗。但获批晚期胃癌适应证的只有纳武利尤单抗和帕博利珠单抗。纳武利尤单抗是在日本、韩国、瑞士、新加坡、中国台湾获批胃癌适应证,帕博利珠单抗则获美国FDA批准胃癌适应证。
关于帕博利珠单抗的研究,Ⅱ期KEYNOTE-059研究队列1入组了259例复发或转移性胃癌或胃食管结合部癌患者,既往都至少接受过2种化疗方案,予以帕博利珠单抗单药治疗2年或直至疾病进展。2017年ESMO上报道的结果[1]显示,客观缓解率达到11.6%,在PD-L1阳性患者中为15.5%,3~5级治疗相关不良事件发生率为18%,安全性总体可控。基于此,美国FDA批准该药用于PD-L1阳性晚期胃或胃食管结合部腺癌的二线及后线治疗。但在2018年ASCO报道的Ⅲ期KEYNOTE-061研究中[2],帕博利珠单抗二线治疗PD-L1阳性的晚期胃癌并未较紫杉醇显著改善总生存期(OS)[9.1个月vs 8.3个月,P=0.0421(单侧)],无进展生存(PFS)在数值上也劣于紫杉醇(1.5个月vs 4.1个月,差异无统计学意义)。帕博利珠单抗组3~5级不良事件发生率低于化疗组(14% vs 35%)。
关于纳武利尤单抗的研究,2017年发表于《柳叶刀》(Lancet)杂志上的随机、双盲、安慰剂对照Ⅲ期研究ATTRACTION-2入组的均为亚洲人群[3],显示纳武利尤单抗用于至少接受过2种化疗方案的晚期胃癌(包括胃食管结合部癌)较安慰剂在客观缓解率(11% vs 0%)、1年OS率(26.2% vs 10.9%)和中位OS(5.3个月 vs 4.1个月,HR=0.63,95% CI 0.51~0.78,P<0.0001)方面都有显著改善,可使死亡风险降低37%,且OS获益不受PD-L1表达状态的影响。在纳武利尤单抗治疗有效的患者中,中位缓解持续时间达9.53个月(95% CI 6.14~9.82个月)。
在2018年的ESMO上,研究者报告了ATTRACTION-2研究的2年随访更新结果[4]。纳武利尤单抗较安慰剂治疗组的OS优势继续保持,2年OS率达安慰剂组的3倍多,分别为10.6% 和3.2%(图1)。进一步按应答状态行亚组分析发现:在完全缓解(CR)或部分缓解(PR)患者亚组中,纳武利尤单抗组的中位OS为26.6个月,1年OS率为87.1%,2年OS率61.3%(图2),而安慰剂组无一例患者获得CR或PR,仅有3例患者达到疾病稳定(SD)。值得注意的是,经过2年的随访发现,纳武利尤单抗组中出现了3例CR患者,其中2例患者经肿瘤检测为微卫星稳定(MSS)患者。此外,纳武利尤单抗组中生存期超过2年的患者中有65.5%(19/29)获得CR或PR,而安慰剂组中仅有获得SD的3例患者生存期超过2年。安全性结果显示,接受纳武利尤单抗治疗的患者,治疗相关不良事件多在前3个月内出现,多为皮肤反应和胃肠道反应,第6个月、12个月和24个月及以后的不良事件发生率很低,且无新的治疗相关不良事件发生。总体来讲,接受纳武利尤单抗治疗的不良事件临床可控。
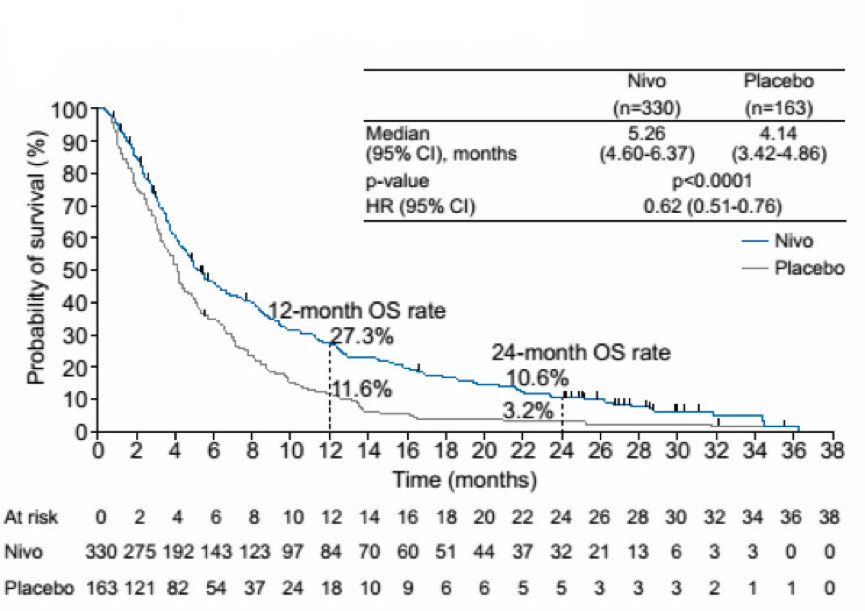
图1.ATTRACTION-2研究的2年OS结果
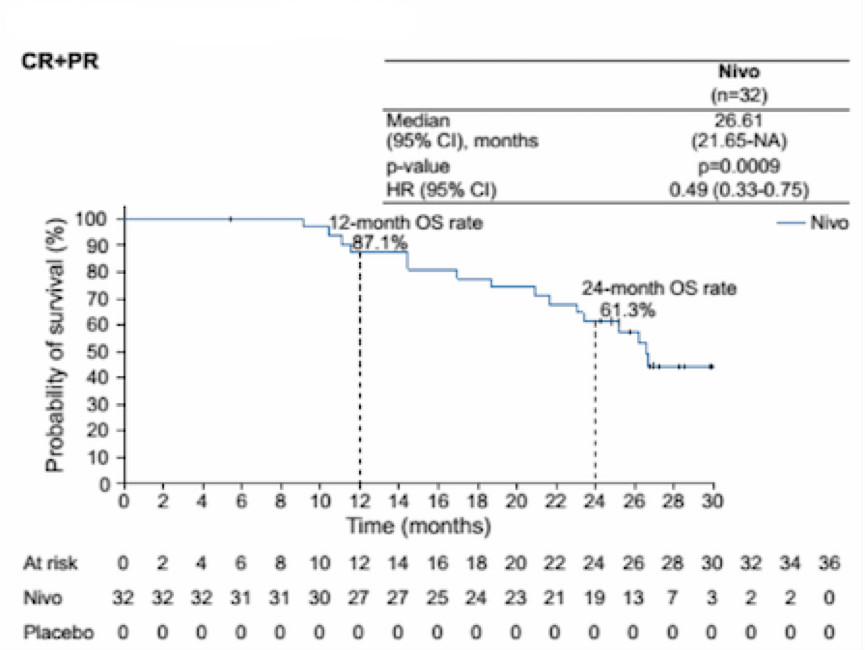
图2.ATTRACTION-2研究中获CR和PR患者的OS结果
胃癌免疫治疗的未来方向
免疫检查点抑制剂在单药治疗晚期胃癌的临床研究中显示出良好的疗效和安全性结果,而且在治疗有效的患者中抗肿瘤作用持久。未来的研究应进一步探索如何根据分子生物学标志物及疾病特征筛选最适合免疫治疗的患者,以及考虑如何将免疫治疗与现有治疗手段如化疗、靶向治疗联合,甚至免疫治疗联合免疫治疗,实现治疗获益的最大化,为晚期胃癌患者带来新希望。
参考文献
1. WAINBERG Z A, JALAL S, MURO K, et al. KEYNOTE-059 update: efficacy and safety of pembrolizumab alone or in combination with chemotherapy in patients with advanced gastric or gastroesophageal (G/GEJ) cancer[R]. 2017 ESMO Abstract LBA-28.
2. FUCHS C S, et al. Pembrolizumab (pembro) vs paclitaxel (PTX) for previously treated advanced gastric or gastroesophageal junction (G/GEJ) cancer: phase 3 KEYNOTE-061 trial[R]. 2018 ASCO Abstract 4062.
3. KANG Y K, BOKU N, SATOH T, et al. Nivolumab in patients with advanced gastric or gastro-oesophageal junction cancer refractory to, or intolerant of, at least two previous chemotherapy regimens (ONO-4538-12, ATTRACTION-2): a randomised, double-blind, placebo-controlled, phase 3 trial[J]. Lancet, 2017,390(10111):2461-2471.
4. SATOH T, CHEN L T, KANG Y K, et al. phase III study of nivolumab (nivo) in previously treated advanced gastric or gastric esophageal junction (G/GEJ) cancer (ATTRACTION-2): two-years update data[R]. 2018 ESMO Abstract 617PD.
内容由百时美施贵宝赞助
NP/IO/3799/02/28/19-02/28/20












 苏公网安备32059002004080号
苏公网安备32059002004080号


