第二届“35 under 35”CSCO-良医汇2018优秀青年肿瘤医师风采大赛评选活动”报名及筛选阶段已正式结束!在众多参与报名筛选的医生中,有100位优秀青年医生脱颖而出!他们将在近期进行三轮PK,展示青年医生风采!第一轮为ASCO最新摘要解读,候选人在主办方指定的2018ASCO口头报告专题中自由选择一份口头报告进行点评(如:背景,结果的评价,对临床的意义,和其他研究的对照,优点和不足等等),目前100位青年医生在规定的时间内已将解读提交,解读很精彩,现展示出来,供各位品读!欢迎转发,让更多的医生同道看到青年力量!欢迎评论,发表您的见解,与青年医师同台论道!

解读三项ASCO 2018“HER2阳性乳腺癌新辅助治疗领域”研究:精准基因诊断如何辅助临床实践获取最高水平的pCR率?精准基因诊断如何辅助“去化疗化”新辅助降阶梯(de-escalation)治疗研究的发展?
在ASCO 2018新辅助治疗板块中,三项涉及HER2阳性乳腺癌新辅助治疗的研究引起笔者极大兴趣。HER2阳性乳腺癌历来是新辅助治疗理念发展的领头羊。这三项同质性研究以一种递进的方式提出了2个具有前景的发展方向。第一,精准基因诊断的价值应引起临床实践的足够重视。在当前抗HER2治疗水平下,我们依靠精准基因诊断可以达到70-80%的pCR率水平。第二,精准基因诊断的价值应引起新辅助“降阶梯(de-escalation)”治疗研究的足够重视。依赖基因诊断,未来可期40-50% HER2阳性乳腺癌新辅助治疗可以”去化疗化“。
Abstract 580:NSABP B-41系列研究:HER2阳性乳腺癌的基因本质分型(Intrinsic subtype)及其与病理完全缓解(pCR)、远期预后的相关性。
背景及目的:NSABP B-41研究纳入529例HER2阳性乳腺癌,随机接受新辅助化疗联合三种不同的靶向治疗(曲妥珠单抗 vs 拉帕替尼 vs 二者联合)。三组亚组间未见pCR率的统计学差异,而获得pCR者的总生存(overall survival,OS)显著优于未获得者。本研究基于NSABP B-41纳入人群,旨在分析HER2阳性乳腺癌中基因本质分型与临床结局的相关性。
方法:采用“RUO-PAM50”CodeSet(NanoString Technologies)判定基因本质分型。定义pCR为ypT0/isypN0(乳腺及腋窝淋巴结无浸润癌残留,乳腺内允许DCIS残留),使用contingence-table分析比较不同分型间的pCR率差异。使用Kaplan-Meier曲线及Cox回归分析比较不同分型间的无事件生存(event-free survival,EFS)及OS差异。
结果:271例HER2阳性乳腺癌中,197例(73%)为HER2-enriched型(97例ER阴性,100例ER阳性),26例(10%)为Basal like型,23例(8%)为Luminal A型,25例(9%)为Luminal B型。HER2-enriched型pCR率为61%,其中ER阴性者为69%,ER阳性者为53%。HER2-enriched型pCR率显著高于其它亚型(Basal like及Luminal A/B型)(61% vs 26%,P < 0.001)。在HER2-enriched型中,含曲妥珠单抗方案两组的pCR率显著高于单用拉帕替尼组(67% vs 49%, P = 0.02)。Basal like型较Luminal A/B型具有更高的pCR率(38.5% vs 13% & 24%)。Basal like型较HER2-enriched型及Luminal A/B型具有更差的远期预后(5年EFS = 0.724,[0.506 - 0.858],P = 0.28;5年OS = 0.808,[0.598 - 0.915],P = 0.005)。在HER2-enriched型中,三组不同靶向治疗亚组间未见EFS、OS的统计学差异。
结论:HER2-enriched型为预测抗HER2治疗疗效的获益亚型,在以曲妥珠单抗为基础的治疗中则有更大获益。在HER2阳性乳腺癌中,基因诊断为其它本质分型的乳腺癌是否需要抗HER2治疗尚需进一步研究。鉴于本研究样本量小及预后事件少的缺陷,远期预后的相关结论需要更多类似研究予以佐证。
Abstract e12634:HER2阳性早期乳腺癌新辅助化疗联合双靶向治疗(曲妥珠单抗+帕妥珠单抗):不同PAM50基因本质分型(Intrinsic subtype)具有不同的病理完全缓解(pCR)率。
背景及目的:本研究纳入免疫组织化学(IHC)诊断的HER2阳性乳腺癌,采用PAM50基因表达分析判定基因本质分型,比较在不同分型中新辅助化疗联合双靶向治疗(曲妥珠单抗+帕妥珠单抗)较联合曲妥珠单抗的pCR率获益情况。
方法:连续性纳入219例IHC诊断的I-IIIC期HER2阳性乳腺癌,A组患者(N = 128)接受新辅助化疗联合曲妥珠单抗,B组患者(N = 91)接受新辅助化疗联合双靶向治疗(曲妥珠单抗+帕妥珠单抗)。使用PAM50基因表达分析判定基因本质分型。采用卡方检验比较不同分型间的pCR率差异(pCR定义模糊,原摘要仅描述评测范围为乳腺+腋窝淋巴结),采用Logistic回归进行多因素分析。
结果:纳入患者的临床病理及基因本质分型特点见表1。在整体人群中,新辅助化疗联合双靶向治疗的pCR率显著高于联合曲妥珠单抗者(66% vs 39%,P = 0.0002)。在HER2-enriched型中,联合双靶向治疗的pCR率显著高于联合曲妥珠单抗者(77% vs 50%,P = 0.002)。在Luminal型中,联合双靶向治疗的pCR率显著高于联合曲妥珠单抗者(54% vs 11%,P = 0.0007)。在整体人群的多因素分析中,更高的pCR率与联合双靶向治疗显著相关(P = 0.00015,OR = 3.22),与临床病理特点不相关(P > 0.05)。亚组分析显示,在HER2-enriched型(P = 0.00168,OR = 3.11)及Luminal型(P = 0.0045,OR = 23.35)中,更高的pCR率与联合双靶向治疗显著相关。
结论:在本研究中,HER2-enriched型乳腺癌新辅助化疗联合双靶向治疗(曲妥珠单抗+帕妥珠单抗)可获得最高的pCR率。在Luminal型中,联合双靶向治疗较联合曲妥珠单抗可显著提高pCR率。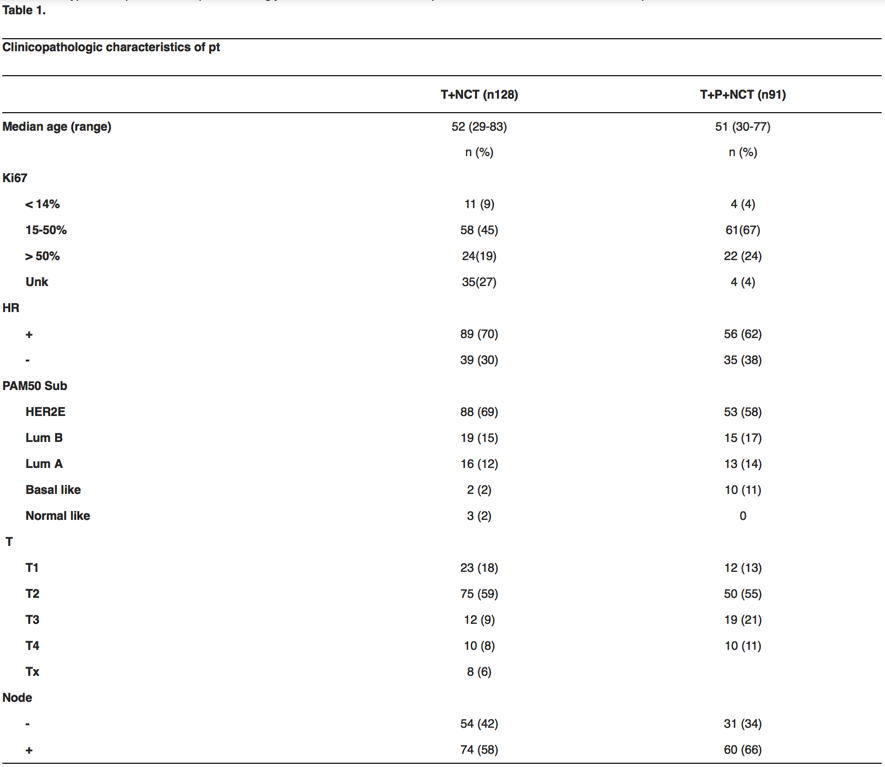
Abstract 509:TBCRC006/023及PAMELA试验的联合分析研究:HER2-enriched基因本质分型(Intrinsic subtype)及ERBB2 mRNA表达水平预测HER2阳性早期乳腺癌新辅助双靶向治疗(曲妥珠单抗+拉帕替尼,无化疗)的 病理完全缓解(pCR)率。
背景及目的:在HER2阳性乳腺癌中,HER2-enriched基因本质亚型具有ERBB2及相关基因高表达的特征。本研究回顾性分析TBCRC006/023及PAMELA试验人群,旨在分析HER2-enriched型和或ERBB2 mRNA表达水平预测pCR率的价值。
方法:纳入病例均为HER2阳性早期乳腺癌且接受新辅助双靶向治疗(曲妥珠单抗+拉帕替尼,无化疗)。激素受体阳性患者接受来曲唑或他莫昔芬内分泌治疗。TBCRC006试验(NCT00548184)纳入66例患者治疗12周,TBCRC023试验(NCT00999804)随机化分配97例患者治疗12或24周,PAMELA试验(NCT01973660)纳入151例患者治疗18周。本研究定义pCR为ypT0/is(乳腺内无浸润癌残留,可伴有DCIS残留,评测范围不包括腋窝淋巴结)。使用nCounter-based PAM50 predictor判定基因本质分型及测定ERBB2 mRNA表达水平。
结果:纳入分析的265例肿瘤中65.7%为HER2-enriched型。HER2-enriched型pCR率显著高于非HER2-enriched型(35.1% vs 9.9%,odds ratio [OR] = 4.92,95% CI 2.31-10.50,P < 0.001)。ERBB2 mRNA高水平者pCR率显著高于低水平者(36.1% vs. 8.2%,OR = 6.51,95% CI 2.96-14.31,P < 0.001)。84.0% ERBB2 mRNA高水平者为HER2-enriched型,46.0% ERBB2 mRNA低水平者为HER2-enriched型。HER2-enriched/ERBB2 mRNA高水平型,非HER2-enriched/ERBB2 mRNA高水平型,HER2-enriched/ERBB2 mRNA低水平型及非HER2-enriched/ERBB2 mRNA低水平型pCR率分别为45.0%,16.1%,10.8%及6.7%。在多因素分析中,HER2-enriched/ ERBB2 mRNA高水平型是高pCR率的独立预测因素(adjusted OR = 6.0,95% CI [3.1-11.8],P< 0.001)。
结论:联合分析HER2-enriched亚型及ERBB2 mRNA表达水平更能确定HER2阳性乳腺癌抗HER2治疗的敏感性。接近50%的HER2-enriched/ERBB2 mRNA高水平型乳腺癌接受“无化疗”的新辅助治疗获得了pCR。未来此类患者在新辅助治疗中,有望接受到合理的“降阶梯(de-escalation)”治疗。
点评:
研究背景:
针对乳腺癌新辅助治疗,传统理念认为其适应症在于降期保乳或降期提高根治性手术的切除率。此种适应症的选择遵循新辅助治疗后外科手术的“降阶梯 (de-escalation)”治疗理念,依赖于新辅助治疗的“降期”疗效判定。在新辅助治疗疗效判定标准中,“降期为0期”即病理完全缓解(pathological complete response,pCR)成为研究最为广泛的判定指标。在随机对照试验中,试验组与对照组间的pCR率提高尚不能和同一试验组与对照组随访的预后(EFS/OS)改善建立线性关系,这使得pCR率在试验水平(Trail Level)尚不能成为预后(EFS/OS)的替代终点(surrogate endpoint)[1-3]。然而,临床实践关注的焦点在于获得pCR的乳腺癌患者究竟有着怎样的预后。目前,高质量循证医学证据表明,获得pCR的患者预后显著优于非pCR者[3]。在患者水平(Patient Level),新辅助治疗后判定为pCR或非pCR可以为分层患者预后带来确定的信息[3]。
新辅助治疗疗效差异带来的预后分层促使大量学者思考两个问题:1、如何提高新辅助治疗的pCR率?2、降低新辅助治疗水平可否获得令人满意的pCR率,何种患者接受新辅助“降阶梯(de-escalation)”治疗就能达到pCR?
此次解读的3项研究针对HER2阳性乳腺癌新辅助治疗,从基因诊断的角度为解决这两个问题提供了更多的思路。
研究启示1:约30% HER2受体阳性乳腺癌为基因诊断层面的Luminal型或Basel like型
基因表达分析将乳腺癌归类为Luminal A,Luminal B,HER2-enriched 及Basal like四类本质亚型(Intrinsic subtype),此种分型既实现了乳腺癌的精准诊断又代表了乳腺癌的生物学本质、临床病理特征及远期预后[4,5]。临床替代分型则选取易于检测的免疫组化指标(ER、PR、HER2等)进行乳腺癌分类,旨在达到与基因本质分型良好的吻合度。然而,高质量循证医学证据表明,免疫组化替代分型不能实现基因层面的精准诊断,两者存在最高可达50%的不吻合率[6]。
此次解读研究带来的第一个启示:HER2阳性乳腺癌(临床检测HER2受体蛋白阳性)中存在不同的基因本质分型。三项研究均使用PAM50基因表达分析判定基因本质分型。研究一271例HER2阳性乳腺癌中,197例(73%)为HER2-enriched型,26例(10%)为Basal like型,23例(8%)为Luminal A型,25例(9%)为Luminal B型。研究二219例HER2阳性乳腺癌中,141例(64%)为HER2-enriched型,34例(16%)为Luminal B型,29例(13%)为Luminal A型,12例(6%)为Basal like型(数据见摘要表一)。研究三265例HER2阳性乳腺癌中,174例(65.7%)为HER2-enriched型。
汇总三项研究,755例HER2阳性乳腺癌中512例(68%)为HER2-enriched型,其余32%则分布于Luminal型及Basel like型中。回顾临床实践,可以推测约30% HER2阳性乳腺癌并非HER2-enriched型,不具有HER2相关基因高表达的特征,可能为Luminal型甚至Basel like型。针对此类HER2受体阳性而非HER2-enriched型乳腺癌,抗HER2治疗及化疗的获益情况值得进一步研究。
研究启示2:基因诊断为HER2-enriched型乳腺癌可达到70-80%的pCR率水平
在新辅助治疗领域,不同临床替代分型的乳腺癌具有差异显著的pCR率,HER2阳性乳腺癌为其中易获得高pCR率的亚型[3]。2014年,新辅助乳腺癌协作试验国际工作组(Collaborative Trials in Neoadjuvant Breast Cancer,CTNeoBC)纳入10项随机性研究共计9440例新辅助治疗乳腺癌,定义pCR为ypT0/isypN0(乳腺及腋窝淋巴结无浸润癌残留,乳腺内允许DCIS残留),1172例仅接受新辅助化疗的HER2阳性乳腺癌pCR率为23.0%,749例接受联合曲妥珠单抗新辅助化疗的HER2阳性乳腺癌pCR率为40.3%[3]。2012年,NeoSphere II期临床试验纳入417例HER2阳性乳癌,定义pCR为ypT0/is(乳腺内无浸润癌残留,可伴有DCIS残留,评测范围不包括腋窝淋巴结),新辅助化疗联合双靶向治疗(多西他赛+帕妥珠单抗+曲妥珠单抗)组患者107例,pCR率为45.8%(95% CI=36.1% - 55.7%)[7]。2017年,GeparSepto III期临床试验入组HER2阳性乳腺癌接受新辅助化疗(紫杉类序贯表柔比星+环磷酰胺)同时联合双靶向治疗(曲妥珠单抗+帕妥珠单抗)。该研究定义pCR为ypT0ypN0(乳腺及腋窝淋巴结无浸润癌残留,乳腺内不允许DCIS残留),229例HER2阳性乳腺癌pCR率为57.8%(95% CI=53.0% - 62.7%)[8]。总结以上研究可以发现,HER2阳性乳腺癌的pCR率从20%水平提高到了60%水平。这依赖于两点:1、抗HER2治疗水平的进步,双靶向治疗优于单靶向治疗;2、联合化疗方案的优化选择。除治疗水平的进步之外,是否有其余研究方向可以为提高HER2阳性乳腺癌的pCR率提供更多思路?
此次解读研究带来的第二个启示:依靠基因诊断,可以在HER2阳性乳腺癌中诊断出HER2-enriched型乳腺癌,联合高水平的新辅助化疗可以进一步获得更高的pCR率。研究一197例HER2-enriched型乳腺癌接受了含曲妥珠单抗或拉帕替尼的新辅助化疗,该研究定义pCR为ypT0/isypN0,曲妥珠单抗组pCR率显著高于拉帕替尼组(67% vs 49%,P = 0.02)。研究二摘要未详细描述pCR定义,可能定义为ypT0/isypN0或ypT0ypN0。88例接受新辅助化疗联合曲妥珠单抗的HER2-enriched型乳腺癌pCR率为50%,53例接受新辅助化疗联合曲妥珠单抗+帕妥珠单抗的HER2-enriched型乳腺癌pCR率为77%(P = 0.002)。
综合以上研究,在准确定义的HER2-enriched基因分型中,新辅助化疗联合曲妥珠单抗有望获得60-70%的pCR率,新辅助化疗联合曲妥珠单抗+帕妥珠单抗有望获得70-80%的pCR率。提高HER2阳性乳腺癌的pCR率,既依靠抗HER2治疗水平的进步,也依赖于基因诊断带来的精准分型。
研究启示3:约40-50% HER2-enriched且ERBB2 mRNA表达高水平患者有望在未来接受“去化疗化”的新辅助“降阶梯(de-escalation)”治疗。
在HER2阳性乳腺癌新辅助治疗领域,新辅助化疗联合抗HER2治疗为标准治疗方式。2012年,NeoSphere II期临床试验一组患者仅接受了新辅助双靶向治疗(曲妥珠单抗+帕妥珠单抗)而无术前化疗,107例病例最终pCR率为16.8%(95% CI=10.3% - 25.3%)[7]。这提示了学者及临床实践,足够水平的抗HER2治疗或许可以使部分HER2 阳性乳腺癌免于化疗。如何定位此类患者成为后续研究热点。2017年,PAMELA II期临床试验纳入151例HER2阳性乳腺癌,所有患者均接受18周新辅助双靶向治疗(曲妥珠单抗+拉帕替尼,无化疗),激素受体阳性患者额外接受来曲唑或他莫昔芬内分泌治疗。该研究定义pCR为ypT0/is,总体pCR率为30%。研究者使用PAM50基因表达分析判定基因本质分型,101例HER2-enriched型乳腺癌pCR率为41%(95% CI = 31% - 51%),50例非HER2-enriched型pCR率为10%(95% CI = 4% - 23%)(OR = 6.2,95% CI = 2.3 - 16.8,P = 0.0004)[9]。PAMELA研究提示:在HER2阳性乳腺癌“去化疗降阶梯(de-escalation)”的新辅助治疗研究中,基因诊断为HER2-enriched亚型为未来更有可能获益的类型。
研究三为一项基于TBCRC006/023及PAMELA试验人群的联合分析研究,纳入HER2阳性乳腺癌均接受只含有曲妥珠单抗和拉帕替尼的新辅助双靶向治疗(无化疗)。研究者使用PAM50分析其基因表达及ERBB2 mRNA表达水平,pCR定义为ypT0/is。HER2-enriched/ERBB2 mRNA高水平型,非HER2-enriched/ERBB2 mRNA高水平型,HER2-enriched/ERBB2 mRNA低水平型及非HER2-enriched/ERBB2 mRNA低水平型pCR率分别为45.0%,16.1%,10.8%及6.7%。在多因素分析中,HER2-enriched/ ERBB2 mRNA高水平型是高pCR率的独立预测因素(adjusted OR = 6.0,95% CI [3.1-11.8],P< 0.001)。
研究三及PAMELA研究表明,HER2阳性乳腺癌“去化疗降阶梯(de-escalation)”新辅助治疗具有研究前景。在PAMELA研究基础上,研究三进一步表明:约40-50% HER2-enriched型伴ERBB2 mRNA表达高水平的患者在未来有望免于接受化疗。
研究缺陷:
1、研究一在HER2-enriched型中,含曲妥珠单抗方案两组的pCR率显著高于单用拉帕替尼组(67% vs 49%,P = 0.02),但三组亚组随访5年EFS/OS未见统计学差异。需要强调,pCR率比较的是两组:含曲妥珠单抗组(包括单用曲妥珠单抗,曲妥珠单抗+拉帕替尼)与单用拉帕替尼组,研究得出了统计学显著的结果。然而,5年EFS/OS却是比较的三组间的差异,研究得出无统计学差异。研究一摘要未报道在HER2-enriched型中,三组亚组的pCR率比较结果;亦未报道含曲妥珠单抗的两组与单用拉帕替尼组间的5年EFS/OS比较结果。此为缺陷一。因为此种比较方式令人疑惑,并难以解释:随机对照试验中亚组间的pCR率提高与最终亚组间的预后改善的相关性。事实上,这种相关性的论证隶属于pCR“替代终点”(Surrogate Endpoint)理论范畴。从现有研究而言,目前pCR率水平仍多处于20-50%水平,随机对照试验中亚组间显著的pCR率提高容易获得,并一般会转换为最终亚组间的预后改善。但当代乳腺癌治疗的EFS/OS已达到很高水平(80-90%水平),这种预后改善能否达到统计学显著的程度需要考虑多种因素,例如入组患者是否预后高危、样本量是否足够大及随访时间是否足够长等。这也反应出研究一第二个缺陷,样本量少会导致预后事件少,亚组间令人兴奋的pCR率差异往往仅能转换为EFS/OS不达统计学显著的获益。
2、在研究二中,Luminal型新辅助化疗联合双靶向(曲妥珠单抗+帕妥珠单抗)较单靶向曲妥珠单抗显示出更高的pCR率(54% vs 11%,P = 0.0007),多因素分析也显示更高的pCR率与联合双靶向治疗显著相关(P = 0.0045,OR = 23.35)。因此研究得出结论:在Luminal型中,联合双靶向治疗较联合曲妥珠单抗可显著提高pCR率。理解此项结论需要具体分析摘要表一数据,可以看到双靶向治疗组Luminal型仅28例(pCR率54%),单靶向组Luminal型为35例(pCR率11%)。在统计学意义上讲,如此少的亚组进行多因素分析是否合适值得商榷,此外多因素分析结果为统计学边缘性显著(P = 0.0045,OR = 23.35,未报道可信区间)。这反应出研究二一大缺陷,排除占比最大的HER2-enriched型,其余亚型乳腺癌病例较少。对比非HER2-enriched亚型间pCR率难以得出其抗HER2治疗的确定疗效信息。在HER2阳性乳腺癌中, Luminal型双靶向较单靶向抗HER2 治疗显著获益的趋势尚需大样本研究予以佐证。但这种趋势却提出了一个值得思考的问题:HER2受体蛋白阳性/非HER2-enriched型能否通过加强靶向治疗水平的方式提高抗HER2治疗疗效?
3、三项研究均获得了令人兴奋的pCR率水平。然而必须强调,新辅助治疗疗效判定标准为pCR率,采用不同pCR定义会直接影响研究结果。研究一采用了更为严格的pCR定义(ypT0/isypN0);研究二摘要未详细描述pCR定义,不能分辨出是ypT0/isypN0还是ypT0ypN0;研究三使用了最易获得高pCR率的定义(ypT0/is)。从横向对比新辅助治疗疗效而言,新辅助治疗研究应采用统一的pCR定义或者报道多个公认定义的pCR率水平。从保护“去化疗降阶梯(de-escalation)”新辅助治疗研究的角度而言,采用ypT0/is定义更易获得高pCR率水平,激发研究者动力进而促进研究发展。
【温馨提示】:如果您觉得刘世伟医生解读的好,请在下方为他点赞并将文章分享给更多的同道!当然,您也可以在下方留下您的个人见解哦!
[1] Berruti A, Amoroso V, Gallo F, et al. Pathologic complete response as a potential surrogate for the clinical outcome in patients with breast cancer after neoadjuvant therapy: a meta-regression of 29 randomized prospective studies. J. Clin. Oncol. 2014;32:3883–91.
[2] Korn EL, Sachs MC, McShane LM. Statistical controversies in clinical research: assessing pathologic complete response as a trial-level surrogate end point for early-stage breast cancer. Ann. Oncol. 2016;27:10-15.
[3] Cortazar P, Zhang L, Untch M, et al. Pathological complete response and long-term clinical benefit in breast cancer: the CTNeoBC pooled analysis. Lancet. 2014;384:164–72.
[4] Perou CM, Sørlie T, Eisen MB, et al. Molecular portraits of human breast tumours. Nature. 2000;406(6797):747-52.
[5] Sorlie T, Tibshirani R, Parker J, et al. Repeated observation of breast tumor subtypes in independent gene expression data sets. Proc Natl Acad Sci. 2003;100(14):8418-23.
[6] Cancer Genome Atlas Network. Comprehensive molecular portraits of human breast tumours. Nature. 2012;490(7418):61-70.
[7] Gianni L, Pienkowski T, Im Y-H, et al. Efficacy and safety of neoadjuvant pertuzumab and trastuzumab in women with locally advanced, inflammatory, or early HER2-positive breast cancer (NeoSphere): a randomised multicentre, open-label, phase 2 trial. Lancet Oncol. 2012;13:25–32.
[8] S. Loibl, C. Jackisch, A. Schneeweiss, et al. Dual HER2-blockade with pertuzumab and trastuzumab in HER2-positive early breast cancer: a subanalysis of data from the randomized phase III GeparSepto trial. Ann Oncol. 2017;28(3):497-504.
[9] Llombart-Cussac A, Cortés J, Paré L, et al. HER2-enriched subtype as a predictor of pathological complete response following trastuzumab and lapatinib without chemotherapy in early-stage HER2-positive breast cancer (PAMELA): an open-label, single-group, multicentre, phase 2 trial. Lancet Oncol. 2017;18(4):545-554.
41本,27种肿瘤,63万字的【肿瘤患者指南丛书】,赶紧扫描或识别下方二维码,即可免费拥有!











 苏公网安备32059002004080号
苏公网安备32059002004080号


