随着基因组学的研究进展,我们对肿瘤分子生物学机制有了更深的了解。乳腺癌目前主要基于病理指导下的分子分型来进行治疗。对于三阴性乳腺癌(TNBC)和难治性耐药性乳腺癌(如内分泌治疗耐药后的激素受体阳性乳腺癌及曲妥珠单抗等耐药后的HER2阳性乳腺癌),缺乏高效的治疗靶点,亟需基因组学的研究,探寻潜在的治疗靶点。Foundation Medicine(以下简称FMI)针对实体瘤的全面基因组测序(CGP)产品可一次检测315个基因,同时还可以提供TMB(肿瘤突变负荷)及MSI信息,此外,FMI还针对血浆样本建立的检测平台。CGP检测在发现新的治疗靶点,探寻耐药机制及预后生物标志物等方面提供了重要信息。以下汇总今年ASCO和ESMO会议上CGP用于乳腺癌的研究新进展。
(一)转移性乳腺癌(MBC)患者循环肿瘤DNA (ctDNA) 基因组测序分析
摘要号1016 转移性乳腺癌(mBC)患者循环肿瘤DNA基因组测序分析
在2017年的ASCO年会上,有一项研究评估临床实践中采用ctDNA进行基因测序的可行性。mBC进展过程中会发生克隆进化和治疗方案的改变,凸显了对近期标本进行基因组测序分析以指导临床决策制定的重要性。这项研究分析了mBC患者临床治疗过程中ctDNA的基因组变异(GAs)特点。
2016年5月至2017年3月,作为常规临床护理的一部分,临床医生采集了328例乳腺癌患者的外周血标本。采用基于杂交捕获的方法,对62个基因进行标本的多重测序(Illumina HiSeq 2500),中位覆盖深度为7503X。所有的试验操作均在FMI实验室进行(实验室得到CLIA认证、纽约州许可、CAP认证)。同时,计算最大体细胞等位基因丰度(MSAF)以估计血液中的ctDNA丰度(fraction),研究共检测了328患者,其中ER+的患者254例,ER-的患者74例。患者的临床特征总结见下表1。
表1. 患者的临床特征
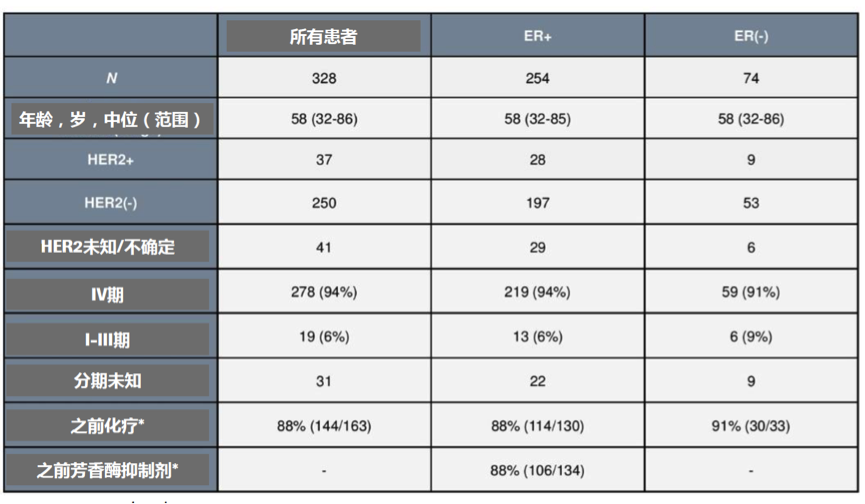
结果显示,77%(253/328)的病例至少有1个GA,平均每个病例有2.8个GA。84%(277/328)的病例血液中有ctDNA存在的证据(MSAF>0)。ER+、ER-和HER2+乳腺癌患者的基因组变异如下图2。检出的与乳腺癌靶向治疗应答相关的基因变异包括PIK3CA、ESR1、ERBB2、FGFR1、BRCA1、BRCA2、EGFR和AKT1。在1%的ER+病例中观察到激酶融合,如NCOA4-RET、FGFR2-INA、FGFR3-TACC3。此外,还在ER+/HER2-(34%)和ER+/HER2+(25%)的乳腺癌患者中均观察到ESR1基因组变异。
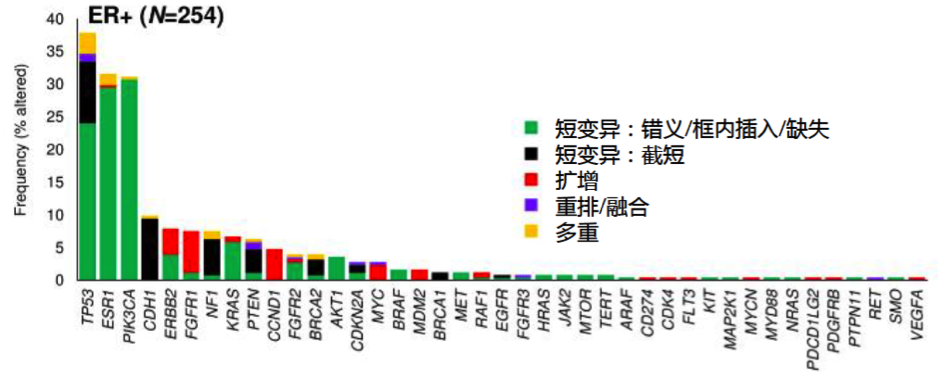
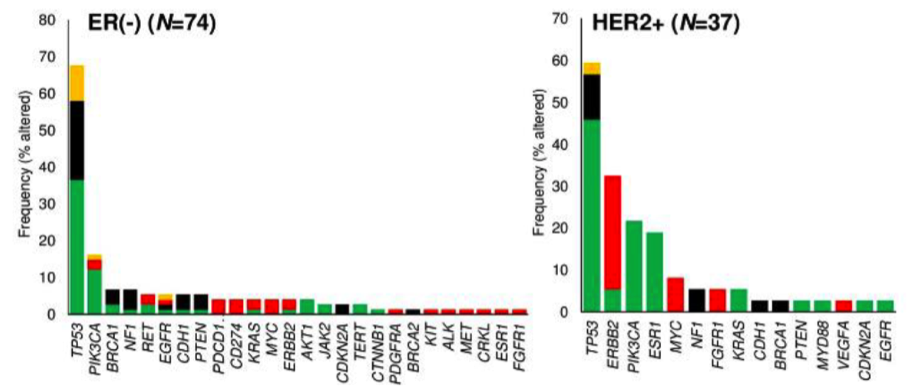
图2. ER+、ER-和HER2+乳腺癌患者的基因组变异
进一步分析本研究中ER+患者(N=254)ctDNA中观察到的最常见的突变(图3左图)和融合基因(图3右图),并比较其与组织基因组数据集的差异。用于比较的ER+乳腺癌组织数据集分别来自:Foundation Medicine数据库(N=851)和已发表的早期乳腺癌(eBC,TCGA:N=594)和晚期乳腺癌(Lefebvre等,PMID:28027327,N=143; Fumagalli等,PMID:27672107,N=182)组织研究。结果显示,在乳腺癌ctDNA中观察到的突变频率与数个组织基因组数据集相似。
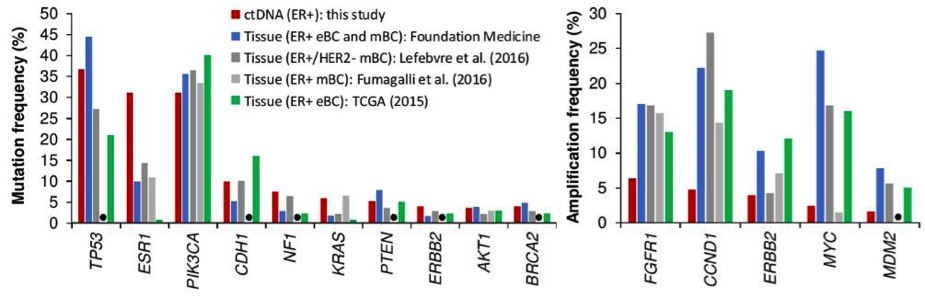
图3. 比较ER+乳腺癌的ctDNA和组织基因组数据集(黑点代表在PMID:27672107中未评估的基因)
比较14例患者的ctDNA和配对的肿瘤组织中发现的基因组变异,ctDNA和组织收集之间的相隔天数如下图所示。结果显示,94%的在组织中检出的突变,在ctDNA中也检出。
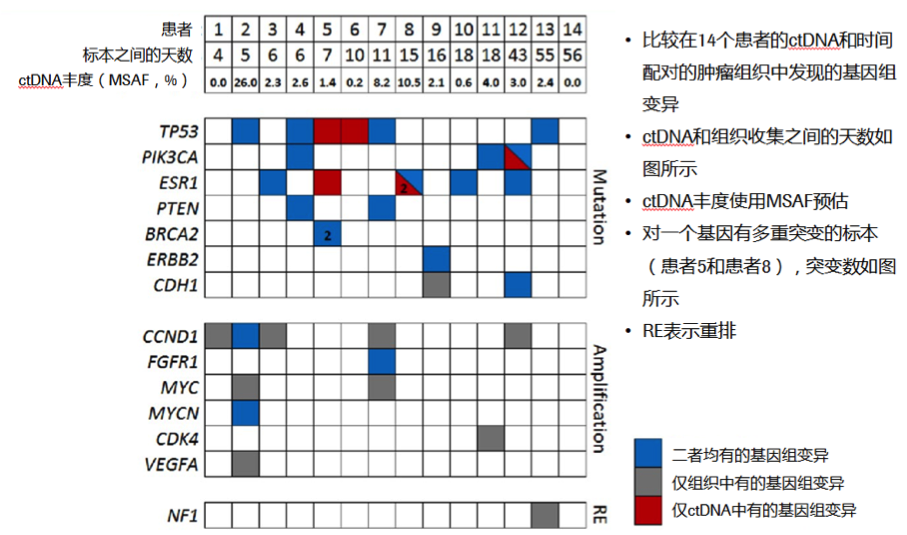
图4. 比较ctDNA和时间配对的组织标本
研究同时计算了MSAF以预估ctDNA丰度。对传统方法(IHC 或者FISH)判定为HER2阳性病例,基于ctDNA 检测有或没有检出ERBB2扩增的病例的MSAF如下图5所示。对所有病例,有或没有检出至少一个扩增的病例的MSAF如图5所示。检出ERBB2扩增的病例的MSAF显著高于无扩增病例(P<0.001),提示可靠的扩增检测需要血液中有足够的ctDNA丰度。这一结果与其他的基于NGS的在乳腺癌ctDNA中检测扩增的研究(PMID:26667234,PMID:28446639)一致,ctDNA中检出的扩增少于组织。在低ctDNA分数的背景下,基于组织的检测可能对检测扩增更为可靠。
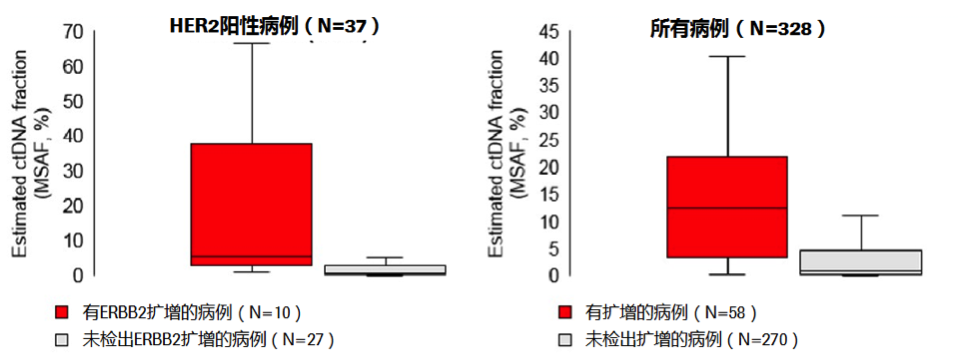
图5. 扩增同ctDNA丰度的相关性
对研究中检测到的ESR1基因组变异情况进行总结,观察到多种ESR1变异,总结如图6,40%的ESR1突变病例带有>1个突变。在2/49个病例中观察到ESR1复合突变,并观察到影响配体结合域的ESR1重排。此外,在80例ESR1变异病例中,与ESR1共同发生的基因组变异提示AI难治性疾病的靶点,总结见下图7。
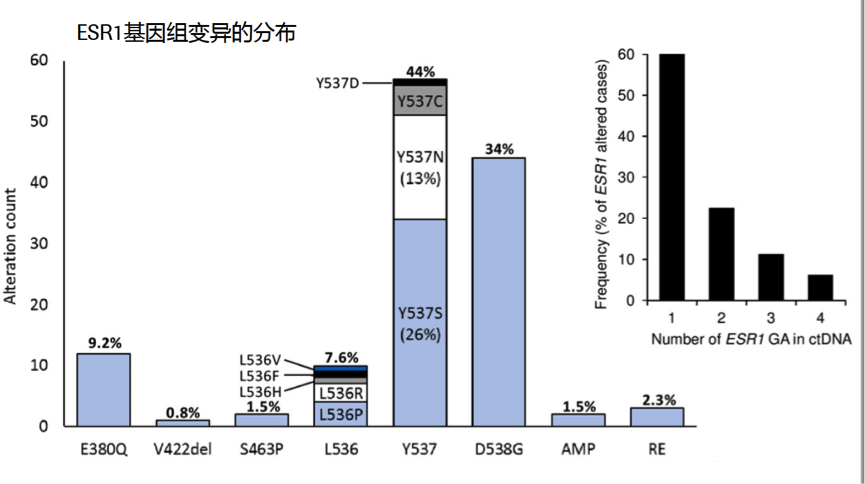
图6. ESR1基因组变异分布
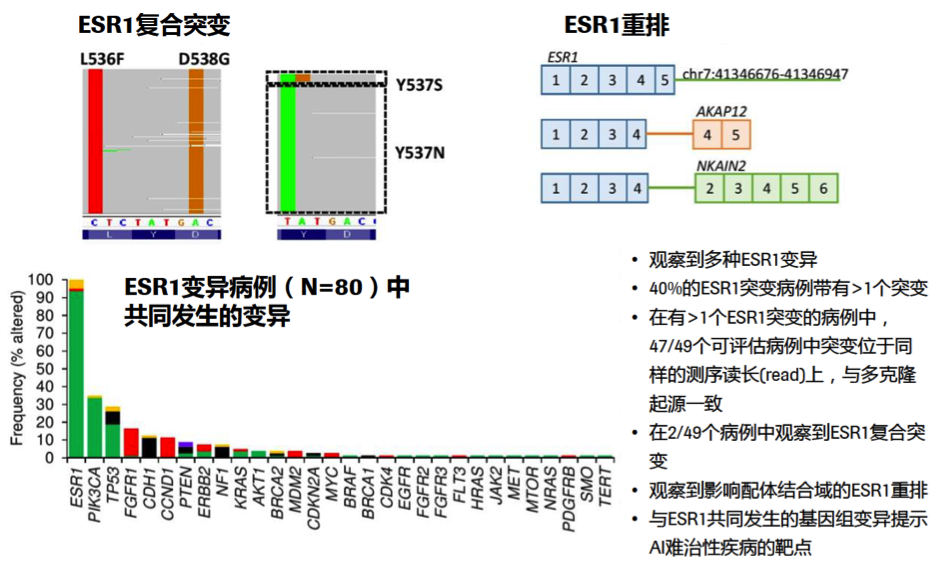
图7. ESR1复合突变,重排和其他共存基因变异
小结:本研究基于对328例乳腺癌患者血液ctDNA的基于杂交捕获的基因组测序分析,提示基于ctDNA的基因组测序分析是检测复发/转移性ER+或ER-乳腺癌相关的基因组变异的可行方法。
(二)血浆ctDNA的CGP检测,发现TNBC中PIK3CA/AKT1的突变
摘要号122P-ctDNA分析发现PIK3CA/AKT1突变同紫杉醇联合ipatasertib治疗三阴性乳腺癌的PFS改善相关
背景:在今年的ESMO会议上,报道了一项安慰剂对照的随机II期LOTUS试验(NCT02162719),结果显示,AKT抑制剂 ipatasertib(IPAT)联合紫杉醇用于不加选择的转移性TNBC患者的一线治疗,可以显著改善患者的PFS。进一步的探索性分析显示,PIK3CA/AKT1/PTEN变异的患者,从联合治疗中获益更多。LOTUS研究的研究设计如下。
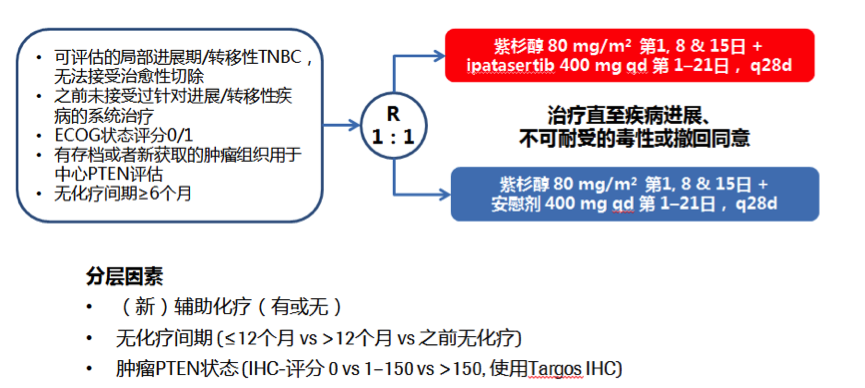
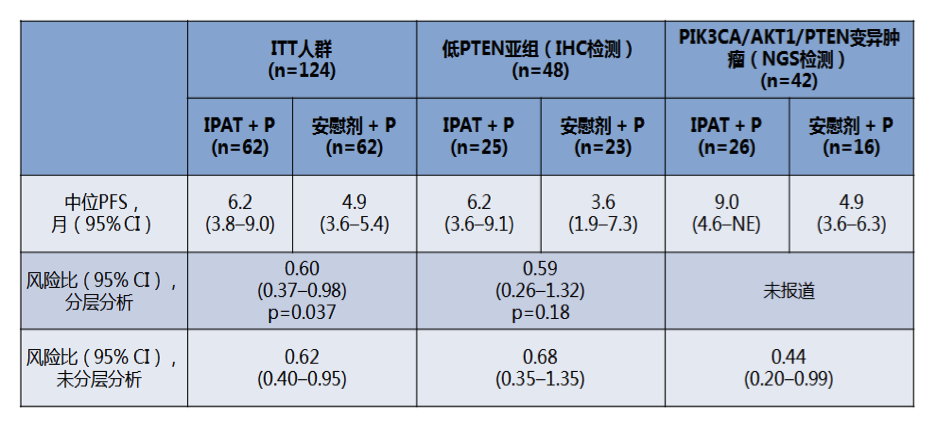
表1. ITT人群和不同亚组患者的疗效数据
方法:研究者分别采用FMI的针对血浆标本的CGP产品和针对组织的CGP产品对患者治疗前的血浆和组织标本进行检测,并比较两种检测方法在常见突变检测上对一致性。为评估ctDNA突变负荷的诊断效果,研究者以所有血浆标本中突变等位基因丰度 (variant allele fraction, VAF) 的中位数作为截断值,将研究人群分为VAF高和VAF低两个组。由于PIK3CA/AKT1/PTEN变异的肿瘤患者中观察到更加显著的PFS改善,使用两种方法PIK3CA/AKT1的突变状态,并评估一致性。
结果:共88例患者的血浆标本可进行ctDNA检测(IPAT+紫杉醇40例,安慰剂+紫杉醇组48例),其中72例患者有可评估的组织标本(52个标本来自原发肿瘤,两组各36例患者)。其余不能进行血浆标本检测的主要原因为血浆中提取的cfDNA量不够。基于血浆检测的患者的PFS比ITT人群略差。在同时有基于血浆和基于组织测序的亚组患者中,PFS同基于血浆检测的患者类似(见下图)。
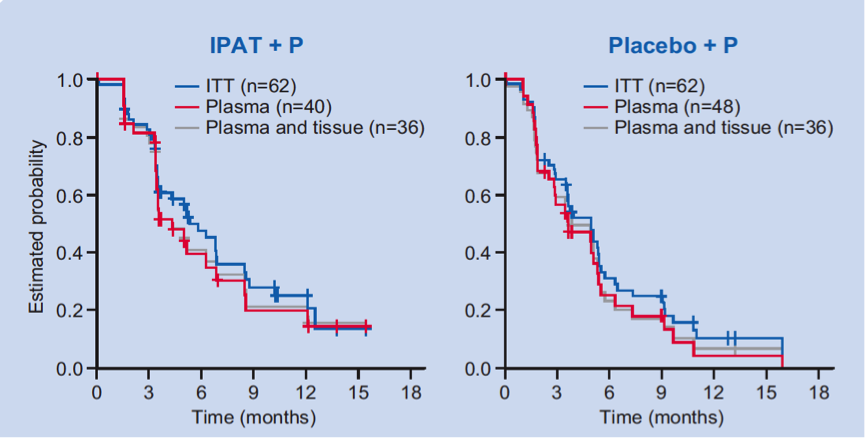
图2. PFS对比(ITT人群 vs. 可以进行血浆检测人群 vs. 同时可以进行血浆和组织检测的人群)
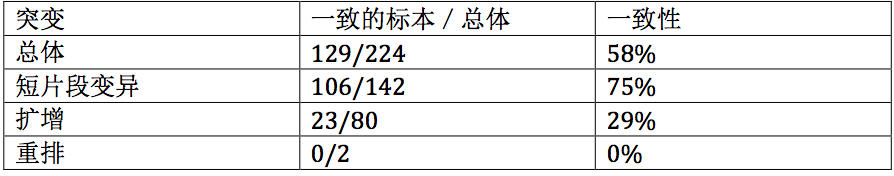
88例进行ctDNA检测的患者,81例(92%)的ctDNA测序中检测到至少1个突变,与组织检测的一致性为75%,见下表2。
表2. 血浆和组织测序的一致性总结
 进一步分析特定基因的突变率,包括PIK3CA和AKT1,结果显示组织和血浆测序的结果相似,见下图3。
进一步分析特定基因的突变率,包括PIK3CA和AKT1,结果显示组织和血浆测序的结果相似,见下图3。
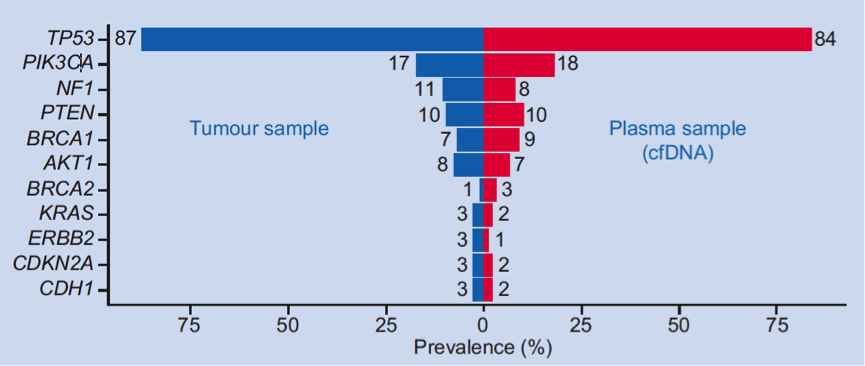
图3. 血浆和组织标本常见基因的突变率比较
在探索性分析中,VAF和基线肿瘤体积没有显著的相关性,见下图4。
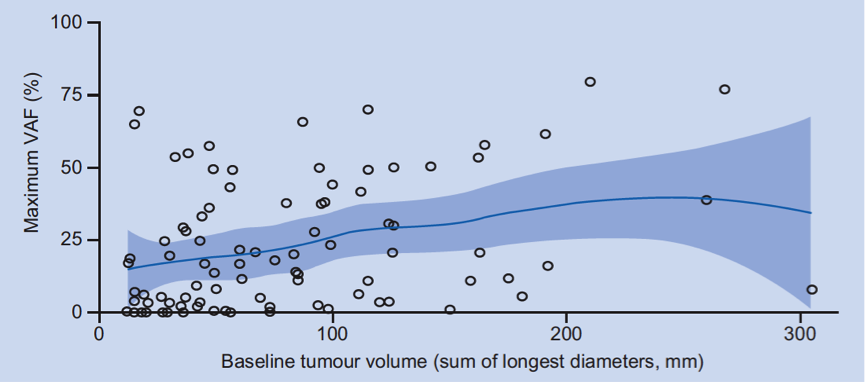
图4. VAF和基线肿瘤体积的关系
进一步分析化疗间期和肿瘤转移病灶的数目与VAF的关系,结果显示,无化疗间期<=12个月的患者和多个肿瘤转移灶的患者,VAF有显著更高的趋势。如下图5所示。
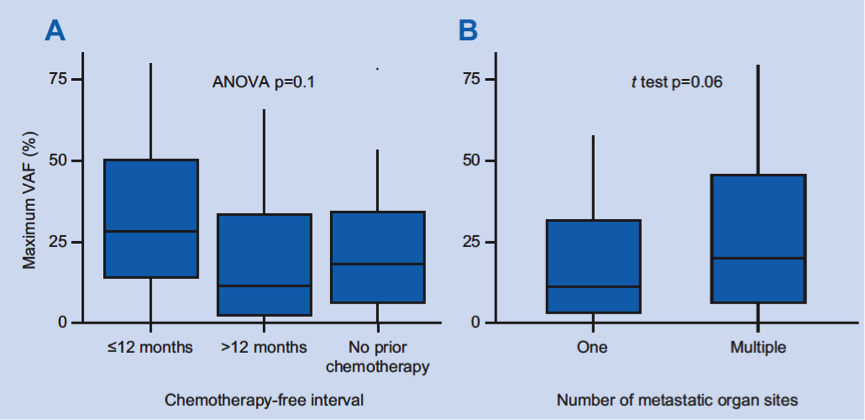
图5. 不同的无化疗间期患者(A)和不同转移病灶数目患者(B)的VAF比较
进一步分析VAF和患者PFS的关系,结果显示,两个治疗组中,VAF低的患者PFS显著更长。
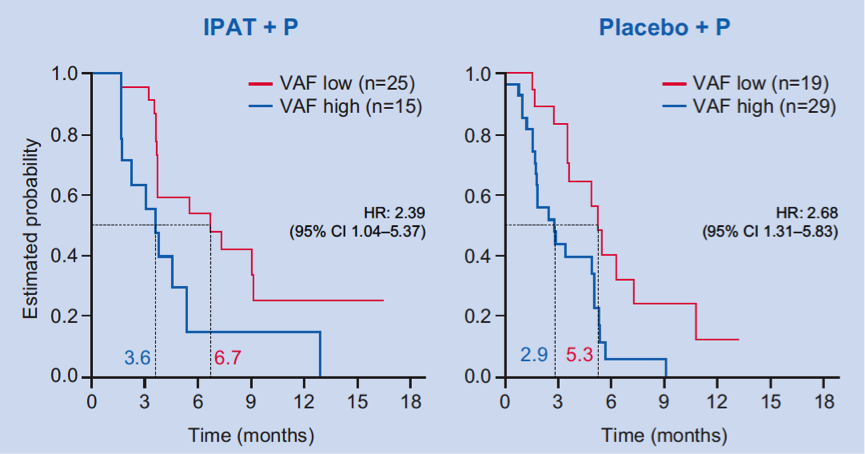
图6. VAF(基于血浆检测)和患者PFS的关系
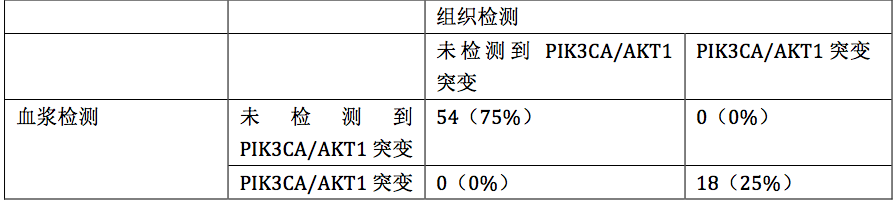
其中25%(n=22)的患者ctDNA中检测到PIK3CA (n=16) 或AKT1(n=6) 的活化突变,与组织检测的吻合度达100%,总结见表3。
表3. 血浆和组织检测PIK3CA/AKT1活化突变的一致性
 在PIK3CA/AKT1活化突变的患者中,IPAT联合紫杉醇组对比安慰剂联合紫杉醇组,PFS显著改善(HR=0.15),而在未检测到PIK3CA/AKT1活化突变的患者中,IPAT联合紫杉醇组对比安慰剂联合紫杉醇组,PFS没有显著差异,如下图7所示。
在PIK3CA/AKT1活化突变的患者中,IPAT联合紫杉醇组对比安慰剂联合紫杉醇组,PFS显著改善(HR=0.15),而在未检测到PIK3CA/AKT1活化突变的患者中,IPAT联合紫杉醇组对比安慰剂联合紫杉醇组,PFS没有显著差异,如下图7所示。
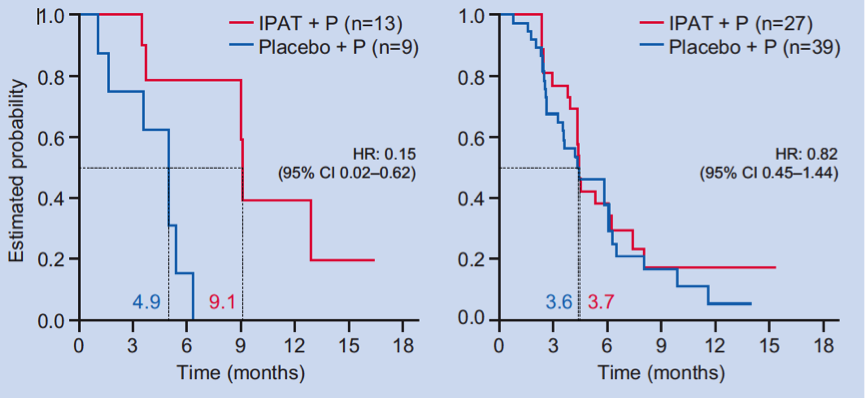
图7. 基于PIK3CA/AKT1活化突变状态对比两组患者的PFS,
左图:PIK3CA/AKT1活化突变患者;
右图:未检测到PIK3CA/AKT1活化突变的患者。
结论:这些结果突显了ctDNA在评估患者预后以及发现同治疗效果改善相关的分子标志物方面的潜在作用。基于血浆和基于组织的测序显示了对于检测PIK3CA/AKT1突变的100%一致性,无论收集标本的间隔如何。这些发现支持PIK3CA和AKT1突变作为早期遗传事件,在原发灶组织标本中存在,并且在转移过程中得以保留。目前FMI正在开发一个针对TNBC的伴随诊断平台,其中PIK3CA和AKT1突变也包括在内,后续这一检测平台将为寻找IPAT的潜在获益人群提供重要的手段。
(三)CGP检测发现经典型浸润性小叶癌和多形性浸润性小叶癌的驱动基因谱不同
摘要号240PD-采用CGP检测CDH1突变的经典型和多形性浸润性小叶癌治疗前后的基因突变谱,明确内分泌耐药机制,探索潜在的治疗靶点
根据乳腺浸润性小叶癌(ILC)的病理特征可以细分为经典型和多形性浸润性小叶癌两种类型,其驱动基因谱可能存在差异,会潜在影响复发性或耐药性患者的治疗选择。研究从10784例乳腺癌DNA标本库中,筛选出454例(4%)CDH1突变的ILC,其中428例为经典型ILC(CILC,94%),26例为多形性ILC(PILC,6%)。
研究采用CGP检测了患者40um的FFPE标本,DNA提取含量>50ng(检测315个癌症相关基因,中位测序深度>600X),并在1.2Mbp的测序DNA上计算肿瘤突变负荷(TMB,mut/Mb)。
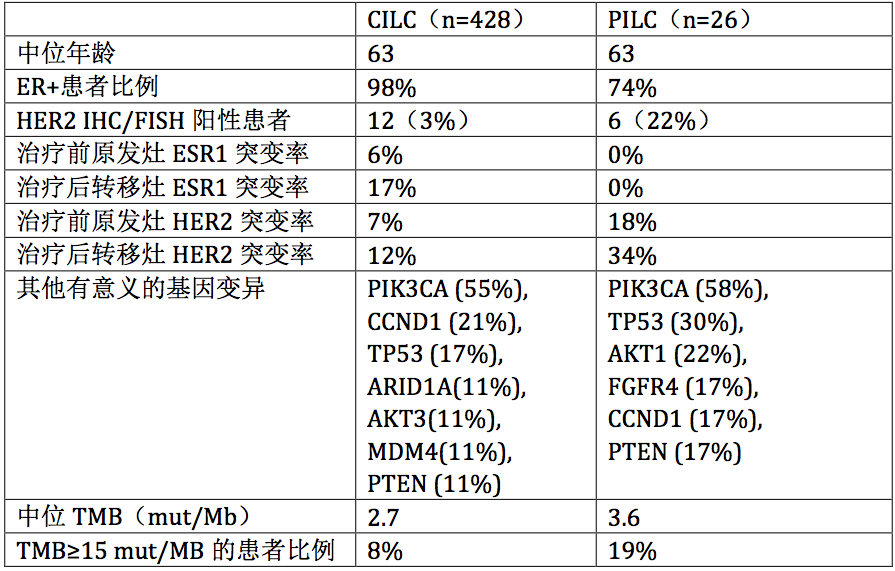
如表1. 所示,CILC和PILC患者的中位年龄相当,为63岁。CILC患者的ER+率更高,而PILC患者的HER2+率更高(P<0.0001)。CILC患者中,ESR1基因变异率显著更高,此外,相比内分泌治疗前的患者,内分泌治疗耐药后的患者(转移灶活检),ESR1突变率显著更高(P < 0.0001)。无论是治疗前还是治疗后的标本,PILC患者中HER2突变率(无论HER2是否扩增)均显著高于CILC患者(P < 0.0001)。内分泌治疗后,无论是CILC还是PILC患者,HER2变异率都增加了一倍。CILC和PILC患者中,PIK3CA都是最常见的基因变异,但PILC患者中TP53突变率高于CILC患者。进一步分析TMB,PILC患者的中位TMB高于CILC,其中TMB≥15 mut/MB的患者比例,PILC是CILC的两倍(P = 0.046)。
表1. CILC和PILC患者的临床和基因特征总结
 在会议壁报展示中,研究者同时分享了2例复发或转移性乳腺癌患者,采用CGP检测发现了新兴的治疗靶点,并从相应靶向治疗中获益。
在会议壁报展示中,研究者同时分享了2例复发或转移性乳腺癌患者,采用CGP检测发现了新兴的治疗靶点,并从相应靶向治疗中获益。
病例1.
一例43岁女性,10年前诊断为ER+,PR-,HER2-阴性的乳腺癌患者,2012年10月复发,出现腹膜和大网膜转移,左肾上腺转移,同时合并肝转移。肝脏转移灶穿刺提示为转移性三阴性乳腺癌,CGP检测发现ERBB2 L755S,MDM2,MYC扩增和APC I1307K。接受来那替尼单药治疗11个月,RECIST 1.0标准评价患者为部分缓解(PR)。
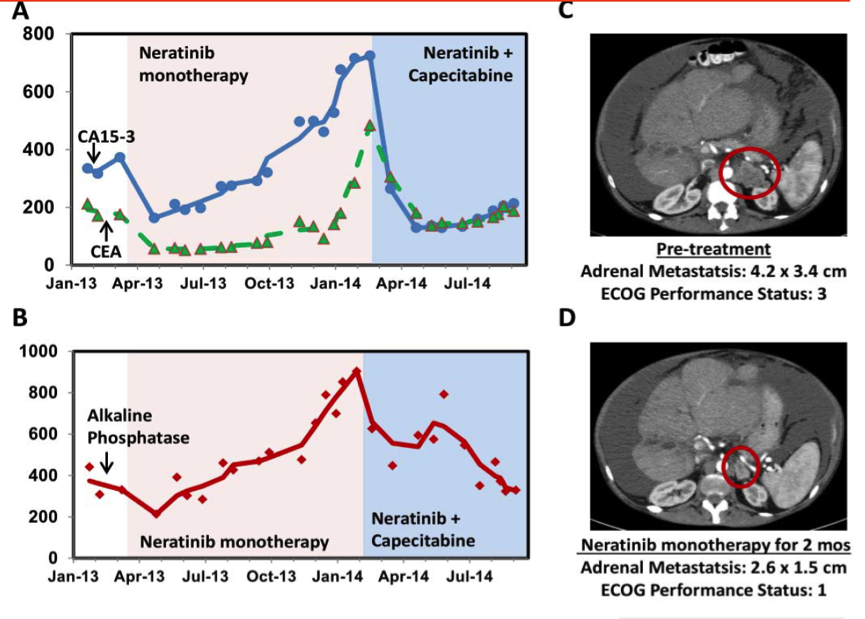
图8. 患者接受来那替尼治疗后的血浆标志物和肾上腺转移灶影响学变化
病例2. CDH1和ERBB2突变的CILC患者
一例58岁女性,5年前诊断为ER/PR阳性,HER2阴性的CDH1突变型CILC,复发进展后出现肝转移。因患者合并有ERBB2 S310F突变和HER2扩增,给予曲妥珠单抗+帕妥珠单抗+氟维司群治疗,患者取得临床获益,CA15-3下降至正常水平(31.3单位/ml,见下图9A)。疾病进展后,患者患者拉帕替尼+曲妥珠单抗,但治疗无效,患者很快进展死亡。
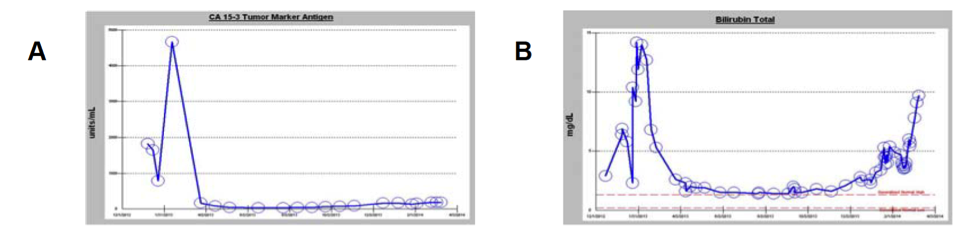
图9. 患者治疗过程中的血浆标志物变化
小结:PILC和CILC患者的基因变异谱存在显著差异。对比分析患者治疗前后的组织标本,无论是CILC还是PILC患者,治疗前后ESR1和HER2的突变均有显著差异,这可能是因为治疗的影响。复发的CILC患者,ESR1突变率更高;而PILC患者,HER2突变率更高。无论是CILC还是PILC,均有一部分患者TMB高,PILC患者中比例更高,提示这类患者可能从免疫治疗中获益。
(三)总结
上述三个研究采用CGP分别检测了乳腺癌血浆ctDNA和肿瘤组织中的癌症相关基因变异谱,为探寻新的治疗靶点和预估免疫治疗可能提供了重要的数据。
(四)专家点评

复旦大学附属肿瘤医院乳腺外科行政副主任
复旦大学附属肿瘤医院乳腺外科副主任医师
中国抗癌协会乳腺癌专业委员会委员
中国抗癌协会肿瘤靶向治疗专业委员会委员
上海市抗癌协会乳腺癌专业委员会常委
国家自然科学基金会评审
香港研究资助局Research Grants Council评审
《Lancet Oncol》《Cancer Res》《中国肿瘤临床》等国内外肿瘤学知名期刊同行评审
随着基因组学的研究进展,很多癌症如NSCLC、黑色素瘤等的分子生物学特征谱逐渐清晰。目前,乳腺癌治疗主要根据临床病理和分子分型为原则进行治疗。三阴性乳腺癌(TNBC)和难治性耐药性乳腺癌(如内分泌治疗耐药后的激素受体阳性乳腺癌及曲妥珠单抗等耐药后的HER2阳性乳腺癌),缺乏高效的治疗靶点。近年来,基因组学研究下的新靶点探寻,是乳腺癌研究的重要课题。FMI针对实体瘤的全面基因组测序(CGP)产品可一次检测315个基因,同时还可以提供TMB(肿瘤突变负荷)及MSI 信息,此外,FMI还针对血浆样本建立的检测平台,为探寻乳腺癌的潜在治疗靶点和评估免疫治疗获益的可能提供了重要信息。
今年的ASCO和ESMO会议上采用CGP检测的三个研究都有重要的临床转化价值。
第一个研究,对临床实践中收集的血浆ctDNA进行检测,研究显示,基于ctDNA的基因组测序分析,用于临床实践检测的可行性,并且与组织检测的一致性较高。
第二个研究聚焦TNBC患者的血浆ctDNA检测,TNBC乳腺癌是一类异质性很大的肿瘤,目前从基因表达层面,可进一步细分为6-7个亚型。当前尚缺乏有效的治疗手段,探寻潜在的治疗靶点是TNBC治疗变革的关键。此研究发现PIK3CA/AKT1突变可以预测TNBC接受ipatasertib联合紫杉醇治疗的疗效。如果这一II期研究结果能得到后续更大样本量的验证,将成为TNBC重要的治疗靶向。基于ctDNA的检测,不仅无创,还能克服肿瘤的异质性,为无法获取组织标本的患者提供重要补充手段。
第三个研究,对比了不同亚型的浸润性小叶癌(ILC)基因突变谱,并进行内分泌耐药前后的基因突变对比,为内分泌治疗耐药后的靶向治疗提供重要思路。此外,研究还发现ILC患者中有一部分属于高TMB人群,这部分患者非常有可能从免疫治疗中获益。
三个研究为晚期乳腺癌的转化研究提供了重要的数据,期待后续更多的研究进展,我们也期望迎来mBC患者靶向和免疫治疗的新的春天。当然,CGP检测也引发了一些重要问题,值得进一步探讨。比如,虽然CGP检测能够发现一系列突变,但对一个患者而言,同时检测出2种及以上突变时,哪一个突变才是真正驱动性突变呢?到底哪一个突变才具有真正意义上靶向价值呢?肿瘤常常通过适应性突变发生逃逸,或者DNA修复相关基因先行突变导致下级基因突变的级联反应,因此有效甄别驱动性和关键性突变,是非常重要的。不仅如此,CGP检测为医学检验开辟了新天地,但不免尴尬的是,我们手中的武器——“靶向药物”的开发和批准速度远远落后,有时我们知道了某一个驱动性突变,但苦于缺乏有效的靶点药物。CGP检测等这些基因工具,也对临床药物开发提出了新要求。
1. Cell-free DNA analysis identifies PIK3CA/AKT1 mutations associated with greater PFS improvement from the addition of ipatasertib to paclitaxel in triple-negative breast cancer. 2017 ESMO abs122P.
2. Genomic profiling of circulating tumor DNA (ctDNA) from patients (pts) with metastatic breast cancer (mBC). 2017 ESMO. Abs1016.
3. Comprehensive genomic profiling of primary and metastatic CDH1 mutated classic and pleomorphic invasive lobular breast carcinomas reveals markers of hormonal therapy resistance and opportunities for targeted therapies. 2017 ESMO. abs240PD .











 苏公网安备32059002004080号
苏公网安备32059002004080号


