三阴乳腺癌患者的PI3K/AKT信号通路常因PIK3CA或AKT1突变激活或PTEN的改变活化。那么AKT抑制剂联合标准化疗一线治疗三阴性乳腺癌是否优于标准化疗?韩国蔚山大学医学院Sung-Bae Kim和Rebecca Dent教授就相关问题于《柳叶刀杂志》报道LOTUS试验的II期结果。
研究背景和目的
PI3K/AKT 信号通路促进细胞的生存和生长,在癌症形成过程中发挥重要作用。AKT是PI3K/AKT信号通路的关键分子。Ipatasertib是高度选择性口服ATP竞争性小分子AKT抑制剂,其敏感性与高磷酸化AKT水平,PTEN蛋白缺失,PTEN基因突变,PIK3CA基因突变有关。
既往I期研究显示Ipatasertib安全性良好(胃肠道反应,虚弱乏力,皮疹)及初步的抗肿瘤疗效。I b期试验PAM4983g显示,Ipatasertib(400 mg,每天一次,连续给药21天)联合紫杉醇90 mg/m² 每周一次(第1,8,15天给药),每28天为一疗程重复给药,结果显示乳腺癌患者耐受良好,且影像学上有缓解。
研究设计及对象
LOTUS筛选来自多国的44个医院的病人。
纳入标准:
女性,年龄≥18周岁,ECOG ≤1,不能手术治愈的局部晚期或转移性三阴性乳腺癌,必须有基于RECIST 1.1 标准可测量的病灶,足够的血液,肾,肝,心脏功能。在随机分组前,所有的患者都需要提供肿瘤标本以分析PTEN状态。
排除标准:
既往接受针对局部晚期或转移性病灶的全身治疗 (末次(新)辅助化疗,放疗,同步放化疗≥6个月可接受),中枢神经系统转移, 2级及以上的周围神经病变或2级及以上未控制的高脂血症或高甘油三酯血症,或活动性小肠及大肠炎症(如克罗恩病或溃疡性结肠炎)。
入选患者按照1:1随机双盲分为2组,分别接受Ipatasertib联合紫杉醇或安慰剂联合紫杉醇。分层因素:既往接受(新)辅助化疗(是 vs否),无化疗间歇期(≤12个月 vs >12个月 vs既往无化疗),IHC分析的PTEN状态(H得分0 vs 1-150 vs >150)。
给药方案:
在疗程第1天,第8天,第15天静注紫杉醇80 mg/m²,联合Ipatasertib 400mg/d或安慰剂口服连续给药21天,28天一个疗程。治疗直至出现疾病进展,不可耐受毒性,或撤回同意。
疗效评估
首要复合终点:
基于意向性治疗(ITT)人群和低PTEN亚组的PFS。
次要终点:
客观缓解(OR),客观缓解的持续时间(DoR),基于ITT人群以及低PTEN亚组的总生存期(OS),PI3K/AKT通路活化的人群的疗效(PFS,客观缓解率(ORR)DoR以及OS)。
其他终点包括药代动力学(PK),疾病或治疗相关症状的患者报告结果(PRO),生活能力,健康相关的生活质量,及进一步的转化研究的探索。
结果
2014年9月~2016年2月,共纳入166名患者, 124名患者按照1:1的比例被随机分配分别接受Ipatasertib治疗(62名)和安慰剂治疗(62名)。两组人群的基线特征相似。生物标记物可评估的PTEN状态和PI3K/AKT1/PTEN变异的人群显示出与ITT人群类似的基线特征。
PIK3CA/AKT1/PTEN变异率在来自原发病灶和转移病灶的标本间无明显差异,同样在来自(新)辅助化疗前的和之后的标本间无明显差异。
至截止日期(2016年6月),中位随访期为Ipatasertib组10.4个月,安慰剂组10.2个月。
基于ITT人群的疗效分析,中位PFS为Ipatasertib组6.2个月(95% CI 3.8-9个月),安慰剂组4.9个月(95% CI 3.6-5.4个月),HR为0.60,p=0.037。敏感性分析中,中位PFS分别为Ipatasertib组5.9个月,安慰剂组5.0个月,HR为0.66,p=0.081. (见图A)
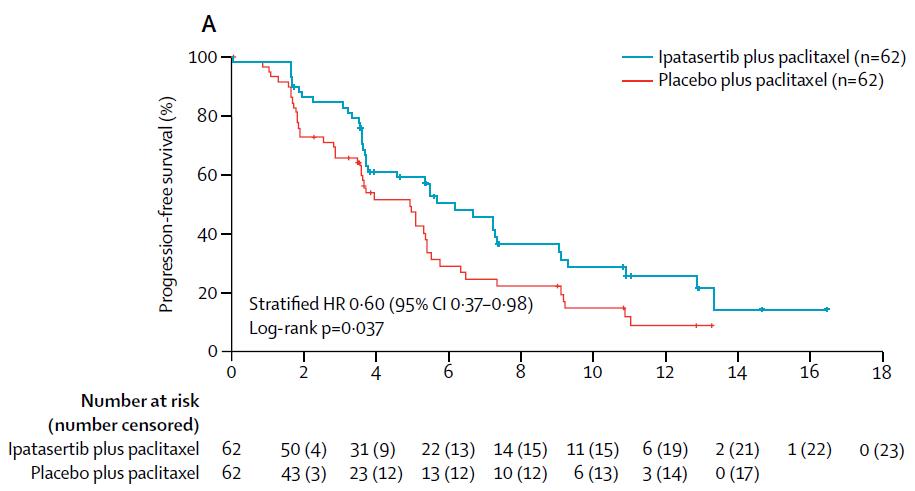
基于48名低PTEN患者的疗效分析,Ipatasertib组中位PFS为6.2个月(95% CI 3·6–9·1个月),安慰剂组中位PFS为3.7个月 (95% CI 1.9-7.3个月),两组对比HR=0.59,p=0.18. (见图B)
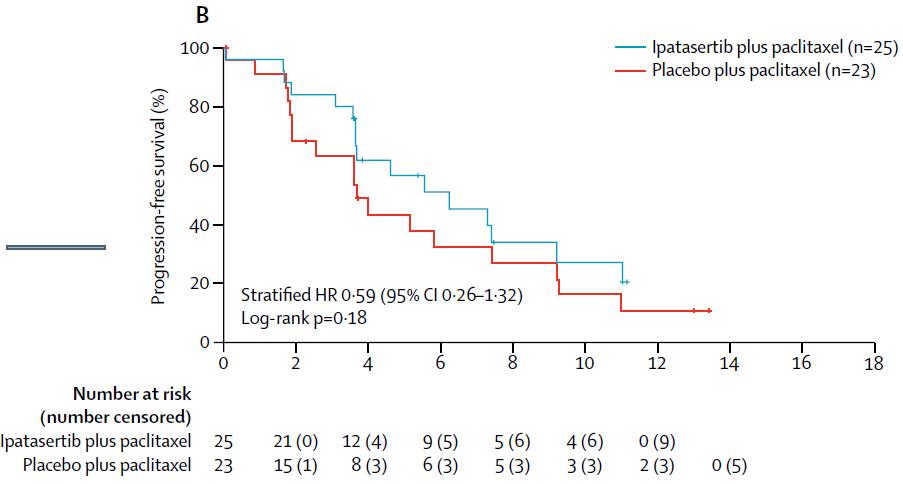
预设的PIK3CA/AKT/PTEN 基因突变亚组共42名患者,其中Ipatasertib组26名患者中位PFS为9个月(95% CI 4.6个月-未达到),安慰剂组的16名患者中位PFS为4.9个月(95% CI 3.6-6.3个月),两组HR为0.44,p=0.041)(见图C)。而在PIK3CA/AKT/PTEN基因未突变亚组的患者中,Ipatasertib组28名患者中位PFS为5.3个月(95% CI 3.6-7.3个月),安慰剂组的33名患者的中位PFS为3.7个月(95% CI 2.9-5.5),HR=0.76,p=0.36。
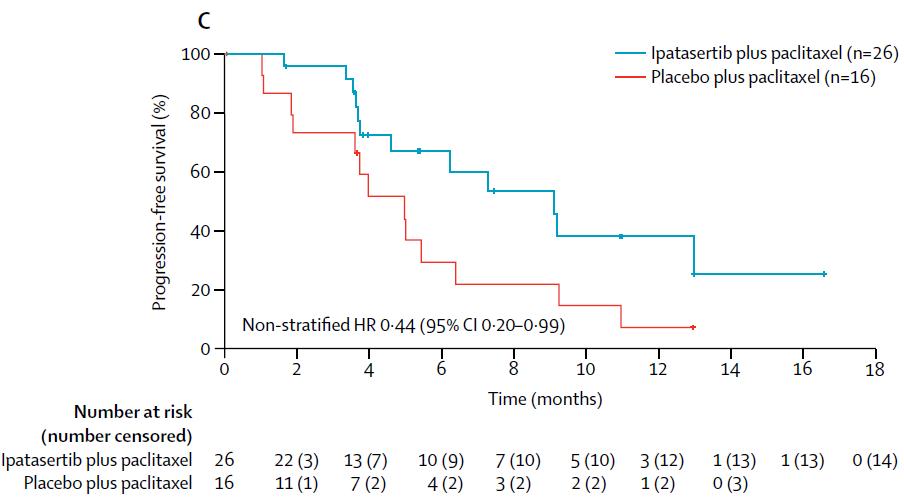
次要终点中,ITT人群和PTEN低表达人群的中位DoR在两个治疗组之间相似,但是PIK3CA/AKT1/PTEN变异亚组人群中,接受Ipatasertib治疗的患者的DoR更长。其余次要终点结果(客观缓解OR,临床获益)见下表。
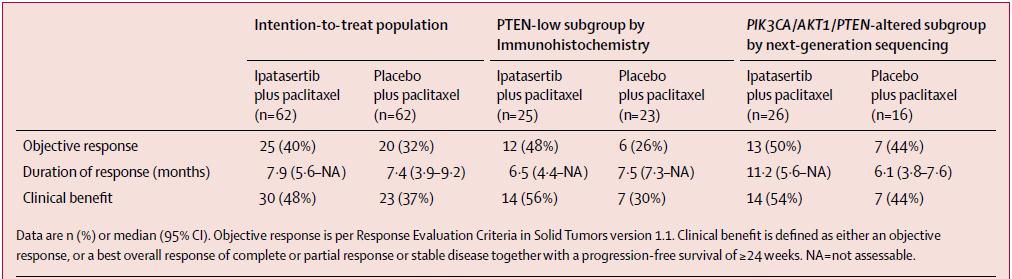
安全性方面,Ipatasertib组常见不良事件(AEs)为胃肠道反应(腹泻,恶心,呕吐),脱发,神经病变,疲劳及皮疹,多为1级或2级。3级及以上AEs发生率Ipatasertib组54%(33例),安慰剂组42%(26例),无4级腹泻和大肠炎。相对于安慰剂组(发生率15%),Ipatasertib组严重不良事件(SAE)更常见,发生率为28%。4名患者因AEs死亡,其中Ipatasertib组1名患者因肺炎死亡(但不考虑与试验用药相关),另外3名死亡患者来自安慰剂组。
PRO方面,在生活能力,整体健康状态/生活质量及疾病或治疗相关症状方面两组均没有临床意义的改变。在Ipatasertib组的第2个疗程,情感功能有临床意义的改善。但腹泻(2至5个疗程),乏力(2至5个疗程),角色功能(2至5个疗程)出现了临床意义的恶化。
本次研究样本中, Ipatasertib血浓度与已知的PK特征及其代谢产物G-037720一致。探索性分析显示,腹泻、中性粒细胞减少症和神经病变的发生率与Ipatasertib的暴露量无关。
结论
LOTUS研究结果表明,Ipatasertib联合紫杉醇对比安慰剂联合紫杉醇一线治疗三阴乳腺癌可以延长患者的PFS,中位PFS在ITT人群和低PTEN人群中适度延长,在PIK3CA/AKT1/PTEN变异人群显著延长。从整体而言Ipatasertib安全性良好。
讨论
试验结果显示,Ipatasertib一线治疗低PTEN亚组患者,与非低PTEN人群及ITT人群相比,疗效相似。而PIK3CA/AKT1/PTEN变异的亚组人群的有效性分析则显示出,其相对于ITT及其他人群,Ipatasertib一线治疗获得的中位PFS更长。PTEN丢失只是PI3K/AKT通络激活的机制之一,而在乳腺癌患者,PIK3CA或AKT1基因突变激活则很常见。同时为未来进一步探索Ipatasertib联合紫杉醇一线治疗PIK3CA/AKT1/PTEN变异的三阴乳腺癌患者提供了证据支持。
最常见的不良反应为胃肠道反应,尤其是腹泻,但无4级及以上的腹泻。并且在认知,体能,社会功能及其他子量表中没有出现临床意义的恶化。这意味着,Ipatasertib联合紫杉醇的方案是安全可接受的。
PK数据与以往的资料相似,表明Ipatasertib与紫杉醇之间没有药物相互作用。尽管在探索性分析中,Iaptasertib的暴露量与腹泻,中性粒细胞减少症,神经病变的发生率之间没有明确的关系,但仅凭一个剂量水平的结果很难评估暴露量-反应关系。
该研究的一个主要缺陷是样本量太少。根据生物标记物选择的人群,Ipatasertib疗效显著的患者仅有42名,同时因没有将NGS结果作为随机分层因素,因此应谨慎解读试验结果,且需要进一步的前瞻性研究进行验证。
点评
Ipatasertib联合紫杉醇是目前处于随机化试验评估阶段的用于三阴乳腺癌的几种新的治疗策略之一,在不久的未来可能会改变三阴乳腺癌的治疗现状。未来治疗方案的选择及定序会日益复杂,而生物标记物的筛选预计会在个体化治疗中发挥重要作用。
尽管目前为止,Ipatasertib的研究集中在三阴乳腺癌,但在HER2阳性和激素受体阳性的细胞系中同样观察到Ipatasertib的敏感性。未来需要进一步评估Ipatasertib联合紫杉醇作用在PI3K/AKT信号通路变异活化高发病率的患者,特别是伴随PIK3CA/AKT1/PTEN变异的人群。
Kim SB, Dent R, Im SA et al. Ipatasertib plus paclitaxel versus placebo plus paclitaxel as first-line therapy for metastatic triple-negative breast cancer (LOTUS): a multicentre, randomised, double-blind, placebo-controlled, phase 2 trial. Lancet Oncol. 2017 Aug 8. pii: S1470-2045(17)30450-3. doi: 10.1016/S1470-2045(17)30450-3.











 苏公网安备32059002004080号
苏公网安备32059002004080号


