脊索瘤是一种罕见的恶性骨肿瘤,局部侵袭性强,术后复发率高,既往靶向治疗客观缓解率(ORR)仅约3.7%,免疫单药ORR亦仅12%,有效系统治疗方案的匮乏始终是全球骨肿瘤领域最大的未满足临床需求之一。2026年5月13日,由上海长征医院肖建如教授、杨诚教授领衔团队完成的首个PD-1抑制剂联合抗血管生成药物治疗难治性脊索瘤的前瞻性Ⅱ期临床试验正式在线发表于Journal of Clinical Oncology(JCO,IF 43.4)[1]。该研究此前已于2025 ASCO年会以口头报告形式发表(摘要号:11503)[2],引发国际学术界广泛关注。研究结果显示,卡瑞利珠单抗联合阿帕替尼(“双艾”方案)治疗难治性脊索瘤,ORR达24.2%(95%CI 11.1%~42.3%, RECIST 1.1标准),疾病控制率(DCR)达90.9%,中位无进展生存期(mPFS)长达28.4个月,超越免疫单药及抗血管生成单药的历史数据,是目前全球在治疗难治脊索瘤方面的最优方案。重要的是,研究首次揭示CDKN2A基因组改变(拷贝数/纯合缺失)是不良预后的潜在生物标志物,为脊索瘤精准治疗的人群筛选提供了关键依据。JCO副主编Robert G. Maki教授指出,该研究为转移性/复发脊索瘤中靶向VEGFR激酶抑制剂联合免疫治疗提供了前瞻性证据,并为未来随机对照研究(RCT)设立了标准。

上海长征医院骨科医院院长
全军骨科研究所所长
上海市重中之重脊柱疾病临床医学中心主任
上海市骨科临床医学研究中心主任
国务院政府特殊津贴/军队优秀技术人才一类岗位津贴
上海市十大科技精英/首届上海杰出人才
上海市十佳医生/国之名医卓越建树奖
上海市领军人才/上海市优秀学科带头人
中国医师协会脊柱肿瘤专委会主任委员
中华医学会骨肿瘤学组副主任委员兼脊柱骨盆组组长
中国抗癌协会肉瘤专业委员会候任主任委员
全军骨科专委会副主任委员
以第一或通讯作者在Nature Medicine,Journal of Clinical Oncology、Lancet Oncology,JBJS等杂志发表SCI论文300余篇
以第一完成人获得国家科技进步二等奖1项、省部级一等奖5项、上海国际高端医疗器械创新大赛特等奖1项、何梁何利基金科学与进步奖
科技部重点研发项目首席科学家/首届东方英才创新团队计划首席科学家
主持国家自然科学基金重点项目、军队重点项目、上海市重大课题等40余项
上海长征医院
中国临床肿瘤学会(CSCO)肉瘤专家委员会委员
中国老年学和老年医学学会精准医疗分会骨与软组织肿瘤学组副主任委员
中国残疾人康复协会肢体残疾康复专业委员会脊柱康复学组委员
中国抗癌协会肉瘤专业委员会靶免治疗学组 副组长
中国抗癌协会肉瘤专业委员会软组织肉瘤学组、四肢肿瘤学组、放化疗学组委员、创新与转化学组委员
中国医师协会骨肿瘤专业委员会3D打印骨科学组委员
中国康复医学会修复重建外科专业委员会骨肿瘤学组委员
中国医药教育协会骨与软组织肿瘤专业委员会委员
上海市抗癌协会肉瘤专业委员会常务委员
上海市抗癌协会多原发和不明原肿瘤专委会委员
教育部学位论文评审专家,上海市科委生物医药基金项目评审专家
以第一/通讯作者在Lancet oncology(IF=41), Journal of Clinical Oncology(IF=43.4)等发表论文30余篇(其中两篇重磅临床研究,均为中国骨科界在该顶刊的第一篇论著)
获得军队医疗成果一等奖1项,中华医学奖一等奖1项、二等奖1项,北京市科学技术进步奖三等奖1项
获得发明与实用专利20余项
破解脊索瘤治疗困境:免疫联合抗血管生成策略的理论基础与研究设计
脊索瘤起源于胚胎脊索残余组织,主要发生于颅底斜坡区、骶骨及脊柱。尽管生长相对缓慢,但其局部侵袭性强,常浸润邻近重要结构。整块切除术是减少复发转移风险的唯一选择,但由于该肿瘤好发颅底和骶骨,毗邻重要的脏器和血管,整块切除不仅风险大而且很容易造成神经功能的严重损失,故该肿瘤术后局部复发率超过50%,5年生存率仅为65%~70%,凸显了对有效辅助及挽救治疗策略的迫切需求。传统细胞毒性化疗对脊索瘤疗效甚微,既往多项靶向治疗临床试验报告的最佳客观缓解率(ORR)仅为3.7%。免疫检查点抑制剂(ICI)虽展现出初步抗肿瘤活性,例如帕博利珠单抗II期试验报告的ORR为12%(4/34)、中位无进展生存期(mPFS)为6.1个月,免疫单药疗效仍无法满足临床需求。
免疫检查点抑制剂与抗血管生成药物的联合应用已在多种实体瘤中证实可协同增效。卡瑞利珠单抗是一种人源化抗PD-1单克隆抗体,阿帕替尼是选择性VEGFR2酪氨酸激酶抑制剂(TKI)。基于国际III期CARES-310研究的阳性结果,卡瑞利珠单抗联合阿帕替尼(“双艾”方案)已获批用于晚期肝细胞癌的一线治疗,并在宫颈癌、食管癌、结直肠癌等多种实体瘤中展现出良好应用前景。肖建如教授、杨诚教授团队在前期阿帕替尼单药治疗晚期脊索瘤II期研究(发表于Lancet Oncology)的基础上,设计并开展了本项研究。
本研究采用Simon两阶段最优设计(单侧α=0.05,power=80%)。纳入18~75岁、经组织学确认的难治性脊索瘤患者(不可切除或无法行根治性手术),要求6个月内影像学证实疾病进展(Choi标准)、ECOG PS 0-2、预期生存>3个月且具有充足的器官功能。治疗方案为卡瑞利珠单抗200 mg静脉注射,每2周一次,联合阿帕替尼250 mg与500 mg隔日交替口服,以4周为一个治疗周期。研究的主要终点为ORR(RECIST 1.1标准),次要终点包括ORR(Choi标准)、PFS、OS、DCR、中位缓解持续时间(mDoR)、安全性及生活质量。
疗效出色,超越历史数据:ORR 24.2%,mPFS长达28.4个月,DCR超90%
2021年9月至2024年10月间,共筛选38例患者,33例符合入组标准并接受治疗(纳入疗效与安全性分析)。患者的中位年龄56岁(IQR:49~61岁),男性20例(60.6%),原发部位包括骶骨(48.5%)和脊柱(51.5%)。23例(69.7%)为局部晚期(术后复发),4例(12.1%)伴远处转移,6例(18.2%)为巨大难治性肿瘤。81.8%有手术史,30.3%曾接受过放疗。全部患者均为经典型脊索瘤。
数据截止日期为2025年5月31日,中位随访时间20.8个月,中位治疗持续时间9个月,12例患者(36.4%)仍在接受治疗。
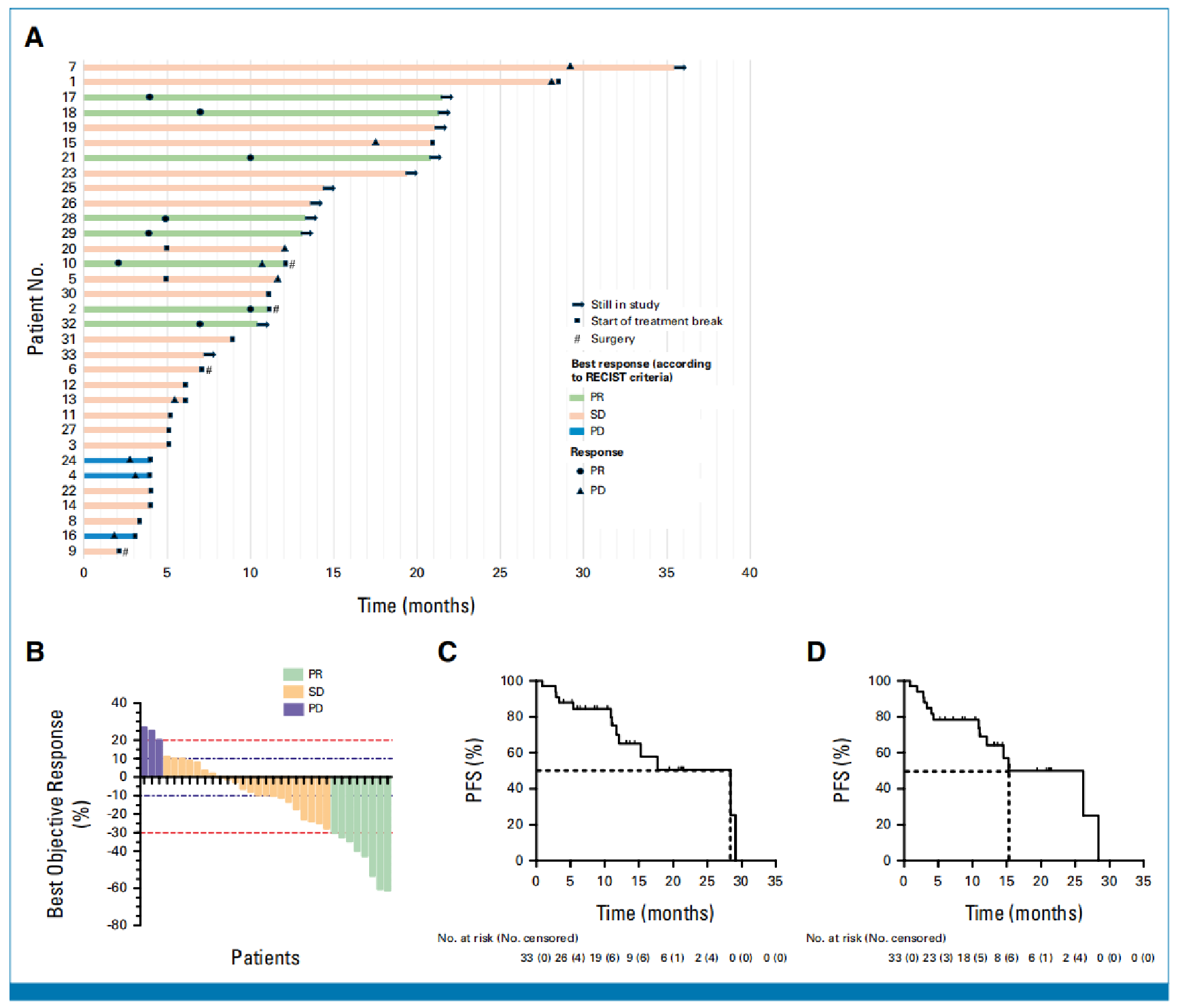
RECIST 1.1标准评估:ORR为24.2%(8/33, 95%CI 11.1%~42.3%),均为部分缓解(PR)。DCR高达90.9%(30/33),肿瘤病灶缩小见于23例患者(69.7%)。中位至缓解时间(mTTR)为6个月(IQR:4~9.25个月),mDoR尚未达到,提示缓解持久。中位PFS为28.4个月,6个月和12个月PFS率分别为84.4%和70.0%(图1)。随访期间中位OS尚未达到。
Choi标准评估:ORR为48.5%(16/33,95%CI 30.8%~66.5%),mTTR仅2.5个月(IQR:2.0~5.5个月),mDoR为22.2个月(95% CI:12.5~未达到)。DCR为81.8%(27/33),中位PFS为15.3个月,6个月和12个月PFS率分别为78.3%和69.1%。
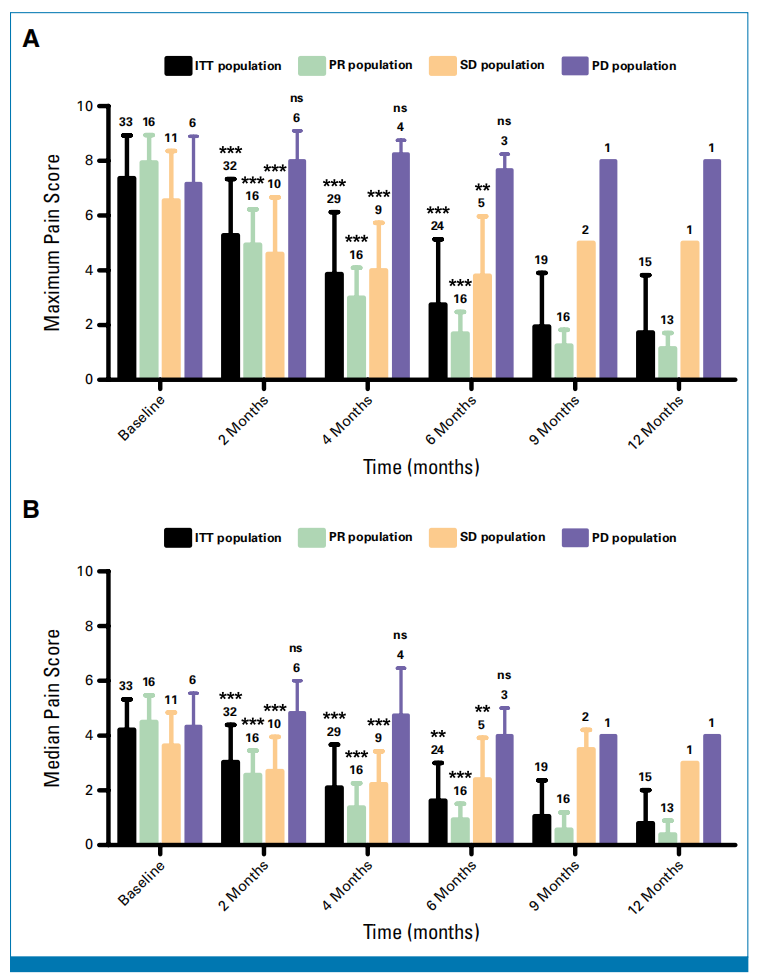
除了肿瘤客观缓解外,该研究还关注了患者的疼痛改善情况。以简明疼痛量表(Brief Pain Inventory, BPI)评估治疗前后疼痛变化。结果显示,经双艾方案治疗,患者的疼痛显著改善——平均最大疼痛评分从基线7.36分(SD 0.56)降至2个月时5.28分(SD 2.05,P<0.001),平均中位疼痛评分从4.18分(SD 1.13)降至3.00分(SD 1.37,P<0.001),尤其在达到PR的患者中改善最为明显(图2)。
首次揭示CDKN2A基因组改变为不良预后生物标志物
鉴于PD-L1表达无法可靠预测脊索瘤对免疫治疗的应答,本研究通过二代测序(NGS)和荧光原位杂交(FISH)技术进行了系统的生物标志物探索。
在20例成功完成NGS检测的患者中,所有患者均表现为PD-L1阴性(<1%)、微卫星稳定(MSS)、肿瘤突变负荷低(<10 mut/Mb),表明传统免疫疗效预测指标对脊索瘤人群的适用性有限,亟需探索替代性标志物。
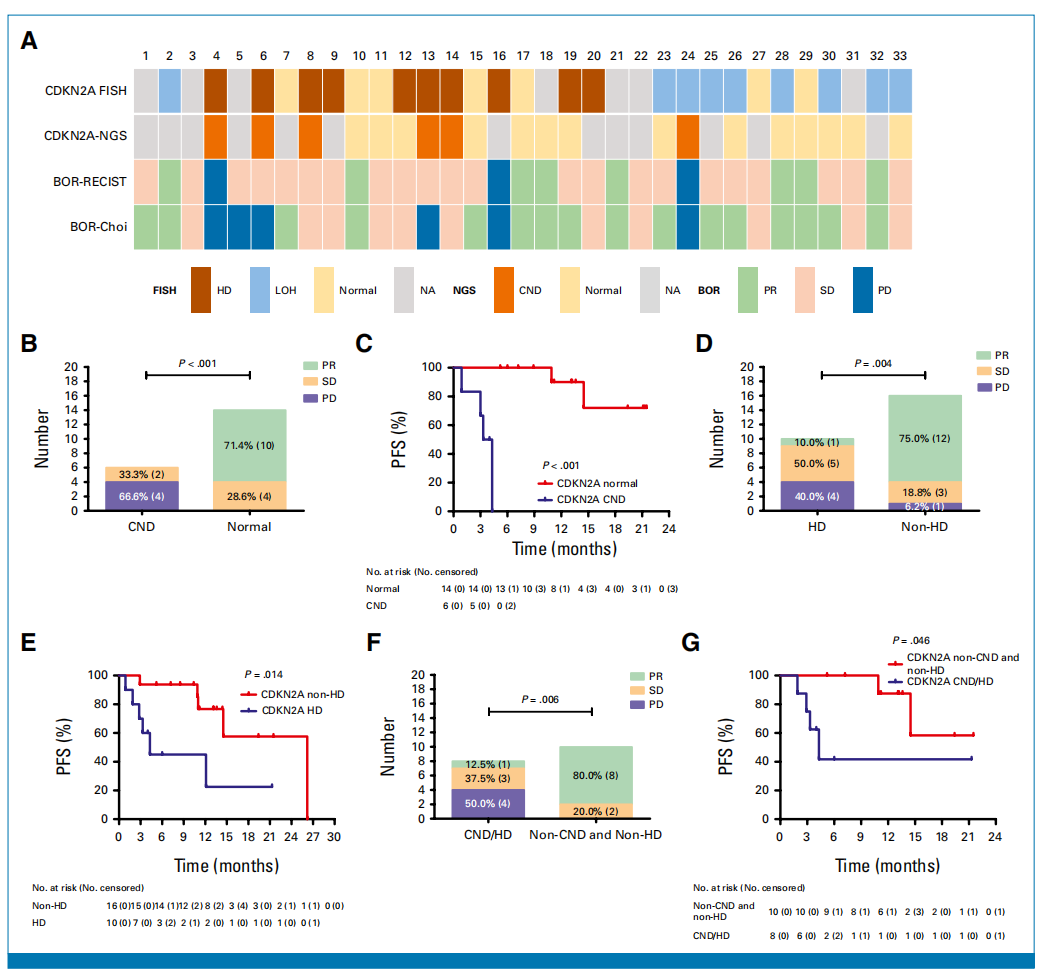
NGS分析发现,CDKN2A拷贝数缺失(CND)是最常见的基因组改变(6/20,30%)。疗效方面差异极为显著:6例CDKN2A CND患者中无一例获得PR,66.7%(4/6)发生疾病进展(PD);而14例CDKN2A正常的患者中71.4%(10/14)获得PR,无一例进展(P<0.001),PFS亦显著更优(P<0.001)。
26例完成FISH检测的患者中,CDKN2A纯合缺失(HD)检出率为38.5%(10/26)。HD亚组仅10%获得PR、40%出现进展,而非HD亚组75%获得PR、仅6.2%进展(P=0.004),PFS同样显著更差(P=0.014)。
综合NGS与FISH数据,CDKN2A CND/HD亚组(n=8)的中位PFS仅4.3个月(95% CI:2.37~6.23个月),而非CND/非HD亚组(n=10)的中位PFS尚未达到;前者疾病进展率50.0%,后者为0%(P=0.006)(图3)。多项敏感性分析(包括缺失数据亚组的log-rank分析、基线特征均衡性验证)进一步证实了上述结论的稳健性。
从机制角度,CDKN2A位于染色体9p21.3区域,是癌症中第二常见的失活抑癌基因,其在脊索瘤中的HD发生率为3%~33%。既往研究提示9p21.3缺失可通过影响干扰素和NF-κB信号通路促进免疫逃逸,从而可能削弱免疫联合治疗的疗效。该发现为未来通过CDKN2A状态对患者进行分层筛选、实现脊索瘤精准免疫治疗提供了重要的分子生物学依据。
安全性可控:毒性谱与既往报道一致
本研究中卡瑞利珠单抗联合阿帕替尼治疗相关不良事件(TRAEs)发生率为93.9%(31/33),3-4级TRAEs发生率为60.6%(20/33)。最常见的3-4级TRAEs为AST和ALT升高,其次为蛋白尿。大多数不良反应通过剂量调整和/或对症支持治疗可获控制。全程无治疗相关死亡事件发生。整体而言,“双艾”方案安全性良好,适合难治性脊索瘤患者的长期持续用药需求。
该研究从机制假说到前瞻性临床验证,系统回答了在抗血管生成基础上加用PD-1抑制剂能否进一步提升难治性脊索瘤疗效这一关键临床问题,为这一长期缺乏有效系统治疗的罕见恶性肿瘤提供了具有突破性意义的循证依据。同时,CDKN2A基因组改变作为不良预后标志物的发现,为后续开展基于分子分层的精准治疗奠定了基础。研究团队已提出未来可推进以CDKN2A状态分层的多中心、前瞻性III期随机对照研究,以进一步明确该标志物的预测价值,并为难治性脊索瘤建立更高级别的治疗证据。
[1] Cheng Yang, Qi Jia, Chenglong Zhao, et al. Efficacy and Safety of Camrelizumab Plus Apatinib in Patients With Refractory Chordoma: A Phase II Clinical Trial. J Clin Oncol 0, JCO-25-02719. DOI:10.1200/JCO-25-02719
[2] Cheng Yang, Qi Jia, Chenglong Zhao, et al. Camrelizumab plus apatinib in patients with advanced or refractory chordoma: A single-arm, open-label, phase 2 trial. 2025 ASCO, Abstract #11503.
排版编辑:肿瘤资讯-小编











 苏公网安备32059002004080号
苏公网安备32059002004080号


