局部进展期直肠癌(LARC)的新辅助治疗是提升手术切除率、改善长期生存的核心环节。微卫星稳定(MSS)/错配修复功能完整(pMMR)亚型因属于“免疫冷肿瘤”,单纯免疫治疗疗效有限;联合放化疗虽能提高病理缓解率,却伴随肠道纤维化、吻合口愈合不良等远期损伤。如何在豁免放疗的前提下,实现高效抗肿瘤与安全可控的双重目标,是全球结直肠肿瘤领域的攻坚重点。
近日,南京医科大学第一附属医院(江苏省人民医院)孙跃明、封益飞、王晓伟教授研究团队在国际权威期刊Signal Transduction and Targeted Therapy(IF=52.7)发表PICS研究(NCT06108596)成果。该项前瞻性、单臂、II期临床研究首次证实,全程新辅助化疗(TNT)联合PD-1抑制剂+IL-2方案用于 MSS/pMMR LARC,可实现42.4%的病理完全缓解(pCR)率,且无放疗相关损伤、安全性可控,为该类患者提供了“去放疗”的全新治疗范式。

研究背景:MSS/pMMR直肠癌治疗困局,去放疗成破局关键
结直肠癌是全球第三大常见恶性肿瘤,其中直肠癌占比超半数,我国以中低位直肠癌和和局部进展期直肠癌(LARC)最为多见。当前临床标准方案为新辅助放化疗,虽能将病理完全缓解(pCR)率提升至15%~20%,但放疗引发的放射性损伤、肠道纤维化、狭窄以及组织愈合受损,严重影响患者术后生活质量。
免疫检查点抑制剂(ICI)仅对微卫星高度不稳定(MSI-H)/错配修复缺陷(dMMR)直肠癌有效,对MSS/pMMR亚型单药治疗几乎无效。既往研究尝试放化疗联合PD-1抑制剂,pCR率可提升至30%~40%,但仍无法规避放疗毒性。
全程新辅助化疗(TNT)的出现为“去放疗”提供可能。PROSPECT等研究证实,单纯TNT的无病生存期(DFS)不劣于新辅助放化疗,但pCR率仅21.9%(以FOLFOX方案6个周期计)。如何通过免疫联合策略,将MSS/pMMR“冷肿瘤”转化为“热肿瘤”,在无放疗条件下进一步提升病理缓解,一直是全球结直肠肿瘤领域的研究热点与难点。
白细胞介素‑2(IL‑2)可激活CD8⁺ T细胞、NK细胞,重塑肿瘤免疫微环境,与PD‑1抑制剂存在协同抗肿瘤效应。基于此,团队创新性设计CapOX方案化疗+信迪利单抗(PD‑1抑制剂)+IL‑2的联合方案,开展PICS研究,探索其在MSS/pMMR局部进展期直肠癌中的疗效与安全性。
研究设计:精准入组,无放疗联合方案探索
该研究为单中心、开放标签、单臂II期试验,严格遵循伦理规范,经南京医科大学第一附属医院伦理委员会批准(批号:2023‑SR‑867),所有患者均签署书面知情同意。
入组标准:
年龄18~75岁,经病理确诊原发性直肠癌;肿瘤距肛缘≤12cm,影像学分期为cT3/4NanyM0或cTanyN+M0;免疫组化证实pMMR,基因检测确认为MSS/低微卫星不稳定性(MSI‑L);ECOG评分0~1分,无远处转移、无自身免疫病、未接受过抗肿瘤治疗。
治疗方案:
采用3周为1个周期的联合方案:第1天:静脉输注奥沙利铂130mg/m²+信迪利单抗200mg;第1~14天:口服卡培他滨1250mg/m²(每天);隔日皮下注射IL‑2(100万IU),共7次;每2个周期评估疗效,肿瘤退缩>20%则继续治疗,完成6个周期后4~6周行全直肠系膜切除术(TME)。
主要终点为pCR率(术后病理无存活肿瘤细胞)。次要终点包括R0切除率、主要病理缓解(MPR)率、肿瘤退缩分级(TRG)、临床完全缓解(cCR)率、无病生存期(DFS)、总生存期(OS)及治疗安全性。
核心结果:pCR率达42.4%,无放疗实现高效缓解
2023年11月至2024年12月,研究共入组33例患者,中位年龄57.9岁,男性占63.6%,ECOG 0分者84.8%;肿瘤分期以cT3(57.6%)、cN2(66.7%)为主;66.7%的患者环周切缘(CRM)阳性,均为高风险局部进展期病例。
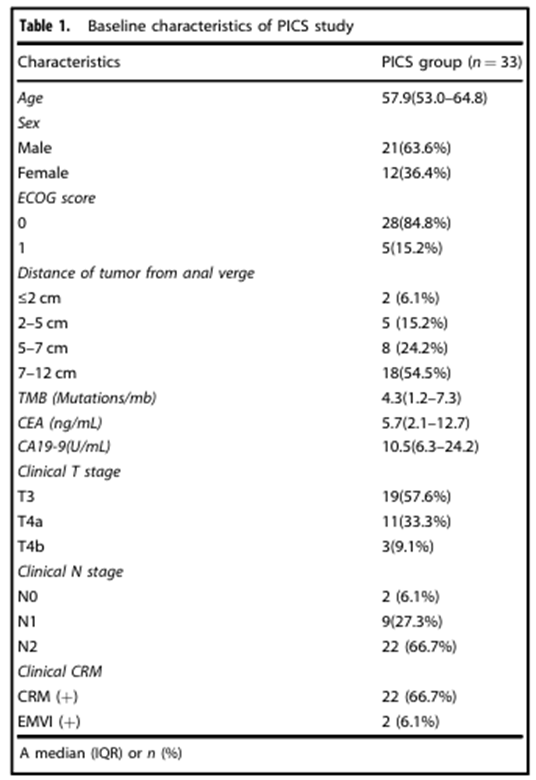
疗效结局:无放疗下病理缓解突破历史数据
手术切除:33例患者均完成根治术,R0切除率100%。末次治疗至手术间隔中位4.9周,显著短于放化疗方案的历史数据,降低了等待期肿瘤进展风险。
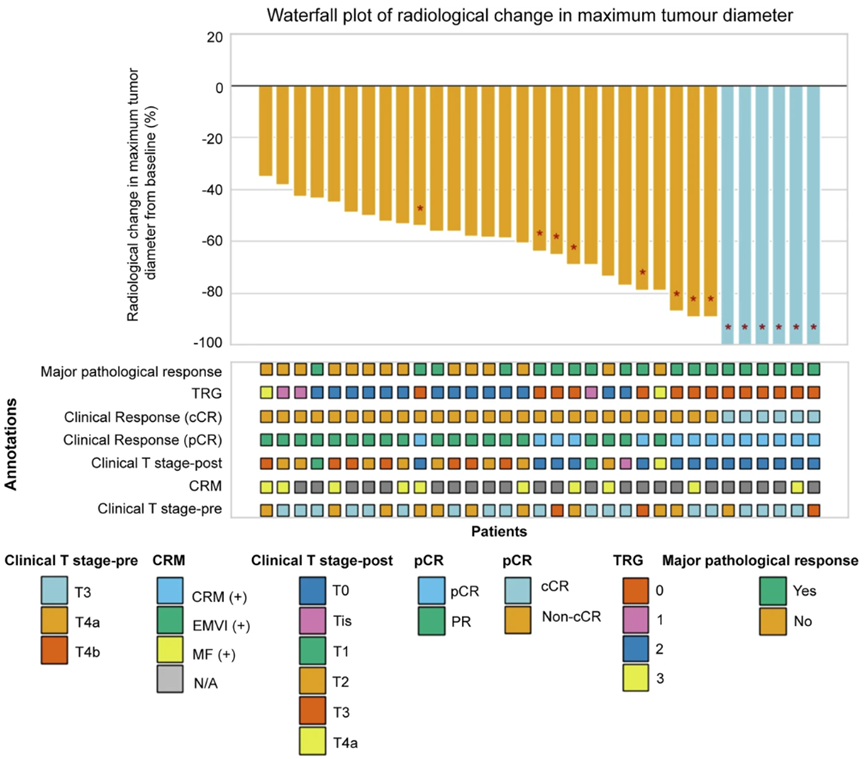
病理缓解:pCR率42.4%(14/33)(95%CI 25.68%~59.16%);MPR率57.6%(19/33);TRG0级(无残留肿瘤)占42.4%,TRG 1~2级占51.5%,仅6.1%患者肿瘤退缩不佳(TRG 3)。
临床缓解:术前cCR率18.2%(6/33);影像学评估肿瘤最大径中位退缩60.7%(IQR 50%~89%),退缩效果显著。
生存数据:中位随访22.6个月(17.7~27.4个月),1年OS率与DFS率均为100%,2年OS率97%(95%CI 84.7%~99.9%),2年DFS率90.9%(95%CI 75.7%~97.1%)。
免疫机制:成功激活抗肿瘤免疫微环境
研究通过流式细胞术、多重免疫荧光检测证实,达到pCR的患者体内出现显著免疫激活:
·外周血CD8⁺ T细胞比例、CD8/CD4比值大幅升高,NK细胞、M1型巨噬细胞显著扩增;
·肿瘤组织中CD8⁺ T细胞、CD56⁺ NK细胞、CD68⁺巨噬细胞浸润明显增多;
·IFN‑γ、TNF‑α等抗肿瘤细胞因子水平显著升高,成功将“冷肿瘤”转化为“热肿瘤”。
安全性:不良反应可控,无放疗相关损伤
·治疗相关不良反应总发生率为93.9%,以1~2级为主;3级不良反应发生率仅21.2%(7/33),无4~5级不良反应,无治疗相关死亡。最常见不良事件为呕吐(93.9%)、腹泻(39.4%)、骨髓抑制(30.3%),经对症处理后均缓解。
·无B/C级吻合口漏或肠梗阻等严重术后并发症,术后直肠系膜完整率为87.9%(29/33),3例预防性回肠造口均完成还纳,手术安全性优异。
深度讨论:去放疗联合免疫,突破MSS直肠癌治疗瓶颈
PICS研究作为全球首个在MSS/pMMR局部进展期直肠癌中探索TNT联合PD‑1抑制剂+IL‑2的II期研究,核心突破在于豁免放疗仍实现42.4%的高pCR率,远超单纯TNT方案的21.9%,与放化疗联合免疫方案疗效相当,且安全性更优。
1. 核心优势:去放疗的多重获益
·规避放疗毒性:彻底消除肠道纤维化、吻合口愈合不良、膀胱及性功能损伤等远期并发症,提升患者生活质量;
·缩短治疗周期:末次治疗至手术间隔缩短至4.9周,减少肿瘤进展风险,降低手术区域水肿与纤维化,提升保肛率;
·免疫协同增效:IL‑2与PD‑1抑制剂联合,重塑免疫微环境,解决MSS亚型免疫耐受难题,实现高效病理缓解。
2. 与既往研究对比:疗效相当,安全性更优
既往放化疗联合PD‑1抑制剂方案的pCR率为30%~44.8%(单臂研究30%~40%,随机对照研究31.9%~44.8%),但3~4级不良反应发生率达36%~48.2%。该研究无放疗、pCR率42.4%、3级不良反应仅21.2%,在疗效相当的前提下,安全性显著提升。
3. 研究局限性与未来方向
该研究为单臂、小样本II期研究,随访时间较短,长期生存获益需进一步验证;且为单中心数据,需多中心随机对照研究确证。此外,研究未纳入患者报告结局(PRO)或生活质量(QOL)数据。未来团队将开展III期研究,探索cCR患者的“等待观察”策略(联合维持免疫治疗),进一步实现器官保留,同时基于免疫标志物筛选优势获益人群。
结语
PICS研究为MSS/pMMR局部进展期直肠癌提供了全新治疗选择。全程新辅助化疗联合PD‑1抑制剂+IL‑2方案,在豁免放疗的前提下,实现100% R0切除、高达42.4%的pCR率,安全性可控、免疫激活明确,突破了传统放化疗的毒性局限,为中低位直肠癌患者保留器官功能、提升生活质量提供了循证医学证据。
Tang J, Wang L, Yang S, et al. Total neoadjuvant chemotherapy combined with PD‑1 blockade and IL‑2 in MSS/pMMR locally advanced rectal cancer: short-term results of a prospective, single-arm phase II study. Signal Transduct Target Ther. 2026;11(1):163.
排版编辑:肿瘤资讯-ZJN











 苏公网安备32059002004080号
苏公网安备32059002004080号


