原发纵隔大B细胞淋巴瘤(PMBCL)是一种罕见的侵袭性非霍奇金淋巴瘤亚型,约占所有非霍奇金淋巴瘤的2%-3%。尽管大多数患者通过标准一线治疗——剂量调整的依托泊苷、多柔比星、环磷酰胺、长春新碱、泼尼松联合利妥昔单抗(DA-EPOCH-R)——可获得治愈,5年无进展生存(PFS)率超过90%,但仍有少数患者面临复发或难治的困境。对于这些患者,挽救治疗策略的选择及后续自体造血干细胞移植(ASCT)的价值,一直是临床决策中的关键问题。
近年来,随着新型治疗手段的不断涌现,如维布妥昔单抗(BV)联合免疫检查点抑制剂、嵌合抗原受体T细胞(CAR-T)疗法等,PMBCL复发后的治疗格局正在发生变化。然而,现有文献关于DA-EPOCH-R一线治疗后复发患者的真实世界数据极为有限,样本量小、治疗方案异质性高,难以指导临床实践。近期,Haematologica杂志发表了一项由美国十家学术医学中心联合开展的大规模回顾性研究结果,系统描绘了复发/难治(R/R)PMBCL患者的挽救治疗结局,为临床决策提供了重要参考。

研究方法:多中心协作的大规模回顾性分析
研究设计与人群:本研究为一项回顾性、多中心队列研究,纳入2011年至2023年间美国十家学术医学中心的R/R PMBCL患者。纳入标准为:经组织学确诊的PMBCL,一线接受DA-EPOCH-R治疗后复发或进展。
治疗方案分类:
传统挽救治疗:以抗CD20单抗(利妥昔单抗或奥妥珠单抗)联合ICE(异环磷酰胺、卡铂、依托泊苷)或DHAP(地塞米松、大剂量阿糖胞苷、顺铂)等化疗方案为主。
新型挽救治疗:BV联合纳武利尤单抗、帕博利珠单抗等免疫治疗。
临床试验:包括R-ICE联合伊布替尼、R-DHAX联合Epcoritamab等。
CAR-T细胞治疗:阿基仑赛、替沙仑赛、利基迈仑赛或临床试验产品。
ASCT:挽救治疗后进行的ASCT。
异基因造血干细胞移植(Allo-SCT):用于部分多次复发患者。
主要研究终点包括客观缓解率(ORR)、完全缓解(CR)率、无进展生存期(PFS)和总生存期(OS)。
研究结果:R/R患者的显著预后差异
患者特征
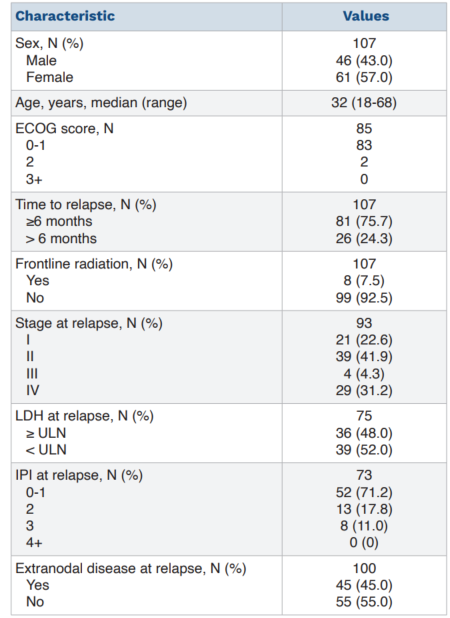
共107例患者纳入分析,中位年龄32岁(范围18-68岁),女性占57%。复发时特征:Ⅰ/Ⅱ期占65%,LDH升高占48%,活检证实复发占73%。一线DA-EPOCH-R治疗后,62%的患者未达到CR,76%的患者在初始治疗后6个月内复发或进展,被定义为“难治性”(refractory);仅24%的患者在6个月后“复发”(relapsed)。8例(7.5%)患者一线治疗后接受了巩固放疗。
中位随访48.9个月,全组中位OS未达到,估计2年OS率为87%(95%CI:80-94),5年OS率为78%(95%CI:70-88)。19例死亡中,17例死于疾病进展,2例死于异基因SCT后的移植物抗宿主病。
表1. 患者基线特征
挽救治疗分析
90例(84%)患者纳入挽救治疗分析,17例因中枢神经系统受累(8例)、直接接受CAR-T作为首次挽救(6例)或未接受挽救治疗即行ASCT(3例)被排除。
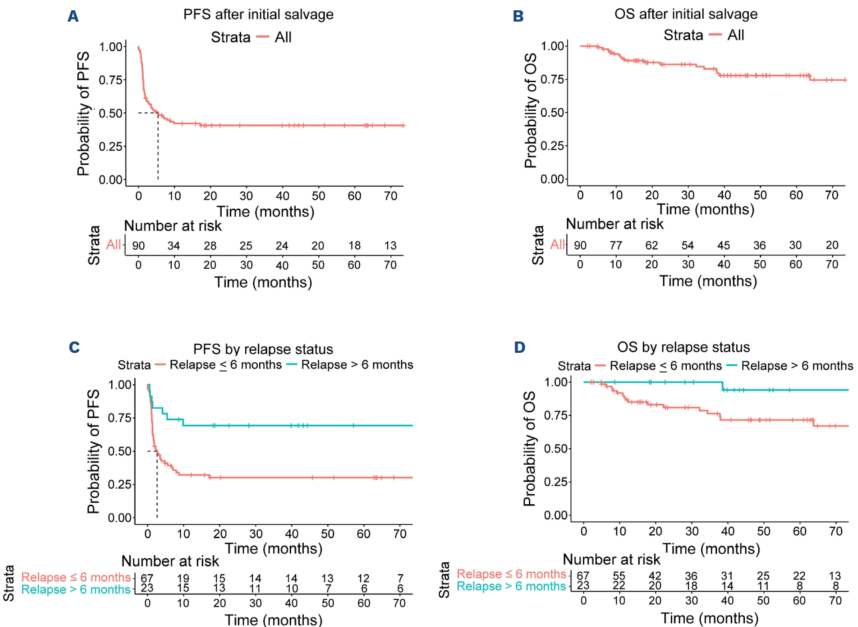
整体挽救治疗结局:首次挽救治疗后,ORR为57%(95%CI:46-67),CR率为26%(95%CI:17-36)。中位随访48.9个月,中位PFS为5.4个月(95%CI:2.3个月-未达到),5年OS率为78%(95%CI:69-88)。
难治性 vs. 复发患者:两组结局差异显著。难治性患者(N=67)的ORR为48%(95%CI:35-60),CR率为19%(95%CI:11-31),2年PFS率为30%(95%CI:21-44),5年OS率为72%(95%CI:60-85)。
复发患者(N=23)的ORR为83%(95%CI:61-95),CR率为44%(95%CI:23-66),2年PFS率为69%(95%CI:53-91),5年OS率为94%(95%CI:84-100)。
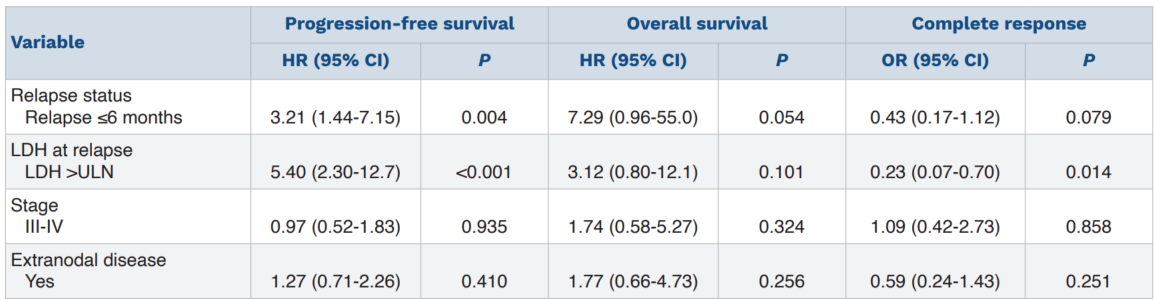
预后因素:单因素分析显示,首次挽救治疗后CR的独立预测因素为复发时LDH正常(OR=0.23,95%CI:0.07-0.70,P=0.014)。PFS的不良预后因素包括难治性疾病(HR=3.21,95%CI:1.44-7.15,P=0.004)和LDH升高(HR=5.40,95%CI:2.30-12.7,P<0.001)。多因素分析中,难治性疾病(HR=2.58,95%CI:1.05-6.32,P=0.04)和LDH升高(HR=5.42,95%CI:2.30-12.8,P<0.001)仍为PFS的独立不良因素。
表2. 单变量Cox和logistic回归模型用于评估进展、死亡和完全缓解的风险
挽救治疗方案:86%的患者首次挽救接受传统化疗,以R-ICE(51%)和R-DHAP(12%)为主。传统挽救治疗的ORR为53%(95%CI:42-65),CR率为22%(95%CI:13-33),2年PFS率为35%(95%CI:26-48),5年OS率为76%(95%CI:66-87)。15例患者接受BV+纳武利尤单抗治疗,其中9例作为首次挽救,ORR为80%(95%CI:52-96),CR率为47%(95%CI:21-73),2年PFS率为70%(95%CI:49-100),5年OS率为91%(95%CI:75-100)。但研究指出,新型挽救治疗的样本量不足以与传统挽救治疗进行有意义的比较。
ASCT
48例患者(难治性30例,复发18例)在挽救治疗后接受ASCT。中位随访56.1个月,中位PFS和OS均未达到,估计5年PFS率为85%(95%CI:75-96),5年OS率为88%(95%CI:79-99)。
移植前缓解状态的关键价值:移植前达到CR的29例患者,移植后无一例复发。移植前为PR的17例患者,2年PFS率为69%(95%CI:49-96)。22例患者移植前接受放疗,11例移植后接受放疗。
CAR-T细胞治疗
42例患者接受CD19 CAR-T细胞治疗。6例作为二线治疗,36例作为三线及以上治疗。4例在CAR-T前接受过ASCT。可评估患者的ORR为74%(95%CI:58-86),CR率为57%(95%CI:41-72),2年PFS率为64%(95%CI:51-81),2年OS率为80%(95%CI:67-95),5年OS率为71%(95%CI:56-90)。
Allo-SCT
9例患者接受Allo-SCT,中位既往治疗线数为2线(范围2-5线)。中位随访48.1个月,中位OS为40.2个月(95%CI:9.8-未达到),2年PFS率和OS率均为67%(95%CI:42-100),5年OS率为50%(95%CI:24-100)。
中枢神经系统复发
8例患者(难治性6例,复发2例)复发时伴中枢神经系统受累。中位随访39.5个月,2年OS率为80%(95%CI:52-100)。7例接受大剂量甲氨蝶呤为基础的方案,5例达CR后行ASCT,目前均维持CR。
总结
这项美国十中心回顾性研究基于107例R/R PMBCL患者的数据,系统描绘了DA-EPOCH-R一线治疗后复发患者的真实世界治疗结局。研究证实,难治性(6个月内复发)患者对挽救治疗的反应显著差于晚期复发患者,而ASCT前达到CR的患者可获得极佳的长期预后。尽管首次挽救治疗的PFS较短,但丰富的后续治疗选择使整体5年OS率维持在78%的较高水平。
这些发现对临床实践具有指导意义:对于DA-EPOCH-R后6个月内复发的难治性PMBCL患者,传统挽救化疗+ASCT的长期无病生存率较低,CAR-T细胞治疗应被强烈考虑;对于晚期复发患者,挽救化疗后ASCT仍是合理选择,但应力争在移植前达到CR;移植前PR的患者需个体化评估,可能需要探索强化策略。未来研究应聚焦于不同挽救策略在前瞻性队列中的比较,以及CAR-T与ASCT作为二线治疗的随机对照评估,以进一步优化R/R PMBCL的治疗格局。
Hess B, Moskowitz A, Davis JA, et al. Outcomes of patients with relapsed or refractory primary mediastinal B-cell lymphoma after frontline DA-EPOCH-R. Haematologica. 2026;111(4):1389-1395.
排版编辑:Mathilda











 苏公网安备32059002004080号
苏公网安备32059002004080号


