在多发性骨髓瘤(MM)诊疗领域,微小残留病(MRD)阴性已被确立为深度缓解的重要标志和独立预后因素。然而,临床实践中的一个现实问题是:并非所有患者都能达到MRD阴性状态,尤其在真实世界环境中,治疗方案常因患者年龄、合并症及耐受性而调整。那么,对于未能实现MRD阴性的患者,或者MRD阴性后再次转阳的患者,如何判断其长期预后?单次时间点的MRD状态是否足以指导临床决策?
基于此,一项基于中国国家级血液病纵向队列(NICHE)的大规模回顾性研究为上述问题提供了重要线索。该研究由中国医学科学院血液病医院(中国医学科学院血液学研究所)邱录贵教授、安刚教授以及深圳市第二人民医院李晓清教授共同作为通讯作者,纳入1048例初治MM(NDMM)患者,通过5406次MRD动态监测数据的深度分析,首次系统揭示了MRD反应时机与持续时间在真实世界中的独立预后价值。近期,该研究成果已发表于International Journal of Cancer杂志,为MM的个体化风险分层和长期疾病监测提供了新的循证依据。

研究背景:从“MRD阴性”到“MRD动态轨迹”
既往研究已证实,MRD阴性与改善的无进展生存期(PFS)和总生存期(OS)密切相关,而MRD由阴性转为阳性则提示预后不良。在MAIA和ALCYONE等关键临床试验中,维持MRD阴性超过6或12个月的患者,其PFS显著延长,且这一效应独立于治疗方案。
然而,现有研究主要聚焦于MRD阴性状态的“有无”或“维持时间”,对MRD反应的“时间动力学”——即达到最佳MRD状态所需的时间(Time to Best MRD Response, TBR)——关注不足。此外,真实世界中的患者群体往往比临床试验更为异质,治疗强度不一,部分患者可能仅达到低水平MRD阳性但长期稳定。对于这类患者,其MRD动态变化是否蕴含预后信息?传统基于常规疗效标准(如完全缓解、非常好的部分缓解)的反应动力学研究提示,缓慢但稳定的深度缓解可能与良好预后相关,但MRD层面的反应动力学证据仍较缺乏。
基于此,研究团队利用中国国家级血液病纵向队列(NICHE, NCT04645199)的真实世界数据,开展了迄今规模较大的MRD反应动力学回顾性分析,旨在回答三个核心问题:(1)达到最佳MRD反应的时间是否与预后相关?(2)MRD反应的持续时间是否具有独立预后价值?(3)将反应时机与持续时间整合,能否识别出超越传统MRD状态的预后模式?
研究方法:大规模真实世界队列的纵向MRD分析
研究设计与人群:研究回顾性纳入2012年至2023年间在NICHE队列中登记的NDMM患者。纳入标准为:经IMWG标准确诊,治疗启动后至少接受两次序贯MRD评估。最终1048例患者纳入分析,中位年龄59岁(四分位距52-66岁),男性占57.0%,ISS Ⅲ期占41.9%。
治疗方案:诱导治疗以蛋白酶体抑制剂(PI)为基础(42.9%)或PI联合免疫调节剂(IMiD)(37.5%),7.8%接受CD38单抗为基础的方案,39.9%接受自体造血干细胞移植(ASCT)。中位随访53.98个月。
MRD检测与定义:2012~2017年采用八色MFC检测,中位灵敏度4.2×10⁻⁵;2018~2023年采用EuroFlow标准NGF检测,中位灵敏度3.5×10⁻⁶。MRD阴性定义为在相应灵敏度阈值下未检测到表型异常克隆浆细胞(MFC: >10⁻⁴;NGF: >10⁻⁵)。对于MRD不可测患者,肿瘤负荷视为低于检测下限。
研究结果:MRD时机与持续时间的独立预后价值
MRD反应时间与生存结局呈正相关
1048例患者共接受5406次MRD评估,中位评估次数5次(范围2-19次)。597例(56.9%)至少一次达到MRD阴性。全队列中位TBR为5.40个月。
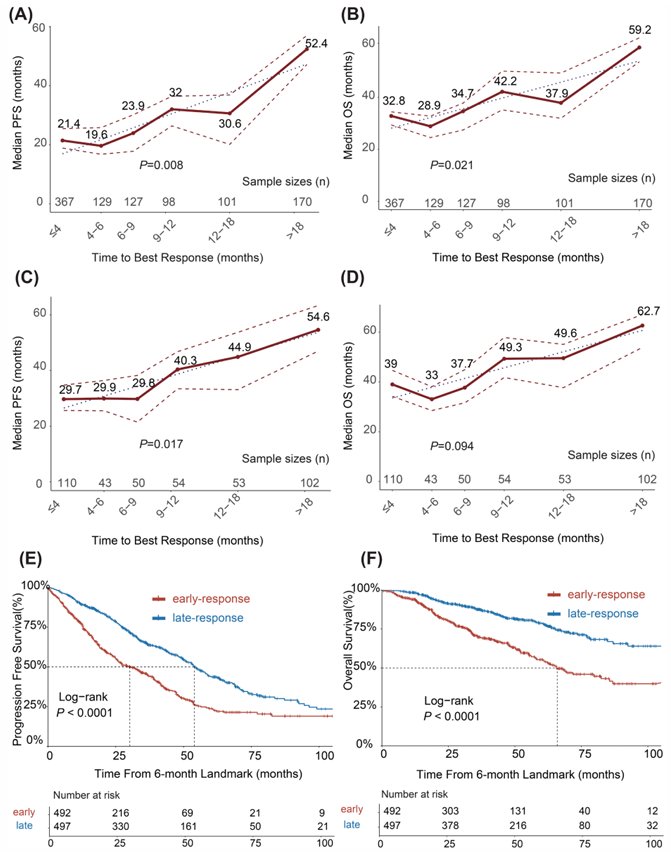
多时间点界碑分析显示,TBR与PFS和OS呈正相关:达到最佳MRD反应时间越长的患者,其生存结局越好。这一趋势在MFC和NGF两个检测方法亚组中均一致存在,在移植患者中尤为明显。
以6个月为界将患者分为早期应答者(≤6个月)和晚期应答者(>6个月)。6个月界碑分析显示,晚期应答者的中位PFS显著优于早期应答者(53.97个月 vs. 30.18个月,P<0.001),OS差异更为显著(中位OS:未达到 vs. 65.58个月,P<0.001)。
值得注意的是,在仅纳入最终达到MRD阴性患者的分析中,从首次MRD阴性起计算的PFS和OS在早期与晚期应答者之间无显著差异(中位PFS:48.42 vs. 48.97个月,P=0.48;中位OS:均未达到,P=0.92)。这提示一旦实现深度缓解,达到该缓解的速度本身不再影响后续预后。然而,在未达到MRD阴性但存在低水平残留病灶(最佳MRD水平10⁻⁵至<10⁻³)的患者中,晚期应答者仍显示出更长的PFS(33.02 vs. 26.60个月,P=0.140)和显著更长的OS(未达到 vs. 55.21个月,P=0.008)。
早期应答者具有更差的基础疾病特征
基线特征比较揭示了一个看似矛盾的现象:早期应答者实际上具有更不利的疾病生物学特征。早期应答者的贫血(55.7% vs. 47.7%,P=0.014)、血小板减少(15.9% vs. 8.5%,P<0.001)和ISS Ⅱ-Ⅲ期比例(79.2% vs. 72.6%,P=0.034)更高,接受PI+IMiD联合诱导治疗的比例更低(33.1% vs. 42.5%,P=0.028)。细胞遗传学方面,早期应答者中t(14;16)的发生率更高(4.4% vs. 1.7%,P=0.023)。
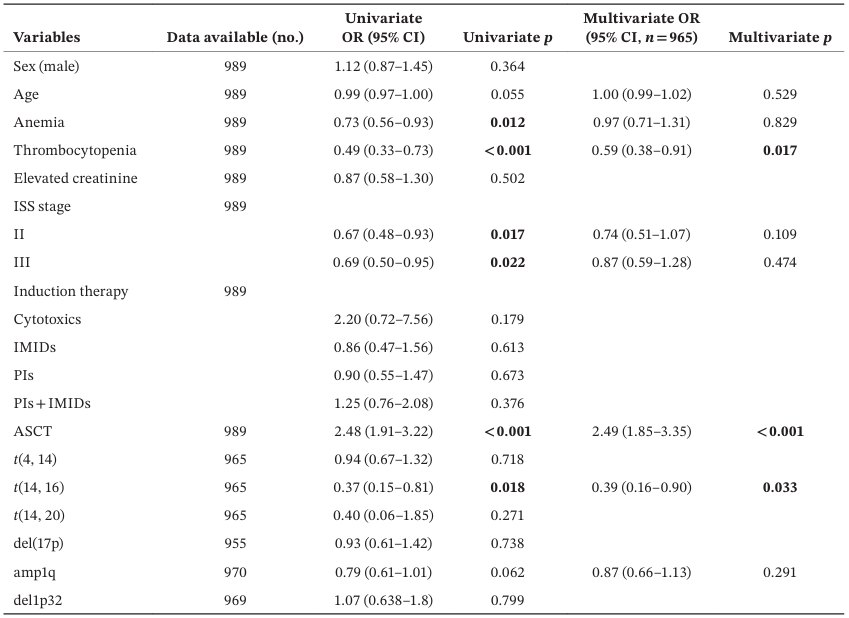
多因素logistic回归分析证实,ASCT与晚期应答独立相关(OR=2.49,95%CI:1.85-3.35,P<0.001),而血小板减少(OR=0.59,95%CI:0.38-0.91,P=0.017)和t(14;16)(OR=0.39,95%CI:0.16-0.90,P=0.033)与早期应答独立相关。这一结果提示,早期应答可能反映了肿瘤负荷较高、疾病侵袭性较强的患者对治疗的快速反应,但这种反应可能伴随较差的长期预后。
表1.MRD早期与晚期应答相关因素的单变量和多变量logistic回归分析
MRD持续时间是独立于MRD状态的预后因素
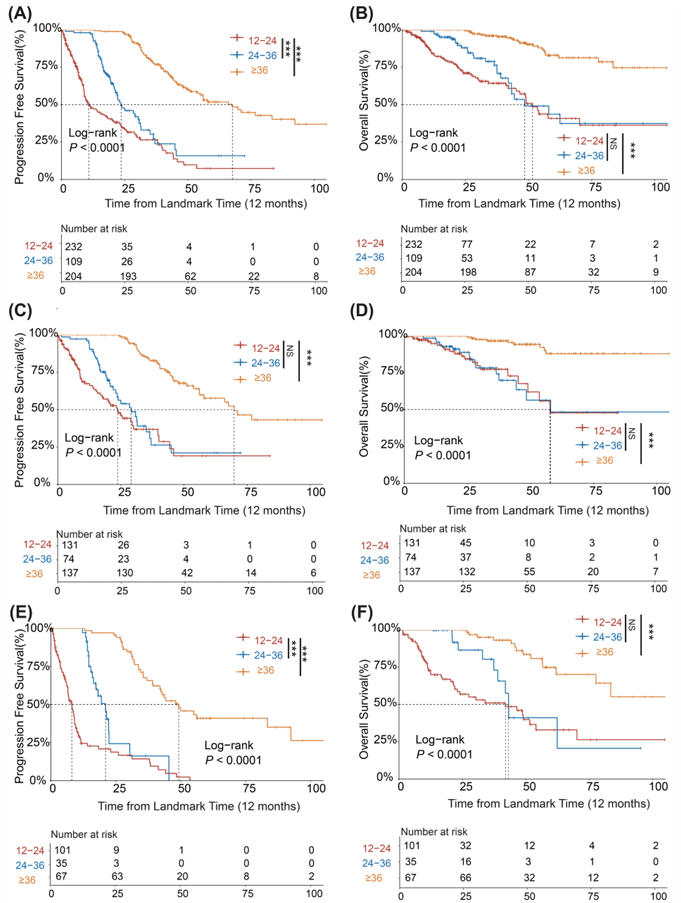
研究进一步评估了MRD反应持续时间的预后意义。12个月界碑分析(排除MRD持续时间<12个月者以减少选择偏倚)显示,在整体队列中,MRD持续时间≥36个月者的中位PFS为67.67个月,显著优于12-24个月者(10.76个月)和24-36个月者(23.60个月)(P<0.001);OS呈现相似模式(≥36个月:未达到;12-24个月:51.54个月;24-36个月:48.36个月,P<0.001)。
亚组分析显示,这一效应在MRD阴性患者和持续MRD阳性患者中均成立:
MRD阴性亚组:持续时间≥36个月者中位PFS达69.88个月,而12-24个月与24-36个月组之间无显著差异(23.69 vs. 29.10个月,P=0.078;OS:57.70 vs. 57.96个月,P=0.91)。这提示MRD阴性持续超过36个月可能是一个关键的预后阈值。
MRD阳性亚组:持续时间≥36个月者中位PFS为49.21个月,OS未达到,显著优于较短持续时间组。
时间依赖Cox回归模型进一步证实,维持在最佳MRD状态与进展风险降低36%(HR=0.64,95%CI:0.57-0.71,P<0.001)和死亡风险降低23%(HR=0.77,95%CI:0.66-0.89,P<0.001)相关。
“晚期+持久”MRD模式:高危患者的预后改善标志
研究的核心发现在于将MRD反应时机与持续时间整合后产生的协同预后效应。多因素时间依赖Cox回归分析(调整贫血、血小板减少、ASCT状态、ISS分期、amp1q、MRD状态及HRCA)显示,晚期应答(HR=0.36,95%CI:0.31-0.42,P<0.001)和持久MRD状态(HR=0.31,95%CI:0.26-0.36,P<0.001)均为PFS的独立保护因素,且两者之间存在显著交互作用(交互HR=3.68,95%CI:2.85-4.74,P<0.001)。
基于12个月界碑分析,将患者分为四组:早期/短暂、早期/持久、晚期/短暂、晚期/持久。“晚期+持久”组预后最佳,中位PFS达99.32个月,而“早期+短暂”组最差(18.95个月)。“晚期+持久”组的中位OS未达到,而“早期+短暂”组仅46.28个月。这一模式在仅纳入MRD阴性患者的分析中同样成立,提示即使在深度缓解者中,“晚期+持久”特征仍能识别出真正预后良好的亚群。
更为重要的发现是,“晚期+持久”模式似乎能够克服传统不良预后因素的影响:
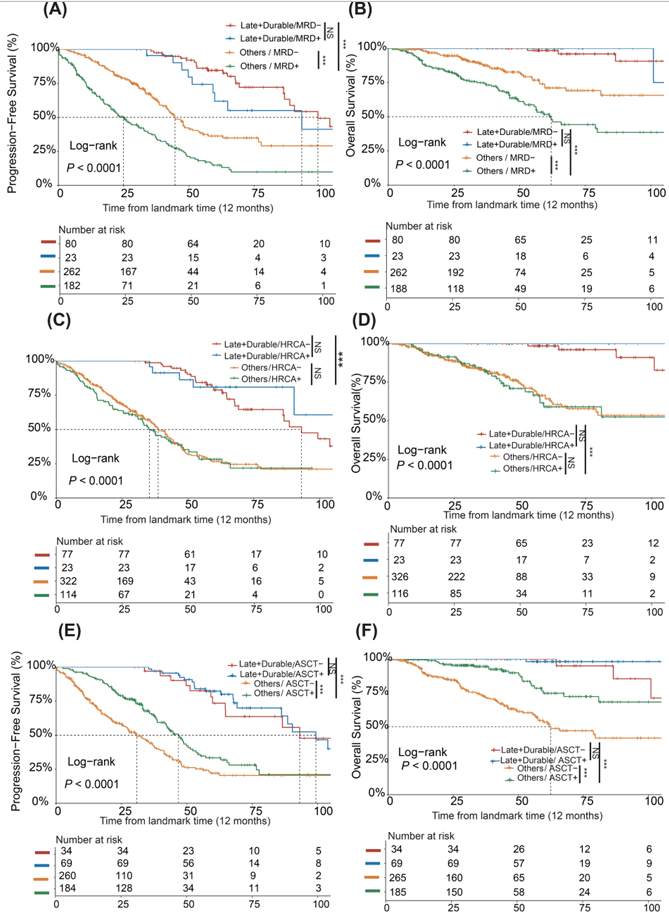
在持续MRD阳性患者中:“晚期+持久/MRD阳性”组的中位PFS(93.13个月)与“晚期+持久/MRD阴性”组(99.32个月)无显著差异(P=0.270),且显著优于其他MRD阴性或阳性组。两组OS均未达到(P=0.981)。
在高危细胞遗传学异常患者中:“晚期+持久/HRCA阳性”组的中位PFS未达到,与“晚期+持久/HRCA阴性”组(93.13个月)无显著差异(P=0.54),两组OS均未达到(P=0.399),但均显著优于“其他/HRCA阳性”组(中位PFS 35.40个月)。
在未移植患者中:“晚期+持久/未移植”组的中位PFS为93.13个月,与移植组(99.32个月)无显著差异(P=0.97),OS均未达到(P=0.13)。
总结
这项基于中国千例真实世界队列的研究表明,MRD反应的时机与持续时间是NDMM的独立预后因素,其价值可能超越单次MRD状态的评估。“晚期且持久”的MRD反应模式——即缓慢达到但长期维持的最佳MRD状态——与改善的PFS和OS密切相关,且这一关联在持续MRD阳性、高危细胞遗传学异常及未接受移植的患者中依然成立。
这些发现提示,临床实践中应重视MRD的动态纵向监测,将反应时机与持续时间纳入综合预后评估体系。对于无法达到MRD阴性的患者,维持长期稳定的低水平疾病状态可能是可行的治疗目标;而对于高危患者,持久的MRD反应——无论最终是否达到阴性——可能意味着不良预后因素的克服。未来研究需在新型治疗背景下验证这些发现,并探索MRD动力学指导下的个体化治疗调整策略。
Zhou J, Yan W, Liu Y, et al. Late and Durable Minimal Residual Disease Response Predicts Favorable Outcomes in Newly Diagnosed Multiple Myeloma. Int J Cancer. 2026. https://onlinelibrary.wiley.com/doi/abs/10.1002/ijc.70465
排版编辑:Mathilda











 苏公网安备32059002004080号
苏公网安备32059002004080号


