滤泡性淋巴瘤(FL)是最常见的惰性B细胞淋巴瘤。传统一线化疗免疫治疗方案虽能使多数患者获得缓解,但毒性问题突出。对于高肿瘤负荷的初治患者,如何在保持疗效的同时降低治疗毒性,仍是临床未满足的需求。近年来,免疫检查点抑制剂与CD20靶向药物的联合应用为FL治疗提供了新思路,但单纯双药联合的疗效尚未达到化疗免疫治疗的水平。放射治疗(RT)具有直接的细胞毒作用和潜在的免疫调节效应,低剂量放疗在FL中已证实有较好的局部控制率。
基于上述背景,澳大利亚研究团队设计了一项Ⅱ期临床试验,探索奥妥珠单抗联合阿替利珠单抗及PET导向的超低剂量放疗在初治FL中的疗效与安全性。近期,该研究结果已发表于British Journal of Haematology杂志,【肿瘤资讯】现将该研究主要内容整理如下,以飨读者。

研究设计:精准筛选与PET适应性策略
FLUORO研究(NCT04962126)是一项多中心、单臂、Ⅱ期临床试验,采用Simon两阶段设计(80%检验效能,单侧α=0.05),以30%的CR率为无效假设。第一阶段计划入组15例患者,若6例及以上达到CR,则扩展至总计46例;若46例中19例及以上达到CR,则拒绝无效假设。
入组标准:年龄≥18岁,初治、组织学确诊的1-3A级FL(WHO 2016分类),Ann Arbor II-IV期,ECOG体能状态0-2分,具有可测量病灶,符合GELF或BNLI高肿瘤负荷标准。
治疗方案:
诱导治疗:6个周期的奥妥珠单抗(1000mg,第1周期第1、8、15天给药,后续周期第1天)联合阿替利珠单抗(1200mg),每21天为一周期。
PET适应性放疗:第2周期后行中期PET/CT评估。对残留FDG摄取病灶(>1cm)者,于第3周期后实施超低剂量受累部位放疗(4Gy/2次,连续两天)。放疗遵循ILROG指南,最多6个照射野。
维持治疗:诱导结束后达疾病稳定、部分缓解或完全缓解者,接受奥妥珠单抗维持治疗(1000mg,每8周,最长12个周期)。
评估与终点:PET/CT于基线、第2周期后、放疗后(可选)、第6周期后及维持期间每6个月进行。主要终点为诱导结束时完全缓解(CR)率(Lugano 2014标准)。次要终点包括总缓解率(ORR)、无进展生存期(PFS)、总生存期(OS)、至下次治疗时间(TTNT)及安全性。探索性终点包括PET影像组学参数(SUVmax、TMTV、TLG)及肿瘤免疫基因表达谱(NanoString PanCancer Immune面板)。
研究结果:疗效显著,安全性良好
患者特征
2021年8月至2022年10月,共入组16例患者。中位年龄53岁(33-79岁),男性7例(43%)。Ann Arbor Ⅳ期13例(81.3%),Ⅲ期3例(18.7%)。FLIPI评分:低危1例(6%),中低危7例(44%),中高危7例(44%),高危1例(6%)。56%存在大包块,44%伴骨髓受累,31%有脾肿大。
表1. 患者特征
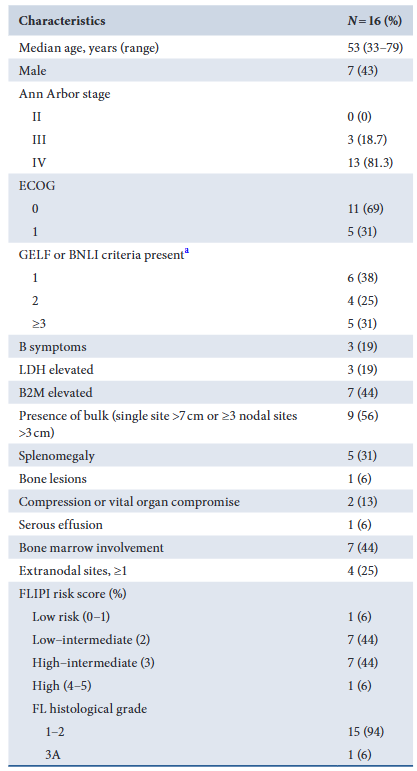
治疗实施
15例(94%)完成6周期诱导治疗。1例因第1周期奥妥珠单抗3级输注反应终止治疗,纳入安全性分析,未纳入疗效分析。
第2周期后PET评估:3例(20%)达CR,直接继续后续奥妥珠单抗+阿替利珠单抗治疗;12例(75%)为PR,接受超低剂量放疗,中位照射3个部位(范围1-5个)。放疗技术包括3D-适形、调强或电子线照射。
疗效数据
主要终点:15例可评估患者中,最佳CR率为93%(14/15,95%CI:70%-99%),ORR为100%(95%CI:75%-100%)。诱导结束时CR率为87%(13/15)。
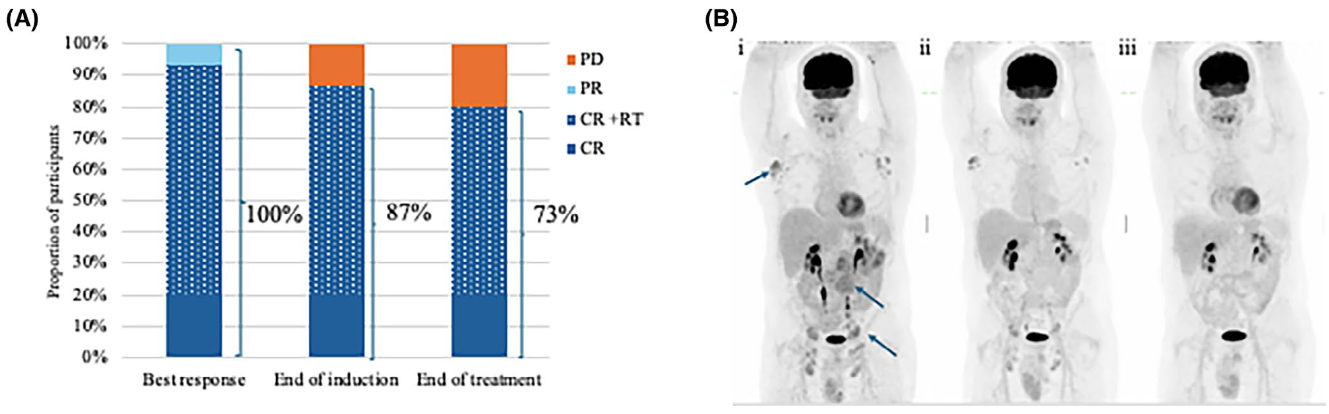
长期随访:中位随访41个月(范围31.25个月-未达到)。治疗全部结束后,73%(11/15)维持CR。共4例疾病进展:2例于诱导结束PET/CT4时进展(1例经活检证实转化为弥漫大B细胞淋巴瘤),1例于维持治疗第9周期后进展,1例于随访期间进展。
生存数据:3年PFS率为80%(95%CI:55%-93%),3年OS率为100%(95%CI:79.6%-100%)。中位PFS和OS均未达到。中位TTNT为27个月(范围8-43个月)。
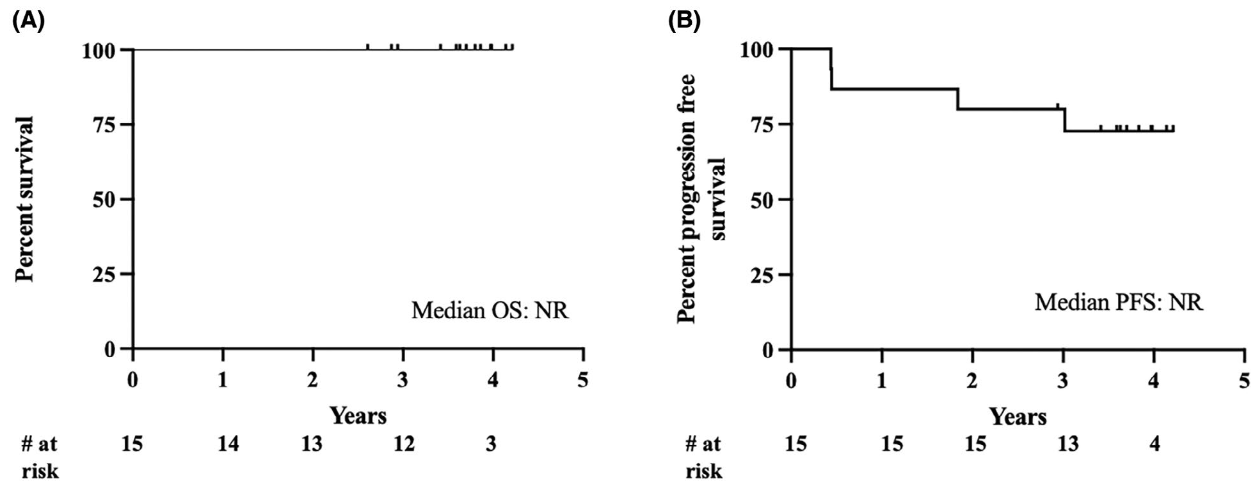
研究满足Simon两阶段设计第一阶段的继续标准,但因申办方战略调整提前终止,未进入第二阶段扩展。
安全性
诱导期间5例(31%)发生3-4级不良事件;维持期间4例(31%)发生3-4级不良事件。全组仅1例4级不良事件(中性粒细胞减少,维持期)。2例(15%)发生3级以上免疫相关不良事件。
11例严重不良事件发生于8例患者,其中8例为感染(4例COVID-19、3例呼吸道感染、1例尿路感染)。中位住院时间4天(范围2-26天)。
1例(6%)因毒性终止治疗(输注反应);诱导期间6例(19%)因感染暂停用药。
未观察到明确归因于放疗的显著急性毒性。
探索性分析
PET影像组学:进展或最佳疗效为PR者基线TLG(4568.8 vs 2160.9)和TMTV(1125.9 vs 535.4)高于早期CR且持续缓解者(P=0.02)。进展者诱导结束delta TMTV低于持续缓解者。
基因表达谱:9例患者基线活检样本中,8例通过质控。进展者肿瘤中IL7R、SELL、AKT3、HLA-G、IFNL1表达下调,但未达到多重检验校正后的显著性阈值。
总结
本研究是首个报道抗CD20单抗、PD-L1抑制剂与放疗联合用于淋巴瘤的临床研究。在16例初治高肿瘤负荷FL患者中,最佳CR率93%,ORR 100%,3年PFS率80%,3年OS率100%。3-4级毒性发生率31%,低于GALLIUM研究中化疗免疫治疗组的70%-75%。
探索性生物标志物结果提示基线TMTV/TLG和中期代谢反应可能与预后相关,IL7R、SELL等基因下调可能与T细胞耗竭状态有关。但这些发现基于极小的样本量,且未通过多重检验校正,目前仅可作为假设生成,需独立验证。
总之,FLUORO研究初步显示,奥妥珠单抗联合阿替利珠单抗及PET适应性超低剂量放疗在初治高肿瘤负荷FL中获得了较高的缓解率和可接受的安全性。然而,由于样本量小、单臂设计及提前终止,该方案的疗效和安全性仍需在更大规模的随机对照研究中验证。目前,这一无化疗策略尚不能取代标准治疗,但为后续研究提供了值得探索的方向,包括与新型药物(如双特异性抗体)的联合及生物标志物指导的个体化治疗。
JMartynchyk A, Chong G, Khor R, et al. Checkpoint inhibitors, obinutuzumab plus PET-adapted ultra-low dose nodal radiotherapy yield high efficacy in treatment-naïve follicular lymphoma: Results from the phase II 'FLUORO' study. Br J Haematol. 2026.
排版编辑:Mathilda











 苏公网安备32059002004080号
苏公网安备32059002004080号


