在慢性淋巴细胞白血病(CLL)的临床试验中,可测量残留病(MRD)检测正被越来越多地用作主要终点,其前提是MRD能够准确预测无进展生存期(PFS),而PFS本身又是总生存的替代终点。然而,MRD与PFS之间的关联强度是否因治疗方式、药物类型和样本来源而异,一直是临床和监管决策中的争议焦点。近期,Leukemia杂志发表了一项纳入43项临床试验、9628例受试者的大型荟萃分析,系统评估了MRD作为PFS替代终点的准确性。
研究发现,尽管MRD在个体层面与PFS显著相关,但在试验层面的替代效度有限,且高度依赖于治疗策略——在BTK抑制剂治疗和持续给药方案中相关性尤其薄弱,仅在固定疗程的化学免疫治疗和骨髓MRD检测中接近预设的有效性阈值。这一发现为MRD在CLL临床试验和监管审批中的应用提供了重要的循证边界。

研究背景:MRD作为替代终点的争议
CLL是西方国家最常见的成人白血病,近年来治疗格局发生了革命性变化。BTK抑制剂和BCL-2抑制剂等靶向药物显著改善了患者预后,RESONATE-2试验中伊布替尼一线治疗的中位PFS达8.9年,维奈克拉联合抗CD20单抗方案使约70%患者达到MRD阴性状态。
在这一背景下,MRD检测因其能够反映治疗后的肿瘤负荷,被欧洲药品管理局(EMA)接受为PFS的中间终点,但在美国FDA尚未获得同等认可。2024年4月,FDA肿瘤药物咨询委员会曾专门讨论这一问题。核心争议在于:MRD能否在不同治疗模式下稳定、可靠地替代PFS,从而加速新药审批并指导临床治疗决策?
理论上,MRD作为替代终点具有多重优势:检测时间早于临床终点、样本量需求较小、可缩短试验周期。然而,其有效性取决于与临床获益之间关联的强度和一致性。既往研究提示,MRD的预测价值可能因治疗机制而异——BTK抑制剂主要通过细胞抑制作用而非深度细胞清除发挥作用,患者可能在MRD可检测的情况下仍维持长期疾病控制;而维奈克拉等BCL-2抑制剂则通过诱导细胞凋亡实现深度缓解,MRD阴性率与PFS的关联可能更为紧密。
为系统回答这一问题,研究团队开展了迄今规模最大的荟萃分析,从个体和试验两个层面量化MRD与PFS的关联,并探索治疗方式、药物类型和样本来源等关键调节变量。
研究方法:双重验证框架与多层次分析
研究检索了PubMed、Web of Science、Embase和Cochrane Library四大数据库,纳入截至2025年2月8日发表的英文文献。纳入标准为报告PFS和MRD检测结果的Ⅱ期或Ⅲ期前瞻性研究,排除回顾性分析、综述、病例报告、重复数据集、移植研究以及MRD/PFS数据不完整的研究。最终纳入43项试验,涵盖9628例受试者,其中个体层面分析纳入28项试验的4636例受试者,试验层面分析纳入18项试验的29个治疗比较。
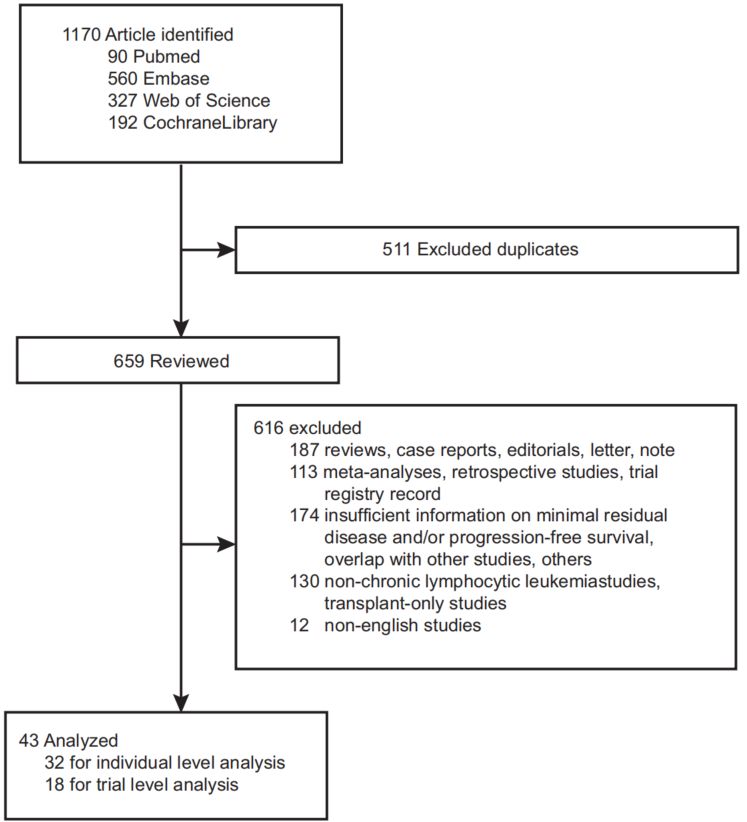
MRD检测方法学特征。 43项试验中,BTK抑制剂相关试验13项,维奈克拉相关12项,联合方案5项,化学免疫治疗和/或单克隆抗体23项。样本来源方面,23项试验检测外周血,7项检测骨髓,9项同时检测两者。MRD分析敏感性阈值主要为≤10⁻⁴(38项),少数为≤10⁻³(1项)或≤10⁻⁶(3项)。检测方法以多参数流式细胞术(MPFC,32项)为主,其次为二代测序(NGS,4项)和PCR(3项)。
统计学方法。 个体层面分析采用贝叶斯Weibull加速失效时间(AFT)模型,通过Engauge Digitizer软件算法重建Kaplan-Meier曲线,结合R语言survival包计算风险比(HR)。试验层面分析采用两阶段方法:首先对logOR(MRD)和logHR(PFS)进行加权Spearman秩相关分析(权重考虑多臂试验的非独立性和样本量),然后进行加权线性回归建模。预设的替代有效性阈值为|Spearman's rho|≥0.85或决定系数R²>0.60。
核心发现:个体层面显著,试验层面存疑
个体层面:MRD可检测与更差PFS显著相关
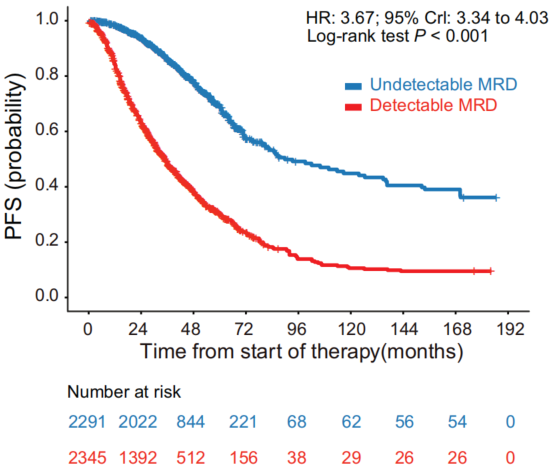
在个体层面,Kaplan-Meier分析显示MRD可检测(dMRD)与MRD不可检测(uMRD)患者的PFS存在显著差异(P<0.01,log-rank检验)。贝叶斯Weibull AFT模型量化显示,dMRD患者的进展或死亡风险是uMRD患者的3.67倍(95%CI:3.34-4.03,P<0.01)。这一关联在多个预设亚组中保持一致:
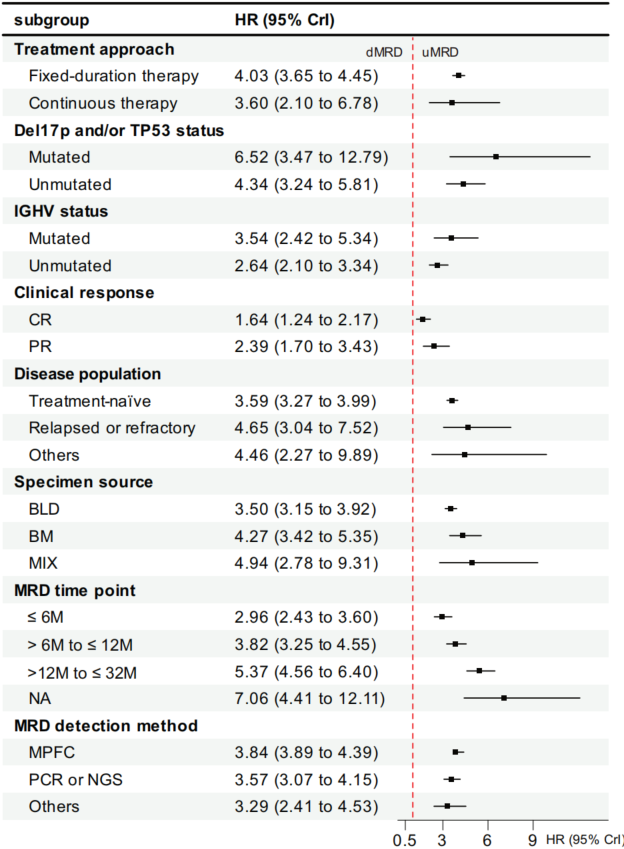
治疗方式亚组。 固定疗程治疗中dMRD的风险比为4.03(95%CrI:3.65-4.45),持续治疗中为3.60(95%CrI:2.10-6.78),两者均显著。
分子特征亚组。 del(17p)和/或TP53突变患者中dMRD的HR高达6.52(95%CrI:3.47-12.79),无此高危特征者为4.34(95%CrI:3.24-5.81)。IGHV突变状态呈现“悖论”:IGHV突变型患者dMRD的HR为3.54(95%CrI:2.42-5.34),高于IGHV未突变型的2.64(95%CrI:2.10-3.34),提示生物学背景影响MRD的预后权重。
疗效反应亚组。 完全缓解(CR)患者中dMRD的HR为1.64(95%CrI:1.24-2.17),部分缓解(PR)患者中为2.39(95%CrI:1.70-3.43),表明即使在CR患者中,MRD可检测仍预示更高风险。
样本来源与时间亚组。 骨髓MRD检测的预测价值优于外周血(HR:4.27 vs 3.50)。MRD检测时间>12至≤32个月的HR最高(5.37,95%CrI:4.56-6.40),提示治疗后期MRD状态可能更具预后意义。
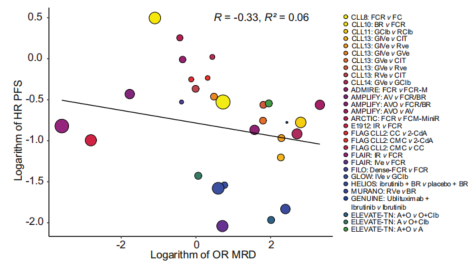
试验层面:整体相关性未达替代有效性阈值
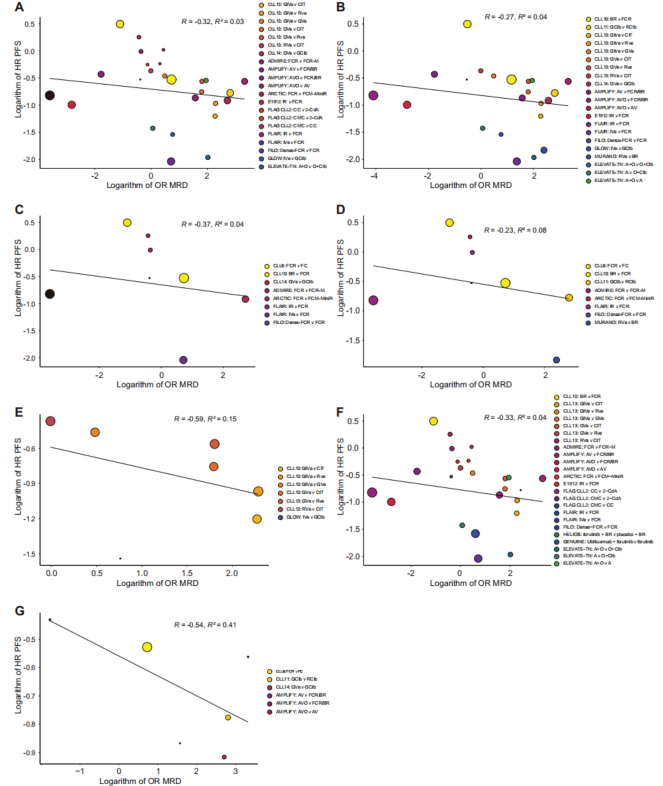
尽管个体层面关联显著,试验层面的替代效度却明显不足。加权Spearman相关分析显示,MRD疗效(logOR)与PFS获益(logHR)的相关系数R=-0.33(95%CI:-0.71至0.04),决定系数R²=0.06,远低于预设的有效性阈值(|R|≥0.85或R²>0.60)。这意味着,在试验层面,MRD检测结果只能解释PFS变异的6%,无法作为可靠的替代终点。
治疗类型分层:BTK抑制剂和维奈克拉方案相关性薄弱
敏感性分析揭示了MRD替代效度的高度异质性:
BTK抑制剂治疗。 BTK抑制剂单药或联合方案的试验层面相关性极低(R=-0.05,95%CI:-0.56至0.53;R²=0.03),几乎无预测价值。这与BTK抑制剂的细胞抑制机制一致——药物通过阻断BCR信号维持疾病控制,而非深度清除肿瘤细胞,因此MRD可检测并不等同于即将进展。GLOW研究中,IGHV突变型患者uMRD率低于未突变型,但PFS反而更优,进一步印证了这一生物学特征。
维奈克拉为基础的治疗。 相关性同样有限(R=-0.28,95%CI:-0.87至0.47;R²=0.02),未达预期。尽管维奈克拉通过诱导凋亡实现深度缓解,但试验层面的MRD-PFS关联仍不够稳健。
化学免疫治疗和/或单克隆抗体。 此类治疗中MRD与PFS呈现强负相关(R=-0.89,95%CI:-1.00至-0.28;R²=0.74),达到了预设的有效性阈值。这可能与这些方案的直接细胞毒性机制相关,MRD阴性更能反映肿瘤负荷的实质性降低。
治疗策略分层:固定疗程接近阈值,持续治疗数据有限
按治疗策略分层分析显示,固定疗程方案的试验层面相关性接近预设阈值(R=-0.80,95%CI:-0.93至-0.53;R²=0.43,P<0.01),提示MRD在此类方案中可能具有较好的替代价值。然而,由于MRD很少作为持续治疗试验的终点,相关数据有限,无法进行充分分析。
样本来源与方法学:骨髓MRD优于外周血
在化学免疫治疗和/或单克隆抗体试验中,骨髓MRD检测达到替代有效性阈值(R=-0.94,95%CI:-1.00至-0.18;R²=0.86,P=0.02),而外周血MRD检测虽R²达标(0.70),但相关系数本身未达阈值(R=-0.81,95%CI:-1.00至1.00,P=0.16)。检测方法方面,PCR和/或NGS的准确性(R=-0.54,R²=0.41)优于MPFC(R=-0.33,R²=0.04),但两者均未达到预设阈值。
临床启示与监管考量
本研究的核心发现是:MRD作为PFS替代终点的准确性具有显著的“情境依赖性”(context-dependent),受治疗方式、药物类型和样本来源的共同影响。这一结论对临床实践和监管决策具有多重启示:
个体层面应用。 对于接受固定疗程化学免疫治疗的患者,骨髓MRD检测仍是强有力的预后工具,可用于指导治疗强度调整和随访策略。对于BTK抑制剂治疗的患者,MRD的预后价值有限,不应将其作为调整治疗的主要依据——即使MRD可检测,患者仍可能维持长期疾病控制。
试验设计与监管审批。 在BTK抑制剂或维奈克拉为基础的临床试验中,单独使用MRD作为主要终点可能不足以支持监管审批,需结合PFS等传统终点。仅在固定疗程的化学免疫治疗中,骨髓MRD检测可能具备替代PFS的潜力。EMA已接受MRD作为中间终点,但本研究提示FDA的审慎态度具有科学依据。
MRD指导的治疗策略需谨慎。 近期FLAIR等试验探索了MRD指导的治疗调整,但本研究发现MRD反应与PFS获益之间存在不一致性,特别是在BTKi治疗中。单纯依赖MRD指导治疗升级或降级可能导致过度治疗或治疗不足,需结合分子特征(如IGHV突变状态)综合判断。
研究局限与未来方向
研究存在若干局限:CLL生物学、疾病状态、治疗类型和采样方法的异质性引入了变异;复发/难治性CLL的试验层面数据有限;持续治疗试验中MRD作为终点的应用较少,限制了相关分析;MRD分析采用最新可及评估,未排除早期进展者,可能影响精确度。
未来研究应聚焦于:在特定治疗模式下验证MRD的替代效度;开发整合分子特征(如IGHV、TP53)的MRD解读框架;探索MRD动力学(如清除速率、反弹模式)而非单次检测结果的预后价值;建立适用于BTK抑制剂等细胞抑制药物的替代终点体系。
总结
这项纳入43项临床试验、9628例受试者的大型荟萃分析,为MRD在CLL中的应用提供了迄今最全面的循证评估。研究明确指出,MRD并非“普遍可靠”(universally reliable)的PFS替代终点——其在个体层面与PFS的显著关联,并不能直接外推至试验层面的替代效度。BTK抑制剂治疗中MRD与PFS的弱相关性,反映了细胞抑制机制与细胞清除机制的本质差异;而固定疗程化学免疫治疗中骨髓MRD的强预测价值,则印证了治疗情境的关键作用。
总之,MRD检测结果的解读应充分考虑治疗方式、药物类型和样本来源,在临床决策和监管审批中保持审慎。对于这一CLL治疗领域的热点议题,本研究划定了清晰的适用边界:MRD是有价值的生物标志物,但非万能的替代终点。在追求精准医疗和加速药物审批的道路上,理解其局限性与应用条件,与认识其价值同等重要。
Wang Y, Li C, Gale RP, et al. Measurable residual disease is not a universally reliable surrogate for progression-free survival in clinical trials of new chronic lymphocytic leukemia therapies. Leukemia. 2026. doi: 10.1038/s41375-026-02970-x
排版编辑:Mathilda











 苏公网安备32059002004080号
苏公网安备32059002004080号


