慢性淋巴细胞白血病(CLL)的治疗格局在过去十年间经历了巨大变革,布鲁顿酪氨酸激酶抑制剂(BTKi)和BCL-2抑制剂(BCL-2i)的相继问世使多数患者获得了长期疾病控制。然而,一个日益严峻的临床挑战正浮出水面:对这两类药物均产生耐药的双重难治性(double refractory)CLL患者群体不断扩大,中位总生存期(OS)不足12个月,亟需新的治疗突破。近日,Clinical Lymphoma, Myeloma and Leukemia杂志发表了一项最新综述,系统梳理了非共价BTKi、BTK降解剂、双特异性抗体及CAR-T细胞疗法等新兴策略的临床证据,并重点分析了美国FDA近期批准的新药物在这一难治人群中的定位,为临床实践提供了重要的循证参考。

研究背景:从治疗革命到耐药困境
CLL是西方国家最常见的成人白血病,年发病率约5/10万,2024年美国新发病例超过2万例。该病好发于老年男性,中位诊断年龄72岁。CLL的临床病程高度异质,从惰性病程到侵袭性表现不等,这种差异与免疫球蛋白重链可变区(IGHV)突变状态、染色体异常(如11q、13q、17p缺失)及TP53、NOTCH1等基因突变密切相关。
2013年共价BTKi(cBTKi)的上市开启了CLL靶向治疗时代。伊布替尼、阿可替尼和泽布替尼通过不可逆共价结合BTK的C481位点,阻断B细胞受体信号通路。RESONATE-2试验显示,伊布替尼一线治疗的中位PFS达8.9年。2016年维奈克拉获批,作为选择性BCL-2i恢复肿瘤细胞凋亡潜能。BTKi联合维奈克拉的固定疗程方案使约70%患者达到微小残留病(MRD)不可检测状态。
然而,耐药问题日益凸显。新近数据表明,约50%先后接受维奈克拉和cBTKi治疗的患者最终对两类药物均产生耐药。双重难治性CLL的定义为:在接受cBTKi和BCL-2i治疗期间或之后出现疾病进展。这一人群预后极差,部分系列报道的中位OS不足12个月,构成了当前CLL治疗领域最迫切的未满足临床需求。
耐药机制:从单点突变到克隆演化
理解耐药机制是开发克服策略的基础。cBTKi耐药主要涉及两大机制:BTK结合位点突变和下游信号通路激活。
BTKi耐药机制。 C481位点突变是最常见的耐药机制,约占伊布替尼耐药患者的80%。该突变将半胱氨酸替换为丝氨酸(C481S),破坏了药物与靶点的不可逆共价结合。非共价BTKi(ncBTKi)正是为克服这一机制而设计。然而,耐药并非仅限于C481突变。守门员突变(T474I/F/L/Y)改变酶构象,影响共价和非共价BTKi的结合;激酶失活突变(V416L、M437R、L528W)虽损害酶活性,但保留支架功能,允许下游信号传导。值得关注的是,泽布替尼耐药后出现的L528W突变对匹妥布替尼也存在交叉耐药。
下游PLCG2突变可导致功能获得效应,使BCR信号在BTK活性被抑制的情况下持续传导。此外,PI3K-AKT、NFκB和MAPK等替代通路的激活,以及肿瘤微环境提供的生存信号,均可绕过BTK介导的信号传导。
BCL-2i耐药机制。 与BTKi耐药不同,维奈克拉耐药更为多因素化。替代抗凋亡蛋白(特别是MCL-1和BCL-XL)的上调可补偿BCL-2抑制;BCL-2蛋白G101V突变直接损害维奈克拉结合;TP53突变可破坏内在凋亡通路;代谢重编程降低细胞对BCL-2的依赖。表观遗传改变影响BCL-2家族蛋白表达、线粒体动力学失调等新型耐药机制也逐渐被揭示。
克隆演化的复杂性。 序贯使用靶向治疗对CLL细胞施加选择性压力,促使具有多重耐药机制的亚克隆产生。不同cBTKi的耐药突变谱存在差异:伊布替尼耐药以C481S为主(80~85%),阿可替尼耐药中T474I突变约占19%,泽布替尼耐药则富集L528W突变。这些突变可在同一细胞系内共存或互斥,为个体化治疗策略的制定带来挑战。
新兴治疗策略与临床证据
非共价BTKi:克服C481S耐药的关键突破
非共价BTKi通过可逆性非共价相互作用结合BTK的ATP结合口袋,保持对C481S突变BTK的活性,是双重难治性CLL治疗的重要进展。
匹妥布替尼。 作为首个获FDA批准的ncBTKi,匹妥布替尼在BRUIN试验中展现了令人瞩目的疗效。在247例既往接受过cBTKi治疗的CLL/小淋巴细胞淋巴瘤(SLL)患者中,总缓解率(ORR)达73.3%,中位PFS为19.6个月,其中40.5%患者曾接受BCL-2i。对于携带BTK C481S突变的患者,匹妥布替尼仍能产生持续缓解。安全性方面,匹妥布替尼的心血管和出血事件发生率低于cBTKi,最常见不良事件为感染(71.0%)、出血(42.6%)和中性粒细胞减少(32.5%),因治疗相关不良事件停药率仅2.8%。
然而,匹妥布替尼的疗效受非C481 BTK突变和下游信号改变的影响。携带T474守门员突变或L528W激酶失活突变的患者缓解率显著降低,PLCG2功能获得性突变可完全绕过BTK抑制。这凸显了治疗前分子检测的重要性。
Nemtabrutinib。 这款可逆性BTKi在Ⅰ/Ⅱ期试验中显示,对携带BTK C481S突变的CLL患者ORR为57.9%,主要不良事件包括疲劳、便秘、味觉障碍和咳嗽。
表1. 双重难治性CLL的临床试验和关键发现总结
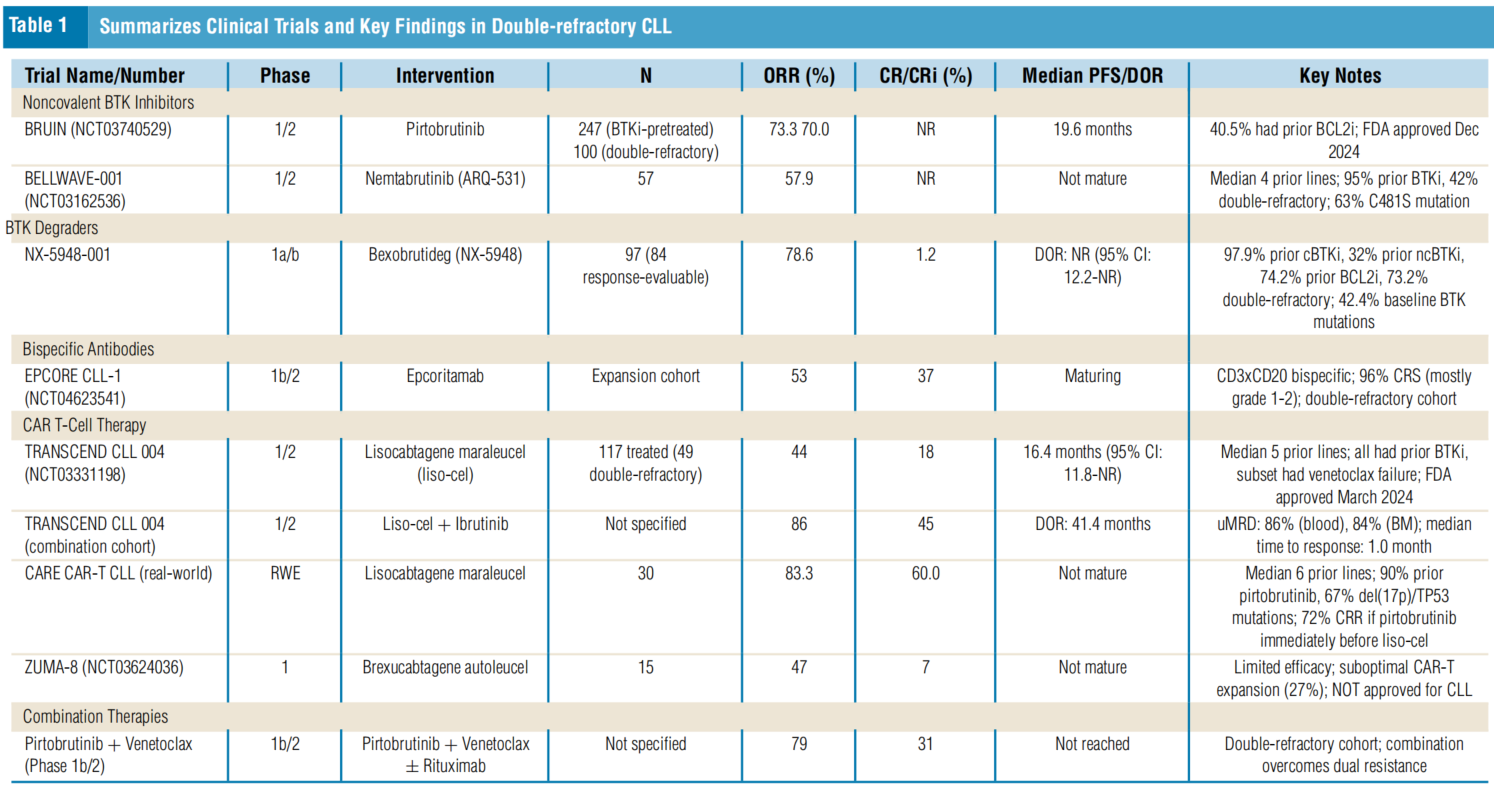
BTK降解剂:从抑制到清除的新范式
BTK降解剂通过泛素-蛋白酶体系统诱导BTK蛋白完全降解,而非仅抑制其酶活性,有望克服cBTKi和ncBTKi的耐药机制。
Bexobrutideg(NX-5948)。 这款口服小分子降解剂通过cereblon E3连接酶复合物诱导野生型和突变型BTK的泛素化及后续蛋白酶体降解。Ⅰa/Ⅰb期试验中ORR达78.6%,安全性特征与cBTKi明显不同:最常见治疗相关不良事件为紫癜/挫伤(38.1%,无≥3级事件)、中性粒细胞减少(29.9%,≥3级占23.7%)和疲劳(25.8%,≥3级占1.0%)。
NX-2127。 作为双功能BTK降解剂和cereblon E3连接酶调节剂,NX-2127在早期临床试验中对重度预治疗的CLL患者(包括双重难治性)ORR约52%,主要不良事件为中性粒细胞减少、血小板减少和皮疹。
双特异性抗体:免疫系统的精准调动
双特异性抗体通过同时结合T细胞CD3和B细胞CD20,介导T细胞对恶性B细胞的杀伤,为双重难治性CLL提供了免疫治疗新选择。
Epcoritamab。 EPCORE CLL-1试验的扩展队列显示,在既往接受过BTKi和BCL-2i治疗的患者中,ORR约53%,完全缓解(CR)率37%。该药在复发/难治性(R/R)CLL中实现了较高的CR率和MRD阴性率。安全性方面,细胞因子释放综合征(CRS)发生率约96%,但多为1-2级;其他常见不良事件包括中性粒细胞减少和贫血。
其他双特异性抗体。 格菲妥单抗采用创新的2:1结构(CD20xCD3),在双重难治性CLL中ORR为53%,CR率33%。莫妥珠单抗和odronextamab等CD20xCD3双特异性抗体也在早期研究中显示出潜力。系统综述分析指出,下一代双特异性抗体在增强疗效和降低毒性方面具有前景,与其他新型药物的联合应用值得探索。
CAR-T细胞疗法:向潜在治愈迈进
CAR-T细胞疗法通过体外基因改造患者T细胞,使其表达靶向CD19的嵌合抗原受体,是双重难治性CLL治疗的重要里程碑。
Lisocabtagene maraleucel(liso-cel)。 作为目前唯一获FDA批准用于CLL的CAR-T产品,liso-cel在TRANSCEND CLL 004试验中展现了确切疗效。在接受过大量治疗的CLL患者中,ORR约44%,CR率18%。值得注意的是,liso-cel联合伊布替尼的疗效显著优于单药:联合队列ORR达86%,CR率45%,中位缓解持续时间41.4个月,86%患者外周血MRD不可检测,84%骨髓MRD不可检测,中位至首次缓解时间仅1个月。
真实世界证据更为鼓舞人心。多中心CARE CAR-T CLL研究纳入中位既往6线治疗的患者,90%曾接受匹妥布替尼,67%携带del(17p)或TP53突变。30例接受liso-cel治疗的患者中,CRR/CRRu达60.0%,ORR达83.3%。有趣的是,末线接受匹妥布替尼后桥接liso-cel的患者CR率达72%,而未接受匹妥布替尼桥接者仅28%,间接支持了TRANSCEND CLL 004中liso-cel联合伊布替尼亚组的结果。
安全性方面,CRS发生率约74%(多为1-2级),神经系统事件42%(多为1-2级);3级CRS占9%(无4-5级),3级神经系统事件18%(1%为4级)。血细胞减少(尤其是中性粒细胞减少和贫血)常见且可能持续较长时间。
其他CAR-T方案。 Brexucabtagene autoleucel在ZUMA-8试验中疗效有限。下一代双靶点CAR和通用型“现货”产品正在开发中。
新一代BCL-2靶向治疗与PI3K抑制剂
索托克拉(BGB-11417)。 作为下一代BCL-2i,索托克拉具有半衰期短、无药物蓄积的优势,能克服维奈克拉耐药相关的BCL-2突变(特别是G101V)。晶体结构分析显示,索托克拉在BCL-2的P2口袋中采用新型结合模式,避免与突变残基发生空间冲突。其对其他维奈克拉耐药突变(D103Y、A113G、V156D、R129L)亦保持活性。Ⅲ期CELESTIAL-RRCLL试验(CLL-RR1)正在评估索托克拉联合抗CD20抗体对比维奈克拉联合利妥昔单抗在复发/难治性CLL/SLL中的疗效。
PI3K抑制剂。 尽管idelalisib、duvelisib和umbralisib已获批用于CLL,但其在双重难治性患者中的应用受限于毒性(免疫介导不良事件、肺炎、结肠炎、转氨酶升高和感染)。新一代PI3Kδ抑制剂如parsaclisib(肝毒性更低)和zandelisib(间歇给药设计)正在开发中,旨在降低不良事件同时维持疗效。
联合策略与治疗选择
匹妥布替尼联合维奈克拉。 Ⅰb期 BRUIN试验评估了固定疗程匹妥布替尼+维奈克拉(PV)或匹妥布替尼+维奈克拉+利妥昔单抗(PVR)在R/R CLL中的疗效,包括既往cBTKi暴露患者。结果显示,PV方案ORR 93.3%、CR率46.7%;PVR方案ORR 100%、CR率30.0%。12周期后外周血MRD阴性率分别为85.7%和90.0%,估计24个月PFS率为79.5%。
治疗选择考量。 双重难治性CLL的治疗选择应个体化,综合考虑患者特征(年龄、体能状态、合并症、偏好)和疾病特征(TP53异常、淋巴结负荷、疾病动力学)。Thompson等专家的综述建议:对于高肿瘤负荷、侵袭性疾病动力学或高危遗传学特征的患者,CAR-T细胞疗法可能是优选;对于疾病侵袭性较低、合并症显著或偏好口服治疗的患者,匹妥布替尼可能更为适宜。2024年NCCN指南更新已将匹妥布替尼和liso-cel列为双重难治性CLL的首选方案。
治疗算法建议。 基于当前证据,双重难治性CLL的治疗算法可首先考虑参加新型药物或联合策略的临床试验。对于携带BTK C481S突变的患者,ncBTKi(如匹妥布替尼)或BTK降解剂适用。对于高肿瘤负荷或侵袭性疾病的患者,应考虑双特异性抗体(epcoritamab、格菲妥单抗)或CAR-T细胞疗法(liso-cel)。对于既往不耐受而非耐药的患者,同类药物替换(如不同BTKi)或新型联合方案可能有效。年轻、体能状态良好的无其他选择患者可考虑异基因造血干细胞移植。对于选择有限的患者,化学免疫治疗或最佳支持治疗仍是必要选项。
未来方向与总结
双重难治性CLL的管理正从“无药可用”转向“多策略可选”。非共价BTKi匹妥布替尼为携带C481S突变的患者提供了新治疗选择;双特异性抗体和CAR-T细胞疗法利用免疫系统力量,在既往接受过大量治疗的患者中实现高缓解率和持久缓解;BTK降解剂、新一代BCL-2i和理性联合策略展现了早期前景。
未来的研究应聚焦于:基于特定耐药突变或信号通路改变的个体化治疗;探索BTK和BCL-2之外的新靶点(如CDK、SYK、LYN激酶);开发下一代双特异性抗体、改进型CAR-T构建体和免疫检查点抑制剂;以MRD和预测性生物标志物指导治疗强度和疗程。
总之,随着治疗格局的持续演进,双重难治性CLL患者的预后正变得愈发乐观。新型药物整合入临床实践,结合对耐药机制和联合策略的持续研究,已将双重难治性CLL从“终末期疾病”转变为“可管理疾病”。然而,最佳治疗顺序和组合仍是活跃的研究领域,需要更多前瞻性研究来明确个体化治疗策略,最终改善这一挑战性患者群体的结局。
Jain E, Sainatham C, Raghavan P, et al. Current Treatment of Double Refractory Chronic Lymphocytic Leukemia: A Focus on Novel Drugs. Clin Lymphoma Myeloma Leuk. 2026. doi: 10.1016/j.clml.2026.03.001
排版编辑:Mathilda











 苏公网安备32059002004080号
苏公网安备32059002004080号


