复发/难治性滤泡性淋巴瘤(R/R FL)是一类预后不良的恶性肿瘤。患者在接受至少两线系统治疗后,疾病缓解期逐渐缩短,临床亟需新的治疗方案。表观遗传失调在滤泡性淋巴瘤(FL)的发生发展中发挥关键作用,组蛋白去乙酰化酶(HDAC)抑制剂在此类患者中初步展现出治疗潜力,但其确切疗效与安全性仍需进一步的循证医学证据支持。
近日,由中国医学科学院肿瘤医院石远凯教授团队领衔的一项多中心II期临床研究发表于Signal Transduction and Targeted Therapy杂志。该研究评估了新型HDAC抑制剂艾贝司他(abexinostat)在R/R FL患者中的疗效与安全性。结果显示,艾贝司他的客观缓解率(ORR)为69.5%,完全缓解(CR)率为14.6%,疾病控制率(DCR)为91.5%,且整体安全性临床可控。研究表明,艾贝司他在R/R FL患者中展现出显著的抗肿瘤活性,有望成为该人群≥3线治疗的新选择。【肿瘤资讯】现将该研究主要内容整理如下,以飨读者。

研究背景
尽管FL病程相对惰性,且一线免疫化疗及维持治疗显著改善了患者生存,但该疾病目前仍无法治愈,临床常表现为缓解与复发交替的模式。约1/5的患者在初始治疗后24个月内即发生疾病进展或复发,整体FL患者人群的5年无进展生存(PFS)率约为60%,提示该领域仍存在大量未被满足的临床需求。
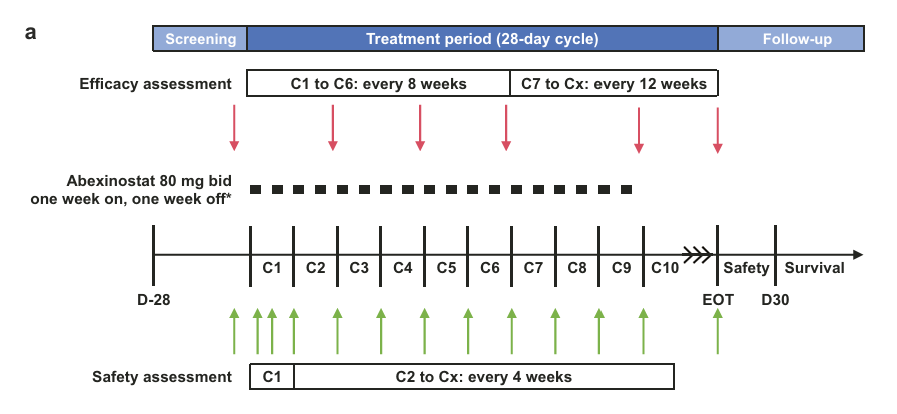
在发病机制方面,表观遗传失调是FL重要的致病驱动因素,近90%的病例存在影响组蛋白修饰酶的基因突变。HDAC抑制剂可通过逆转组蛋白乙酰化水平的降低发挥治疗作用。目前,多款同类药物已在包括R/R FL在内的多种淋巴瘤中初步展现出抗肿瘤活性。艾贝司他作为一种新型HDAC抑制剂,其前期的I期临床研究已确定了在中国R/R B细胞淋巴瘤患者中的II期推荐剂量(80 mg,每日两次,连续用药7天后停药7天)。为进一步明确艾贝司他单药在R/R FL患者中的疗效与安全性,研究者开展了本项多中心、单臂、关键性II期临床研究。
研究方法
研究方法
本研究为一项多中心、单臂、关键性Ⅱ期临床试验。研究纳入了年龄≥18岁、美国东部肿瘤协作组(ECOG)体能状态评分为0~2分、经中心实验室病理确诊为1~3a级的R/R FL患者;入组患者既往至少接受过2线系统治疗,包括细胞毒类药物和/或抗CD20单抗等;实际入组患者均既往接受过抗CD20单抗治疗。所有入组患者均接受口服艾贝司他80 mg、每日2次的治疗,采用连续服药7天后停药7天的给药模式,每28天为一个治疗周期,持续治疗直至出现疾病进展、不可耐受的毒性或符合其他停药标准。
研究的主要终点为由独立审查委员会(IRC)依据Lugano 2014标准评估的ORR;次要终点包括DCR、缓解持续时间(DoR)、PFS、总生存期(OS)及安全性;探索性终点则关注不同生物标志物(如CREBBP和KMT2D蛋白表达水平)亚组中的疗效与安全性差异。疗效分析基于FAS人群进行,即有艾贝司他暴露记录、既往至少接受过两线系统治疗,并具有可评价治疗后疗效数据的患者。
研究结果

患者基线特征与治疗情况
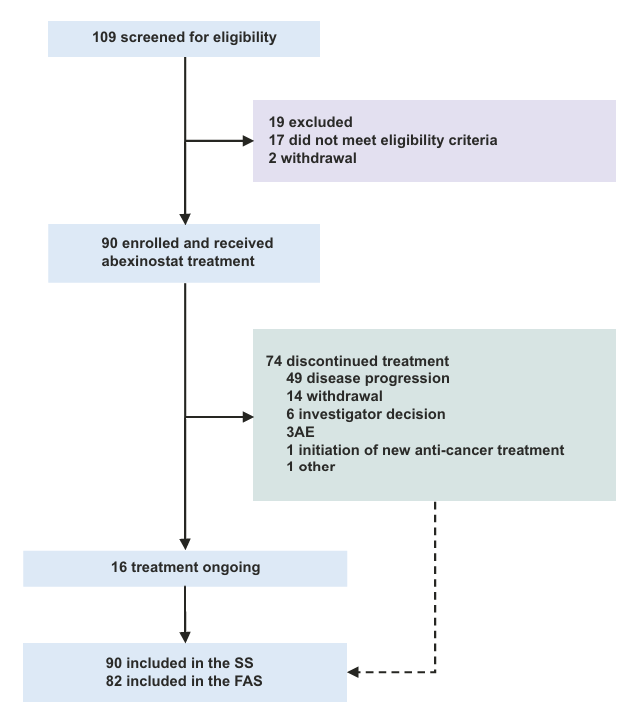
本研究分两个阶段,于2019年5月至2023年11月期间共入组90例患者。所有患者均至少接受过1剂艾贝司他治疗。治疗终止原因包括出现不可接受的毒性、疾病进展、失访、撤回知情同意或死亡等(图1)。
研究共入组90例患者,并在完成82例患者的疗效评估后终止。入组患者总体处于疾病晚期且经过多线治疗,其中92.2%(83/90)为Ⅲ–Ⅳ期;入组前中位既往治疗线数为3线(范围:2~线),且100%曾接受过抗CD20单抗治疗。末次治疗后,75.6%(68/90)为复发患者,24.4%(22/90)为难治患者(表1)。
表1 安全性数据集(SS)队列患者的基线特征(N = 90)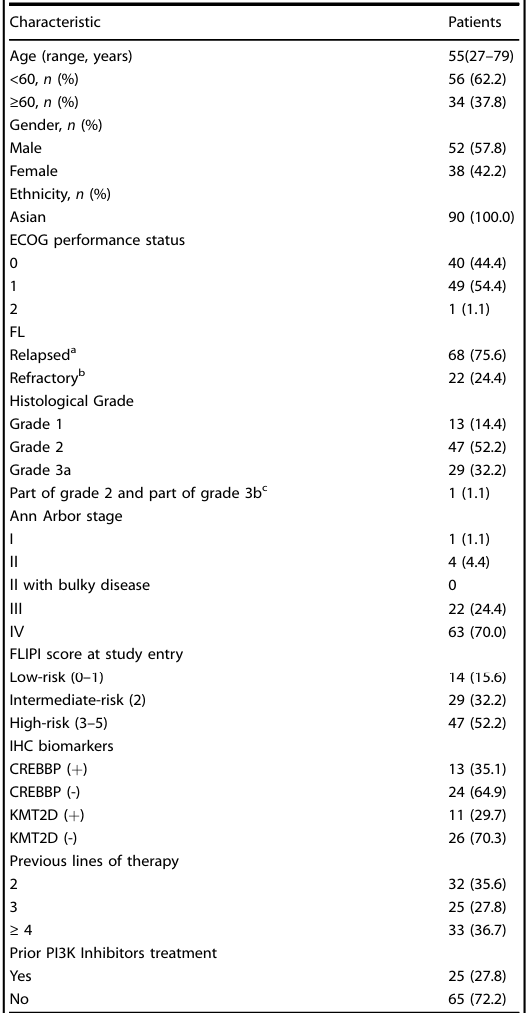
截至2024年10月8日,中位随访时间为30.55个月(95% CI 23.72–33.64)。在90例患者中,共有82.2%终止了研究治疗,最主要原因为疾病进展(占54.4%)。目前,仍有17.8%(16/90)的患者在继续接受研究性治疗,47.8%(43/90)进入随访阶段,34.4%(31/90)已退出研究(图2)。

疗效评估
疗效评估FAS共纳入82例患者。结果显示,IRC评估的ORR为69.5%(57/82,95% CI 58.4–79.2),其中14.6%(12/82)达到CR。ORR的95% CI下限为58.4%,显著超过了30%的预设有效性界值。此外,患者DCR为91.5%,且89%(73/82)的患者观察到肿瘤体积较基线缩小(图3),治疗持续时间与疗效对应关系详见图4。
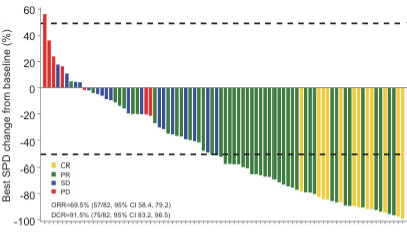 图3 FAS人群(N = 82)中接受艾贝司他治疗患者靶病灶大小较基线的最佳百分比变化
图3 FAS人群(N = 82)中接受艾贝司他治疗患者靶病灶大小较基线的最佳百分比变化
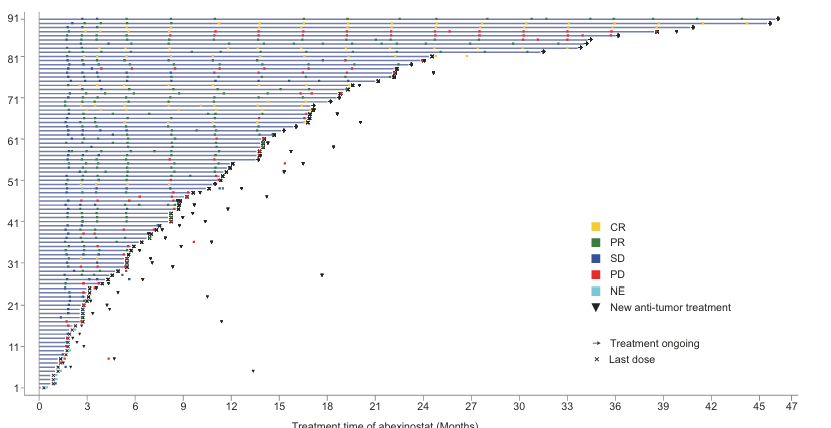
图4 显示SS人群(N = 90)中接受艾贝司他治疗的每例患者的治疗持续时间及疗效结局
在生存获益方面,患者的中位DoR为13.96个月(图5a)。中位PFS为13.80个月(95% CI 9.69–30.26;图5b),其12、24和36个月的PFS率分别为55.3%、39.2%和33.6%(表2)。此外,OS方面,中位OS为47.18个月(95% CI 45.70–NR)(图5c)。
亚组分析进一步表明,无论患者既往是否接受过PI3K抑制剂治疗,其ORR均保持一致(均为69.6%);但在PFS方面,既往未暴露于PI3K抑制剂的患者中位PFS更长(15.38个月 vs 8.25个月)(图5d)。同时,在不同生物标志物亚组中,艾贝司他均表现出抗肿瘤活性,例如在免疫组化检测为CREBBP阳性和KMT2D阳性的患者中,ORR分别达到76.9%和72.7%。
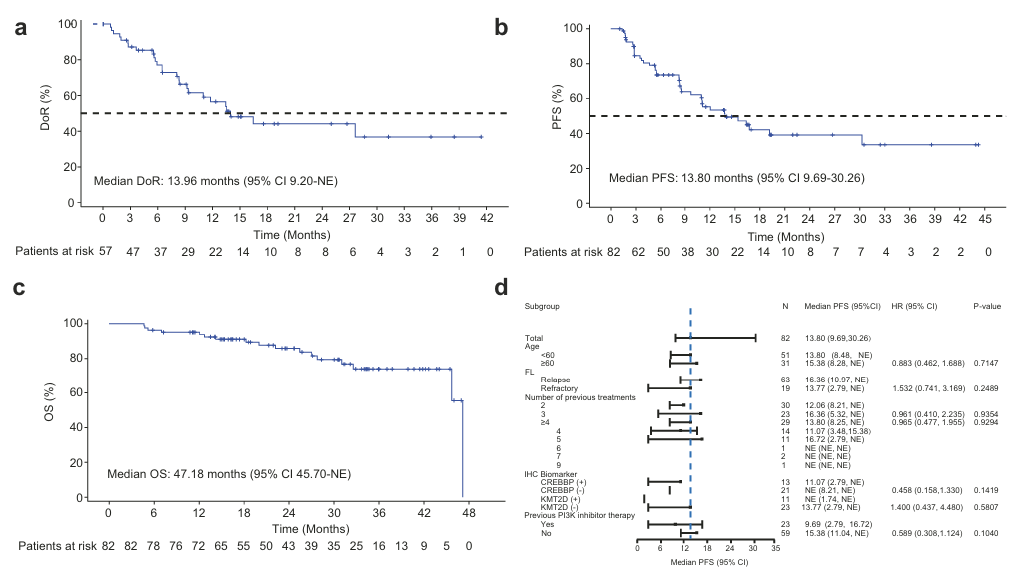 图5 (a) IRC 评估的DoR Kaplan–Meier 曲线;(b) IRC 评估Kaplan–Meier 曲线;(c) 总生存期(OS)Kaplan–Meier 曲线;(d) IRC 评估的 PFS 亚组分析森林图
图5 (a) IRC 评估的DoR Kaplan–Meier 曲线;(b) IRC 评估Kaplan–Meier 曲线;(c) 总生存期(OS)Kaplan–Meier 曲线;(d) IRC 评估的 PFS 亚组分析森林图
表2 艾贝司他在FAS人群(N = 82)中的疗效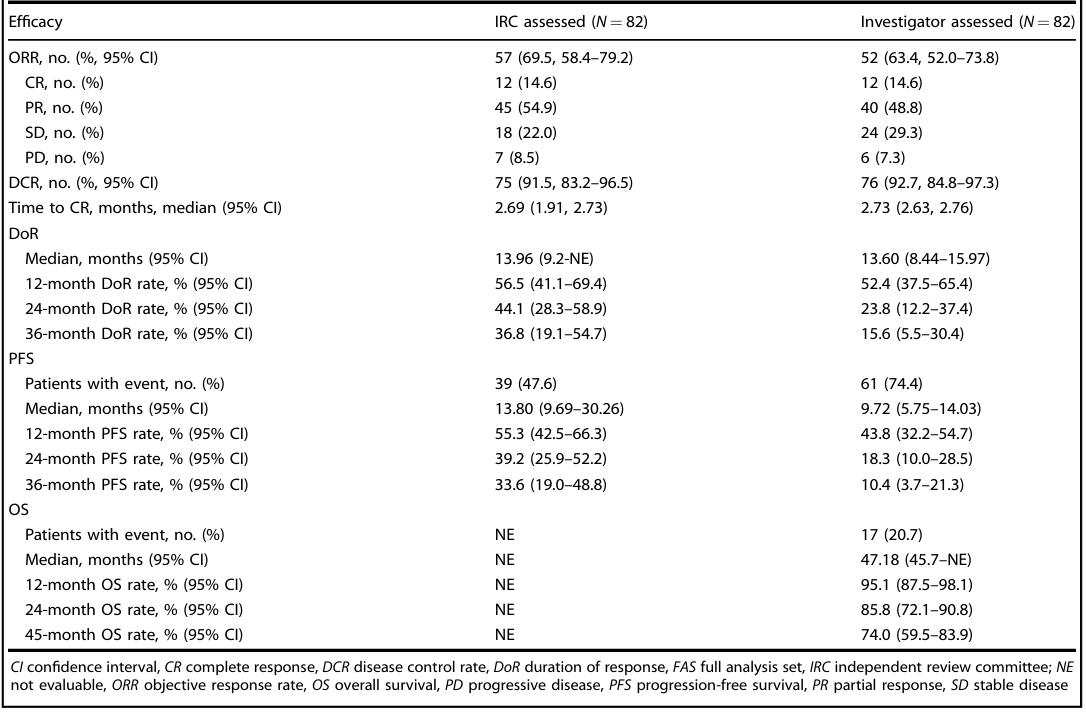

安全性
SS纳入的90例患者整体耐受性良好,发生率最高的治疗出现的不良事件(TEAE)主要为血液学毒性,包括血小板减少(85.6%)、中性粒细胞减少(58.9%)和白细胞减少(52.2%)。其中≥3级TEAE最常见的是血小板减少(42.2%)和中性粒细胞减少(25.6%)。非血液学3-4级不良事件仅包括低钾血症(5.6%)和腹泻(4.4%)(表3)。尽管有24.4%的患者报告了严重不良事件(SAE),但因不良事件导致研究治疗终止的比例极低,仅为3.3%(其中仅1例4级血小板减少被研究者判定为与艾贝司他相关)。研究期间发生2例死亡事件(1例蛛网膜下腔出血,1例COVID-19感染),均被判定与研究药物无关。本研究未发生任何与艾贝司他治疗相关的死亡事件。整体而言,艾贝司他在R/R FL患者中的安全性特征明确且临床可控。
表3 SS人群(N = 90)中的TEAEs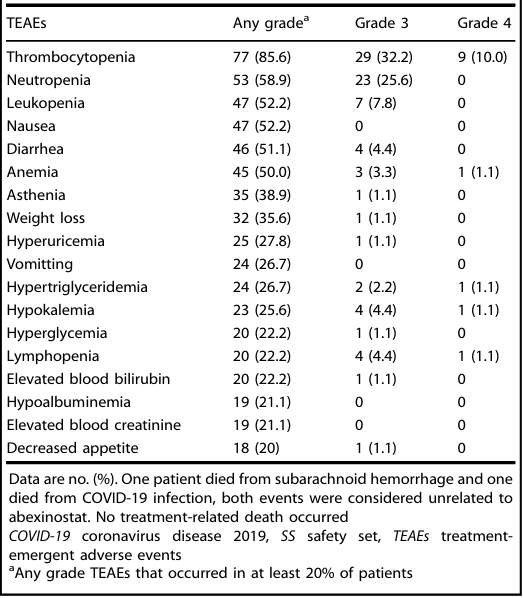
研究结论
综上所述,本项多中心、关键性II期临床研究初步证实,新型HDAC抑制剂艾贝司他在既往接受过多线治疗(含抗CD20单抗)的R/R FL患者中,展现出令人鼓舞且持久的抗肿瘤活性。其单药治疗不仅实现了高达69.5%的ORR和近4年的中位OS,且在不同基因突变及既往治疗亚组中均显示出一致的临床获益。同时,艾贝司他的整体安全性良好,无治疗相关死亡事件发生。面对R/R FL患者多线治疗后复发、后续手段有限的临床困境,艾贝司他单药有望成为R/R FL患者三线及以后治疗的新选择,为打破现有治疗僵局提供了坚实的循证医学证据。
Gui, L., Liu, H., Wang, H. et al. Abexinostat, a histone deacetylases inhibitor, for patients with relapsed or refractory follicular lymphoma: a multi-center, single-arm phase 2 study. Sig Transduct Target Ther 11, 154 (2026). https://doi.org/10.1038/s41392-026-02646-z
排版编辑:肿瘤资讯-Harbor
版权声明











 苏公网安备32059002004080号
苏公网安备32059002004080号


