福建省抗癌协会癌痛专业委员会和福建省抗癌协会中西医整合肿瘤专委会青年委员会主办的【十邑论坛】开播啦!论坛于每周二推出,带您用中文听原汁原味的2026年美国临床肿瘤学会胃肠道癌症研讨会(ASCO-GI)研究。本期由泉州市第一医院的洪燕妮教授进行分享,内容源自Elena Elez教授关于BRAF突变新型治疗策略的报告。该报告深入探讨了BRAF突变在结直肠癌中的临床意义,并详细梳理了从基础研究到临床实践的靶向治疗演进过程,为实现患者的定制化治疗提供了重要参考。
泉州市第一医院 肿瘤内科副主任医师
福建省抗癌协会癌痛专委会委员
福建省抗癌协会中西医整合肿瘤专业委员会青年委员
福建省抗癌协会肿瘤营养与支持治疗专业委员会青年委员
泉州市抗癌协会免疫治疗专业委员会委员

BRAF突变的生物学特征与临床意义
BRAF突变的发现已有25年之久,它之所以如此重要,是因为它广泛存在于多种肿瘤类型中,不仅包括实体恶性肿瘤,也涉及血液系统恶性肿瘤。在胃肠道癌症中,特别是在结直肠癌中,有8%~12%的患者携带BRAF突变,其中以BRAF V600E最为常见。除了结直肠癌,其他肿瘤也存在该突变,例如甲状腺癌的发生率高达44%,皮肤癌或黑色素瘤占比18%。在具体的癌种分布上,小细胞癌、结直肠腺癌中比较多见,而在胃食管肿瘤或神经内分泌肿瘤中,发生率相对较低。
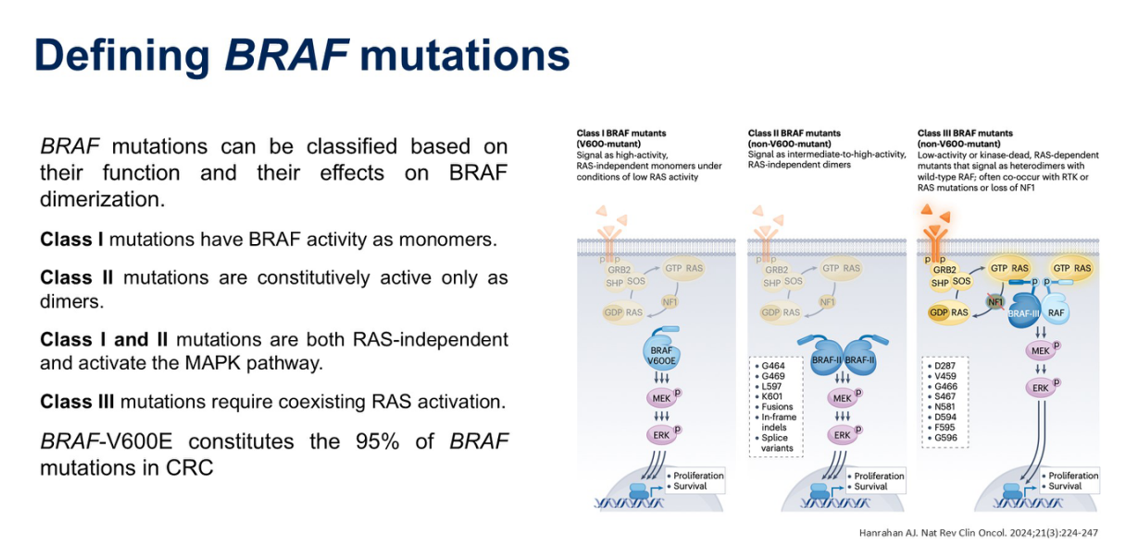
我们需要认识到BRAF突变存在不同的功能类型,这决定了后续治疗策略的选择。目前主要分为三类:
I类突变:主要是指BRAF V600E。其不需要上游信号,也不需要形成二聚体,在单体状态下就具有很高的激酶活性,能直接激活下游的MEK/ERK通路,导致细胞无节制地增殖。
II类突变:属于非V600E突变。它以构成型活跃的“二聚体”形式存在,虽然也不需要上游RAS信号触发,但必须两个分子结合形成二聚体才能激活。
III类突变:同样是非V600E突变。这类突变的激酶活性很低,必须依靠上游RAS激活并与野生型BRAF形成异二聚体。在结直肠癌中,遇到第III类突变必须关注RAS状态,如果RAS是野生型的,抗EGFR治疗可能依然有效。
跨癌种靶向治疗探索:从VE-BASKET到ROAR研究
在BRAF靶向治疗的发展初期,研究者尝试了“异病同治”的策略。VE-BASKET研究评估了维莫非尼在多种BRAF V600突变实体瘤中的疗效。在黑色素瘤中,维莫非尼单药的客观缓解率(ORR)可超过50%,表现出强劲的临床活性。但在结直肠癌中,维莫非尼单药的ORR仅为5%。
这种差异并非偶然,而是由组织学背景决定的。在结直肠癌中,抑制BRAF V600会导致EGFR的迅速反馈激活。尽管BRAF通路被封锁,癌细胞却会通过EGFR这条备用通道维持ERK通路的活性,支持细胞继续增殖。研究显示,单用BRAF抑制剂或单用EGFR抑制剂对肿瘤的生长减缓作用都非常有限,只有当两者联用实现双重封堵时,肿瘤生长曲线才趋于平缓甚至下降。基于此理论,VE-BASKET研究后期修改了方案,在结直肠癌队列中将方案调整为维莫非尼联合西妥昔单抗。这种组织学差异也解释了为何黑色素瘤中ERK抑制更持久,因为其信号维持机制与结直肠癌截然不同。
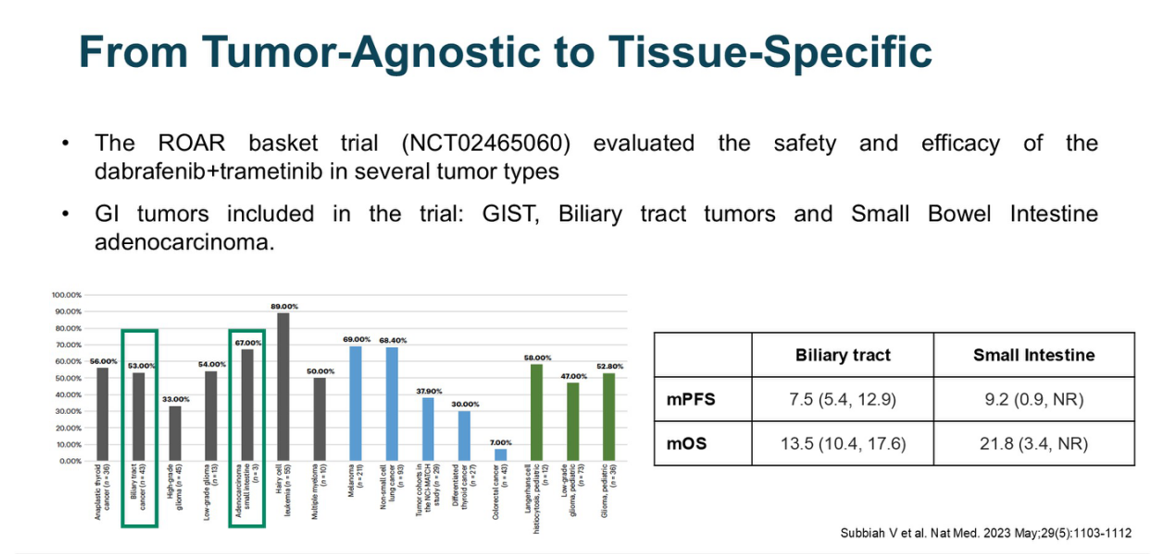
针对非结直肠肿瘤,ROAR篮子试验具有重要意义。该研究讨论了达拉非尼联合曲美替尼(D+T)的双靶方案在不同V600E突变肿瘤中的有效性。在胃肠道领域,该研究涵盖了胆道肿瘤、胃肠道间质瘤和小肠腺癌。数据结果令人印象深刻:胆道癌的ORR达到了53%,小肠肿瘤更是高达67%,中位总生存(OS)分别达到13.5个月和21.8个月,中位无进展生存(PFS)为7.5个月和9.2个月。基于此,D+T方案获批用于既往治疗后进展且无其他替代疗法的BRAF V600E突变实体瘤。从安全性看,该方案具有一定优势,最常见的副作用为发热和疲劳。此外,该方案半衰期较短,使得临床在调节治疗毒性时更加灵活容易。
结直肠癌靶向治疗的突破:BEACON研究与联合策略
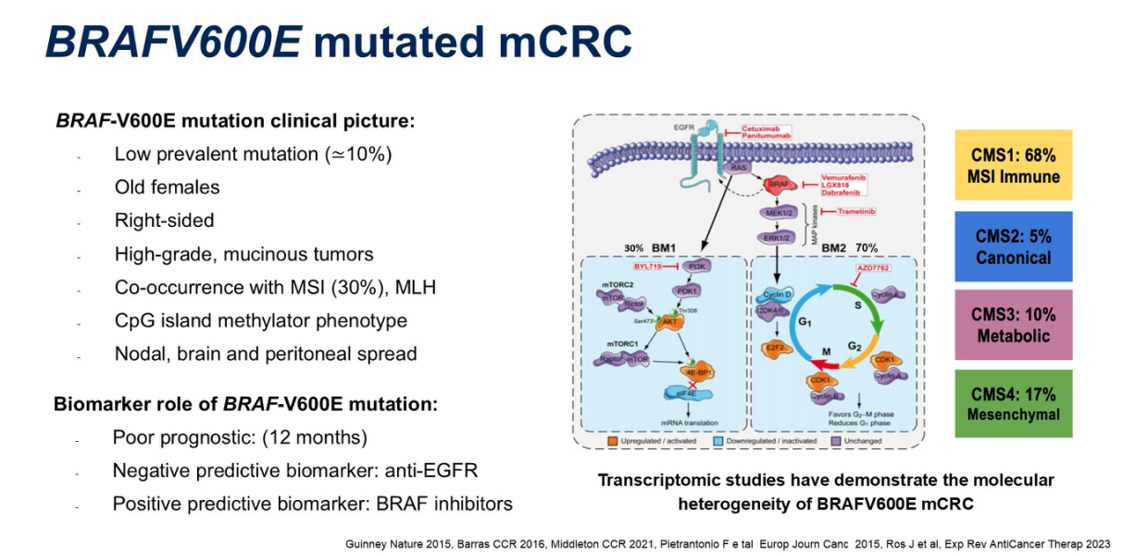
具体到结直肠癌领域,BRAF V600E突变呈现出独特的临床画像与分子异质性。临床上,这类患者多见于老年女性,病灶常发于右半结肠,病理学表现为高级别形态且常含有黏液成分。此外,该突变常伴随CpG岛甲基化表型(CIMP),且患者极易发生淋巴结、大脑及腹膜转移。值得关注的是,BRAF V600E突变与微卫星高度不稳定(MSI-H)高度相关,两者重叠率约为30%,这对于规划治疗顺序至关重要。从预后来看,携带该突变是典型的预后不良指标,传统中位生存期仅约12个月。
深入分子层面,转录组学研究揭示了这类肿瘤内部的异质性。约68%的患者属于CMS1型(免疫型),具有强烈的免疫炎性提示,可能从免疫治疗中获益;而CMS4型(间质型)则伴有明显的间质浸润,是预后最差的亚型。根据BM1和BM2亚型划分,BM1型(约30%)主要通过PI3K-mTOR信号通路激活,代谢旺盛,信使RNA翻译活跃;BM2型(约70%)则主要受细胞周期通路驱动,由Cyclin D及CDK4/6介导,细胞具有快速分裂倾向。
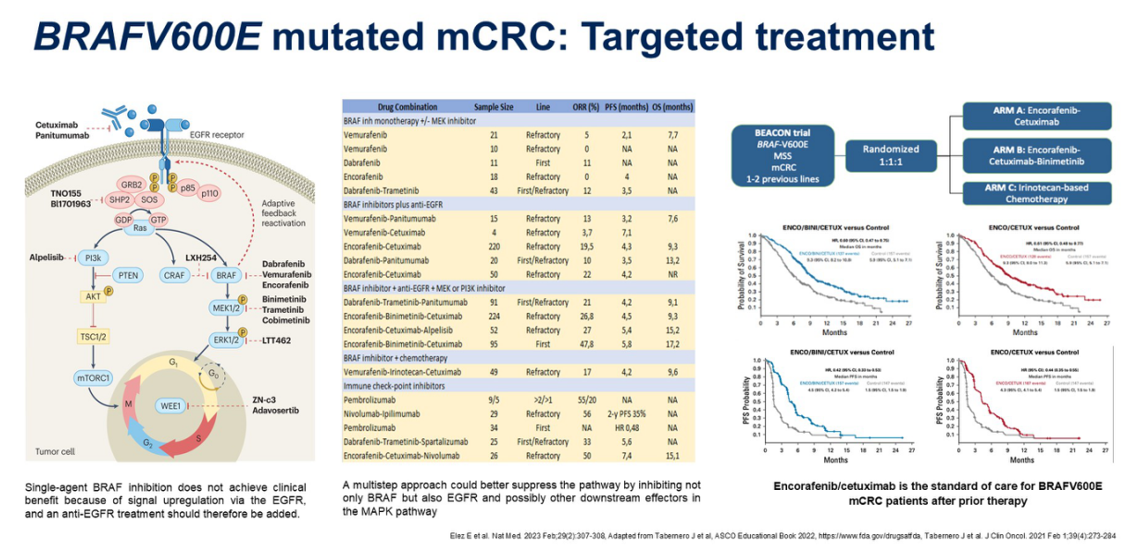
在标准治疗的早期探索中,临床最初尝试像治疗黑色素瘤那样,采用BRAF抑制剂联合MEK抑制剂,但这种策略在结直肠癌中归于失败。基于EGFR反馈激活的理论,研究者认识到必须将BRAF抑制剂与EGFR抑制剂联合使用。为了进一步探索是否需要加入第三种药物(如 MEK 抑制剂或 PI3K 抑制剂)以提升疗效,BEACON研究应运而生。
这项随机临床研究对比了恩考芬尼联合西妥昔单抗的双药方案、在此基础上加入比美替尼的三药方案以及含伊立替康的标准化疗。结果显示,双药和三药方案在生存获益上均显著优于标准治疗,但双药与三药方案之间并未观察到显著差异。这奠定了双药联合方案(EC 方案)作为携带BRAF V600E突变转移性结直肠癌二线或三线标准治疗的地位。
一线治疗的最新进展:BREAKWATER研究
然而,如果我们希望在这一群体中进一步提升疗效,采取何种策略?我们知道,一旦识别出驱动因素,越早阻断对患者越有利。正是基于“策略前移”的逻辑,我们迎来了BREAKWATER研究。
BREAKWATER研究是一项随机III期临床试验,旨在解答两个核心问题:联合疗法能否增强应答,以及尽早开始一线治疗是否能带来更多益处。该研究比较了恩考芬尼联合西妥昔单抗(EC方案)、EC联合改良的FOLFOX6方案,以及标准治疗方案(化疗联合或不联合贝伐珠单抗)。结果证明,EC联合mFOLFOX6的联合疗法相较于标准治疗展现出压倒性优势:试验组中位OS达到了30.3个月,比标准治疗组的15.1个月实现了翻倍增长。在PFS方面,试验组以12.8个月对比标准组的7.1个月,同样具有突破性意义。
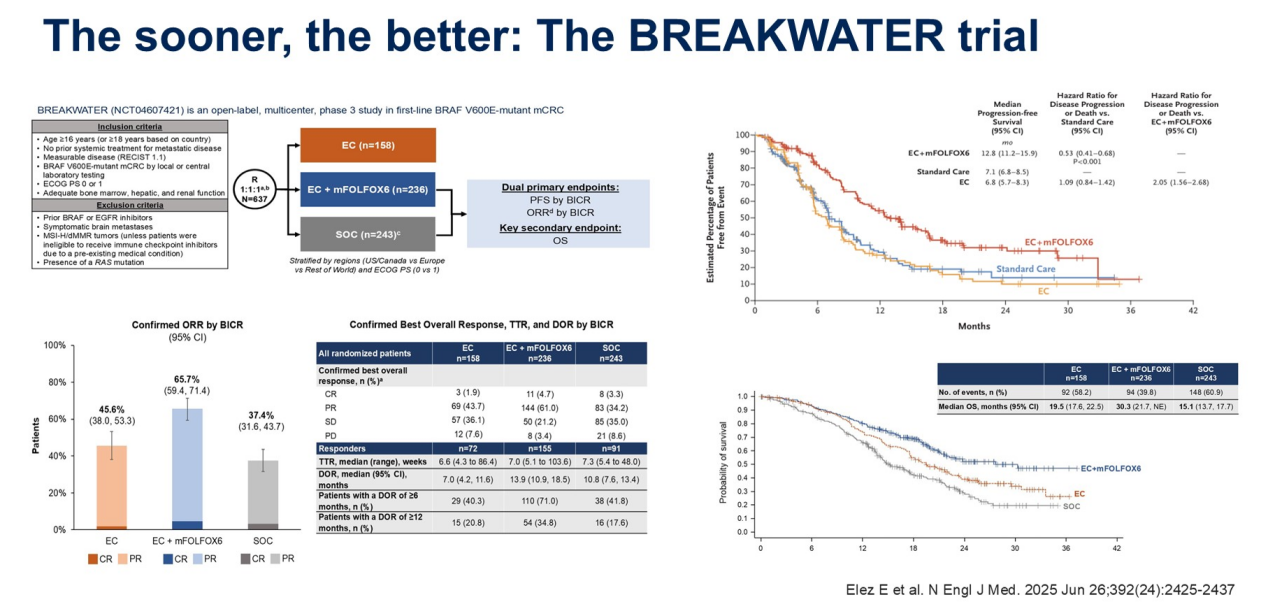
值得深入探讨的是关于EC双靶组的招募问题。由于另一项II期研究数据显示,单纯靶向二联或三联方案在没有化疗配合时,一线表现出的强度可能不足以挑战标准方案。因此BREAKWATER提前终止了EC纯靶向组的招募。但在特定情况下,对于不适合化疗的患者,EC双靶方案的中位OS仍可达到20个月,仍是一种可行的选择。
在BRAF突变的结直肠癌治疗中,缓解率至关重要,因为这类患者通常肿瘤负荷大且进展极快。BREAKWATER研究显示,接受EC联合mFOLFOX6治疗的患者,其ORR高达65.7%,在所有预设亚组中均观察到了OS获益。安全性方面,该联合疗法整体可控,最常见的副作用(≥25%)为恶心、发热、便秘和疲劳。值得强调的是,联合方案中奥沙利铂的剂量强度和持续时间与标准治疗相当。基于此研究,EC联合mFOLFOX6已正式被NCCN和ESMO指南纳入,作为该患者一线治疗的首选方案。
此外,该研究还带给我们一些关于耐药机制的深刻思考。生物标志物分析发现,组织活检与液体活检中BRAF突变检测具有高度一致性。更重要的是,接受EC联合化疗方案治疗的患者,获得性耐药突变(如 KRAS、NRAS和MAP2K1)的发生率更低。这很可能与化疗的作用相关:由于BRAF突变人群本身存在异质性,化疗或许能够清除那些对单纯靶向治疗不敏感的亚克隆细胞,从而延缓耐药的发生。
未来方向:免疫联合与新型药物
针对BRAF V600E突变伴随MSI-H的患者,免疫治疗联合靶向治疗正成为研究热点。初步研究显示,康奈非尼+西妥昔单抗+纳武利尤单抗该类患者中的ORR达到50%,疾病控制率(DCR)高达96%。这表明BRAF抑制与免疫检查点抑制之间存在协同效应,可能通过诱导免疫微环境的改变(如增加T细胞浸润和吞噬作用标志物)来增强抗肿瘤反应。
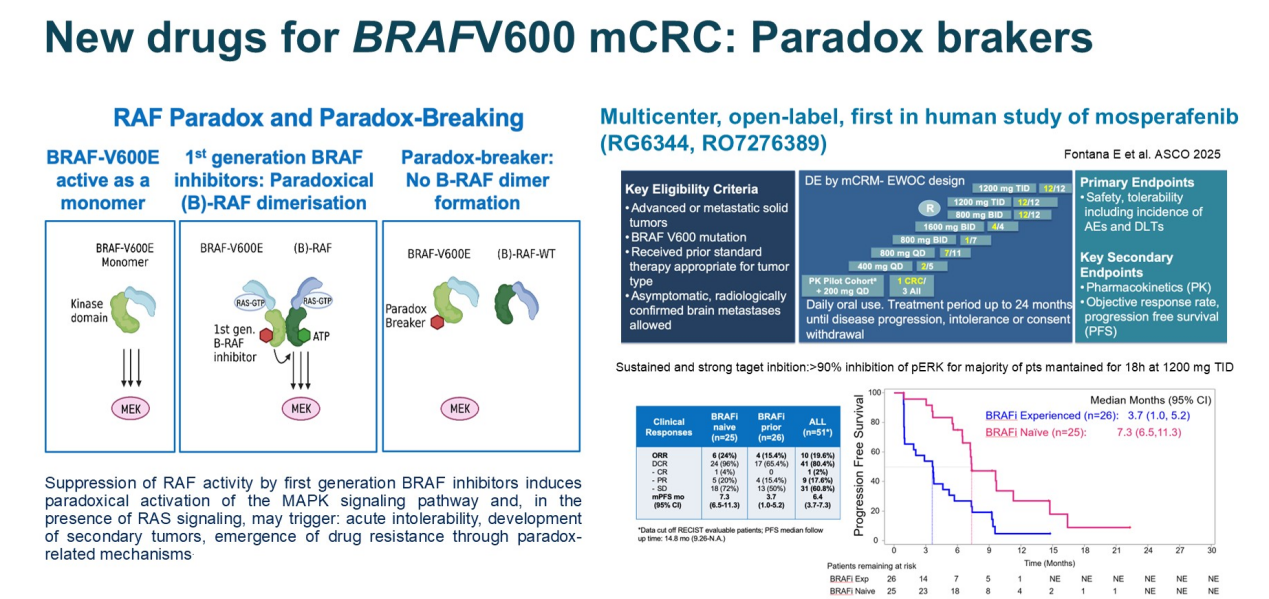
此外,为应对BRAF抑制剂带来的“RAF悖论”——即第一代BRAF抑制剂可能通过激活C-RAF导致MAPK信号反弹,新一代“悖论打破者”正在开发中。例如,mosperafenib(RG6344)在初步研究中显示,在经BRAF抑制剂治疗后的患者中仍有3.7个月的中位PFS,且在初治患者中获益更佳(PFS 7.3个月)。另一种新型药物BRAF降解剂(如CFT1946)则通过诱导蛋白降解来抑制BRAF信号,初步数据已显示出良好的剂量依赖性生物利用度和抗肿瘤活性迹象。
小 结
BRAF突变肿瘤的治疗已从最初的单药尝试,演进到了基于生物学机制的精准联合策略。从跨癌种的异质性获益,到结直肠癌中联合EGFR抑制的突破,再到一线治疗中靶向联合化疗的成功,每一步都体现了转化医学与临床研究的紧密结合。未来的挑战在于如何通过更精细的分子分型指导个性化选择,以及如何利用免疫联合方案和新型降解剂彻底攻克耐药难题,为患者带来更长久的生存获益。
排版编辑:肿瘤资讯-YXD











 苏公网安备32059002004080号
苏公网安备32059002004080号


