肺癌脑转移是晚期非小细胞肺癌(NSCLC)管理中的重要难点。脑转移灶与原发肺肿瘤之间可能存在分子差异,其中MET扩增等改变具有潜在治疗指向性,但脑转移组织取样困难,限制了相关分子特征在临床中的动态评估。
2026年AACR年会上,来自美国匹兹堡大学UPMC希尔曼癌症中心的Laura P. Stabile教授报告了血浆ctDNA检测肺癌脑转移特异性改变的相关研究。结果显示,脑转移患者血浆中更易检出MET改变,尤其是MET扩增;但前瞻性配对分析提示,血浆循环肿瘤DNA(ctDNA)虽可捕捉部分脑转移相关信号,对MET扩增等拷贝数异常的敏感性仍不足。未来仍需提高检测灵敏度、优化采样时机,并结合脑脊液(CSF)ctDNA和影像基因组学,提升脑转移分子检测的准确性。【肿瘤资讯】整理了其中精华内容,以飨读者。
肺癌脑转移治疗仍需特异性靶点突破
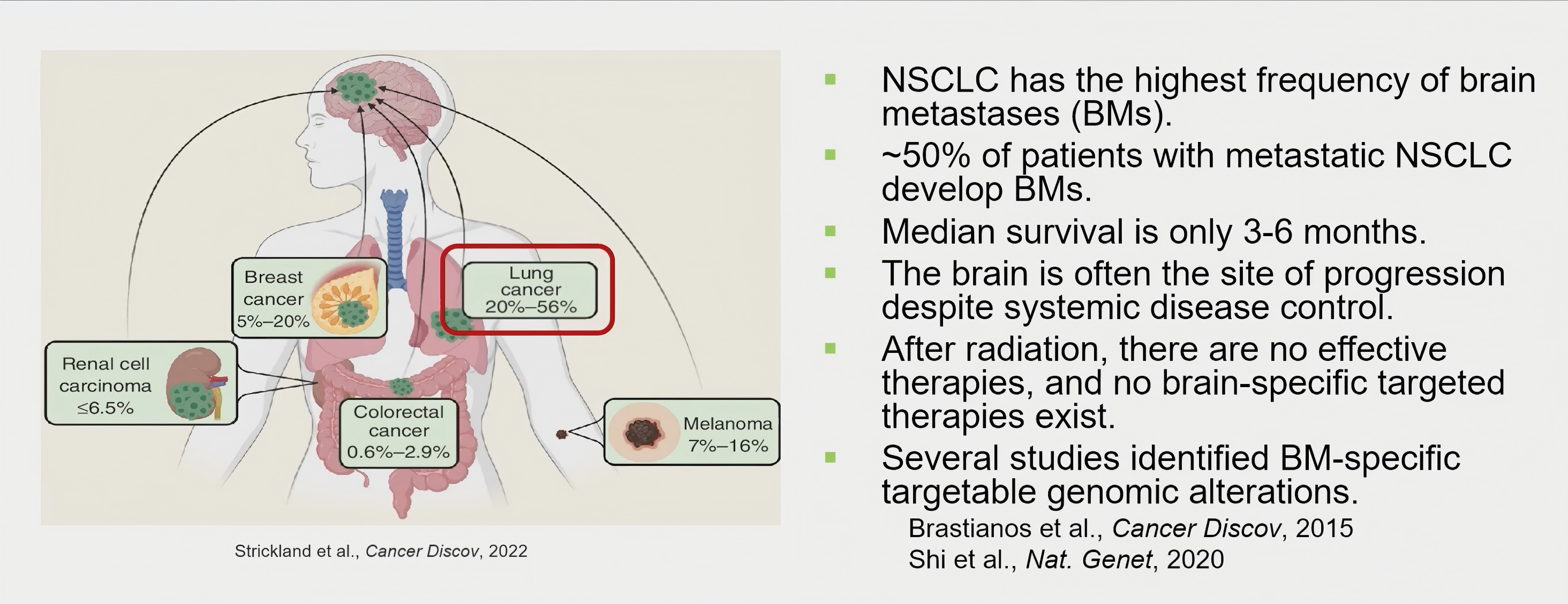
发生率高、预后差:NSCLC是脑转移高发肿瘤类型,约半数转移性NSCLC患者可能发生脑转移,患者生存获益仍有限。
治疗选择不足:脑部常在全身疾病控制后继续进展,放疗后缺乏有效后续治疗,也缺少脑转移特异性靶向策略。
靶点探索必要:脑转移灶可能存在独立于原发灶的可靶向分子改变,提示有必要进一步寻找脑转移特异性治疗靶点和非侵入性检测方法。
MET扩增成为脑转移治疗的潜在切入点
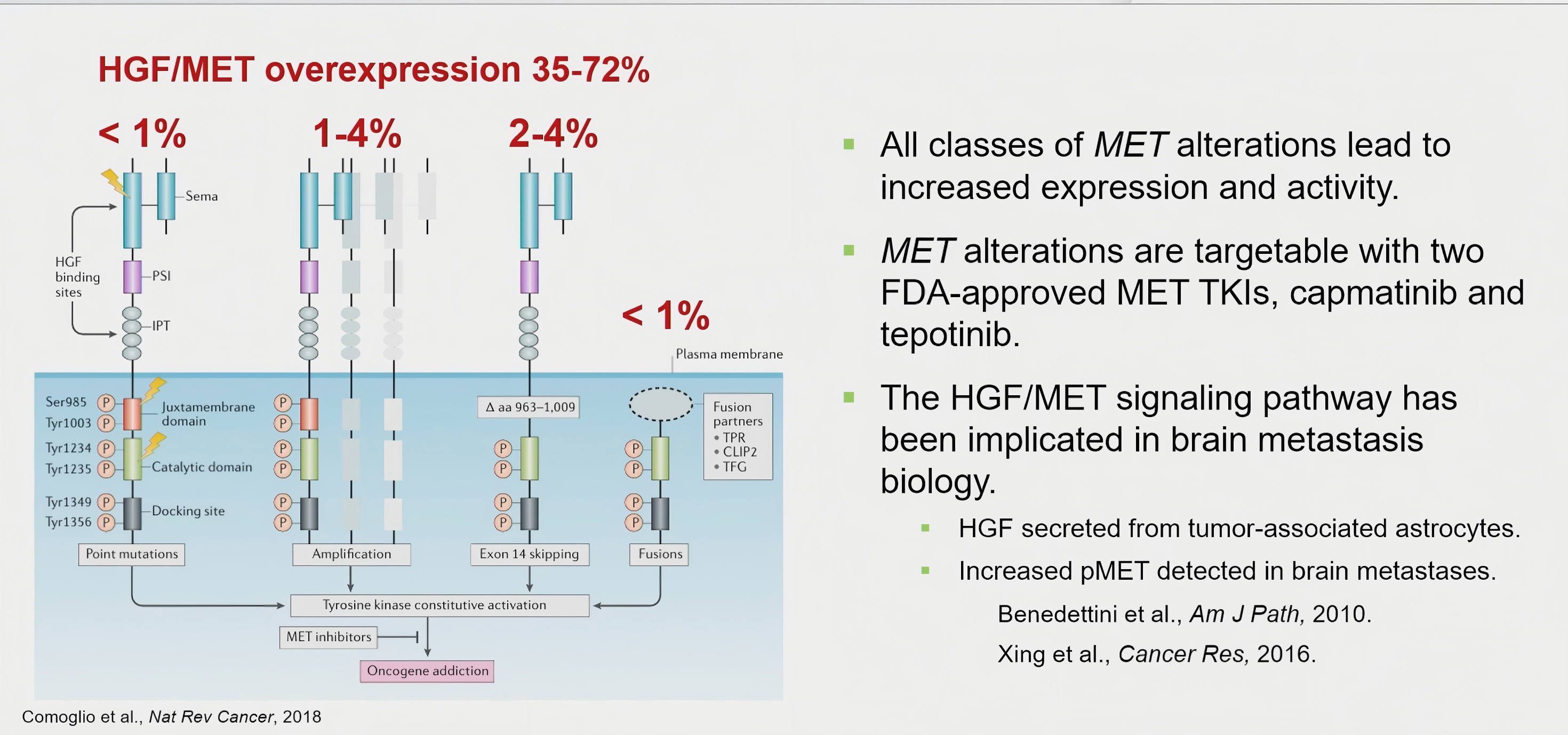
HGF/MET通路在肺癌中常被激活,MET过表达、扩增、突变、14号外显子跳跃及融合等改变均可增强通路活性,促进肿瘤进展。由于MET已有相应靶向药物可用于临床干预,因此其不仅是分子异常,也具有明确的治疗转化价值。
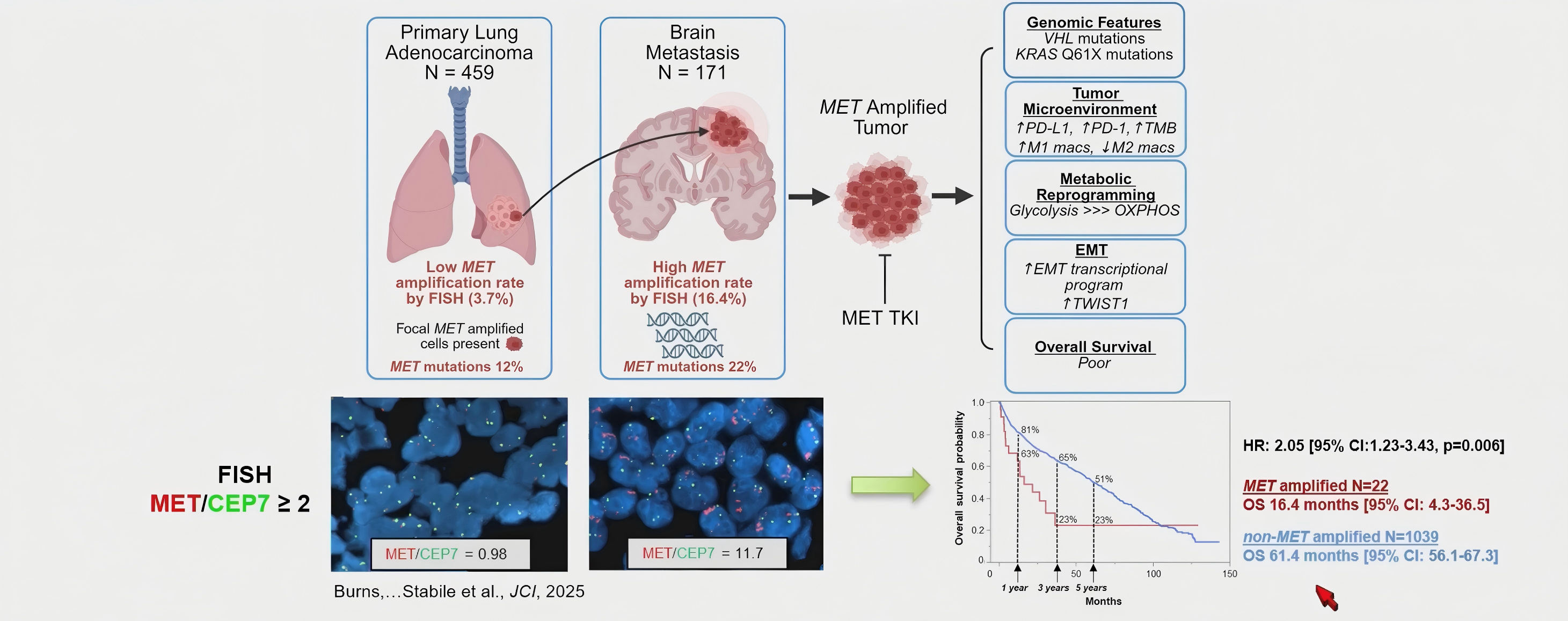
在脑转移场景中,MET的重要性进一步凸显。既往研究提示,脑转移微环境可能促进HGF/MET信号活化;同时,肺腺癌脑转移灶中MET扩增比例高于原发灶,说明脑转移可能形成区别于原发肿瘤的分子特征。
因此,MET扩增既反映了脑转移灶的分子异质性,也可能对应潜在治疗机会。对脑转移相关MET改变进行识别,有助于筛选可能从MET-TKI治疗中获益的患者,并为后续探索ctDNA非侵入性检测提供依据。
血浆ctDNA显示检测可行性但敏感性受限
脑转移灶可能具有独立分子特征,但组织取样难以反复开展,血浆ctDNA因此成为连接脑转移分子检测与临床可及性的关键路径。本部分内容提示ctDNA能够捕捉部分脑转移相关改变,但对MET扩增等拷贝数异常的检出仍不稳定,说明其临床应用仍受到检测敏感性的限制。
回顾性分析显示,在277例转移性NSCLC患者中,伴脑转移者血浆ctDNA中MET改变检出率更高,差异主要来自MET扩增,而非MET突变。这一结果提示,血浆ctDNA可能具备捕捉脑转移相关MET扩增的潜力。

前瞻性研究进一步采用配对样本设计,重点评估ctDNA对脑转移相关改变的检测能力:
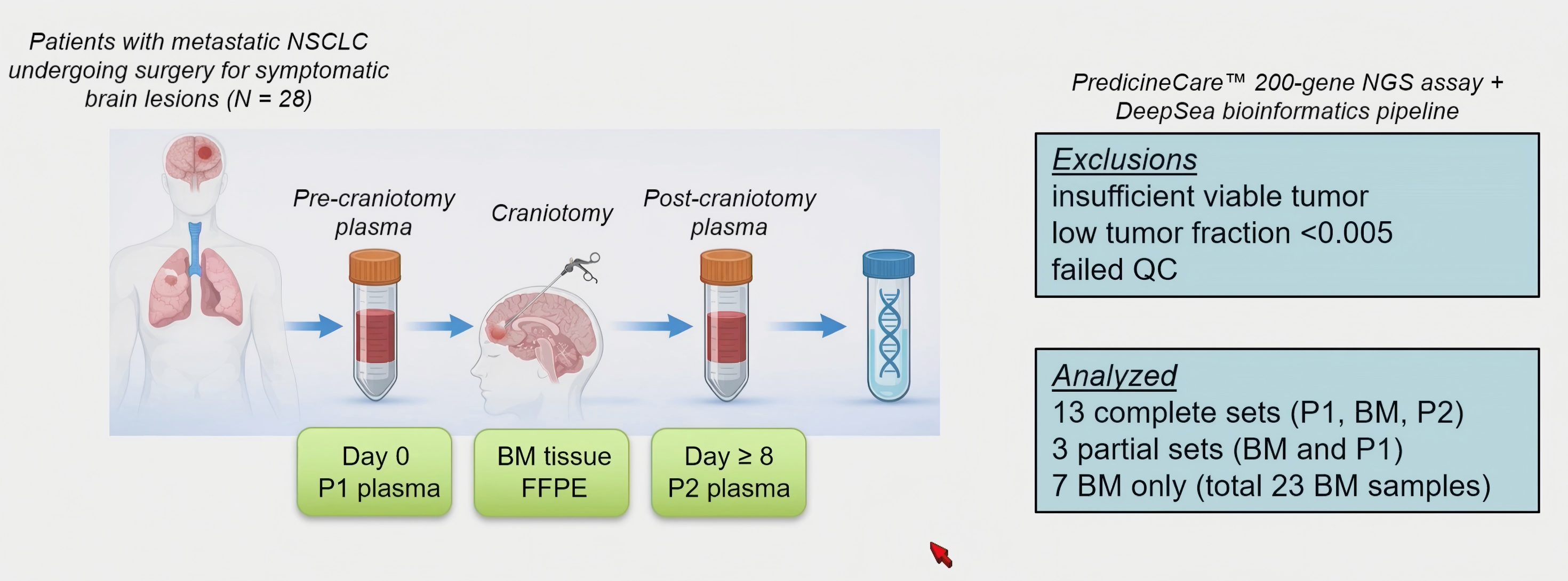
研究对象:纳入因症状性脑转移病灶接受手术的转移性NSCLC患者,共28例。
采样流程:分别采集术前血浆P1、脑转移组织 BM,以及术后第 8 天或之后的血浆P2。
检测方法:采用PredicineCare™200基因NGS assay,结合DeepSea生物信息学流程进行分析。
最终分析样本:包括13组完整配对样本、3组部分配对样本,以及7例仅有脑转移组织样本,总计23 份脑转移组织样本。
通过术前血浆、脑转移组织和术后血浆的动态对照,研究能够从信号变化中判断血浆 ctDNA 与脑转移病灶的关联。
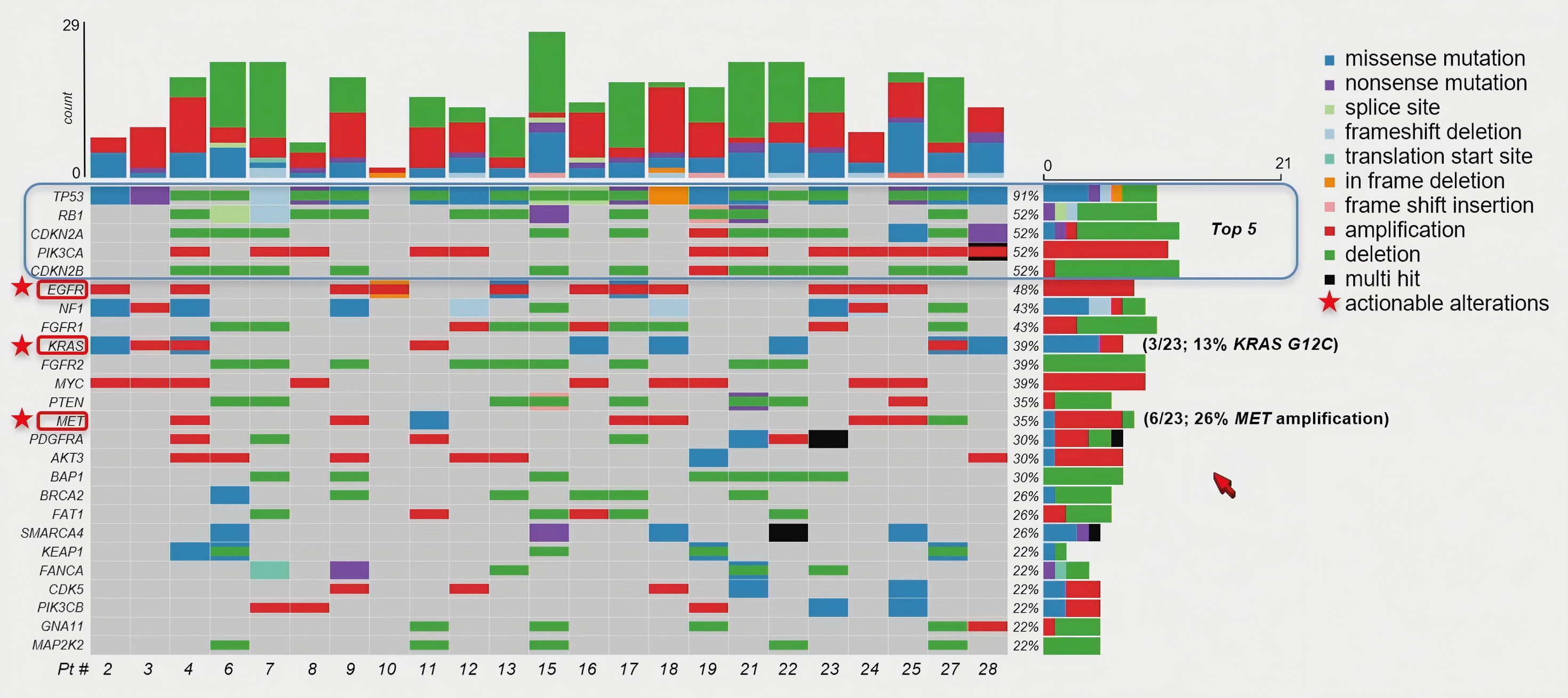
脑转移组织存在可靶向改变:脑转移样本中可见TP53、RB1、CDKN2A/B、PIK3CA等常见异常,同时检测到EGFR、KRAS、MET等可能影响靶向治疗选择的基因改变,其中MET扩增见于6/23例。
血浆ctDNA可反映部分脑转移信号:通过术前血浆、脑转移组织和术后血浆的动态对照,部分共同检出的改变在病灶切除后下降或消失,支持ctDNA可捕捉部分脑转移来源信号。
拷贝数改变仍易漏检:MET扩增等脑转移相关拷贝数异常在血浆中检出不稳定,提示血浆ctDNA目前仍难以作为可靠的独立检测依据。
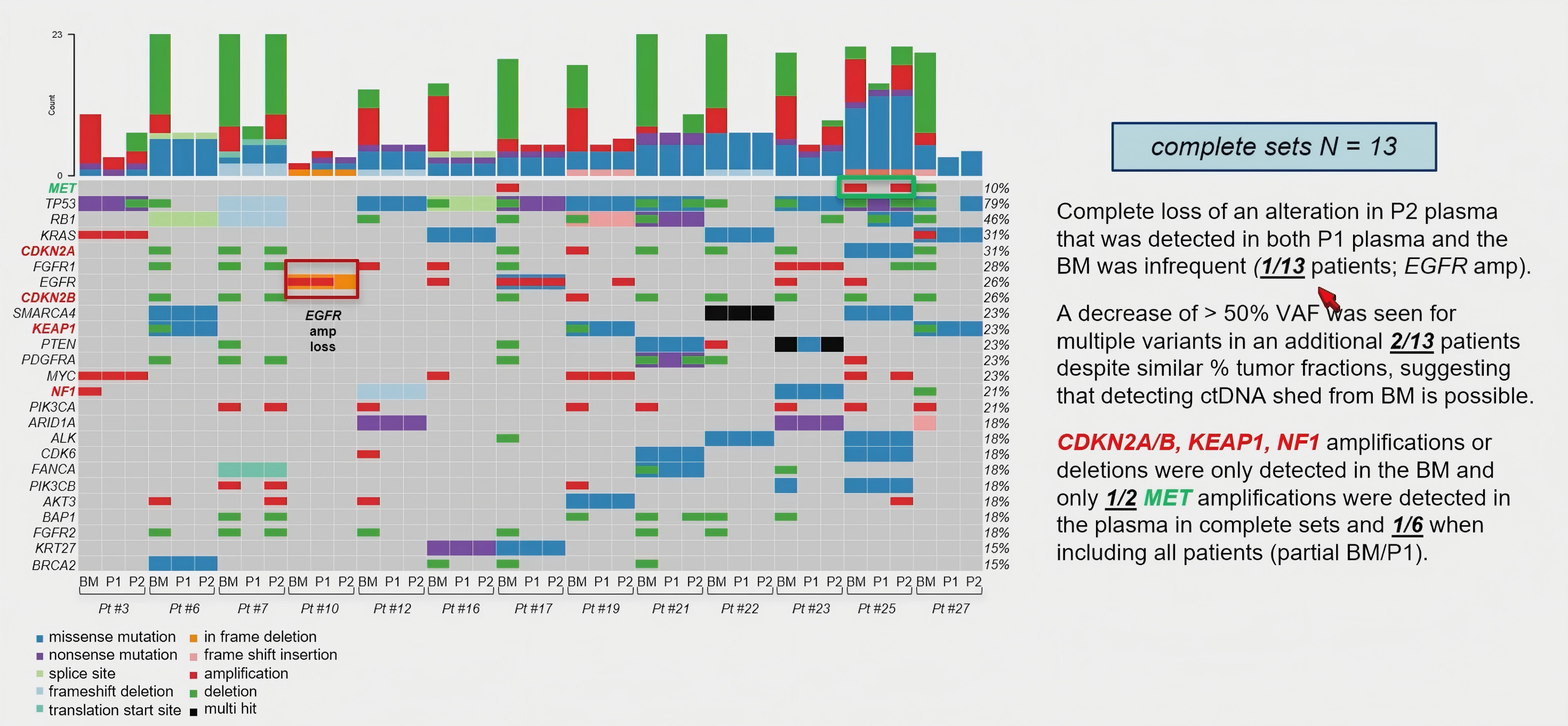
总体来看,血浆ctDNA具备非侵入性检测脑转移相关改变的潜力,但敏感性不足仍是限制其应用的核心问题。
提升ctDNA检测可靠性的后续方向
血浆ctDNA对脑转移相关改变具有检测潜力,但对MET扩增等拷贝数异常的检出仍不稳定。值得注意的是,脑部放疗后P2血浆中出现了MET扩增、MYC扩增和TP53缺失等放疗前未明显检出的改变,这一现象提示,治疗后肿瘤DNA释放增加,可能使脑转移相关分子信号更容易进入外周血,也为优化采样窗口提供了重要线索。
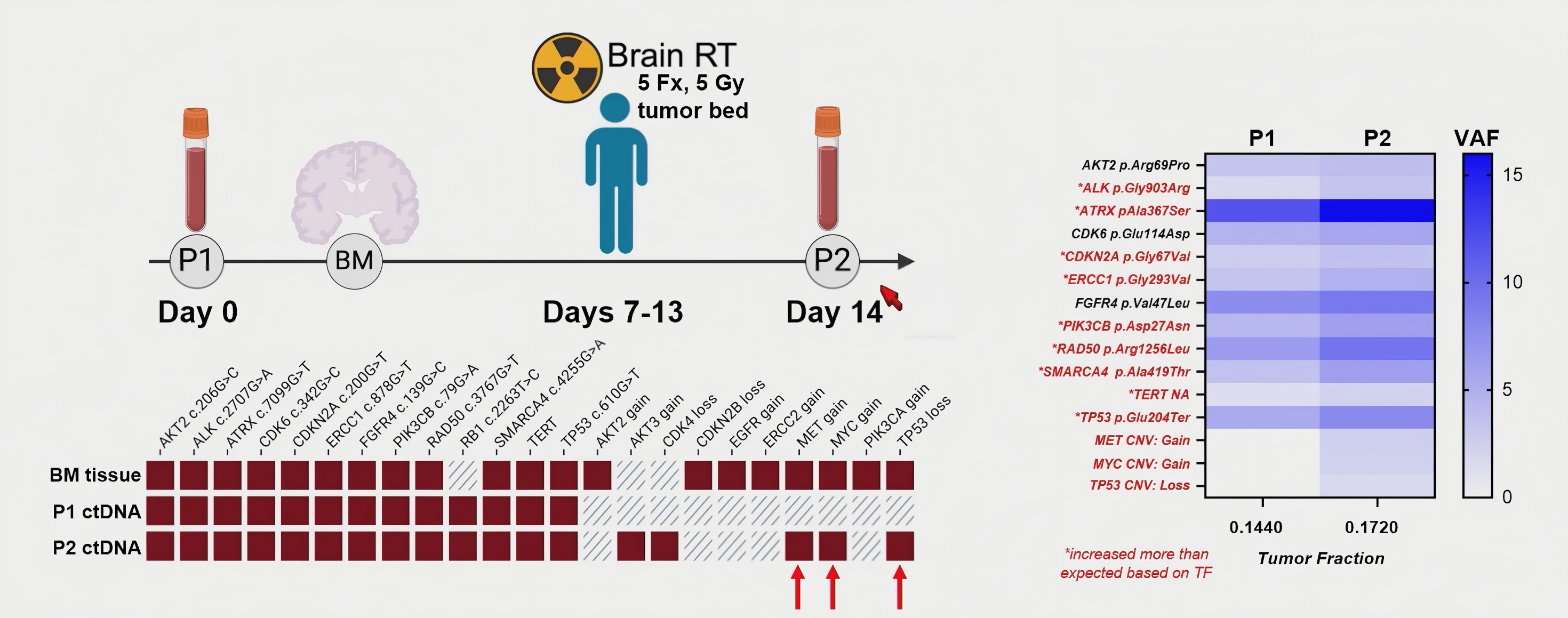
因此,提高ctDNA检测可靠性不能只依赖检测平台本身,还需要关注采样时机。可以进一步结合CSFctDNA和影像基因组学,更全面地反映脑转移病灶的分子特征,提升非侵入性检测的临床应用价值。
总结
总体来看,肺癌脑转移灶可能存在不同于原发灶的分子改变,这也使非侵入性检测具有更明确的应用需求。
1.靶点识别需求:肺癌原发灶与脑转移灶存在分子差异,需进一步识别脑转移特异性基因改变。
2.ctDNA检测可行:血浆ctDNA可捕捉部分脑转移相关信号,为非侵入性检测提供了可能。
3.敏感性仍待提升:血浆ctDNA对MET扩增等拷贝数异常检出不稳定,仍难作为独立检测依据。
未来需提高检测敏感性,优化采样时机,并结合CSFctDNA和影像基因组学,提升脑转移分子检测准确性。
1.Strickland MR, Alvarez-Breckenridge C, Gainor JF, Brastianos PK. Tumor Immune Microenvironment of Brain Metastases: Toward Unlocking Antitumor Immunity. Cancer Discov. 2022 May 2;12(5):1199-1216. doi: 10.1158/2159-8290.
2.Comoglio PM, Trusolino L, Boccaccio C. Known and novel roles of the MET oncogene in cancer: a coherent approach to targeted therapy. Nat Rev Cancer. 2018 Jun;18(6):341-358. doi: 10.1038/s41568-018-0002-y.
3.Burns TF, Dacic S, Chakka A, Miller E, Velez MA, Somasundaram A, Bhattacharya S, Gaither-Davis A, Devadassan P, Jin J, Kumar V, Pennathur A, Xiu J, Oberley M, Glantz MJ, Aulakh S, Chandran UR, Bao R, Tatsuoka C, Stabile LP. MET alterations are enriched in lung adenocarcinoma brain metastases, defining a distinct biologic subtype. J Clin Invest. 2025 Dec 18;136(4):e194708. doi: 10.1172/JCI194708.
排版编辑:肿瘤资讯-Yume











 苏公网安备32059002004080号
苏公网安备32059002004080号


