在晚期非小细胞肺癌(NSCLC)的诊疗实践中,EGFR突变患者的精准治疗始终是研究重心。尽管近年来EGFR靶向治疗取得了长足进步,但耐药机制的复杂性及高危人群的预后改善仍是临床亟待攻克的难题。近日,《中国临床肿瘤学会(CSCO)非小细胞肺癌诊疗指南2026》正式发布,最新版指南针对EGFR突变晚期NSCLC的治疗推荐进行了多项重要更新。基于此,【肿瘤资讯】特邀上海市东方医院周彩存教授和周斐教授,针对最新指南中关于EGFR突变晚期NSCLC的治疗推荐进行解读。
EGFR敏感突变一线治疗:埃万妥单抗皮下剂型联合兰泽替尼治疗方案获得本次指南最新推荐,联合方案推荐等级进一步提升
针对EGFR敏感突变(ex19del、L858R)晚期NSCLC患者,第三代EGFR酪氨酸激酶抑制剂(TKI)单药是目前标准的初始治疗方案。然而,单药治疗的获益已达瓶颈,特别是对于合并高危因素的患者,疗效亟待提升。因此,探索以多靶点、新机制为基础的联合治疗策略已成为一线治疗的重要方向。在此背景下,埃万妥单抗联合兰泽替尼的新型联合方案展现出卓越的疗效,并且实现了“Chemo-free”,为EGFR敏感突变晚期一线NSCLC患者提供一种新的治疗模式。埃万妥单抗作为一种EGFR/MET双特异性抗体,能够通过胞内胞外深度抑制EGFR和MET通路,并协同激活特异性免疫系统杀伤肿瘤细胞[1]。
MARIPOSA研究对比了埃万妥单抗联合兰泽替尼与奥希替尼单药作为EGFR敏感突变一线治疗的疗效和安全性。结果显示,联合组中位无进展生存期(mPFS)达23.7个月,较单药组(16.6个月)显著延长,疾病进展或死亡风险降低30%(HR=0.70,P<0.001)[2]。在中位总生存期(mOS)方面,联合组mOS尚未达到,相较于单药组mOS 36.7个月,展现出强劲的临床获益,改善预计超过一年(HR=0.75,P=0.005),这标志着联合方案显著改善了患者长期生存[3]。值得一提的是,亚洲人群亚组分析显示,联合治疗的生存获益更为突出,mPFS达27.5个月,较全人群数据(23.7个月)更具优势,并且HR值更低(HR=0.65)[4]。OS获益与全人群趋势一致,HR为 0.74(图1)[5],并且基于5种统计学模型预估的亚洲人群联合组最佳mOS预计可达64.5个月,有望突破5年大关[6]。
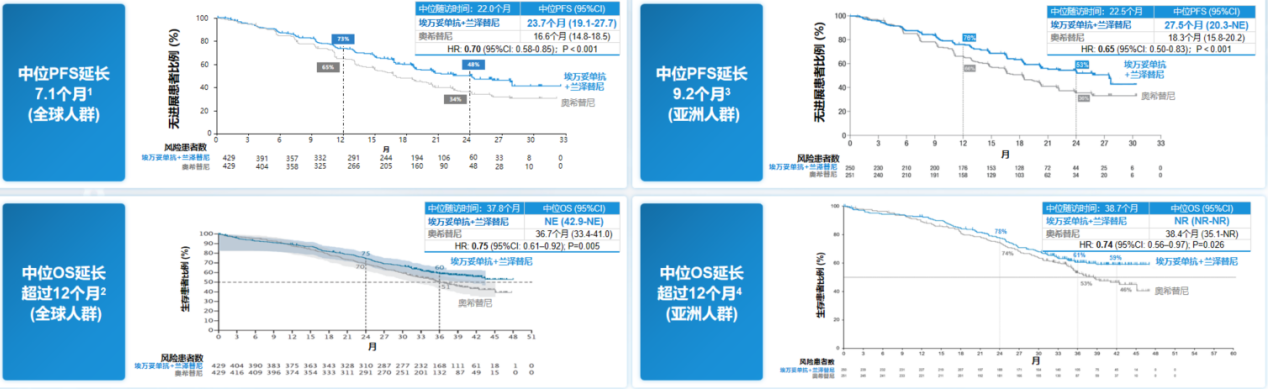
另外,MARIPOSA研究的多项亚组分析表明,埃万妥单抗联合兰泽替尼方案为脑转移、肝转移、TP53共突变等预后较差的人群带来了显著获益。针对脑转移患者,该联合方案的颅内疗效优势尤为突出:3年颅内PFS(icPFS)率达到单药组的2倍(36% vs 18%),颅内缓解持续时间(icDoR)较单药组延长半年(35.7个月 vs 29.6个月)[7]。OS亚组分析显示,基线脑转移患者也可获得显著OS获益[3],这说明埃万妥单抗联合兰泽替尼不仅可高效控制颅内病灶进展,还可将其转化为患者切实的生存获益。值得注意的是,亚洲人群的颅内获益与全球数据一致甚至更优[8]。基于此,最新NCCN CNS指南(2025. V3)推荐埃万妥单抗联合兰泽替尼作为EGFR突变晚期NSCLC 脑转移优选(Preferred)治疗方案。此外,肝转移患者接受联合治疗后,mPFS较奥希替尼单药组显著延长(18.2 vs 11.0个月;HR=0.58,P=0.017)[9]。在伴有TP53共突变的患者中,联合治疗将mPFS从12.9个月延长至18.2个月,疾病进展或死亡风险降低35%(HR=0.65,P=0.003)[9]。
为优化给药便利性,PALOMA系列研究对埃万妥单抗皮下注射(SC)剂型相较于传统静脉注射(IV)剂型的疗效和安全性进行了验证。其中,PALOMA-2研究队列1、5和6探索了埃万妥单抗SC剂型联合兰泽替尼一线治疗EGFR敏感突变晚期NSCLC。结果显示,埃万妥单抗SC剂型Q2W/Q4W联合兰泽替尼均与MARIPOSA研究中IV剂型ORR一致。安全性方面,SC剂型使给药相关反应(ARR)的发生率由IV剂型的63%显著降至12%-15%[10, 11]。
此外,埃万妥单抗SC剂型还显著提高了临床使用的便捷性和患者用药体验,并进一步提升了患者OS获益。SC剂型单次给药时间由IV剂型的数小时缩短至约5分钟,85%患者认为埃万妥单抗SC剂型的给药方式方便或非常方便,这极大提升了临床操作效率和患者依从性[12]。PALOMA-2研究队列1生存期分析显示,埃万妥单抗SC Q2W联合兰泽替尼mPFS为27.6 个月,数值上较MARIPOSA研究中IV 剂型(mPPF为 23.7个月)更有优势;埃万妥单抗SC Q2W联合兰泽替尼的OS获益也令人振奋,12个月OS率为94%,18个月OS率为88%[13]。另外,在III期PALOMA-3研究的探索性分析中发现,埃万妥单抗SC剂型联合兰泽替尼较IV剂型降低38%死亡风险,进一步带来显著生存获益(HR 0.62, p-0.02)[12]。上述证据表明,埃万妥单抗SC 剂型在保持与IV剂型相当疗效的同时显著降低了ARR,并提升患者的耐受性和用药体验,使患者可以接受更长期的治疗,为EGFR敏感突变晚期NSCLC一线治疗提供更便捷的用药选择。
基于疗效与安全性数据的完善,2026 NCCN NSCLC指南(2026. V5)已将埃万妥单抗联合兰泽替尼作为EGFR敏感突变晚期NSCLC一线治疗的优选(Preferred)。《CSCO非小细胞肺癌诊疗指南2026》也将埃万妥单抗(含IV与SC剂型)联合兰泽替尼一线治疗EGFR敏感突变晚期NSCLC的推荐等级从Ⅲ级提升至Ⅱ级推荐(图2)。尽管该联合方案在疗效(PFS及OS的双重获益)和安全性方面均表现出高度的可靠性,理应获得更高的推荐等级。但由于该方案暂未进入2025版国家医保目录,因此目前定位为临床优选的Ⅱ级方案。

克服EGFR敏感突变耐药瓶颈:ACP方案给后线治疗带来新曙光
第三代EGFR-TKI是EGFR突变晚期NSCLC的标准一线治疗,但部分患者仍会面临耐药问题。由于第三代EGFR-TKI耐药机制复杂,表现出高度的异质性,因此克服第三代EGFR-TKI耐药问题一直是临床难点。MET扩增和EGFR C797S突变是第三代EGFR-TKI中最常见的耐药机制,因此,EGFR/MET双特异性抗体埃万妥单抗在克服第三代EGFR-TKI耐药方面展现出巨大的潜力。
MARIPOSA-2研究结果显示,在奥希替尼进展后的患者中,埃万妥单抗联合化疗(ACP方案)显示出显著优势。ACP方案的mPFS由化疗组的4.2个月延长至6.3个月(HR=0.48,P<0.001),ORR从36%提升至64%[14]。随访时间延长后,ACP方案OS获益趋势愈发显著,ACP方案的mOS为17.7个月,可降低死亡风险27%(HR=0.73),呈现持续的生存获益趋势[15]。mPFS在亚洲人群中有同样获益趋势(6.8 vs 4.2个月,HR=0.54,P=0.002)[16]。在SC剂型的探索方面,PALOMA-2研究队列3b结果[17]表明,对于奥希替尼进展后的EGFR突变患者,埃万妥单抗SC剂型在保持疗效的同时,显著提升了便利性与安全性,为后线治疗提供了更优的给药选择。
基于此,2026 NCCN NSCLC指南(2026. V5)已将ACP方案作为EGFR敏感突变晚期NSCLC奥希替尼治疗失败后的优选(Preferred)。同样由于受到医保政策的影响,《CSCO非小细胞肺癌诊疗指南2026》也将埃万妥单抗联合化疗作为EGFR敏感突变晚期NSCLC耐药后治疗的Ⅱ级推荐(图3)。

EGFR ex20ins的治疗突破:埃万妥单抗开启高效治疗新时代
EGFR ex20ins是第三种常见的EGFR突变类型,由于其独特的激酶活性位点构象改变,传统EGFR-TKI对该突变疗效有限,预后显著差于EGFR敏感突变[18]。埃万妥单抗主要通过3个潜在的作用机制激发其抗肿瘤活性:配体阻断、受体降解和免疫细胞导向活性,得益于此,针对EGFR ex20ins这一“难治靶点”,埃万妥单抗也交出了令人满意的答卷。
PAPILLON研究确立了ACP方案在EGFR ex20ins患者中的一线治疗价值。结果显示,ACP组和化疗组经BICR评估的mPFS分别为11.4个月和6.7个月,ACP组降低了60%的疾病进展或死亡风险(HR=0.40,P<0.001)。值得注意的是,尽管化疗组有66%的患者在进展后交叉接受埃万妥单抗二线治疗,ACP组仍显示出OS获益趋势(HR=0.675),降低30%死亡风险[18]。此外,中国人群亚组的获益与全球人群一致且安全性更优[19]。针对EGFR ex20ins患者,PALOMA-2研究的队列2结果显示,埃万妥单抗SC剂型同样展现了与IV剂型相当的疗效和更好的安全性[20]。除了以ACP联合治疗方案在EGFR ex20ins突变NSCLC发挥优越疗效,埃万妥单抗单药也凭借在CHRYSALIS 研究中的疗效数据获得临床认可[21]。
鉴于PAPILLON研究的突破性贡献,2026 NCCN NSCLC指南(2026. V5)已将ACP方案作为EGFR ex20ins突变晚期NSCLC一线治疗的优选(Preferred),并推荐埃万妥单抗单药用于EGFR ex20ins突变晚期NSCLC后线治疗。《CSCO非小细胞肺癌诊疗指南2026》也将埃万妥单抗联合化疗作为EGFR ex20ins突变晚期NSCLC一线治疗的Ⅰ级推荐,并将埃万妥单抗单药作为EGFR ex20ins突变晚期NSCLC后线治疗的Ⅲ级推荐(图4)。
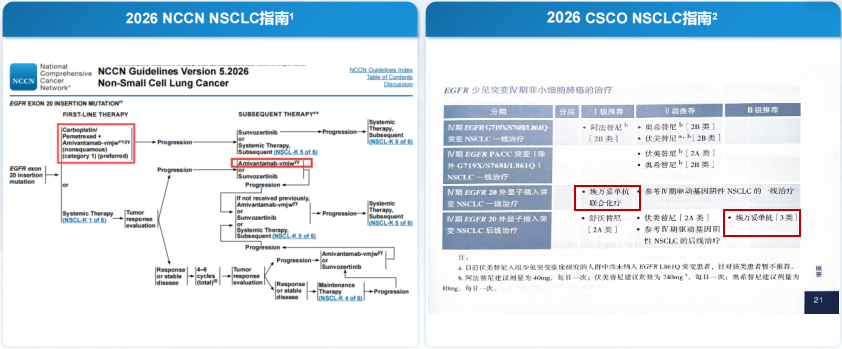
总结与展望
值此指南更新之际,周斐教授表示,《CSCO非小细胞肺癌诊疗指南2026》的更新反映了EGFR突变NSCLC精准治疗的最新趋势,其中最重磅的更新之一就是埃万妥单抗联合兰泽替尼一线治疗EGFR敏感突变晚期NSCLC的推荐等级从Ⅲ级提升至Ⅱ级推荐。这一联合治疗以“Chemo-free”模式成功打破了单药TKI疗效瓶颈,体现了多机制联合方案的临床价值。纵览埃万妥单抗在EGFR突变晚期NSCLC领域的适应症布局,无论在EGFR敏感突变一线治疗和后线治疗不断突破疗效上限,还是在EGFR ex20ins突变一线治疗领域填补治疗空白,埃万妥单抗凭借着EGFR/MET双特异性抗体的机制优势,为EGFR突变NSCLC患者提供了精准、高效且具有长生存潜力的全新治疗选择。
周彩存教授表示,此次《CSCO非小细胞肺癌诊疗指南2026》的更新也充分肯定了埃万妥单抗SC剂型的应用价值。PALOMA系列的成功,不仅在药代动力学和疗效上提供了埃万妥单抗SC剂型和IV剂型等效依据,更证实了SC剂型在安全性、便捷性和患者生活质量上实现了优化,为临床实践中IV和SC剂型的灵活选择提供科学依据。PALOMA-3研究的OS结果更为埃万妥单抗临床剂型的选择增添了关键证据,这一结果有望让SC剂型的临床角色从“备选项”转变为“优选项”,真正实现“精益求精”。展望未来,SC剂型等创新给药方式的大规模应用,不仅显著降低不良反应、节约医疗资源,更大幅提升患者的生存期和生活质量,使“去住院化”和“门诊化”治疗成为可能。期待未来随着真实世界数据的不断积累,更多创新方案早日纳入国家医保体系,进一步打破可及性壁垒,让前沿科学成果惠及更多中国肺癌患者,推动肺癌诊疗向更高的治愈目标稳步迈进。
上海市东方医院肿瘤科主任
同济大学医学院肿瘤研究所所长
国际肺癌研究协会(IASLC)主席
中国医促会胸部肿瘤学分会 主任委员
中国临床肿瘤学会转化医学专家委员会 主任委员
中国抗癌协会非小细胞肺癌专委会 主任委员
中国抗癌协会肿瘤药物临床研究专业委员会 主任委员
上海市抗癌协会肺癌分子靶向和免疫治疗专委会 主任委员
中国医师协会肿瘤分会 常委
上海市抗癌协会 副理事长
上海市医师协会肿瘤分会 副会长
上海市医学会肿瘤分会 副主任委员
上海市东方医院 肿瘤科
IASLC 全球多学科实践标准委员会 委员
中国临床肿瘤学会非小细胞肺癌专委会 委员兼秘书
中国临床肿瘤学会小细胞肺癌专委会 委员
中国临床肿瘤学会转化医学专委会 委员
中国抗癌协会非小细胞肺癌专委会 委员兼秘书
中国抗癌协会青年理事会 青年理事
上海市申康青年岗位能手
上海市青年科技英才“扬帆”计划
上海市“医苑新星”青年医学人才
上海市浦东新区卫健委拔尖人才青年项目
CSCO“35 under 35”“最具潜力青年肿瘤医师”、“科研达人奖”
以一作或通讯作者在Nat Rev Clin Oncol, Lancet Oncol, Signal Transduction Targeted Ther, J Thorac Onocl等期刊发表SCI论文20余篇
担任Ann Oncol, Cell Host & Microb, JNCC, BMC Medicine等期刊审稿人人
[1] Cho BC, et al. Clin Lung Cancer. 2023 Mar;24(2):89-97.
[2] Cho BC, et al. N Engl J Med. 2024 Oct 24;391(16):1486-1498.
[3] Yang JCH, et al. N Engl J Med. 2025 Oct 30;393(17):1681-1693.
[4] Cho BC, et al. Lung Cancer. 2025 Jun:204:108496.
[5] Hayashi H, et al. ESMO ASIA 2025. 920O.
[6] Hidetoshi Hayashi, et al. Lung Cancer. 2026 Feb 4:214:109305.
[7] James Chih-Hsin Yang, et al. 2025 ELCC 4O.
[8] Hidetoshi Hayashi, et al. 2025 ESMO Asia 972O.
[9] Felip E, et al. Ann Oncol. 2024;35(9):805-816
[10] Lim SM, et al. 2024 ASCO abstr LBA8612.
[11] Scott SC, et al. 2025 WCLC. MA.0805.
[12] Natasha BL et,al. 2024 ASCO LBA8505
[13] Nicolas Girard, et al. ELCC 2026. 13P.
[14] Passaro A, et al. Ann Oncol. 2024 Jan;35(1):77-90.
[15] Sanjay Popat, et al. 2024 ESMO, LBA54.
[16] Victor H. Lee et al. ESMO Asia 2023, LBA11.
[17] Nadal E, et al. 2025 ESMO. 1960P.
[18] Zhou C, et al. N Engl J Med. 2023;389(22):2039-2051.
[19] Ke-Jing Tang et al. JCO 42, 8606-8606(2024).
[20] Lim SM, et al. 2025 WCLC. MA.0803.
[21] Park K, et al. J Clin Oncol. 2021 Oct 20;39(30):3391-3402.
CRC Code:EM-202157
Approved Date:2026-4-25
排版编辑:肿瘤资讯-Zika
✅ “本资料仅用于医学、科学交流,可能涉及尚未在中国获批的产品和适应症。强生创新制药不支持、不鼓励任何未被批准的药品/适应症使用。”
✅“本材料中涉及的AE/SS/PQC已按照强生创新制药的要求上报”











 苏公网安备32059002004080号
苏公网安备32059002004080号


