本期精选5篇在2026年3月份发表的结直肠癌领域文献,部分研究邀请到四川大学华西医院的王辛教授进行深入解读。
专家介绍
四川大学华西医院
腹部肿瘤科副主任/兼放疗科副主任
四川省学术技术带头人
中国医师协会肿瘤医师分会结直肠癌学组副组长
中国抗癌协会肿瘤人工智能专委会常务委员
中国医促会放射治疗学分会常务委员
四川省医师协会肿瘤医师分会青年委员会副主任委员
四川省肿瘤学会副理事长
四川省肿瘤学会人工智能与大数据专委会主任委员
四川省国际医学交流促进会精确放射治疗专委会主任委员
中国抗癌协会放疗专委会胃癌/肠癌学组委员
中国抗癌协会大肠癌专业委员会(CACA)放疗学组委员
四川省抗癌协会老年肿瘤治疗专委会常务委员
成都高新区医学会肝胆胰恶性肿瘤多学科专业委员会主任委员
恩考芬尼联合西妥昔单抗 vs 伊立替康/西妥昔单抗或FOLFIRI/西妥昔单抗治疗中国BRAF V600E突变型转移性结直肠癌患者的随机试验:NAUTICAL研究[1]
NAUTICAL CRC(NCT05004350)是一项在既往接受1~2线治疗后进展的BRAF V600E突变转移性结直肠癌(mCRC)中国患者中开展的Ⅱ期、多中心、随机、开放标签研究。该研究作为一项桥接研究,用于确认在BEACON研究中观察到的治疗效果在中国人群中是否具有一致性。研究包含用于评估双靶方案(恩考芬尼/西妥昔单抗)治疗耐受性的安全导入期(SLI),以及一项对比双靶方案与以伊立替康为基础方案疗效的随机期,有望填补这一中国患者人群的治疗空白,并评估其安全性、疗效与生活质量(QoL)结局。SLI阶段(N=10)未发现剂量限制性毒性。在随机阶段(N=97),双靶组(N=65)的无进展生存期(PFS)为4.2个月,显著优于对照组(N=32)的2.5个月[风险比(HR):0.37,P=0.0004](图1A),所有PFS亚组分析的HR均有利于双靶组,与改善PFS相关的显著因素包括男性、原发肿瘤完全切除、基线C反应蛋白(CRP)水平较低以及基线CA19-9较低;总生存期(OS)也更长,为11.6个月对比8.2个月(HR:0.55)(图1B);客观缓解率(ORR)分别为24.6%和6.3%。治疗相关不良事件(TRAE)较为常见,但对照组的严重程度更高。生活质量(QoL)评估结果始终偏向双靶联合组,显示其健康状态改善,病情恶化风险降低。
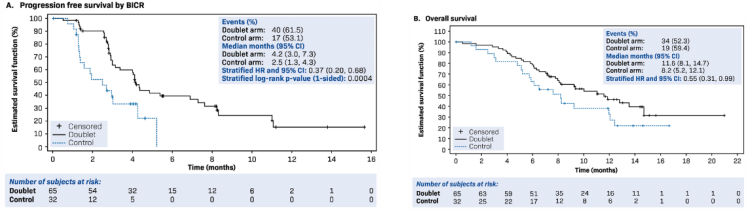
恩考芬尼联合西妥昔单抗联合方案是首个为经治的mCRC中国患者中提供显著临床优势的chemo-free治疗方案,可改善PFS和OS,安全性可控,QoL获益;这些结果支持双靶治疗应被视为经治BRAF V600E突变mCRC中国患者的新治疗选择。
王辛教授:BRAF V600E突变在结直肠癌中占比约10%,该亚型恶性程度高、传统化疗疗效有限,临床亟需有效的靶向治疗方案。全球多中心的BEACON研究确立了西妥昔单抗联合恩考芬尼(双靶方案)在既往经治BRAF V600E突变mCRC的标准地位,但在中国人群中尚缺乏高级别循证依据。因此,NAUTICAL研究应运而生,旨在验证 “去化疗”双靶方案在既往经1线或2线治疗后进展的中国BRAF V600E突变mCRC患者中的有效性与安全性。该研究的核心亮点:
第一,临床获益显著提升,西妥昔单抗联合恩考芬尼较化疗联合西妥昔单抗显著提升临床获益,改善PFS和OS,证实了双靶方案在中国患者中的优越性。
第二,填补中国人群治疗的空白,该研究作为BEACON的中国桥接试验,成功将国际标准治疗方案落地中国,为国内患者提供了首个有效的“chemo-free”靶向选择。
第三, QoL的优化,该研究的核心价值之一在于证明了双靶方案在改善患者健康状态、功能症状方面的优势,显著推迟了健康状况恶化时间。
第四,双靶方案安全性可管理,与对照组相比,与治疗相关的严重不良事件的发生率更低。
研究的局限性:随访时间较短,限制了对OS的长期评估,研究观察到在随机分组后对照组的退出率较高,反映了开放标签设计可能引入偏倚风险,并且两组样本量相对较小。
未来展望:基因检测指导下的精准治疗是肠癌的发展方向,NAUTICAL研究为中国BRAF V600E突变患者确立了高效、低毒的二线靶向标准方案,未来将有望继续前移治疗线数,探索双靶及联合方案在一线治疗的应用价值,或前移至围手术期的可能性,并进一步探索BRAF突变人群在靶向治疗耐药后的免疫联合策略。
TP53突变与接受西妥昔单抗联合帕博利珠单抗治疗的晚期RAS野生型结直肠腺癌患者的疾病控制改善相关[2]
以PD1/PD-L1和CTLA4通路为靶点的免疫检查点抑制剂治疗,在微卫星稳定型(MSS)结直肠腺癌(CRC)患者中的活性有限。在既往研究中,西妥昔单抗联合帕博利珠单抗未能改善晚期RAS野生型(RASwt)CRC患者的结局。在本篇事后二次分析中发现,与携带TP53野生型(p53wt)肿瘤的患者(N=8)相比,接受西妥昔单抗联合帕博利珠单抗治疗的TP53突变型(p53mt)肿瘤患者(N=27)PFS显著延长,分别为5.5个月vs 2.0个月,但OS无差异(图2)。此外,更多p53mt肿瘤患者的靶病灶出现缩小(61% vs 0%,P=0.005)。p53mt肿瘤患者的靶病灶中位缩小比例为10%(范围:缩小60%~增大30%),而p53wt肿瘤患者的靶病灶中位增大比例为30%(范围:增大10%~40%,P=0.001)。基因集富集分析显示,多个代谢和免疫相关基因集呈一致性上调,包括自然杀伤细胞(NK)介导的免疫通路和IL-12通路,而IL6通路呈下调趋势。无论是否进行治疗干预,p53mt组和p53wt组之间均不存在持续一致的转录改变。两组在治疗后均出现增殖、免疫及代谢通路的功能重叠。在基线肿瘤样本中,p53mt肿瘤中PD-L1+肿瘤细胞数量显著更高;而p53wt肿瘤中,LAG3、CTLA4或TIM3任一呈阳性、OX40⁻/AE1_AE3⁻/PD-L1⁻非肿瘤细胞数量显著更高。综上,在RASwt CRC患者中,TP53状态可预测西妥昔单抗联合帕博利珠单抗治疗的PFS改善情况。未来针对MSS、RASwt CRC患者开展免疫肿瘤药物相关研究时,应将TP53纳入整合生物标志物,并评估其作为阳性预测生物标志物的效能(ClinicalTrials.gov NCT02713373)。
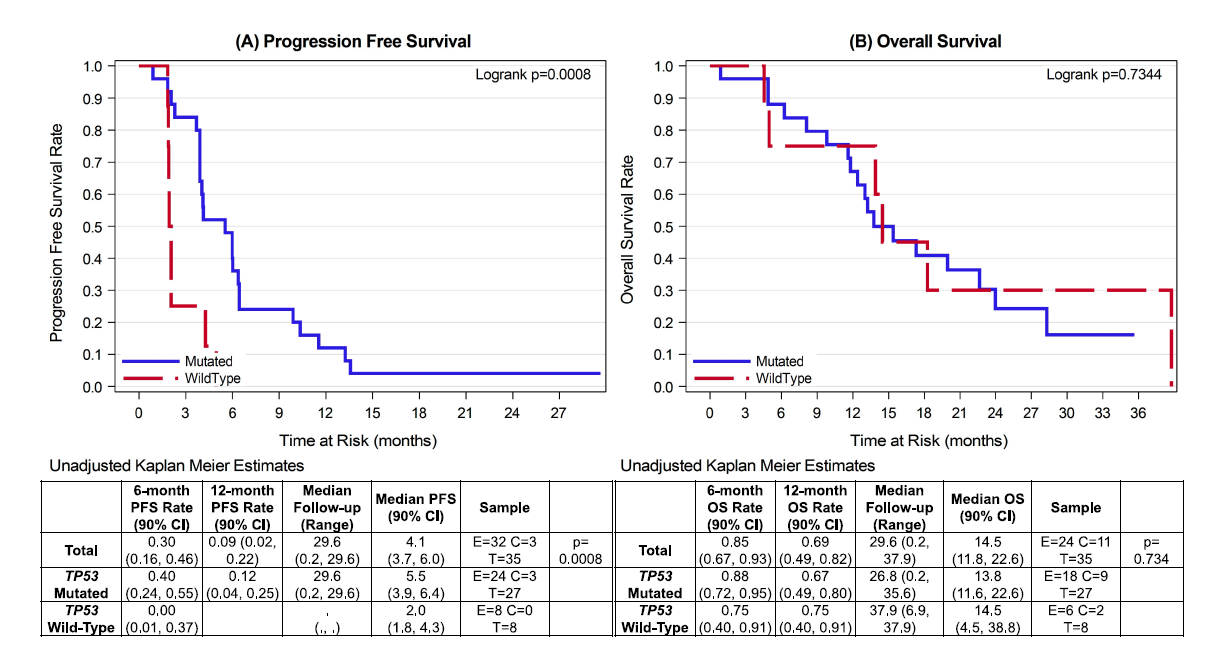
王辛教授:本项研究既往公布的数据显示西妥昔单抗联合帕博利珠单抗在RASwt CRC患者中的整体疗效有限。该事后探索性分析聚焦于探讨TP53突变状态是否能作为预测该联合方案疗效的潜在生物标志物?核心之处在于:
第一,肿瘤TP53状态可能影响基于免疫检查点抑制剂的联合治疗在MSS CRC中的短期疗效。相较于TP53野生型,TP53突变患者具有更佳的疾病控制和更长的PFS(5.5个月 vs 2.0个月)。
第二,免疫微环境重塑,基因富集分析(GSEA)显示,TP53突变肿瘤中NK细胞介导的免疫和IL-12通路上调,且PD-L1阳性肿瘤细胞比例更高。此外,西妥昔单抗可通过NK细胞介导的抗体依赖细胞毒作用(ADCC),增强与免疫联合产生协同作用,促进TP53突变患者更明显的免疫细胞浸润。
第三,TP53作为预测标志物的潜力,提出TP53状态可作为MSS/RAS wt结直肠癌中筛选免疫治疗优势人群的关键指标,具有重要的精准治疗指导价值。
第四,PFS获益未能转化为OS延长,本研究中TP53突变患者虽然显示了PFS获益优势,但未能转化为OS获益,提示后续治疗或耐药机制可能抵消了初期的疗效优势;
局限性:作为一项事后探索性分析,其样本量非常有限(仅18例具有完整测序数据),限制了结果的统计效力。研究纳入右半和左半结直肠癌患者涉及免疫检查点抑制剂和抗EGFR单克隆抗体在肿瘤微环境、血浆细胞因子及抗肿瘤疗效中的可能作用引入了更多的异质性,相关标记物的价值还需要更多验证。
综上,需在更大规模的前瞻性临床试验中验证TP53突变的预测价值,并深入探究TP53突变驱动免疫激活的具体分子机制,此外如何将TP53状态与其他生物标志物(如RAS、TMB等)整合构建更准确的预测模型值得深入探讨。
一线纳武利尤单抗联合FOLFOXIRI/贝伐珠单抗治疗RAS/BRAF突变型mCRC:II 期NIVACOR研究的疗效、安全性与生物标志物发现[3]
NIVACOR研究(NCT04072198)旨在评估纳武利尤单抗联合FOLFOXIRI /贝伐珠单抗作为RAS/BRAF突变mCRC一线治疗的疗效、安全性及生物标志物。
研究共纳入73例未经治的不可切除RAS/BRAF突变mCRC患者,其中86.3%为pMMR/MSS型,13.7%为dMMR/MSI型。结果显示(表1),研究达到主要终点ORR 76.7%,疾病控制率(DCR)97.3%;中位PFS 10.1个月,中位OS未达到。亚组分析中,RAS 突变和 BRAF 突变患者ORR分别为75.8%和81.8%,pMMR/MSS和 dMMR/MSI患者ORR分别为77.8%和70.0%。安全性方面,86.3%的患者出现任意级别的TRAEs,65.8%出现3级以上TRAEs,常见TRAEs包括腹泻、疲劳、中性粒细胞减少等,整体可控。
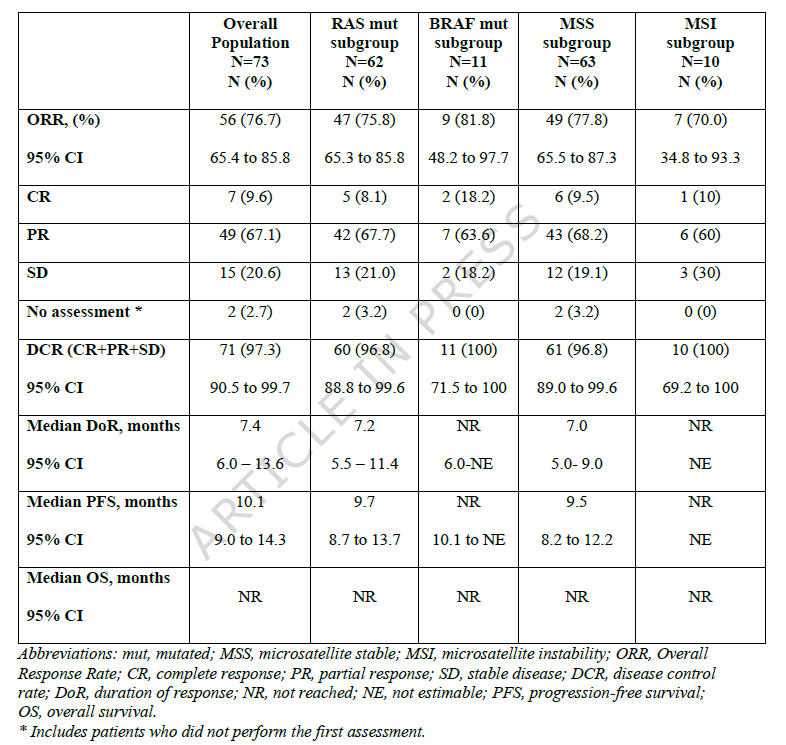
全面基因组分析及RNA测序分析揭示了pMMR/MSS患者中与治疗应答相关的基因组和转录组特征。分析发现,PI3K/AKT、趋化因子信号传导及DNA修复等通路的改变与治疗活性存在相关性。这些研究结果凸显了在经筛选的pMMR/MSS mCRC患者中,免疫检查点抑制剂与细胞毒性化疗联合应用的潜在协同作用。高TMB(>10.4 mutations/Mb)的pMMR/MSS患者比低TMB患者PFS更长(18.1个月 vs 9.35个月,P=0.083);同时识别出与预后相关的耐药(RES)和敏感(SENS)基因特征,RES +患者PFS显著短于RES -患者,SENS +患者PFS显著长于SENS -患者。
综上,在难治性mCRC人群中,将免疫检查点抑制剂治疗与强化化疗、抗血管生成治疗联合应用具有潜力。将分子谱分析整合到临床实践中或可改善患者筛选效果、优化治疗疗效。未来有必要开展纳入更大规模队列、进行可靠生物标志物验证的随机研究,以证实这些研究结果,并确立该联合疗法在mCRC治疗格局中的地位。
瑞康曲妥珠单抗(Trastuzumab Rezetecan)用于HER2阳性的晚期胃癌或胃食管交界处腺癌及CRC的多中心、开放标签Ⅰ期临床试验[4]
HER2 ADC或可为HER2表达型胃癌/胃食管结合部腺癌(GC/GEJ)及CRC提供一种极具前景的治疗策略。研究者开展了一项Ⅰ期临床试验(NCT04513223),旨在评估新型HER2靶向ADC——瑞康曲妥珠单抗在HER2表达晚期GC/GEJ及CRC患者中的应用。
本研究入组100例为经标准治疗后疾病进展、无可用标准治疗或不适用标准治疗的HER2表达型晚期GC/GEJ及CRC患者(其中GC/GEJ患者57例、CRC患者43例)。采用i3+3剂量递增方案,为患者静脉输注3.2、4.8、6.4、8.0 mg/kg剂量的瑞康曲妥珠单抗(每3周1次),随后在选定剂量组开展药代动力学拓展研究,再进行临床拓展研究。主要研究终点为剂量限制性毒性(DLT)及安全性。
8.0 mg/kg剂量组出现1例DLT事件。66例(66.0%)患者出现≥3级TRAEs,仅5例(5.0%)患者因TRAE停药。大多数≥3级TRAE为血液学毒性,属于瑞康曲妥珠单抗的典型毒性,可通过标准支持治疗和剂量调整逆转。鉴于本研究中观察到的血液学毒性特征,未来研究将探索每2周1次的给药方案,以潜在提高耐受性。在HER2阳性GC/GEJ患者(N=40)中,ORR为45.0%,中位PFS为9.0个月(95% CI:7.0~11.3个月),中位OS为16.3个月(95% CI:12.4个月~ NR)。在HER2免疫组化2+且原位杂交阴性的GC/GEJ患者(N=12)中,ORR为25.0%,中位PFS为12.2个月(95% CI:2.8~14.0个月),中位OS尚未成熟。在HER2阳性CRC患者(N=37)中, ORR为40.5%,中位PFS为9.5个月(95% CI:7.3~11.2个月),中位OS为22.7个月(95% CI:17.5个月~NR)。
综上,瑞康曲妥珠单抗在HER2表达型晚期GC/GEJ及CRC患者中表现出可耐受的安全性及初步疗效,有望成为经治HER2阳性以及HER2 IHC 2+伴ISH-晚期GC/GEJ和HER2阳性mCRC患者的一种治疗选择。
王辛教授:HER2在约3%~11%的CRC患者中过表达,尽管NCCN指南推荐曲妥珠单抗/帕妥珠单抗、T-DXd等用于HER2扩增mCRC治疗,目前中国尚无HER2靶向药物获得结直肠癌适应症,亟需在中国进一步探索可及的HER2靶向药物。这项研究聚焦于在既往标准治疗失败或缺乏标准方案的HER2表达GC/GEJ以及CRC患者,评估新型HER2 ADC药物瑞康曲妥珠单抗的安全性和初步疗效。研究亮点在于:
第一,瑞康曲妥珠单抗在GC/GEJ以及CRC患者中展现出较强的抗肿瘤活性,具有重要的临床价值。
第二,对“HER2低表达”人群的潜在覆盖,研究观察到在HER2 IHC 2+/ISH- 的GC/GEJ患者中,ORR仍可达25.0%,中位PFS达12.2个月。提示ADC药物具有较强的“旁观者效应”,有望扩宽HER2靶向治疗的获益群体。
第三,可接受的安全性特征与较低的间质性肺病(ILD)风险:尽管66%的患者出现了3级及以上TRAEs,仅5%的患者因不良反应停药,安全性整体可控。ILD的发生率仅为2.0%(T-DXd在相关研究中ILD发生率约9.6%~26.4%)。
局限性:本研究为单臂、开放标签的I期临床试验,样本量相对有限,且全部受试者均为中国人群,其结论还需要在之后的II/III期研究中验证。OS数据仍需更长时间的随访。
未来展望:需开展大规模、随机对照的研究,以进一步确立其在不同线数/瘤种治疗的价值。探索该类新型ADC药物与免疫检查点抑制剂或靶向药物的联合治疗方案,以期进一步克服后续的耐药。
结直肠癌患者肝转移的检出时间与生存情况[5]
结直肠癌肝转移(CRLM)的临床决策较为复杂。根据欧非肝胆胰协会(European-African Hepato-Pancreato-Biliary Association)共识指南,将CRLM检出时机分为三类:同时性(在原发性结直肠癌诊断前、诊断时或手术期间检出)、早发性异时性(在诊断或术后12个月内检出)、晚发性异时性(在术后12个月以上检出)。理论上认为该时机可能影响生存结局,但上述分类的预后意义仍不明确。本多中心队列研究旨在明确CRLM的检出时机是否与初始可局部治疗或初始不可局部治疗的CRLM患者的OS相关。
研究纳入1250例自2000年至2024年间来自阿姆斯特丹结直肠癌肝转移登记库和Ⅲ期CAIRO5试验的成年患者,采用多变量Cox回归模型分析生存结局,多变量分析纳入了肿瘤数量、大小、突变状态、癌胚抗原水平及治疗策略等因素。纳入标准为初始可局部治疗或初始不可局部治疗的CRLM,且记录有关键临床和人口统计学特征。
患者的中位随访时间(四分位距,IQR)为44(41~48)个月。基线特征中,中位年龄(IQR)为63(56~72)岁,男性823例(65.9%); 817例(65%)为同时性CRLM,208例(17%)为早发性异时性CRLM,225例(18%)为晚发性异时性CRLM。随访期间共有676例(54%)患者死亡。与早发性异时性CRLM相比,同时性CRLM患者的OS更差(HR 0.79;95% CI 0.64~0.97);与晚发性异时性CRLM相比,同时性CRLM患者的OS也更差(HR 0.54;95%CI 0.43~0.68)。不同治疗策略间的OS对比显示:与初始局部治疗(LT)相比,诱导全身治疗与更差的生存期相关(HR 1.38;95% CI 1.14~1.67;P=0.001),而仅接受全身治疗后续未接受LT的患者死亡风险显著更高(HR 6.50;95% CI 5.25~8.04;P<0.001)。此外,在同时性、早发性异时性和晚发性异时性亚组中,OS整体相似,但在接受初始局部治疗的人群中,晚发性异时性CRLM患者的OS显著优于同时性或早发性异时性CRLM患者。
在多变量Cox回归分析中,校正所有潜在混杂因素后,无论是在整体分析中,还是对比同时性CRLM与早发性异时性CRLM(aHR, 0.99;95%CI, 0.75-1.31)、同时性CRLM与晚发性异时性CRLM(aHR, 0.80;95%CI, 0.58-1.08)时,CRLM的检出时机均与OS预后无独立关联。即使校正临床及基于肿瘤大小的变量后,确诊时结直肠癌肝转移的数量、年龄以及是否接受LT仍是与OS相关性最强的因素(图3)。
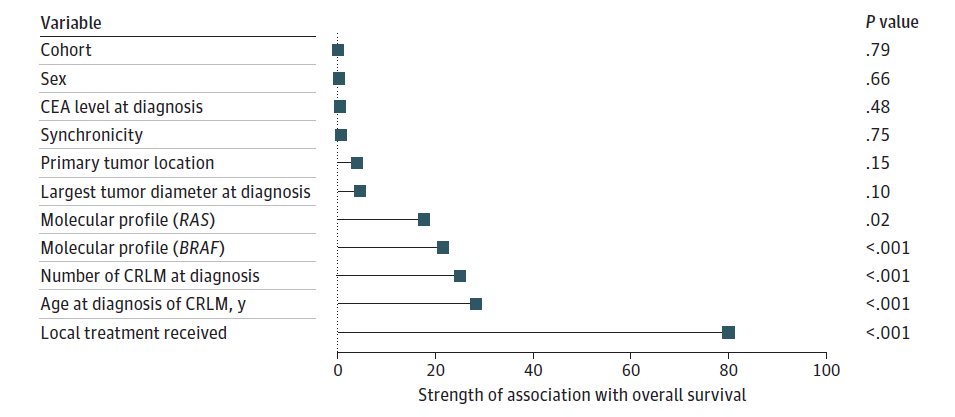
本期看点:
1.NAUTICAL CRC Ⅱ期研究表明,恩考芬尼联合西妥昔单抗带来显著的临床获益,改善PFS和OS,同时安全性可控,且在QoL方面具备重要优势,是经治BRAF V600E突变mCRC中国患者的一种宝贵治疗选择。
2.一项研究探讨了p53mt作为RASwt CRC患者接受西妥昔单抗联合帕博利珠单抗免疫治疗的预测指标的价值。结果显示,与TP53野生型患者相比,p53mt肿瘤患者的PFS延长、肿瘤缩小,但OS无差异。研究还观察到基线及治疗相关的免疫模式,支持TP53状态可作为MSS CRC的潜在预测生物标志物。
3.NIVACOR研究结果显示,在FOLFOXIRI联合贝伐珠单抗的基础上加用纳武利尤单抗,可提高RAS/BRAF突变型mCRC患者一线治疗的ORR,且不受MMR状态影响。
4.一项多中心、开放标签Ⅰ期临床研究表明,瑞康曲妥珠单抗具有可耐受的安全性特征,且在经治的HER2表达阳性GC/GEJ及CRC患者中显示出初步活性。
5.一项回顾性多中心队列研究分析表明,在校正肿瘤特征和治疗策略后,CRLM检出时机与OS无相关性。结果提示,转移同步性可能主要反映了肿瘤的内在生物学特性,而非直接影响生存,强调临床决策应结合转移同步性、肿瘤负荷、突变状态和局部治疗情况综合考量。
1. Wang XC, et al. A Randomized Trial of Encorafenib and Cetuximab Versus Irinotecan/Cetuximab or FOLFIRI/Cetuximab in Chinese Patients With BRAFV600E Mutant Metastatic Colorectal Cancer: The NAUTICAL Study. Cancer Med. 2026 Mar;15(3):e71697. doi: 10.1002/cam4.71697. PMID: 41852303.
2. Fountzilas C, et al. TP53 mutation is associated with improved disease control in patients with advanced RAS wild-type colorectal adenocarcinoma treated with cetuximab and pembrolizumab. Int J Cancer. 2026 Mar 7:10.1002/ijc.70434. doi: 10.1002/ijc.70434. Epub ahead of print. PMID: 41793309; PMCID: PMC13019156.
3. Damato A, et al. First-line Nivolumab plus FOLFOXIRI/Bevacizumab in advanced RAS/BRAF-mutated colorectal cancer: efficacy, safety and biomarker discovery from the phase II NIVACOR trial. Nat Commun. 2026 Mar 25. doi: 10.1038/s41467-026-70620-y. Epub ahead of print. PMID: 41876503.
4. Liu T, et al. Trastuzumab Rezetecan in Human Epidermal Growth Factor Receptor 2-Expressing Advanced Gastric Cancer or Gastroesophageal Junction Adenocarcinoma and Colorectal Cancer: A Multicenter, Open-Label, Phase I Trial. J Clin Oncol. 2026 Mar 4:JCO2500716. doi: 10.1200/JCO-25-00716. Epub ahead of print. PMID: 41779980.
5. Kemna R, et al. Time of Detection of Liver Metastases and Survival in Patients With Colorectal Cancer. JAMA Netw Open. 2026 Mar 2;9(3):e262088. doi: 10.1001/jamanetworkopen.2026.2088. PMID: 41842895.
排版编辑:Zika











 苏公网安备32059002004080号
苏公网安备32059002004080号


