对于携带EGFR、ALK等驱动基因改变的晚期非小细胞肺癌(NSCLC)患者而言,靶向治疗对比化疗改善了患者的预后[1],推动晚期NSCLC进入精准治疗时代。然而,临床实践中一个重要挑战依然存在:即便使用新一代的酪氨酸激酶抑制剂(tyrosine kinase inhibitor, TKI),仍有部分患者在初始治疗后的1-2年内出现疾病进展[1]。究其原因,靶向治疗虽能高效杀伤大部分肿瘤细胞,但往往无法彻底清除体内所有残留病灶。这些残留的、对药物相对不敏感的“顽固分子”,成为了后续获得性耐药和疾病进展的“种子”[2]。
如何清除这些“种子”,延长靶向药的有效时间?局部巩固治疗(local consolidative therapy,LCT)的定位正在发生转变:从过去疾病全面进展后的局部补救措施,转变为一线靶向治疗有效后,主动出击、精准清除残余病灶的巩固策略。通过立体定向放疗、手术或消融等“定点清除”手段,尽可能清除残余病灶、进一步降低肿瘤负荷,延缓耐药发生[3-9]。本文将系统梳理该策略在EGFR和ALK阳性晚期NSCLC中的研究进展,并探讨其临床应用现状及未来发展方向。
EGFR阳性NSCLC:TKI联合局部巩固治疗的证据积累
在EGFR阳性晚期非小细胞肺癌(NSCLC)的治疗中,如何利用LCT延长TKI的疗效持续时间是重要的研究方向。SINDAS研究表明,对于初治的EGFR敏感突变寡转移患者,与单纯使用第一代EGFR-TKI相比,一线采用TKI联合对所有病灶进行立体定向体部放疗(SBRT)能显著延长中位无进展生存期(PFS,20.2 vs. 12.5个月,p<.001)和总生存期(OS,25.5 vs. 17.4个月,p<.001)[3],该研究为“系统治疗基础上主动联合局部治疗”策略提供了较强的前瞻性证据支持。
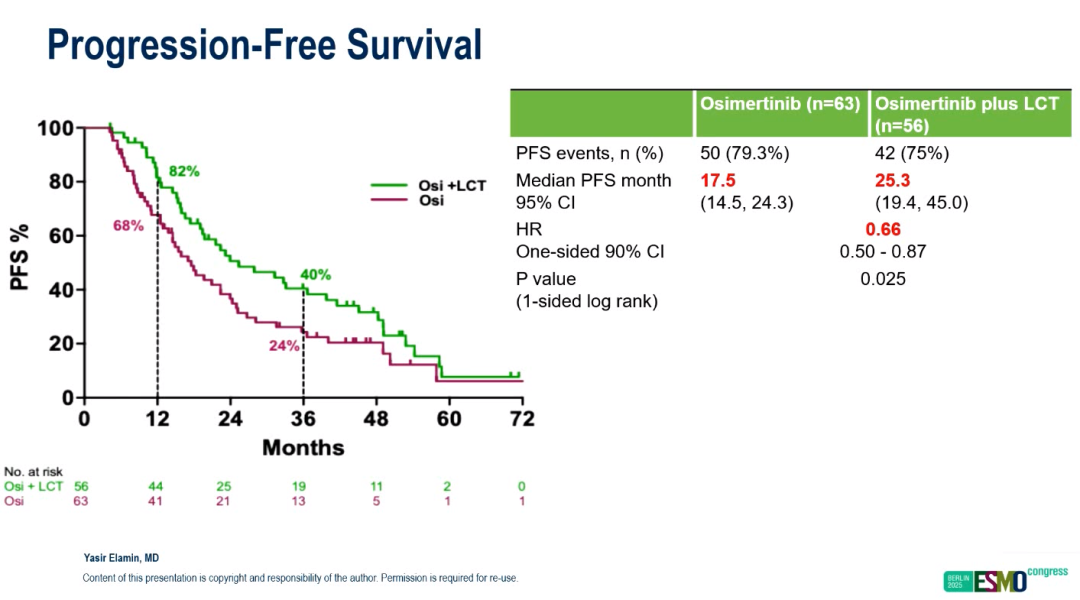
随着奥希替尼成为EGFR突变晚期NSCLC一线标准治疗,研究者开始进一步探索其联合LCT的临床价值。NorthStar研究[4]是一项多中心、随机对照、II期临床试验,旨在探索在奥希替尼系统治疗基础上联合LCT(放疗和/或手术)对EGFR突变转移性或晚期NSCLC患者的影响。结果显示,在奥希替尼治疗的基础上联合LCT具有较好的安全性和可行性,并有望进一步延长PFS(从17.5个月延长至25.3个月;HR=0.66,90%CI 0.50–0.87;p=0.025),为奥希替尼时代推行巩固治疗提供了前瞻性支持。2026 ELCC上公布的该研究的二次分析结果[5]进一步锁定了精准获益人群:奥希替尼诱导治疗后胸内淋巴结转移灶清除的患者从联合治疗中获益显著,中位PFS达到41.5个月(单纯奥希替尼组为19.6个月,HR=0.43,90%CI 0.23–0.78;p=0.008);诱导后无胸腔积液的患者也显示出获益趋势,中位PFS为32.7个月(单纯奥希替尼组为22.3个月,HR=0.63,90%CI 0.39–1.02;p=0.057)。相反,诱导后仍存在持续性胸内淋巴结转移或胸腔积液的患者,未能从联合LCT中取得显著的PFS改善。此外,联合治疗后的失败模式以远处新发转移为主,放疗野内复发率低(仅8%),提示了局部巩固治疗对野内病灶的良好控制。
另一项发表于EClinicalMedicine的II期研究[6]评估了奥希替尼联合巩固性放射治疗在晚期EGFR突变NSCLC患者中的疗效与安全性。结果显示,在接受奥希替尼治疗8至10周并达到最佳疗效时,序贯实施巩固放疗患者的中位PFS可达 32.3个月,(95%CI, 21.9-51.7),优于既往奥希替尼单药治疗的历史数据。此外,该联合方案安全性良好,总体耐受性佳,进一步支持了奥希替尼联合巩固放疗的可行性与临床获益潜力。
ALK阳性NSCLC:BRIGHTSTAR研究提供‘诱导-巩固-维持’策略潜力
在ALK阳性晚期NSCLC领域,BRIGHTSTAR研究[7,8]以前瞻性设计和令人瞩目的生存数据,为“TKI诱导后实施LCT”这一新模式提供了重要依据。
BRIGHTSTAR研究共纳入34例TKI初治或初始治疗不超过8周的ALK阳性晚期NSCLC患者,中位年龄55岁(33~73岁),女性占59%。基线评估时,82%的患者存在多发转移灶(>3个),41%患者伴有脑转移,可见纳入的患者肿瘤负荷较高。患者接受布格替尼诱导8周后对未进展患者实施放疗和/或手术的局部巩固治疗,之后继续布格替尼维持至疾病进展。94%(32/34)的患者在布格替尼诱导治疗后可接受LCT,其中62%的患者接受了完全LCT(即对所有基线残留病灶进行处理)。LCT方式包括放疗(n=27)、手术(n=3)和手术+放疗(n=2)。在5例接受手术的患者术后标本分析显示:2例患者达到完全病理缓解,1例患者原发病灶达到完全病理缓解。

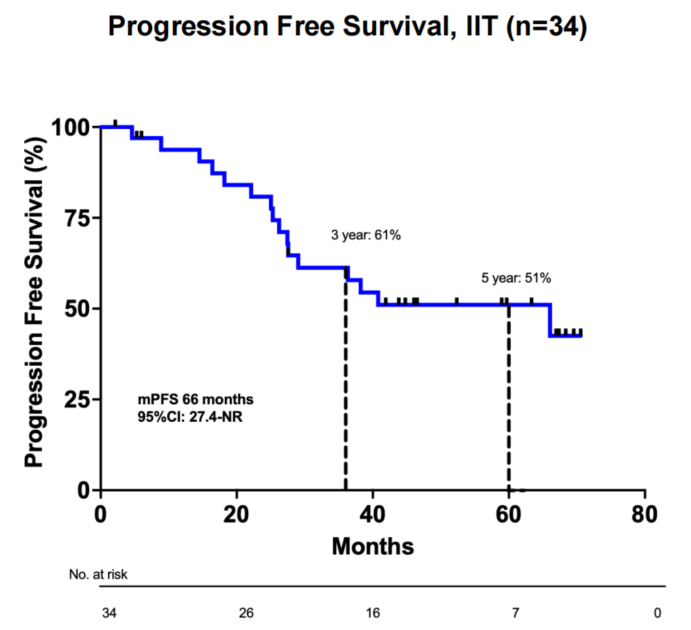
结果显示,中位PFS达66个月,5年PFS率为51%;1年和2年PFS率分别为94%和81%,这一结果提示,在ALK阳性晚期NSCLC中,TKI联合LCT策略可能带来持久的疾病控制获益。研究中82%的患者基线时为多发转移(>3个病灶),结果显示出持久的PFS获益,提示该策略的潜在适用人群可能不局限于传统定义的寡转移患者。
分层分析结果进一步显示,与仅接受部分LCT(仅对部分残留病灶进行处理)的患者相比,接受全面LCT(对所有残留病灶进行处理)的患者的中位PFS显著更长(P<0.001;HR 0.19),提示局部治疗覆盖范围可能是影响疗效的重要因素之一。
探索性分析发现,基线循环肿瘤DNA/RNA(ctDNA/ctRNA)阴性、较小基线肿瘤总体积(≤56.2cm³)的患者中位PFS尚未达到,提示这部分患者可能从联合策略中获得更显著获益,也为未来基于生物标志物筛选优势人群提供了方向。
安全性方面,研究中未观察到与局部治疗相关的5级不良事件,仅报告1例3级相关性肺炎,提示该策略总体可控、具有较好的安全性。
此外,来自卡罗林斯卡大学医院的长期回顾性数据[9]显示,对于ALK阳性寡转移患者,采用包含局部消融治疗在内的多模式治疗策略,可实现中位OS超过10年的长期生存,进一步提示了局部治疗在延长ALK阳性患者长期预后方面具有较大潜力。
临床实践的思考:获益人群、治疗时机与实施方式
尽管TKI联合LCT前景广阔,但在广泛应用于临床前,仍有几个核心问题需要达成共识,这些问题直接关系到治疗的精准化实施和患者获益的最大化
1.谁受益?——获益人群筛选:ctDNA、肿瘤负荷等生物标志物指导
BRIGHTSTAR研究提示,基线ctDNA状态、肿瘤负荷、是否实现全面LCT是关键因素[7,8]。未来的方向是借助肿瘤负荷、ctDNA动态变化、特定基因亚型等生物标志物,构建预测模型,精准筛选出那些单药治疗可能不足、最需要“强化巩固”的患者,实现治疗的“量体裁衣”。
2.何时做?——诱导后最佳窗口期
LCT的介入时机同样至关重要。过早,肿瘤退缩不充分,局部治疗范围大、损伤大;过晚,耐药克隆可能已成气候。目前研究多在靶向治疗8-12周,患者达到初步缓解或最佳疗效时进行LCT评估[4-8]。未来,随着微小残留病灶检测及动态生物标志物监测技术的发展,LCT时机的选择有望更加个体化。
3.如何做?—— 方式:全面 vs 部分LCT选择;放疗 vs 手术 vs 消融
在实施层面,首先需要回答的是局部治疗范围问题,即应尽可能对全部残留病灶进行处理,还是仅对高风险病灶进行重点干预。现有研究提示,全面LCT可能带来更优的PFS获益[7,8],但其适用性仍需结合病灶数量、分布部位、治疗风险及患者整体状态综合判断。
其次,放疗、手术和消融等不同LCT方式各具特点,适用于不同部位和不同特征的病灶。如何在多学科团队(MDT)框架下,根据病灶解剖位置、中枢神经系统受累情况、局部治疗可及性及患者意愿,制定个体化治疗方案,是该策略成功落地的关键。
小结
TKI联合局部巩固治疗已成为驱动基因阳性晚期NSCLC具前景的治疗方向。在EGFR阳性领域,现有证据不断表明,在一线靶向治疗有效的基础上,积极联合局部巩固治疗,是一种能够进一步深化疗效、延长疾病控制时间的治疗策略。在ALK阳性领域,BRIGHTSTAR研究以突破性的66个月中位PFS数据[7,8],引领了“诱导治疗-局部巩固-维持治疗”的新范式。当前证据表明,全面LCT、基线低肿瘤负荷及ctDNA阴性可能是从联合策略中最大化获益的特征[7,8]。未来,该模式的精准化应用有赖于更高等级循证证据的积累、基于多维度生物标志物的获益人群筛选,以及在高水平MDT团队支持下的个体化方案实施。通过解决“谁受益、何时做、如何做”的核心问题,TKI联合LCT策略有望帮助更多患者突破生存瓶颈,迈向更长期的生存。

1. Kastelijn, E. A., de Langen, A. J., & Peters, B. J. M. (2019). Treatment of oncogene-driven non-small cell lung cancer. Current opinion in pulmonary medicine, 25(3), 300–307. https://doi.org/10.1097/MCP.0000000000000572.
2. Russo, M., Chen, M., Mariella, E., et al. Cancer drug-tolerant persister cells: from biological questions to clinical opportunities. Nat Rev Cancer. 2024 Oct;24(10):694-717.
3. WANG X S, BAI Y F, VERMA V, et al. Randomized trial of first-line tyrosine kinase inhibitor with or without radiotherapy for synchronous oligometastatic EGFR-mutated non-small cell lung cancer. J Natl Cancer Inst, 2023, 115(6):742-748.
4. Yasir Y. Elamin, Saumil Gandhi, Mara Antonoff, et al. NorthStar: A phase II randomized study of osimertinib (OSI) with or without local consolidative therapy (LCT) for metastatic EGFR-mutant non-small cell lung cancer (NSCLC). 2025 ESMO. Abstract LBA72.
5. Saumil Ghandi, et al. Predictors of benefit from local consolidative therapy and patterns of failure for metastatic EGFR-mutant NSCLC: A secondary analysis of NorthStar, a phase II randomized clinical trial. 2026 ELCC, LBA3.
6. Sagus Sampath, Sawsan Rashdan, Puneeth Iyengar. et al. Osimertinib plus consolidative radiotherapy for advanced EGFR mutant non–small cell lung cancer: a multicentre, single-arm, phase 2 trial. eClinicalMedicine 2025;87: 103435.
7. Elamin Y, et al. BRIGHTSTAR Local Consolidative Therapy with Brigatinib in Tyrosine Kinase Inhibitor-Naive ALK-Rearranged Metastatic NSCLC, 2023 WCLC. OA22.04.
8. Yasir Y Elamin, et al. BrightStar: LCT With Brigatinib in Tyrosine Kinase Inhibitor-Naïve ALK-Rearranged Metastatic NSCLC. 2025 WCLC, Abstract OA07.01.
9.Caroline Kamali, Luigi De Petris, Rolf Lewensohn, et al. Prolonged Survival in Oligometastatic ALK-Positive NSCLC: Impact of Local Ablative Therapy in a Multimodal Treatment Approach. 2025 WCLC, Abstract EP.12.16.
审批编号:VV-MEDMAT-136230
获批日期:2026年4月
仅供医疗卫生专业人士使用
排版编辑:肿瘤资讯-LWT












 苏公网安备32059002004080号
苏公网安备32059002004080号


