肾功能损伤是多发性骨髓瘤(MM)常见且严重的并发症,约半数患者在诊断时即合并肾功能不全,复发难治阶段发生率更高,常因药物代谢受限、毒性风险增加而被排除在关键临床试验之外,成为临床治疗中的“高危盲区”。近期,American Journal of Hematology杂志发表了一项由雅典国立卡波季斯特里安大学医学院Meletios-Athanasios Dimopoulos教授及其团队完成的系统综述,首次全面汇总双特异性抗体(BsAbs)在合并肾功能不全的复发/难治性MM(RRMM)中的证据。结果证实:BCMA/CD3、GPRC5D/CD3双抗在肾功能不全患者中疗效稳定、安全性可控,无需常规剂量调整,为这一长期被忽视的高危人群提供了高级别循证依据。【肿瘤资讯】现将该研究主要结果整理如下,以飨读者。

关键性临床试验:肾功能并非疗效屏障
MajesTEC-1研究(特立妥单抗):这项奠定特立妥单抗获批地位的关键性试验共纳入165例患者,其中44例(26.7%)合并肾功能不全(eGFR ≤60 mL/min/1.73m²)。需要指出的是,该试验排除了eGFR ≤40 mL/min/1.73m²的重度肾功能不全患者。亚组分析显示,肾功能正常患者的总缓解率(ORR)为63.6%(77/121),肾功能不全患者为61.4%,两组间无统计学差异(OR=0.91,95%CI:0.45-1.85)。进一步独立分析显示,肾功能不全患者的中位缓解持续时间(DOR)为21.6个月,中位无进展生存期(PFS)为9.9个月,中位总生存期(OS)为20个月,充分证明肾功能不全并未对关键生存结局产生不利影响。
MonumenTAL-1研究(塔奎妥单抗):作为塔奎妥单抗获批的关键试验,该研究(排除TCR组后)共纳入297例患者,其中86例(29.0%)合并肾功能不全(eGFR ≤60 mL/min/1.73m²),同样排除了eGFR ≤40 mL/min/1.73m²的患者。在0.4 mg/kg每周给药组(n=143)中,40例(28.0%)合并肾功能不全,ORR分别为77.7%(肾功能正常)和65.0%(肾功能不全),组间无显著差异(OR=0.53,95%CI包含1.0)。在0.8 mg/kg每两周给药组(n=154)中,46例(29.9%)合并肾功能不全,ORR分别为71.3%和65.2%,同样未见显著差异(OR=0.75)。
MajesTEC-3研究(特立妥单抗联合达雷妥尤单抗):这项关键性Ⅲ期试验评估了特立妥单抗联合皮下注射达雷妥尤单抗(Tec-Dara)在既往接受1-3线治疗的RRMM患者中的疗效,共纳入587例患者。与上述两项试验不同,该试验未排除重度肾功能不全患者。亚组分析一致显示各预设亚组(包括不同肾功能水平患者)均获益,肾功能不全患者的疾病进展或死亡事件发生率为25%(HR:0.31),肾功能正常患者为12.8%(HR:0.14),差异无统计学意义,提示联合方案在肾功能不全患者中的相对获益得以保持。
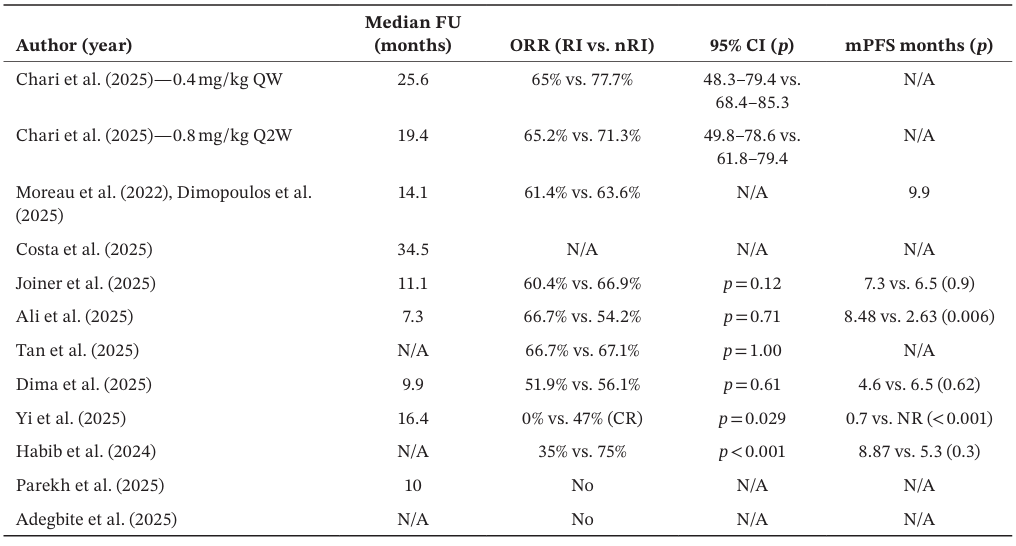
表1. 肾功能不全患者与肾功能正常患者的中位随访(FU)、ORR和中位PFS的研究水平分析
真实世界证据:从临床实践验证疗效一致性
塔奎妥单抗真实世界数据:Joiner等开展的多中心协作登记研究纳入417例患者,其中91例肾功能不全(肌酐清除率<40 mL/min/1.73m²,含20例需血液透析患者)。该研究证实,尽管肾功能不全患者属于高危亚群,但其OS和PFS结局与整体队列相比未受肾功能状态的显著影响——中位PFS分别为7.3个月和6.5个月(P=0.9),BCMA初治患者12个月OS率分别为71%和73%(P=0.53)。Ali等的单中心研究(36例患者,完全嵌套于Joiner等登记研究中)报告了相似的ORR(66.7% vs. 54.2%,P=0.71),并意外观察到肾功能不全患者的中位PFS显著优于肾功能正常患者(8.48 vs. 2.63个月,P=0.006),尽管这一发现未被更大规模的Joiner等研究证实。
特立妥单抗美国真实世界数据:多项回顾性分析聚焦肾功能亚组,共评估了1114例接受商业标签下特立妥单抗治疗的RRMM患者记录。其中,Dima等(USMIRC数据库)报告的最成熟数据显示,81例(21.1%)肾功能不全患者(eGFR ≤40 mL/min/1.73m²)的ORR为51.9%,肾功能正常患者为56.1%,无显著差异(OR=0.84)。值得关注的是,重度肾功能不全(eGFR ≤30,n=45)患者的ORR仍达60.0%,透析患者(n=18)为55.5%。中位PFS(4.6 vs. 6.5个月,P=0.62)和中位OS(未达 vs. 16.1个月)均未显示统计学差异。
在肾功能动态变化方面,Dima等的研究提供了重要洞见:18例治疗开始时需透析的患者中,14例在治疗后仍无进展生存并继续透析;63例eGFR ≤40但未透析的患者中,55.6%维持基线肾功能范围,17.5%改善至eGFR >40,仅3.2%恶化至eGFR <20。这一发现提示特立妥单抗治疗不仅未加重肾功能不全,部分患者还出现了肾功能改善,很可能反映了疾病控制后骨髓瘤相关肾损伤的缓解。
Tan等(IMWG数据库)和Parekh等(TriNetX数据库)采用更严格的肾功能损害定义(eGFR ≤30 mL/min/1.73m²),同样证实了肾功能不全与肾功能正常患者间相似的ORR和OS。Adegbite等(MSKCC数据库)评估了36例eGFR ≤60的患者和48例肾功能正常患者接受特立妥单抗或埃纳妥单抗治疗,也未报告PFS或OS的显著差异。
韩国真实世界数据(Yi等):这一较小队列(15例肾功能不全,27例肾功能正常)在中位随访16.4个月时,却显示出与美国研究不同的结果——肾功能正常组的CR率显著更高(47% vs. 0%,P=0.029),中位PFS显著延长(未达 vs. 0.7个月,P<0.001)。研究者指出,由于样本量较小且为独立患者队列,该研究结果的可靠性受限,可能反映了人群特征或治疗模式的差异,而非药物本身在肾功能不全患者中的疗效不足。
安全性特征:整体一致,血小板减少需警惕
安全性分析显示,特立妥单抗和塔奎妥单抗的安全性特征在肾功能不全与肾功能正常患者中总体保持一致,毒性可控。
表2.治疗相关毒性的研究水平分析,包括CRS、ICANS和感染以及重度事件(≥3级),以及相应的P值
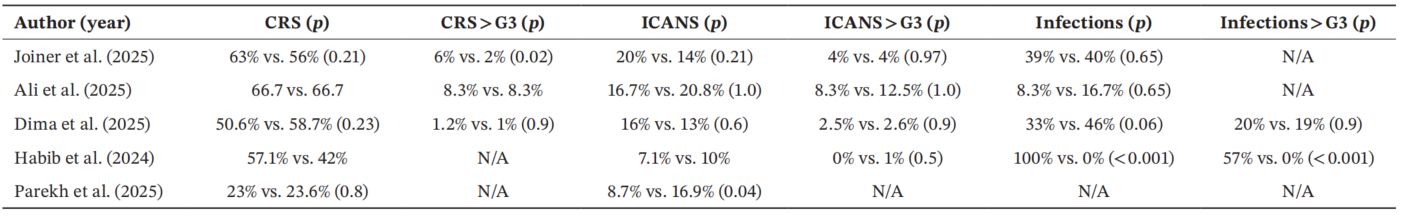
CRS与ICANS:各研究中CRS和ICANS的发生率在两组间基本相当。唯一的例外是Parekh等报告的特立妥单抗数据中,非肾功能不全患者的ICANS发生率略高(16.9% vs. 8.7%,P=0.04),但这一发现的临床意义需谨慎解读。整体而言,肾功能不全并未增加这两种特征性毒性的发生风险。
感染:在最大规模、最可靠的Dima等队列中,感染谱显示稳定性,两组间严重感染率相似。早期较小样本的研究(如Habib等)曾报告肾功能不全患者100%感染率而肾功能正常患者0%感染的极端统计异常,这与Dima等的成熟数据集严重矛盾,应归因于方法学噪声和小样本偏倚,而非真实的药物安全性信号。
血液学毒性:贫血在肾功能不全人群中更为常见,在Parekh等队列中达到统计学显著性(26.4% vs. 16.2%,P=0.033),在Dima等队列中呈相似趋势(59% vs. 44%,P=0.053)。这一发现符合预期,因为肾功能不全患者本身即具有高发的贫血基础。中性粒细胞减少的发生率不受肾功能影响,各研究中总体和重度(>3级)率在两组间均无统计学差异。
血小板减少:血液学毒性中最具统计学意义和临床意义的信号是血小板减少。尽管Parekh等和Habib等队列未报告差异,但Dima等数据集识别出肾功能不全患者血小板减少的总体发生率(49% vs. 6%,P=0.002)和重度发生率(17% vs. 6%,P=0.002)均显著升高。这一发现提示,虽然特立妥单抗总体上未加重骨髓抑制,但在肾功能不全患者中血小板减少的发生确实更为频繁,临床实践中需加强血小板监测和管理。
机制解读
双特异性抗体在肾功能不全患者中保持疗效和整体安全性的机制,与其独特的药代动力学特征密切相关。与单克隆抗体类似,双特异性抗体主要通过吞噬细胞或靶细胞的细胞内分解代谢进行清除,而非经肾脏排泄。这种不依赖肾脏的清除途径,使其在肾功能不全时的药代动力学保持相对稳定,无需因肾功能下降而调整剂量——这与特立妥单抗和塔奎妥单抗的药品说明书推荐一致。
对于终末期肾病和透析依赖患者,尽管本综述纳入的临床试验数据有限,但多项病例报告和小型病例系列显示,埃纳妥单抗和特立妥单抗在透析患者中均可产生持久的血液学缓解和可控的安全性,甚至有病例报告描述了特立妥单抗治疗后达到透析独立和MRD阴性CR的年轻患者。这些证据虽然级别较低,但与系统综述的主要发现方向一致,支持在严密监测下将双特异性抗体用于这一最高危人群。
总结
这项系统综述与汇总分析提供了迄今为止最全面的证据,证实双特异性抗体在合并肾功能不全的RRMM患者中保持了实质性的疗效和可接受的安全性。ORR、PFS和OS在肾功能不全与肾功能正常患者间具有可比性,安全性特征整体一致,仅血小板减少的发生率显著升高。
这些发现与双特异性抗体经网状内皮系统清除、不依赖肾脏排泄的药代动力学机制高度一致,从科学机制上解释了临床观察到的疗效和安全性特征。对于长期被排除在临床试验之外的肾功能损害患者群体,这一证据无疑为临床决策提供了重要支撑。
Ntanasis-Stathopoulos I, Manganas S, Filippatos C, et al. The Role of Bispecific Antibodies in Relapsed/Refractory Multiple Myeloma With Renal Impairment: A Systematic Review. Am J Hematol. Published online April 2, 2026. doi:10.1002/ajh.70312
排版编辑:Mathilda











 苏公网安备32059002004080号
苏公网安备32059002004080号


