胰腺癌是预后最差的消化道恶性肿瘤,免疫单药及多数联合策略在未经选择的患者中收效甚微。2026年4月,一项针对转移性胰腺癌(mPDAC)的Ib期临床试验(ARC-8)的结果,在国际顶级期刊Nature Medicine(IF:50)重磅发表。该研究由美国多家肿瘤中心联合开展,首次在初治mPDAC患者中证实,CD73抑制剂Quemlliclustat联合吉西他滨/白蛋白紫杉醇(G/nP)化疗可显著延长总生存期(OS)(中位OS 15.7个月vs历史数据对照9.8个月,HR 0.634),并通过深入的转化分析发现NR4A家族基因可作为预测疗效的组织生物标志物,为后续III期试验及精准免疫治疗提供了关键依据。

为何在转移性胰腺癌中靶向CD73腺苷通路?
转移性胰腺癌(mPDAC)预后极差,5年生存率仅13%,标准吉西他滨联合白蛋白紫杉醇(G/nP)化疗的中位总生存期(OS)不足1年,且肿瘤微环境高度免疫抑制,单纯免疫检查点阻断疗效甚微。
胞外核苷酶CD73是催化三磷酸腺苷(ATP)转化为免疫抑制性腺苷的关键酶,化疗会促使肿瘤释放三磷酸腺苷,进一步加重腺苷介导的免疫抑制。Quemliclustat是一种针对CD73的强效、高选择性小分子抑制剂,可阻断腺苷生成、逆转肿瘤免疫抑制,但其联合化疗±PD-1抑制剂赛帕利单抗(Zimberelimab)用于mPDAC的安全性与疗效尚未明确。基于此,ARC-8研究旨在评估Quemlliclustat + G/nP联合或不联合赛帕利单抗的情况下,用于一线mPDAC的安全性和疗效。
研究设计:剂量探索+随机扩展,双方案并行验证
ARC-8(NCT04104672)是一项多中心、开放标签的Ib期试验,在美国 18 个临床中心开展,共纳入138例经病理证实、未接受过转移性疾病治疗的mPDAC患者(年龄≥18岁,ECOG PS 0~1)。试验分为两大阶段:
1. 剂量递增阶段(n=22):评估Quemlliclustat(25 mg、50 mg、75 mg、100 mg或125 mg,静脉注射)联合G/nP+赛帕利单抗的安全性与推荐Ⅱ期剂量(RP2D)。
2. 剂量扩展阶段(n=116):先进行单臂非随机队列(Quemlliclustat 100mg+G/nP+赛帕利单抗),随后按2:1随机分配至Quemlliclustat+G/nP组(Q+G/nP组,n=29)或Quemlliclustat+G/nP+赛帕利单抗组(Q+G/nP+Z组,n=61)。
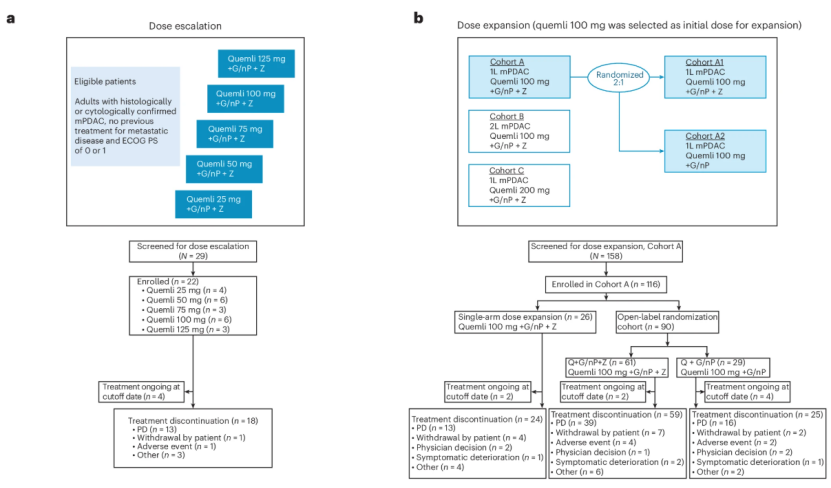
ARC-8研究设计、患者流程
主要终点为安全性和耐受性,次要终点包括客观缓解率(ORR)、疾病控制率(DCR)、无进展生存期(PFS)和总生存期(OS),同时开展 NR4A 家族基因等生物标志物探索分析。
核心结果:安全可控,生存获益显著,生物标志物精准分层
1. 安全性:方案耐受性良好,毒性以化疗为主
所有治疗组的不良事件谱与G/nP单药一致,≥3级治疗相关不良事件(TRAE)主要源于化疗,而非 Quemliclustat或赛帕利单抗。
· 剂量递增阶段仅1例剂量限制性毒性(2级自身免疫性肝炎),经类固醇治疗后缓解。
· 剂量扩展阶段,两组免疫介导的TRAE发生率约10%,无Quemliclustat或赛帕利单抗相关死亡事件。
基于安全性、耐受性、药代动力学和药效学,在拓展研究中推荐Quemliclustat的RP2D为100 mg,且未确定最大耐受剂量。
2. 疗效:联合化疗生存获益优于历史对照
在随机扩展的两组中,Q+G/nP组经确认的ORR为38%(95%CI 21~58),DCR为86%(95% CI 68~96),中位PFS为8.8个月(95%CI 6.4~12.6),中位OS为19.4个月(95%CI 12.1~23.0);Q+G/nP+Z组经确认的ORR为25%(95%CI 15~37),DCR为72%(95% CI 59~83),中位PFS为4.9个月(95%CI 3.7~6.0),中位OS为14.6个月(95%CI 10.6~21.5)。两组差异可能与赛帕利单抗的免疫相关毒性或患者基线肝转移比例不均衡有关(Q+G/nP+Z组肝转移比例更高)。
事后分析将剂量递增与扩展阶段所有接受Quemlliclustat 100mg及G/nP治疗的患者汇总为Quemli100队列(n=122),中位OS为15.7个月(95%CI 12.4~20.9),中位PFS为6.3个月(95%CI 5.4~7.7)。与倾向性评分匹配后的合成对照臂(SCA,中位OS 9.8个月)相比,Quemli100队列的中位OS显著延长(HR 0.634,95%CI 0.471~0.854,P=0.003)。无肝转移患者(占35%)的中位OS达21.5个月,显著优于有肝转移患者(12.1个月),这提示肝转移状态是重要的预后因素。
3. 生物标志物:NR4A家族是疗效预测关键因子
该研究首次证实NR4A家族基因(NR4A1、NR4A2、NR4A3)是腺苷通路的下游靶点,可精准预测 Quemliclustat治疗获益。
(1)肿瘤NR4A高表达患者的中位PFS为11.0个月、中位OS为26.1个月,显著优于NR4A低表达患者(4.9个月和12.4个月),HR分别为0.42(95%CI 0.23~0.76,P=0.0034)和0.41(95%CI 0.20~0.86,P=0.015)。
(2)治疗后NR4A表达最大幅度下调的患者,T细胞活化显著增强,中位OS显著延长(HR 0.24,95%CI 0.08~0.67,P=0.0035)。空间分析显示,NR4A高表达区域存在免疫抑制梯度,活化T细胞远离肿瘤细胞。
研究意义与临床价值
·积极的生存信号:Quemlliclustat联合G/nP化疗在初治mPDAC患者中取得中位OS 15.7个月,较历史数据中G/nP单药(9.8个月)延长近6个月(HR 0.634)。该结果虽为Ib期非随机数据,但经倾向性评分匹配后差异显著,为正在进行的III期PRISM-1试验(NCT06608927)奠定基础。
·生物标志物:NR4A家族基因表达兼具基线筛选与动态监测价值,高表达者中位OS达26.1个月,而治疗期间NR4A下调幅度与疗效正相关。该发现将腺苷生物学与临床终点直接关联,为CD73抑制剂的精准应用提供了可行工具。
·联合抗PD-1的启示:该研究中添加赛帕利单抗未带来额外生存获益,可能与两组基线肝转移负荷不均衡及样本量有关。CD73抑制剂解除腺苷抑制后是否需要联合PD-1阻断,尚需进一步研究验证。
·空间免疫抑制梯度概念的临床转化价值:该研究首次在患者肿瘤组织中直观展示了腺苷调控的NR4A高表达区域与效应T细胞之间的空间排斥关系,为靶向腺苷通路的治疗提供了直接的机制证据。
总结
ARC-8研究验证了CD73抑制剂Quemlliclustat联合化疗在mPDAC中的安全性、良好的生存获益及以NR4A为核心的预测性生物标志物谱。目前,评估Quemlliclustat联合化疗与安慰剂联合化疗的III期PRISM-1研究正在开展,后续结果值得关注。
Wainberg ZA, Manji GA, Bahary N, et al. Quemlliclustat and chemotherapy with or without zimberelimab in metastatic pancreatic adenocarcinoma: a randomized phase 1b trial. Nat Med. 2026. DOI: 10.1038/s41591-026-04283-z.
排版编辑:肿瘤资讯-ZJN











 苏公网安备32059002004080号
苏公网安备32059002004080号


