中国台湾肿瘤消融学会 (TATA) 肝细胞癌消融治疗共识


摘要
肝细胞癌 (HCC) 发病率居全球第六位,死亡率居第三位,凸显了其对公共卫生的重大负担。消融治疗是早期 HCC 的根治性治疗方法之一。随着全身治疗的最新进展,将消融与其他治疗方式相结合已显示出改善疗效的效果,并将其适用范围扩展至部分中晚期患者。与此同时,消融技术也取得了显著进步。新一代微波设备、多针系统和高功率发生器的引入,使得能够产生更大且更可预测的消融区域。非热消融方式扩展了位于胆管或大血管附近肿瘤的治疗选择,这些部位的热损伤风险较高。此外,自动融合成像技术提高了对不明显或小病灶的检测和靶向能力,从而增强了精准度和安全性。这些进展凸显了更新治疗指南以反映当代临床实践的必要性。本文所述指南由中国台湾肿瘤消融学会发起,由肝病学、外科学、放射学和肿瘤学专家协作制定。制定过程遵循循证医学原则,并采用德尔菲法达成共识。第一阶段通过系统文献综述和专家调查形成初步建议,并通过在线讨论进行完善。第二阶段进行结构化投票和统计分析,以评估一致性和共识强度。最终指南提供了详细的循证建议及解释说明,纳入了新兴技术,反映了最新临床进展,并展望了未来趋势,包括人工智能和自动化在 HCC 消融治疗中的整合。
引言
肝细胞癌 (HCC) 是全球最常见的恶性肿瘤之一,仍然是主要的全球健康挑战,特别是在慢性乙型和丙型肝炎感染高发的地区。在中国台湾, HCC 发病率较高,主要原因是慢性乙型肝炎病毒、丙型肝炎病毒 (HCV) 感染,以及代谢功能障碍相关脂肪性肝病日益增加的患病率。尽管监测项目和治疗策略有所改善,但 HCC 的预后仍然较差,主要是由于其侵袭性强且常在晚期才被诊断。
近年来, HCC 的治疗格局发生了实质性演变。局部区域治疗 (LRTs) 对早期 HCC 患者至关重要。其中,消融治疗已成为关键的治疗选择,为不适合手术切除或肝移植 (LT) 的早期 HCC 患者提供了一种微创的根治性治疗方案,并成为多学科 HCC 管理的基石。消融治疗最常采用射频消融 (RFA) 、微波消融 (MWA) 和冷冻消融,通过不同机制诱导肿瘤坏死。多项研究和专家指南表明,对于肿瘤≤ 3cm 的患者, RFA 和 MWA 可达到与手术切除相当的生存结局。
然而,消融治疗的成功受肿瘤大小和位置的影响;对于 >3cm 的肿瘤或靠近大血管的肿瘤,由于热沉效应,局部复发率较高。在中期 HCC 中,单独消融往往不足,常需要与经动脉或全身治疗相结合。缺乏标准化治疗方案和消融后监测进一步凸显了对综合指南的需求,以优化患者选择、技术操作和随访管理。
本共识指南由中国台湾肿瘤消融学会 (TATA) 制定,整合当前证据和专家意见,为 HCC 消融治疗提供循证建议。指南涵盖了患者选择、影像学、治疗方式、疗效、并发症、随访实践和消融前景等方面的进展。通过解决现有空白,本指南旨在改善治疗结局,促进 HCC 管理的标准化、循证化方法。
方法
TATA 指南委员会通过结构化的德尔菲共识程序制定建议,基于对关键文献的结构化专家审查,包括随机对照研究 (RCT) 、系统综述、荟萃分析、观察性研究、病例系列以及现有 HCC 管理相关指南。文献综述旨在支持专家共识过程,而非构成正式的系统综述。
采用德尔菲法,由 16 名专家组成专家小组——包括 11 名肝病学家、 3 名放射学家、 1 名肿瘤学家和 1 名外科医生——代表 HCC 管理涉及的多个学科,制定共识声明。该过程包括开放式问卷、在线讨论、结构化投票、声明定稿和面对面审查。共进行了三轮德尔菲程序。
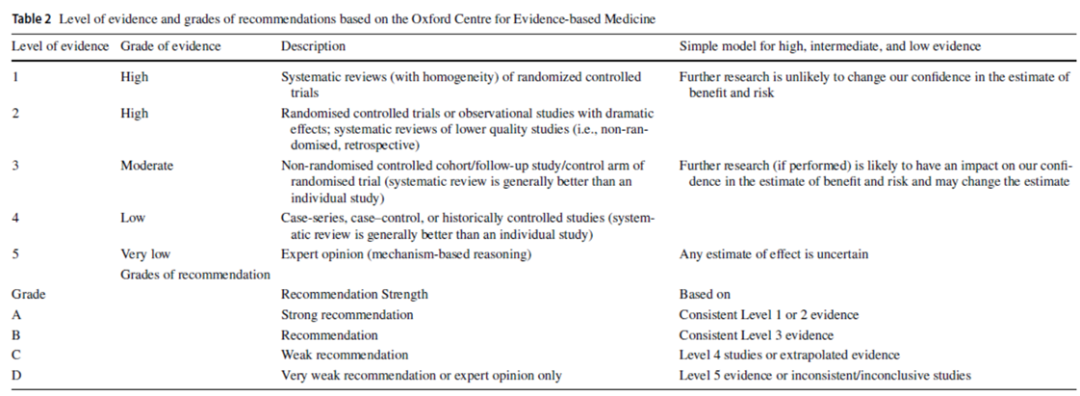
德尔菲法首先涉及确定主题和选择专家小组。第一轮发放 18 份问卷,回收 15 份。这些主要是开放式问卷,允许专家提出 3-5 条声明。整理回复后,形成 28 条初步声明。第一轮未回复者被排除在后续分析之外。第二轮发放 16 份问卷,全部回收 (100% 回复率 ) 。专家审查内容、证据等级和推荐强度,提供修订建议和重要性评级。结果汇总后反馈给专家组。第三轮再次发放 16 份问卷,回收 16 份,完成最终投票。采用五级同意量表: A , " 强烈同意 " ; B , " 同意 " ; C , " 中立 " ; D , " 不同意 " ; E , " 强烈不同意 " 。建议获得≥ 75% 专家同意 (" 强烈同意 " 或 " 同意 ") 方可通过。两条获得≥ 60% 同意的观点性声明也被纳入。每条建议均考虑证据的强度和一致性以及专家组的临床经验。采用牛津循证医学中心 (OCEBM) 框架对证据和推荐强度进行分级。
除 RFA 和 MWA 等主要消融方式外,专家小组还包括具有其他方式直接临床经验的临床医生:两名成员 (1 名放射学家和 1 名外科医生 ) 曾实施不可逆电穿孔 (IRE) ,三名成员 (2 名放射学家和 1 名外科医生 ) 具有冷冻消融经验,两名成员曾实施组织损毁术 (1 名放射学家和 1 名外科医生 ) 。对于高强度聚焦超声 (HIFU) ,讨论主要基于文献回顾而非直接临床经验。
消融适应证
声明 1 :推荐将消融作为极早期 HCC 患者或早期 HCC 非手术候选患者的一线根治性治疗。
证据等级: 1 。推荐强度: A 。共识度: 100% 。
经皮消融技术包括热消融和非热消融方式—— RFA 、 MWA 、冷冻消融和 IRE ——以及化学消融,如经皮乙醇注射。对于极早期 HCC 患者,通常定义为单发肿瘤≤ 2cm ,随机对照研究显示消融可提供与手术切除相当的生存结局,且更具成本效益。然而,对于 >3cm 的肿瘤,消融显示出较低的客观缓解率、较高的复发率和较差的总生存期 (OS) 。在这种情况下,手术切除通常可实现更优的局部控制和 OS 。尽管存在这些局限性,消融具有多项优势,包括与手术相比并发症发生率更低、保留肝功能、住院时间更短、恢复日常活动更快。它特别适用于因肿瘤位于中央需行大肝切除、肝储备功能受损、合并严重疾病或患者偏好等原因不适合手术的患者。鉴于其微创性、疗效和保留肝功能的能力,消融仍然是极早期 HCC 的重要治疗选择,也是早期 HCC 不适合切除患者的重要替代方案。
声明 2 :消融治疗联合经动脉化疗栓塞 (TACE) 可改善部分中期 HCC 患者的结局。
证据等级: 2 。推荐强度: B 。共识度: 100% 。
单独 TACE 治疗中期 HCC 患者的长期结局仍不理想。将 TACE 与 RFA 或 MWA 等消融治疗相结合,可通过减少动脉血流和最小化热沉效应来增强疗效。对于米兰标准内的患者, TACE 联合 RFA 已达到与手术切除相当的生存结局。一项纳入 189 例 HCC ≤ 7cm 患者的随机对照研究显示,与单独 RFA 相比, TACE 联合 RFA 显著改善了总生存期 (HR=0.525) 和无复发生存期 (RFS)(HR=0.575) 。长期随访证实对 >3cm 肿瘤有特别获益, OS 和无进展生存期 (PFS) 显著改善。一项纳入 10 项研究 (1799 例患者 ) 的荟萃分析进一步报告,与单独 TACE 相比, TACE 联合 RFA 或 MWA 改善了 OS(HR=0.50) 、 PFS(HR=0.47) 和局部肿瘤控制 (OR=0.36) ,且未增加主要并发症。
声明 3 :消融治疗是初始根治性治疗后复发 HCC 患者的可行选择。
证据等级: 2 。推荐强度: B 。共识度: 100% 。
HCC 在初始根治性治疗 ( 包括手术切除或消融 ) 后的复发率仍然很高, 5 年可达 70% 。复发 HCC 的管理应个体化,考虑复发部位和范围以及残余肝体积和功能。对于复发肿瘤负荷有限的患者,重复肝切除术或消融是主要治疗选择。重复 RFA 在肝硬化患者中显示出疗效,完全缓解 (CR) 率高达 96.5% 。其可重复性使 RFA 在控制肝内复发方面特别有价值。一项荟萃分析显示,重复肝切除术和重复消融之间的 OS 和无病生存期相当,但接受消融治疗的患者第二次复发的可能性更高。重要的是,重复肝切除术后的总体和主要并发症发生率显著更高,表明 RFA 是适合选择的复发 HCC 患者的安全有效替代方案。
声明 4 :消融是减少等待肝移植 (LT) 的 HCC 患者肿瘤进展和退出率的桥接治疗之一。
证据等级: 2 。推荐强度: B 。共识度: 100% 。
LT 对于终末期肝病合并 HCC 患者仍是根治性选择,但成功取决于基于肿瘤特征和肝功能的仔细候选者选择。等待名单上的患者面临肿瘤进展风险,可能导致除名和移植资格降低。新辅助局部区域治疗——包括 TACE 、经动脉放射栓塞、消融和外照射放疗——常作为桥接策略用于稳定疾病。虽然没有普遍偏好的特定方式,选择取决于患者和肿瘤相关因素。证据表明,消融可有效减少肿瘤负荷并帮助维持 LT 资格。尽管随机对照数据仍然有限,指南推荐在可行时采用消融治疗,主要目标是预防疾病进展和降低退出风险。通过控制肿瘤生长,消融提高了成功 LT 的可能性并改善总体结局。
声明 5 :消融是免疫治疗后达到降期的部分患者的根治性治疗。
证据等级: 3 。推荐强度: C 。共识度: 88% 。
尽管大规模证据有限,新兴数据支持消融作为免疫治疗诱导降期后部分 HCC 患者的根治性选择。在一项多中心研究中, Kudo 等报告 35% 接受阿替利珠单抗联合贝伐珠单抗治疗的中期 HCC 患者通过根治性转化达到 CR ,其中 13/35 例 (37%) 应用了消融。 Heckman 等评估了 123 例等待 LT 的 HCC 患者,发现 24% 通过局部区域治疗 (TACE 、 RFA 或切除 ) 成功降期,生存结局与未降期患者相似。 Shi 等证明,接受 TACE 降期后 RFA 治疗的患者长期结局与初始符合米兰标准并接受 RFA 作为一线治疗的患者相当。尽管证据主要为回顾性,这些数据支持消融作为肿瘤降期 ( 包括免疫治疗后 ) 的有前景的根治性方法。
声明 6 :对于免疫治疗持久应答后出现寡进展的患者,可考虑消融治疗。
证据等级: 3 。推荐强度: C 。共识度: 94% 。
Liu 等的一项多中心研究评估了 91 例免疫检查点抑制剂 (ICI) 治疗后达到持久应答 (PR 或 SD ≥ 8 个月 ) 的晚期 HCC 患者。其中 59.3% 随后出现进展,最常见为寡进展 ( ≤ 3 个病灶, 66.7%) 。在这些患者中,局部区域治疗 ( 包括消融 ) 与显著改善的 OS 相关 ( 中位 OS : 48.4 vs. 20.5 个月; P<0.001) 。多进展患者未从局部区域治疗中获益,凸显其在寡进展环境中的特定作用。其他恶性肿瘤也有类似观察:在转移性黑色素瘤中, ICI 治疗后寡进展的局部区域治疗产生 32 个月的中位寡进展后 PFS , 75% 的患者在长期随访中存活。在非小细胞肺癌中,全身治疗后寡进展的手术切除产生了有前景的 PFS 和 OS 结局。尽管证据主要为回顾性,这些发现支持消融作为免疫治疗后寡进展 HCC 持续控制的潜在策略,有待前瞻性研究验证。
患者相关因素
声明 7 :肝功能评估是 HCC 患者消融治疗安全性和结局的关键决定因素。
证据等级: 1 。推荐强度: A 。共识度: 100% 。
在一项纳入 499 例接受 RFA 患者的前瞻性研究中, Ho 等评估了多项肝功能检测的预后价值,发现白蛋白 - 胆红素 (ALBI) 分级是最有效的无创预测指标。 Jo 等的一项纳入 188 例单发 HCC<3cm 患者的回顾性研究报告, ALBI 3 级与延迟出院 ( 超过标准 3 天 RFA 方案 >1 天; OR=21.17 ; 95%CI:0.98-458.38 ; P=0.052) 相关。 Chen 等分析了 271 例单发 HCC<2cm 患者,确定 ALBI 2 或 3 级是较差 OS(HR=2.191 ; 95%CI:1.261-3.805 ; P=0.005) 和 PFS(HR=1.825 ; 95%CI:1.288-2.585 ; P=0.001) 的独立危险因素。这些发现强调肝功能是 HCC 患者 RFA 预后的关键决定因素, ALBI 分级是有价值的预测工具。
声明 8 :推荐对病毒相关 HCC 进行抗病毒治疗,以降低复发风险、改善肝功能并提高 OS 。
证据等级: 2 。推荐强度: B 。共识度: 100% 。
强烈推荐对病毒相关 HCC 患者进行抗病毒治疗。在乙型肝炎中,核苷 ( 酸 ) 类似物可降低新发 HCC 和肝失代偿的风险。一项全国性队列研究表明,抗病毒治疗与肝切除术后较低的复发率和改善的 OS 相关。对于丙型肝炎,推荐直接抗病毒药物 (DAAs) 预防肝硬化相关并发症并降低 HCC 风险。尽管 DAAs 对 HCC 复发的影响仍有争议,多项研究和指南——包括中国台湾共识和 APASL 指南——显示 DAA 治疗后达到持续病毒学应答 (SVR) 与生存改善相关,主要通过改善肝功能和减少肝失代偿实现。中国台湾的一项研究表明, HCV 根除显著降低 HCV 相关 HCC RFA 后的远处复发,主要通过改善肝功能和减少肝失代偿。
声明 9 :术前仔细评估凝血状态,包括国际标准化比值 (INR) 和血小板计数,对避免出血并发症至关重要。
证据等级: 2 。推荐强度: B 。共识度: 94% 。
许多 HCC 患者有肝硬化相关血小板减少或凝血酶原时间延长,增加 RFA 期间出血风险。不可纠正的凝血障碍和严重血小板减少被视为禁忌证。指南通常采用血小板计数 <50,000/mm ³或 INR>1.5 作为阈值。然而,多项研究报告凝血酶原时间延长或血小板减少并未显著增加出血风险。预防性输注血小板或新鲜冰冻血浆可降低出血风险,但应个体化以确保成本效益,考虑患者因素、操作者经验和影像质量。因此,术前仔细的凝血评估对最小化并发症至关重要。
声明 10 :有胆肠吻合术史或内镜下括约肌切开术史的患者消融后胆道感染或肝脓肿风险增加。推荐消融前预防性使用抗生素。
证据等级: 3 。推荐强度: B 。共识度: 100% 。
因胆肠吻合术或内镜下括约肌切开术导致 Oddi 括约肌功能缺失与消融后胆管炎或肝脓肿强烈相关 (OR=36.4 ; 95%CI:9.67-136.9 ; P<0.01) 。关于预防性抗生素的最佳类型或持续时间尚无共识。有报告建议消融前一天开始应用抗生素。在一项纳入 226 例经皮消融患者的前瞻性研究中,所有 3 例既往有胆肠吻合术的患者尽管接受了 5 天阿莫西林克拉维酸疗程仍发生肝脓肿。在一项回顾性研究中, 1 例 (12.8%) 有胆肠吻合术的患者尽管接受长期预防 ( ≥ 10 天 ) 仍发生肝脓肿。然而,由于缺乏对照组,证据仍然有限。需要进一步研究以确定最佳抗生素方案。由于即使预防后肝脓肿风险仍高,对于部分高危患者可考虑替代非热方法,如放疗。
肿瘤相关因素
声明 11 :消融治疗最适合肿瘤数目不超过 3 个、每个直径≤ 3cm 的 HCC 患者。
证据等级: 1 。推荐强度: A 。共识度: 100% 。
RFA 在小 HCC( ≤ 3cm) 中实现高完全坏死率,因为充足的能量沉积可最小化复发并改善生存结局。多项荟萃分析和系统综述显示,对于早期 HCC ≤ 3cm , RFA 提供与手术切除相当的疗效和 OS ,且具有微创、并发症少、住院时间短的优势。对于 >3cm 的肿瘤, RFA 疗效下降,局部和远处复发率较高;部分病例可考虑辅助治疗。
声明 12 :在肿瘤边界外获得足够的消融边缘 ( ≥ 5mm) 对完全消融和持久局部肿瘤控制至关重要。
证据等级: 2 。推荐强度: B 。共识度: 100% 。
至少 5mm 的消融边缘对减少 HCC 消融后局部肿瘤进展 (LTP) 至关重要。研究一致证明,≥ 5mm 的边缘相比 <5mm 的边缘显著降低局部复发风险。使用影像融合技术评估最小消融边缘进一步证实,达到该阈值可独立预测改善的局部肿瘤控制。
声明 13 :对于部分较大肿瘤 (>3cm) 患者,优先选择消融联合 TACE 、或使用开关控制 (SWC) 模式的 MWA 或 RFA 。
证据等级: 2 。推荐强度: B 。共识度: 100% 。
传统单电极 RFA 伴重叠穿刺对 >3cm HCC 效果较差。在此类肿瘤中,消融联合 TACE 与单独 RFA 或 MWA 相比可改善生存并降低复发。这种协同效应弥补了每种方式的局限性。然而,联合治疗的标准化治疗方案仍未确定。带开关单极或双极模式的多电极 RFA 系统可在更短时间内产生更大的消融区域,支持 >3cm 肿瘤的持久肿瘤控制和改善 OS 。无接触 RFA 技术显示优于传统 RFA 的局部控制,尽管 OS 获益尚不确定。 MWA 具有理论优势,包括更大的消融区域、更短的手术时间、更少的疗程和减少的热沉效应;然而,随机对照研究仅显示相当或轻度改善的局部控制,无明确优于 RFA 的证据。治疗选择应考虑当地政策、设备可及性、操作者专长、手术可行性和成本效益。
声明 14 :位于高危部位的 HCC 对邻近器官热损伤风险更高。
证据等级: 2 。推荐强度: B 。共识度: 100% 。
经皮热消融对某些解剖区域肿瘤的消融技术上具有挑战性且被视为高风险。包膜下肿瘤 ( 定义为距离肝包膜 10mm 以内 ) 因靠近肝脏表面而存在风险。胆管周围肿瘤 ( 距离主胆管或段胆管 <10mm) 有胆管损伤风险。血管周围肿瘤 ( 距离门静脉或肝静脉一或二级分支 [ 直径≥ 3mm] 或下腔静脉 <5mm) 有血管并发症风险。此外,距离肝外器官 ( 如心脏、膈肌、肺、胆囊、右肾、胃或结肠 )<5mm 的肿瘤因潜在附带热损伤被视为高风险。已开发多种技术以提高这些高危部位的安全性和疗效。对于包膜下肿瘤,人工腹水、无接触多极消融和腹腔镜辅助消融可改善治疗结局。对于胆管周围肿瘤,经鼻胆管导管行胆管内冷盐水灌注可能有助于消融期间保护胆管。根据文献,胆管周围结构热消融时建议与胆管保持至少 5-10mm 的安全距离。
声明 15 :对于包膜下或膈下 HCC 消融治疗,推荐采用人工腹水或胸腔积液以减少邻近器官热损伤风险。
证据等级: 2 。推荐强度: B 。共识度: 100% 。
超声引导下 RFA 对某些包膜下肿瘤有限制,因显示不清、电极入路受限和附带损伤风险。人工腹水可改善超声可视化并创建热屏障将肿瘤与邻近器官分离。人工胸腔积液为膈下 HCC 提供类似的超声窗口并保护肺部,但不保护膈肌。
影像方式
声明 16 :增强磁共振成像 (MRI) ,特别是钆塞酸二钠 (Gd-EOB) 增强 MRI ,是消融术前规划的首选参考影像方式;当 MRI 不可用时,多期相计算机断层扫描 (CT) 是合适的替代方案。
证据等级: 3 。推荐强度: B 。共识度: 100% 。
MRI 通常对 HCC 检测的敏感性优于 CT ,特别是对小病灶。 Gd-EOB 的使用进一步增强了 MRI 性能。一项荟萃分析支持 MRI 作为 HCC 诊断的首选方式,因其具有更高的每病灶敏感性。 Gd-EOB 增强 MRI 在识别低血管化肝结节和检测额外 HCC 病灶方面优于 CT 。尽管如此,当前指南推荐多期相 CT 和动态增强 MRI 均为可接受的 HCC 无创诊断工具,考虑成本、可及性和工作流程复杂性。
声明 17 :术前影像与实际消融手术之间的时间间隔理想情况下应少于一个月,以确保准确的肿瘤范围特征和治疗规划。
证据等级: 3 。推荐强度: B 。共识度: 100% 。
关于术前影像最佳时机的研究缺乏;然而,间隔过长可能导致肿瘤进展并影响准确的术后反应评估。一项调查报告 65.7% 的操作者和 86.4% 的肝病学家倾向于消融前 1 个月内进行影像检查。在高危人群中,结节可基于典型影像表现诊断为 HCC ,具体为动态 CT 或 MRI 上动脉期强化后门静脉期或延迟期洗脱。术前影像与实际手术之间的间隔理想情况下不应超过 1 个月。
声明 18 :影像引导,包括超声 (US) 、 CT 、 MRI 或融合成像,对确保消融治疗期间准确的肿瘤靶向至关重要。
证据等级: 1 。推荐强度: A 。共识度: 100% 。
准确的肿瘤定位对安全有效的消融治疗至关重要。超声、 CT 、 MRI 或融合成像的影像引导确保精准靶向、最小化邻近器官损伤并允许评估手术成功。超声提供实时、无辐射引导,但在肥胖患者或病灶被肠气遮挡时可能受限。 CT 提供优越的解剖细节但缺乏实时能力且涉及电离辐射。融合成像和技术 ( 包括人工腹水或胸腔积液 ) 可减轻超声局限性,特别是对不明显的小肿瘤。在中国台湾,大多数消融手术在超声引导下进行,常辅以对比增强或融合成像,而 CT 引导消融保留用于具有挑战性的肿瘤位置。近期一项荟萃分析发现,超声、 CT 或 MRI 引导方式在治疗疗效或安全性方面无显著差异。
声明 19 :融合成像和 / 或超声造影 (CEUS) 在靶向不明显肿瘤或消融后局部复发病灶方面具有优势。
证据等级: 2 。推荐强度: B 。共识度: 100% 。
肿瘤靶向对 HCC 消融达到满意反应至关重要。不明显肿瘤——小、等回声、边界不清或受超声因素限制——对消融构成挑战。消融后识别局部存活肿瘤也可能困难。融合成像结合、空间对齐并共同显示来自不同方式 ( 超声、 CT 、 MR 、正电子发射断层扫描 ) 或同一方式不同时间点 ( 超声 - 超声 ) 的数据。实时超声 -CT/MR 融合与 B 模式超声相比显著改善不明显 HCC 的可见性和 RFA 可行性。自动配准技术提高效率同时保持配准准确性。 CEUS 通过静脉注射超声造影剂 (UCA) 可视化 HCC 血管模式的动态变化。 CEUS 与实时 CT/MR 联合可能增强复发 HCC 的定位,在 B 模式超声 -CT/MR 融合基础上增加 CEUS 进一步提高不明显病灶的肿瘤可见性和技术可行性评分。尽管 CEUS-CT/MR 融合可能改善局部肿瘤控制,但缺乏长期生存获益的证据。
声明 20 : CEUS 可在消融治疗期间实现实时监测,并作为有造影剂禁忌证患者的 CT 或 MRI 替代方案。
证据等级: 2 。推荐强度: B 。共识度: 100% 。
CT 造影剂有造影后急性肾损伤风险,特别是肾功能受损患者 ( 估算肾小球滤过率 <30 mL/min/1.73 m ² ) 。钆基 MRI 造影剂与肾源性系统性纤维化风险增加相关,特别是肾功能受损、急性肾损伤或终末期肾病透析患者。 CEUS 通过 UCA( 通常为含气微泡 ) 评估局灶性肝脏病变的动态特征。破坏后,气体经肺排泄,磷脂壳被代谢。 UCA 在现实临床实践中显示出极佳的安全性,无肾毒性或辐射暴露。因此, CEUS 对严重肾功能受损、急性肾损伤或终末期肾病患者是安全的。 CEUS 允许从动脉期到晚期血管期的连续实时对比增强可视化,实现消融后即刻评估残余存活肿瘤。
声明 21 :使用融合影像进行超声引导消融时, MRI 图像比 CT 图像提供更好的同步性。
证据等级: 5 。推荐强度: C 。共识度: 75% 。
融合成像越来越多地用于超声引导消融以改善肝脏肿瘤的可视化,特别是传统 B 模式超声上不明显的肿瘤。 MRI ,特别是 Gd-EOB 增强 MRI ,与 CT 相比具有更优越的软组织对比度和更精确的亚厘米 HCC 描绘,可能在融合期间实现更准确的图像配准。对于 CT 融合,患者通常在吸气末屏气,而 MRI 融合一般要求在呼气末屏气以匹配原始采集时的呼吸状态。这些调整优化了平面和点配准的空间对齐。尽管如此,由于 CT 更广泛的可及性、更快的图像处理和更好的平台兼容性, CT 融合仍然更常用。鉴于这些局限性和缺乏高级别比较研究, MRI 融合可能在部分病例中改善同步性,但 CT 在大多数临床环境中仍是实用标准。
MWA vs. RFA( 表 3)
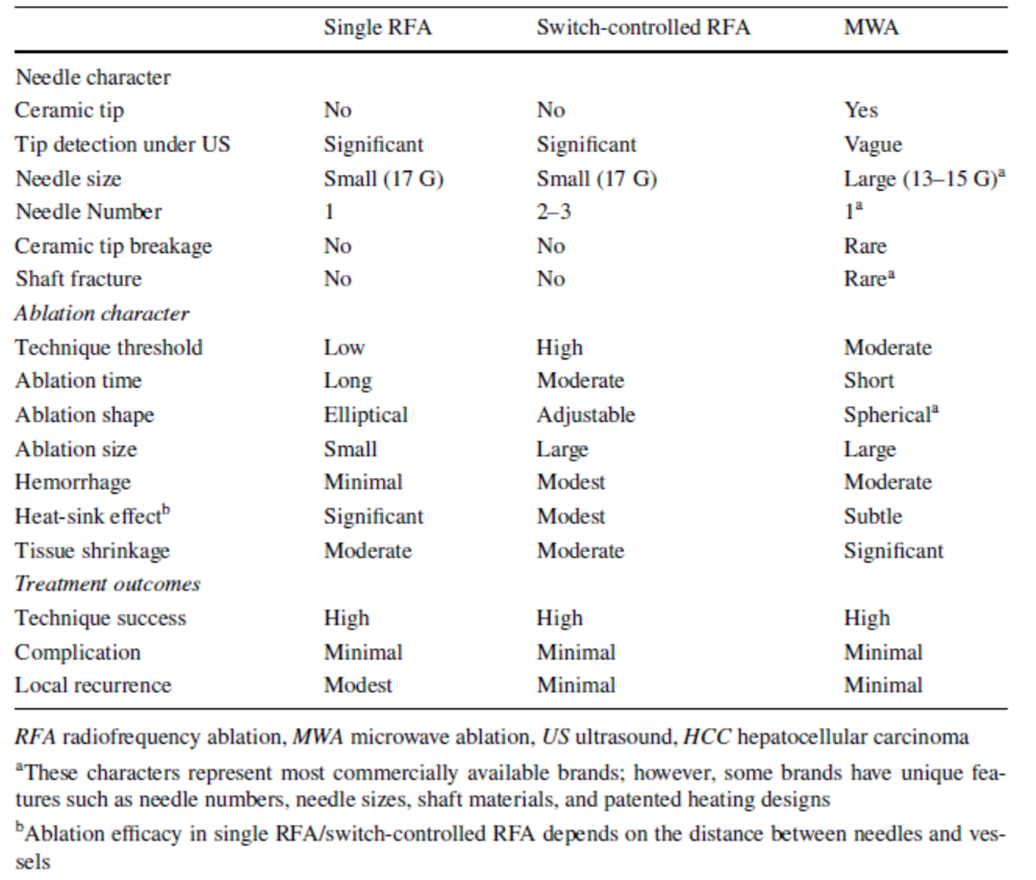
声明 22 :与传统单电极 RFA 相比, MWA 消融时间更短,减少手术时间和麻醉风险。
证据等级: 2 。推荐强度: B 。共识度: 100% 。
RFA 和 MWA 是早期 HCC 的两种主要局部区域治疗。在一项随机对照研究中, Sugimoto 等比较了 MWA 与单电极 RFA 治疗 <4.0cm 肿瘤。 OS 和 RFS 相当,但 MWA 显示出更优的局部肿瘤控制。主要机制差异在于热量产生: RFA 通过电极周围电阻加热然后向外热扩散诱导热损伤,而 MWA 产生电磁场在消融区内均匀加热组织,产生更一致、组织依赖性更低的热分布。 MWA 允许更高的能量输送,实现更快加热和更短消融时间。另外两项随机对照研究证明了手术效率差异。 Vogl 等报告 MWA 在更短时间内达到比 RFA 更大的消融体积 (66.5cm ³ vs. 29.2cm ³; 11.2 vs. 16.3 分钟 ) 。 Kamal 等同样发现 MWA 比 RFA 更快达到目标消融终点 (4.41 vs. 14.21 分钟, P<0.001) 。采用高功率 MWA 系统,现在可在 10 分钟内消融达 4.1cm 的肿瘤,降低麻醉风险并提高手术效率。
声明 23 :对于靠近大血管的肿瘤,优先选择 MWA 而非 RFA ,因其对热沉效应的敏感性较低。
证据等级: 2 。推荐强度: B 。共识度: 100% 。
热消融可能受热沉效应限制,邻近血管中的血流消散热能并降低消融疗效。 MWA 通过在组织内 (" 活性区 ") 均匀高效地沉积能量解决这一问题,允许在血管周围区域更好地热量累积并最小化热沉效应。一项纳入 6 项随机对照研究的荟萃分析报告,与 RFA 相比, MWA 显著降低 LTP(OR=0.70) 。在血管周围 HCC 中, MWA 与低于 RFA 的 LTP 相关 (P=0.017) 。 An 等发现 RFA 治疗的门静脉周围 HCC 与 MWA 治疗病灶相比 LTP 更高 (P=0.045) 。这些数据支持 MWA 作为邻近大血管肿瘤的首选方法。
疗效
声明 24 :对于单发 HCC ≤ 3cm 患者,消融治疗 ( 包括 RFA 和 MWA) 显示与手术切除相当的 OS 率。
证据等级: 1 。推荐强度: A 。共识度: 100% 。
多项前瞻性随机对照研究和荟萃分析显示,对于早期 HCC ≤ 3cm , RFA 或 MWA 提供不劣于手术切除的生存结局。横跨 49 家日本机构的多中心 SURF 研究比较了手术切除和 RFA 治疗 HCC ≤ 3cm( 最多 3 个结节 ) ,显示两组间 OS 或 RFS 无显著差异。一项系统综述和贝叶斯网络荟萃分析得出结论, RFA 和 MWA 对极早期和早期 HCC 同样有效。消融治疗具有减少围手术期发病率、缩短住院时间和更快恢复的优势,同时在适合选择的患者中保持极佳的局部肿瘤控制。
并发症与安全性
声明 25 :消融治疗的并发症发生率低,但需要在消融期间和之后仔细监测。
证据等级: 2 。推荐强度: B 。共识度: 100% 。
消融治疗的并发症可根据标准化分级系统进行分类,包括介入放射学会 (SIR) 标准和 Clavien-Dindo 分级和分类,为跨方式解释手术安全性提供一致框架。肝脏消融后的主要并发症发生率约为 2.8-4.6% 。一项系统综述报告 RFA 的主要并发症合并发生率为 4.1% , MWA 为 4.6% ,单项研究范围为 1.52-4.7% 。手术相关死亡率罕见, RFA 合并发生率为 0.15% , MWA 为 0.23% 。一项大型日本研究报告 RFA 的死亡率极低,为 0.064%(6/9,411 例患者 ) 。最常见的主要并发症包括出血、肝脓肿、胆管损伤、门静脉血栓形成和肝衰竭。一项研究中出血是最常报告的事件 (1.1%) ,通常早期识别,凸显术后及时监测的重要性。根据代表性研究和荟萃分析,各消融方式的主要并发症发生率约为: RFA 2-4% , MWA 3-6% ,冷冻消融 4-7% , IRE 2-7% 。次要并发症发生率各异,估计 RFA 为 5-9% , MWA 为 3-9% ,冷冻消融为 20-30% , IRE 为 20-30% 。对于组织损毁术和 HIFU 等新兴技术,证据仍然有限;报告的主要并发症发生率约为组织损毁术 1-7% , HIFU 0-10% 。次要并发症发生率估计组织损毁术为 4% , HIFU 为 20-70% 。
经皮消融被认为是安全有效的治疗选择,严重并发症风险低。最佳患者选择、充分的术前评估和勤勉的术后护理对最小化发病率和实现良好临床结局至关重要。
随访
声明 26 :治疗后一个月应进行影像检查 ( 如动态 CT 或 MRI) 联合肿瘤标志物检测,以评估反应和检测残余存活肿瘤。此后应每 3-6 个月重复随访影像。
证据等级: 3 。推荐强度: B 。共识度: 94% 。
HCC 消融后定期随访至关重要,因复发率高。尽管最佳随访方案尚未明确确定,消融后监测仍是长期监测的基本组成部分。已提出基于影像的随访策略联合肿瘤标志物。鉴于高复发风险,推荐首次随访采用动态 CT/MRI( 如无禁忌证 ) ,用于早期评估治疗反应、残余未消融肿瘤和疾病进展。由于超声仍是监测的基石,超声联合肿瘤标志物可作为后续随访的替代方案,取决于个体风险评估。由于常需重复消融手术 / 疗程以达到技术疗效,建议首次随访在 4-6 周内采用动态影像,以确定是否需要额外消融。完全消融后,鉴于肿瘤倍增时间和高复发风险,前 2 年每 3-6 个月随访影像被认为是合理的。随访持续时间尚未明确界定,但可能是无限期的。然而,当前推荐主要基于专家共识而非有力证据,凸显需要高质量研究以建立循证随访方案。
前景
声明 27 :消融治疗与免疫治疗联合可能增强全身免疫反应并改善 HCC 患者结局。
证据等级: 3 。推荐强度: C 。共识度: 63% 。
消融治疗通过物理或热机制可诱导肿瘤细胞凝固性坏死或细胞破坏。历史上,消融被视为局部治疗。然而,肿瘤组织破坏释放肿瘤相关抗原,改变局部肿瘤微环境并在前瞻性患者队列研究中触发涉及免疫细胞和细胞因子的全身免疫反应。当这种全身免疫反应导致未直接治疗的肿瘤缩小时,通常称为远隔效应。大量临床病例报告证明了这种肿瘤反应的潜在发生。然而,这种效应往往不常见。 HCC 即使根治性消融后的高复发率间接支持了这一观察。
鉴于这些发现,将消融与免疫治疗相结合以增强全身免疫反应——从而改善患者生存——已成为当前临床实践中备受关注和有前景的方法,主要来源于回顾性研究、前瞻性研究和单臂研究。一项概念验证前瞻性研究显示, RFA 或 MWA 可将纳武利尤单抗或帕博利珠单抗在 50 例晚期 HCC 患者中的抗肿瘤效应和缓解率从 10% 提高至 24% 。提出的机制涉及 T 细胞活性增加和 PD-1 表达上调。除与 ICI 联合治疗外,过继免疫治疗或疫苗也在探索中。最近,一项前瞻性对照研究显示, RFA 联合特瑞普利单抗 ( 抗 PD-1) 可改善既往仅接受 RFA 治疗的复发 HCC 患者的无复发生存期。关键挑战仍然存在,包括协同效应不佳、最佳药物选择和给药时机。尽管正在进行消融联合免疫治疗的临床研究,证据仍为初步阶段。专家小组认为该策略有前景但尚未验证,强调需要大规模随机研究确认其临床获益。
未来方向
声明 28 :组织损毁术是一种无创、高精度超声消融技术,无热损伤,特别适合靠近血管或胆管的肿瘤。
证据等级: 4 。推荐强度: C 。共识度: 69% 。
组织损毁术是一种新兴消融方式,使用聚焦超声通过控制空化机械性破坏组织。与传统热消融方法 ( 如 RFA 或 MWA) 不同,它避免热相关损伤,最小化对邻近关键结构 ( 如大血管、胆管或其他热敏感器官 ) 的风险。临床研究已证明组织损毁术能够实现精确消融边缘同时保留附近重要解剖结构。此外,该技术允许实时超声监测,并与低比例的操作错靶相关。尽管大规模研究仍在进行中,组织损毁术的非热、机械机制为因解剖限制不适合传统消融的患者代表了一种有前景的选择。
结论
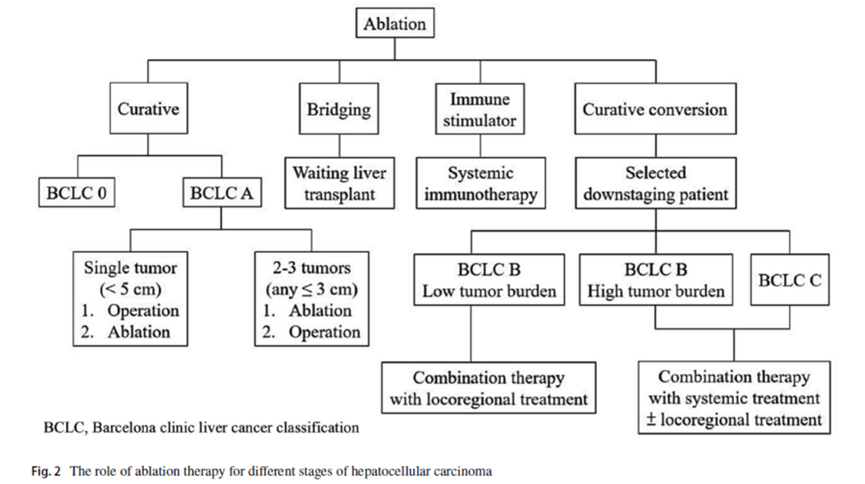
肿瘤消融是 HCC 的根治性治疗选择,具有微创、恢复快和保留肝功能的优势。消融可与其他局部或全身治疗联合,可能促进肿瘤降期并通过肿瘤坏死后抗原释放增强免疫治疗疗效。本指南提供循证建议,涵盖不同 HCC 分期的适应证 ( 图 2) 、患者和肿瘤相关因素、消融设备和技术进展、治疗结局、风险和随访策略。此外,随着医疗技术的快速发展——特别是人工智能和机器人技术——未来预期将出现更精准、更高效的消融手术。
参考文献: Chang CW, Wu MS, Kao WY, Chiang MF, Hsu SJ, Wang SY, Hung CH, Wu CH, Chen SC, Cheng YM, Lee IC, Hsieh YC, Chen WT, Lin CC, Liang PC, Hwang JI, Lin SM, Huang KW, Dai CY, Huang YH, Wang CC. Taiwan Academy of Tumor Ablation (TATA) consensus on hepatocellular carcinoma ablation. Hepatol Int. 2026 Feb 24. doi: 10.1007/s12072-026-11050-2. Epub ahead of print. PMID: 41733829.
排版编辑:肿瘤资讯-as











 苏公网安备32059002004080号
苏公网安备32059002004080号


