2026年3月30日,欧洲药品管理局人用药品委员会(EMA/CHMP)同时发出两项积极意见,推荐批准斯鲁利单抗(欧盟商品名为Hetronifly®)联合化疗用于一线治疗局部晚期或转移性非鳞状非小细胞肺癌(nsqNSCLC),以及一线治疗PD-L1阳性不可切除的局部晚期、复发或转移性食管鳞状细胞癌(ESCC)。根据欧盟法规,CHMP积极意见将提交欧盟委员会进行最终审议,若顺利获批,斯鲁利单抗将在欧洲经济区30个国家进一步拓宽适应症覆盖范围。
同一天,两项积极意见,两个瘤种,而这并非斯鲁利单抗第一次进入欧洲审评机构的视野。2025年2月,斯鲁利单抗已作为全球首个获批用ES-SCLC一线治疗的PD-1抑制剂(First in Class),正式获得欧盟委员会批准上市。此后不到14个月,斯鲁利单抗在欧盟12个国家实现上市,并进入奥地利、丹麦、德国、爱尔兰、意大利、西班牙和瑞典等7个国家的医保体系。
支撑这次两项积极意见的,是两项III期临床研究的数据,一项是由中国医学科学院肿瘤医院石远凯教授主导的ASTRUM-002研究[1,2],以及由中国医学科学院肿瘤医院黄镜教授主导的ASTRUM-007研究[3,4]。这两项在中国已获批上市的III期临床研究,在欧洲审评体系中再次得到积极回应,其数据究竟说明了什么,值得我们详细分析。
斯鲁利单抗进入欧盟市场的第一步,从SCLC开始,First in Class高分入场快速落地
EMA对临床数据质量与试验设计规范性要求严格,各成员国依托ESMO-MCBS(欧洲肿瘤学会临床效益量表,是ESMO推出的临床获益量表,用于标准化评估抗肿瘤治疗的临床价值)对药物价值进行独立评估,评分结果直接影响后续的医保谈判走向;在已有多款成熟产品覆盖的治疗领域,后进入者需以数据证明自身的临床价值。
在ES-SCLC适应症上,ASTRUM-005研究[5]所支持的斯鲁利单抗获得了ESMO-MCBS评分4分,在同类研究中属于较高的评级(表1),意味着在欧洲专业机构的独立评估框架下,其临床效益得到了正面认定。基于这一基础,斯鲁利单抗在欧盟各国的落地推进顺畅,一年内在12个国家完成上市,7个成员国完成医保或公共支付体系准入。
表1. 在SCLC领域ESMO-MCBS的评分情况,来自官网:https://www.esmo.org/guidelines/esmo-mcbs/esmo-mcbs-for-solid-tumours/esmo-mcbs-scorecards
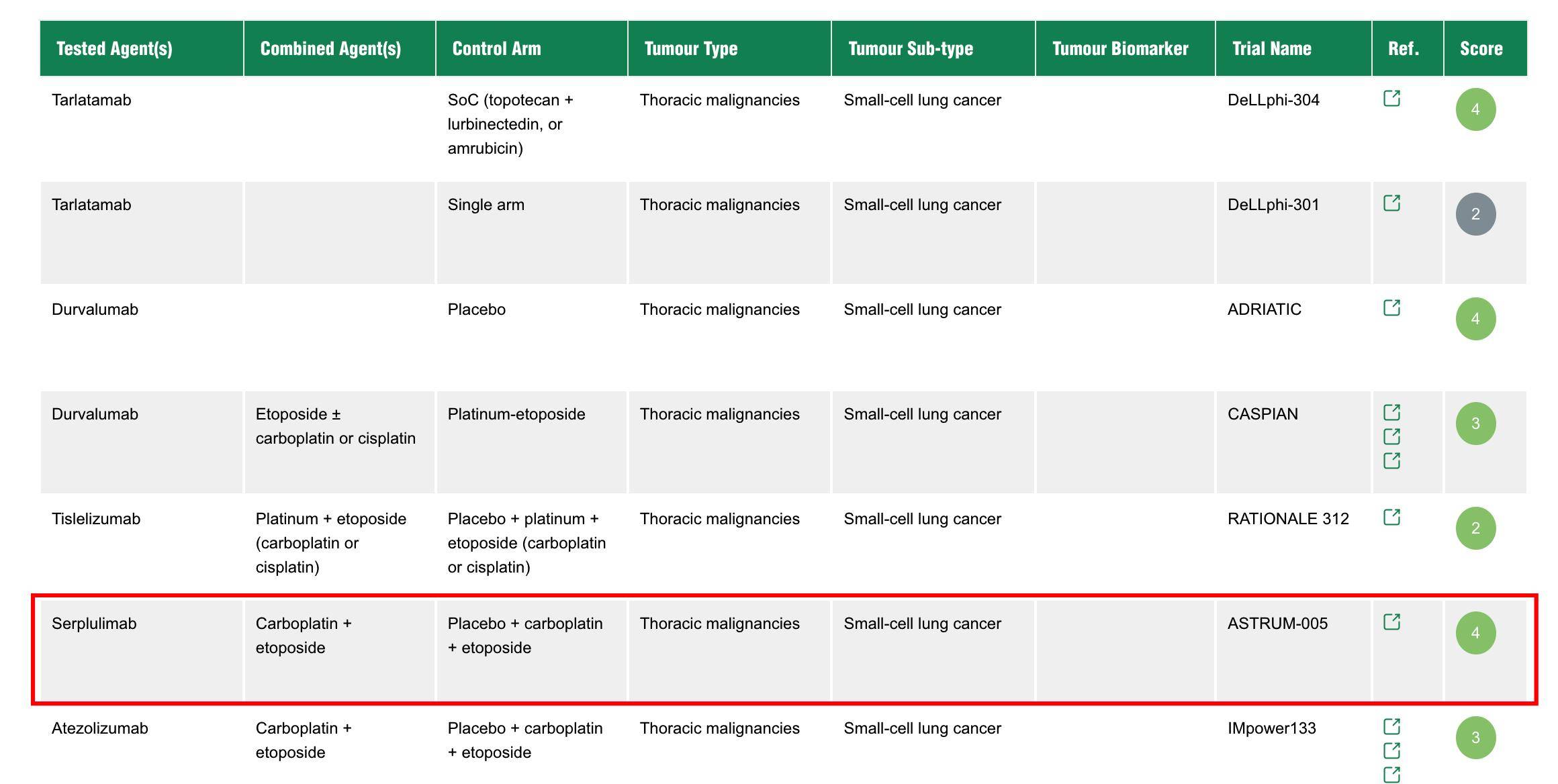
ES-SCLC的获批与商业化路径,为斯鲁利单抗进一步推进NSCLC适应症的欧洲布局提供了基础。而相较于SCLC,NSCLC无论在患病人数还是治疗格局的复杂程度上,都代表着更大的临床场景,竞争也更为激烈。
一线nsqNSCLC,ASTRUM-002用26.8个月的中位OS给出答案
驱动基因阴性的晚期nsqNSCLC,是肺癌中占比较大的一个亚型。免疫联合化疗已成为该人群一线治疗的标准方案,多项III期研究相继证实了PD-1/PD-L1抑制剂联合含铂化疗在这一人群中的生存获益,数据相似。在此背景下,ASTRUM-002研究[2]评估了斯鲁利单抗联合培美曲塞和铂类化疗,对比安慰剂联合化疗,用于EGFR/ALK阴性晚期nsqNSCLC患者一线治疗的疗效与安全性,给出了自己的答案。
ASTRUM-002是一项随机、双盲、多中心III期研究,共纳入636例晚期nsqNSCLC患者,随机分为三组:斯鲁利单抗联合贝伐珠单抗生物类似药HLX04及化疗(A组)、斯鲁利单抗联合化疗(B组)、单纯化疗(C组),化疗方案均为卡铂联合培美曲塞。研究的主要终点为经盲态独立中心审评的PFS,关键次要终点包括OS、ORR和DoR。2025年ESMO年会上,最终分析结果以Late-breaking Abstract(LBA71)形式口头报告,中位随访时间约47个月。
在OS方面,斯鲁利单抗联合化疗组的中位OS为26.8个月,单纯化疗组为20.3个月(HR=0.66,p=0.0004)。在PFS方面,中位PFS为11.0个月,对照组为5.7个月(HR=0.54,p<0.0001)。ORR方面,斯鲁利单抗联合化疗组为53%,对照组为28%;中位DoR分别为15.4个月和8.3个月。在已发表的同类III期研究(部分)中,各方案报告的主要生存数据汇总于表2。
表2. 已发表的针对nsqNSCLC人群的同类III期研究(部分)中,各方案报告的主要生存数据(各研究在入组人群、随访时间、数据截止节点及化疗方案等方面存在差异,跨研究的直接数值比较需审慎解读)
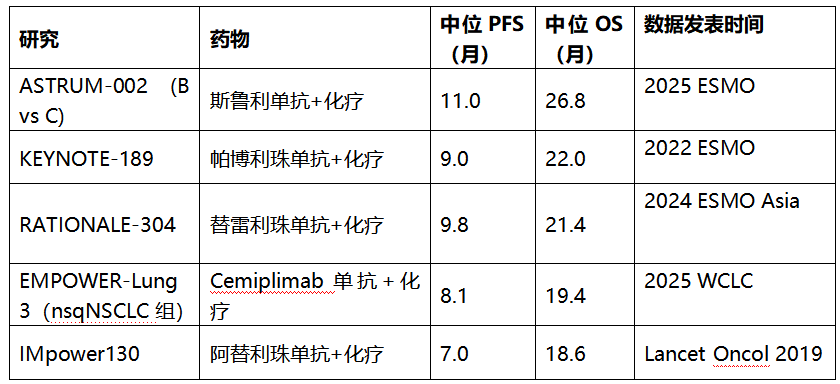
ES-SCLC适应症凭借ASTRUM-005研究的数据获得ESMO-MCBS 4分(较高评级),nsqNSCLC的MCBS评分尚未公布,但从ASTRUM-002最终分析所呈现的OS绝对获益幅度和数据成熟度来看,其在欧洲卫生技术评估(HTA)框架下具备同等竞争力的基础。
亚组分析显示,无论PD-L1 TPS≥50%还是存在脑转移的患者,B组相较C组的获益在大多数亚组中均保持一致,提示该方案的疗效不依赖于PD-L1表达水平或脑转移状态,在全人群中均可使用。
一线ESCC,ASTRUM-007的数据得到了中国与欧洲双重认可
斯鲁利单抗的III期临床研究,并不止于肺癌。在消化道肿瘤领域,ASTRUM-007研究同样在欧洲审评体系中得到了正面回应,一线ESCC适应症与nsqNSCLC适应症在同一天获得CHMP积极意见。
ASTRUM-007研究[3,4]是一项随机、双盲、安慰剂对照III期研究(NCT03958890),纳入551例PD-L1阳性(CPS≥1)的局部晚期或转移性ESCC患者,评估斯鲁利单抗联合顺铂+5-FU方案的疗效与安全性,结果于2023年发表于Nature Medicine[3],并在2023年ASCO年会报告了更新数据[4]。
结果显示斯鲁利单抗联合化疗的中位OS为14.6个月,对照组为11.2个月(HR=0.70);中位PFS为6.5个月,对照组为5.3个月(HR=0.58);PD-L1高表达亚组(CPS≥10)获益进一步放大,中位PFS的HR值为0.48,在目前已发表的同类一线ESCC免疫治疗III期研究中处于领先水平。
基于上述数据,斯鲁利单抗联合化疗已获《CSCO食管癌诊疗指南》一线治疗I级推荐(1A类证据),并在国内获批ESCC一线治疗适应症。
差异化机制决定不一样的PD-1,多瘤种管线持续拓展
斯鲁利单抗是一款全人源化IgG4型抗PD-1单克隆抗体,其差异化的机制特征体现在两个层面:一是具备较强的PD-1受体内吞效应,能够减少T细胞表面PD-1受体的数量,从而实现更快速、更强效的免疫激活[6];二是对CD28共刺激信号通路的保留程度相对较高,有助于维持T细胞的持续活化状态,增强下游AKT蛋白活性[6]。这一机制上的特点,是其在ES-SCLC、nsqNSCLC和ESCC三个适应症中均能呈现出持续且一致疗效信号的生物学基础。
在已获批适应症之外,斯鲁利单抗的临床探索仍在多个方向同步推进。胃癌围手术期方向,ASTRUM-006研究是全球首个且目前唯一胃癌围手术期III期注册研究成功的PD-1抑制剂,也是全球首个以术后免疫单药替代辅助化疗的胃癌围手术期方案,研究达到主要终点EFS,pCR率较对照组大幅提升,已获CDE突破性治疗品种认定,且上市申请已获受理并纳入优先审评;结直肠癌方向,斯鲁利单抗联合贝伐珠单抗联合化疗用于一线治疗转移性结直肠癌患者的国际多中心III期临床研究ASTRUM-015已完成入组,有望填补一线免疫治疗MSS转移性结直肠癌的临床空白;肺癌方向,斯鲁利单抗已全面覆盖肺癌一线治疗,值得一提的是,其鳞状非小细胞肺癌(sqNSCLC)的上市申请在欧盟已获受理,局限期小细胞肺癌(LS-SCLC)的国际多中心III期研究也在全球同步推进。此外,斯鲁利单抗在美国和日本同步开展ES-SCLC桥接试验,2025年6月完成日本桥接首例患者给药,同年10月完成美国桥接试验全部受试者入组,全球注册研究正在实质性推进,加速惠及全球更广泛患者。
结语
从ES-SCLC的全球首个获批,到nsqNSCLC在竞争最激烈的治疗领域上交出26.8个月的OS数据,再到ESCC获得中国和欧盟的双重认可,斯鲁利单抗在三个适应症中相继积累的III期临床证据,呈现出跨瘤种的一致性获益。此次EMA/CHMP两项积极意见,是这一证据体系在欧洲审评框架内的阶段性体现,是斯鲁利单抗从国内获批走向国际市场的重要一步。
在PD-1抑制剂的临床应用已趋成熟的今天,后来者能走多远,最终取决于数据能走多远。斯鲁利单抗给出的,是一款有Best in Class潜力的PD-1抑制剂的临床答案。
[1] Wang L, et al. First-line serplulimab plus chemotherapy with or without HLX04 versus chemotherapy in locally advanced or metastatic non-squamous non-small-cell lung cancer (ASTRUM-002): a randomised, double-blind, multicentre phase 3 trial. Lancet Respir Med. 2026 Feb;14(2):117-128.
[2] Shi Y. Final analysis of first-line serplulimab plus chemotherapy with or without HLX04 in advanced nonsquamous non-small cell lung cancer: The ASTRUM-002 phase III study. 2025 ESMO LBA71.
[3] Song Y, et al. First-line serplulimab or placebo plus chemotherapy in PD-L1-positive esophageal squamous cell carcinoma: a randomized, double-blind phase 3 trial. Nat Med. 2023 Feb;29(2):473-482.
[4] Huang J, et al. Updated results of first-line serplulimab versus placebo plus chemotherapy in PD-L1–positive esophageal squamous cell carcinoma: A randomized, double-blind, multicenter phase 3 study (ASTRUM-007). 2023 ASCO #e16016.
[5] Cheng Y, et al. Effect of First-Line Serplulimab vs Placebo Added to Chemotherapy on Survival in Patients With Extensive-Stage Small Cell Lung Cancer: The ASTRUM-005 Randomized Clinical Trial. JAMA. 2022 Sep 27;328(12):1223-1232.
[6] Zhang Y, et al. Insights into the mechanisms of serplulimab: a distinctive anti-PD-1 monoclonal antibody, in combination with a TIGIT or LAG3 inhibitor in preclinical tumor immunotherapy studies. MAbs. 2024 Jan-Dec;16(1):2419838.
排版编辑:肿瘤资讯-Yael
版权声明











 苏公网安备32059002004080号
苏公网安备32059002004080号


