抗体偶联药物(ADC)的发展正在改变晚期非小细胞肺癌(NSCLC)的治疗格局。TROP2 ADC在杀伤肿瘤的同时,其独特的毒性谱也对临床管理提出了更高要求。【肿瘤资讯】特邀四川大学华西医院黄媚娟教授深度解析TROP2 ADC药物的安全性特征及临床管理。
TROP2 ADC药物及安全性概述
自1913年Paul Ehrlich博士提出魔法子弹的构想以来,人类对理想抗癌药物的追求已历经一个多世纪。随着生物技术的迭代,现代ADC通过特异性抗体、连接子及高活性有效载荷三位一体的结构,实现了将高效细胞毒药物精准递送至靶病灶的愿景。这一创新疗法开启了抗肿瘤治疗的新时代,并正在改变实体瘤治疗的现有诊疗格局。
核心作用机制:ADC通过结合抗原、内化进入细胞,主要通过溶酶体中释放小分子药物,干扰癌细胞的DNA及微管蛋白功能,发挥抗肿瘤效应;还能发挥旁观者效应,有效克服肿瘤异质性。另外,ADC还能介导抗体依赖的细胞介导的细胞毒性(ADCC)等免疫效应,并干扰下游信号通路、抑制肿瘤生长。
约64%的肺腺癌病例中可观察到TROP2的高表达[1],且TROP2高表达肺腺癌患者与较短的OS、较高的死亡率风风险、较差的TNM分期以及较差的组织学分级相关。靶向TROP2的ADC是研究热点,目前进展较快的三款药物包括德达博妥单抗(Dato-DXd)、芦康沙妥珠单抗、戈沙妥珠单抗。
ADC毒性谱特征受到各结构组分的影响。抗体对正常组织的靶向性、连接子的循环稳定性以及有效载荷的毒性,共同决定药物的耐受性。TROP2 ADC不良反应管理需要包括肿瘤科、呼吸科、眼科等多个科室的参与。据文献报道,TROP2 ADC常见不良反应包括眼表毒性4%~9.6%、口腔炎13.2%~64.4%、间质性肺病(ILD)1%-8.8%、血液学不良反应3%~84.6%、消化系统不良反应10.1%~52.7%[2,3]。
不同TROP2 ADC的安全性有所差异
TROPION-Lung01/05研究显示,Dato-DXd的≥3级治疗相关不良事件(TRAE)主要包括口腔炎(6.7%)、食欲下降(2%)、疲劳(1%)、呕吐(1%)、贫血(4%)、中性粒细胞减少(0.7%)、ILD/肺炎(3.7%)、角膜炎(1.3%)。EVOKE-01研究中,戈沙妥珠单抗≥3级治疗期间不良事件(TEAE)包括口腔炎(1%)、中性粒细胞减少(24.7%)、发热性中性粒细胞减少(7.8%)、白细胞减少(5.1%)、贫血(6.4%)、疲劳(13%)、腹泻(10%)、恶心(2%)。OptiTROP-Lung03研究中,芦康沙妥珠单抗≥3级TRAE包括中性粒细胞减少(25%)、白细胞减少(12%)、贫血(12%)、口腔炎(16%);OptiTROP-Lung04研究中,≥3级TRAE包括中性粒细胞减少(39.9%)、白细胞减少(27.7%)、贫血(11.2%)、血小板减少(2.1%)、淋巴细胞减少(3.2%)、口腔炎(4.8%)、疲劳(4%)[4-7]。
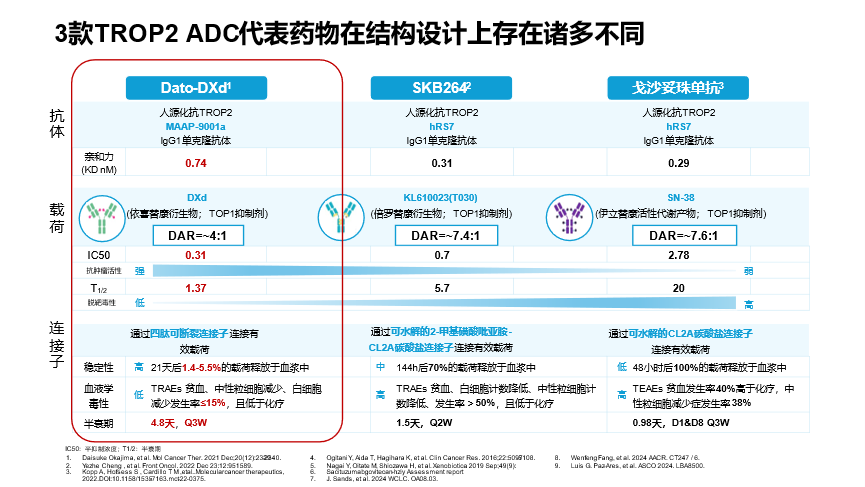
不同TROP2 ADC的安全性特征主要取决于药物结构及设计差异。由于TROP2广泛表达于皮肤、肺、乳腺等正常组织器官,过高的药物抗体比(DAR)值可能损害正常组织。①在抗体及DAR设计上,Dato-DXd将DAR值优化为约4:1,在保证药效的同时以扩大治疗窗,降低药物聚集及脱靶毒性风险。Dato-DXd采用经改造的人源化MAAP-9001a抗体,仅能与TROP2高表达肿瘤细胞结合,以减少药物在正常组织中的积蓄。②有效载荷DXd的IC50数值最低(IC50仅0.31),具备更强的抗肿瘤活性。同时,游离DXd的半衰期极短仅1.37小时,意味着进入血液循环的游离载荷可被快速清除,全身暴露及组织滞留风险低,不易出现严重的脱靶毒性问题,进一步提升了安全性。③Dato-DXd采用的四肽可断裂连接子具有高稳定性。临床前研究显示,Dato-DXd在血浆循环21天后的有效载荷释放率仅1.4%-5.5%,这种高稳定性使载荷在血液循环中极少提前脱落,是Dato-DXd血液学毒性发生率低(≤15%)且低于化疗的重要因素。此外,由于Dato-DXd整体药物半衰期较长(约4.8天),支持每三周一次(Q3W)的给药方案。
TROP2 ADC主要不良反应的管理
中性粒细胞减少症的预防和治疗
中性粒细胞减少症的管理以ANC分级为基础,其中4级定义为ANC<0.5×10⁹/L。若患者ANC<0.5 × 10⁹/L(或预计48h内降至该水平),且体温≥38.3°C(或≥38°C持续1h),则判定为发热性中性粒细胞减少(FN)。管理重点在于风险评估与分级预防:一级预防指首次化疗后24-72h内使用 G-CSF,建议 FN 风险≥ 20%的高危患者启动。二级预防指在既往化疗周期中发生过 FN 或剂量限制性中性粒细胞减少事件的患者,在后续周期化疗前重新评估风险,并积极给予rhG-CSF支持,必要时需调整化疗方案以降低再次发生的风险[8,9]。
血小板减少症的诊断、评估和治疗
肿瘤治疗所致血小板减少症(CTIT)的诊断以血小板计数<100×109 为标准,结合分级(1-5级)及出血严重程度进行病情评估。临床需结合分级(1-5级)与出血严重程度(轻中度/重度)进行综合评估。治疗策略以临床出血表现为核心,动态参考血小板阈值。对于合并出血者,无论血小板水平如何,均应积极通过输注血小板、使用 rhTPO、TPO-RA 等方案止血;若无出血症状,则依据血小板计数水平进行分层管理[10]。
贫血的治疗
根据ESMO临床实践指南,贫血的治疗应基于血红蛋白(Hb)水平与病因分析(如缺铁、B12/叶酸缺乏等)进行个体化决策。当Hb 8-10g/dL时,需针对不同类型的缺铁状态(绝对性、功能性或无缺铁)匹配 ESA 联合静脉补铁等治疗策略;而当Hb水平7-8 g/dL或需快速提升指标时,则应启动红细胞(RBC)输注,并全程动态监测Hb与铁状态,以维持在最低限度的治疗水平[11]。
口腔炎的预防、监测和管理
口腔炎的管理涵盖预防、监测、管理三个环节。预防策略包括贯穿治疗全过程的皮质类固醇漱口水含漱、严格的口腔卫生及输注期间的冷冻疗法(如含冰块)。监测上,应由肿瘤护理团队定期进行口腔检查。管理上,在排除感染等其他诱因后,可利用利多卡因漱口水缓解疼痛,或局部涂抹氟倍他索凝胶促进愈合。
基于 CTCAE 分级的剂量调整:口腔炎的管理遵循CTCAE分级原则,采取“局部支持与动态调整”相结合的策略。1级(轻症)通常无需调整剂量,管理重点在于饮食优化及局部类固醇制剂(凝胶、漱口水)的对症护理。针对2级及以上中重度毒性,应先行暂停给药,直至症状消退至安全范围。恢复后,由临床医生根据患者对预防药物的依从性及个体状态,按照说明书综合判定维持原剂量或进行梯度减量。若发生4级危及生命的严重毒性,需立即实施紧急干预[12,13]。
ILD/肺炎的管理
ILD是ADC药物需严密监测的不良反应。给药前,临床应重点识别高危人群,并通过CT/HRCT获取基线数据。治疗期间,一旦患者出现咳嗽、发热或呼吸困难等疑似症状,应暂停用药,并启动由呼吸科等多学科协作(MDT)的排除性诊断流程,利用影像学及肺功能测试进行确诊。
ILD的管理遵循严格的分级原则:对于1-2级毒性,需暂停治疗直至症状完全缓解,并依据缓解时长决定是否下调剂量或启用糖皮质激素;对于3-4级或伴有症状的2级毒性,通常要求永久停药。随访阶段应维持高频率的影像学监测并辅以肺康复训练,以最大限度保障患者的呼吸安全[14]。
眼表毒性的管理
眼表毒性的管理遵循CTCAE及角膜毒性分级量表,采取分级管控与对症支持相结合的策略。针对1级毒性,患者通常无症状,管理上无需调整药物剂量,可通过使用润滑剂缓解,并可考虑进行眼科评估。针对2级毒性,应延迟给药直至事件恢复至1级及以下;在重新起始治疗时可维持原剂量,但管理全程必须进行眼科评估。针对3级毒性,患者视力显著下降,日常活动受限,影像可见角膜溃疡或基质混浊。此时应延迟给药直至恢复至1级及以下,且必须执行降低一个剂量水平的策略,并严格进行眼科评估。针对4级毒性,应永久停药,并立即启动紧急眼科评估[15]。
TROP2 ADC安全性的未来展望
ADC药物的安全性管理正经历从“事后补救”向“前瞻预防”的模式转变。临床研究驱动的AE管理优化已成为提升患者获益的关键,通过借鉴COCOON、SKIPPirr及PALOMA等研究的成功范式,实施分层干预与早期预处理(如皮肤保护、输注前给药及预防性抗凝),可降低高等级皮肤毒性、输注相关反应及血栓事件的发生率,从而实现减毒增效的终极目标。
剂量优化策略是提升ADC长期耐受性的重要探索方向,包括基于药代动力学确定的剂量上限管理、针对累积毒性的治疗持续时间限制、通过改变给药频次优化血药峰值,以及依据个体治疗反应实施自适应剂量调整等路径[16]。
整体而言,ADC的安全性管理应遵循用药全程监测原则,通过积极预防、及时诊断、梯度处置及多学科协作,构建覆盖治疗全周期的科学管理体系,以最大化患者获益。
[1]Lenart S, et al. Cancers(Basel). 2020-12(11)-3328
[2]Nguyen TD, Bordeau BM, Balthasar JP. Cancers (Basel). 2023 Jan 24;15(3):718.
[3]Xinlin Liu, et al. Theranostics . 2024 Jun 11;14(9):3674-3692.
[4]Myung-Ju Ahn, et al. ESMO ASIA. 2024.
[5]Luis G Paz-Ares, et al. J Clin Oncol.2024 Aug 20;42(24):2860-2872.
[6]Li Zhang et al. 2025 ASCO Abstract 8507.
[7]Wenfeng Fang, et al. N Engl J Med..2026 Jan 1;394(1):13-26.
[8]2025CSCO抗肿瘤治疗所致中性粒细胞减少症诊断、预防和治疗指南
[9]NCCN指南-造血生长因子(2026 V3)
[10]2025 CSCO肿瘤治疗所致血小板减少症诊疗指南
[11]Apro M et al. Ann Oncol. 2018; 29(4):iv96-iv110
[12]Hope Rugo, et al. Support Care Cancer . 2025 Aug 5;33(9):756.
[13] 芦康沙妥珠单抗说明书
[14]Chunwei Xu, et al. Cancer.2024 Sep 1;130(S17):3054-3066
[15]US Department of Health and Human Services. Common Terminology Criteria for Adverse Events (CTCAE) Version5.0.Available.at:https://ctep.cancer.gov/protocoldevelopment/electronic_applications/docs/ctcae_v5_quick_reference_5x7.pdf
[16]Paolo Tarantino , et al. Nat Rev Clin Oncol . 2023 Aug;20(8):558-576.
排版编辑:肿瘤资讯-Alex











 苏公网安备32059002004080号
苏公网安备32059002004080号


