近期,国际顶尖肿瘤学期刊Journal of Clinical Oncology(JCO)在线发表了一项具有里程碑意义的肝癌随机、开放标签II期临床研究(CHANCE2005/CARES-005)。该研究由东南大学附属中大医院滕皋军院士牵头,联合国内22家中心共同完成。研究聚焦伴有极高肿瘤负荷及大血管侵犯的不可切除肝细胞癌(HCC)患者,证实了“经导管动脉化疗栓塞术(TACE)+PD-1单抗(卡瑞利珠单抗)+VEGFR2抑制剂(阿帕替尼)”的三联疗法,相比于单纯TACE,能够带来无进展生存期(PFS)的显著延长(10.8个月 vs 3.2个月;HR 0.34) 及客观缓解率(ORR)的大幅提升(65% vs 29%)。
在同期发表的社论中,香港中文大学陈林(Stephen L. Chan)教授与Landon L. Chan教授对CHANCE2005/CARES-005的研究价值给予了肯定,同时也以其极具穿透力的视角,向学界提出了关于总生存期(OS)、安全性与临床决策的客观思考。
【肿瘤资讯】特此整合研究核心内容及同期社论精粹,以飨读者。
东南大学医学与生命科学部主任;现任东南大学附属中大医院介入治疗中心主任,主任医师;东南大学首席教授;教育部医药基础研究创新中心主任,国家医学攻关产教融合创新平台负责人,国家综合介入技术质控中心主任。
从事医学影像与介入治疗临床工作40余年,发明和创制多项介入新器械、新技术及新理论,包括建立放射粒子支架的相关技术与理论;阐明肝内门腔静脉分流术(TIPS)支架再狭窄机制;发现多个分子影像和功能影像新靶点;首创了经血管腔内治疗交感神经术治疗2型糖尿病和恶性肿瘤新技术,引领国际前沿。近年来,在人工智能介入机器人领域的创新与转化再获突破。获国家科技进步二等奖3项,发表中英文论文500余篇,授权国内外发明专利30余项,获多个三类医疗注册证。
担任中国医师协会介入医师分会会长,中国医院协会影像中心分会主任委员,国际介入与多学科肿瘤学会(ISMIO)创始主席,EngMedicine期刊主编,亚太心血管与介入放射学会主席(2016-2018)等学术职务。获美国、欧洲及亚太三大主流介入学会最高荣誉奖、中国医师奖、卫生部有突出贡献中青年专家等荣誉。
研究背景与临床需求
1. TACE的临床地位与局限性
经导管动脉化疗栓塞术(TACE)二十多年来一直是中期肝细胞癌(HCC)的标准治疗,在真实世界中(尤其在亚洲)也广泛用于无肝外转移的不可切除HCC患者。然而,受限于肿瘤负荷、肝功能储备及免疫抑制微环境,TACE治疗后的肿瘤复发或进展几乎不可避免,单纯TACE已难以满足高肿瘤负荷患者的生存需求。
2. 免疫+抗血管生成+局部治疗的理论基础
TACE导致的肿瘤坏死可释放肿瘤新抗原,激活抗肿瘤免疫反应;同时,TACE诱导的缺氧微环境会上调VEGF表达。此时联合PD-1单抗(卡瑞利珠单抗)与VEGFR2抑制剂(阿帕替尼),理论上能够通过改善异常血管和逆转免疫抑制微环境,产生强大的协同抗肿瘤作用。
3. 同期社论的时代视角
社论指出,继靶向药物(如索拉非尼)联合TACE在既往随机对照试验(RCT)中未能带来总生存期(OS)获益后,学界曾对此类联合策略热情减退。但近期免疫治疗的进展重新带来了探索方向。该研究(CHANCE2005/CARES-005)成为继EMERALD-1、LEAP-012及TALENTACE三项大型III期临床试验之后,证明“免疫+抗血管生成联合TACE”在不可切除肝局限性HCC中具有类效应(Class effect)和显著无进展生存期(PFS)获益的第四个重要RCT证据。
核心设计:精准定位与中国特色的结合
研究设计
CHANCE2005/CARES-005是一项在中国22个中心开展的随机、开放标签、II期临床试验,入组了200例不可切除、Child-Pugh A级且无肝外转移的HCC患者(BCLC A~C期/CNLC Ib~IIIa期)。患者按1∶1随机分配:
· 试验组(TACE-C-R):在首次TACE后2周内启用卡瑞利珠单抗(200 mg,每3周一次)和阿帕替尼(250 mg,每日一次)。后续TACE治疗遵循“按需(on-demand)”原则实施。
· 对照组(TACE):仅接受按需TACE治疗。
该研究的主要终点采用了具有高度临床实用性的复合无进展生存期(Composite PFS)。该标准不仅包含常规的影像学进展(按RECICL 5标准),还整合了临床决策中的关键因素,包括TACE术后1周内肝功能恶化至Child-Pugh C级,以及依据JSH-LCSGJ标准定义的TACE失败或耐药。
独特的入组人群(高肿瘤负荷)
同期社论特别强调了该研究人群的特殊性与高危特征。与EMERALD-1和LEAP-012试验相比,该研究入组了极高比例的预后不良患者。其中,90%的患者肿瘤负荷超出up-to-7标准,且高达42%伴有大血管侵犯(包括27%具有门静脉主干或一级分支侵犯的Vp3~4型)。在国际通用标准(BCLC分期)中,此类具有严重门静脉侵犯的高肿瘤负荷患者通常被推荐首选系统性治疗而非TACE,这凸显了该研究直面真实世界难治性人群的临床探索价值。
核心数据:突破性的PFS获益与OS的“冷思考”
研究结果显示,TACE联合免疫及抗血管治疗在多个维度上均表现出优于单纯TACE的疗效。
1. PFS的显著获益与肿瘤缓解
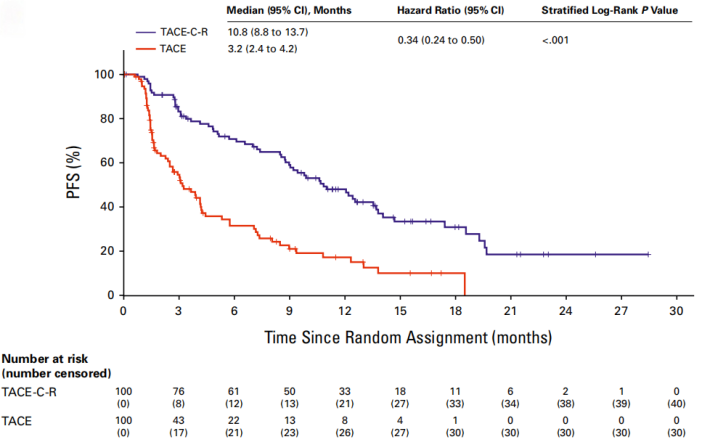
PFS获益:截至数据截止日期(中位随访14.3个月),试验组的中位复合PFS达到了10.8个月,而对照组仅为3.2个月(HR 0.34,95% CI 0.24~0.50, P<0.001)。这一结果意味着疾病进展或死亡风险降低了66%。社论指出,0.34的HR在同类研究中体现了较为明显的获益水平,即便在排除既往治疗干扰后的敏感性分析中,该获益依然稳健。
肿瘤缓解率(ORR)与疾病控制率(DCR):根据RECICL 5标准,试验组的ORR高达65%,对照组为29%;试验组的DCR为87%,对照组为63%;试验组的中位缓解持续时间(DoR)显著延长(11.4个月 vs 6.9个月)。这为后续可能的转化治疗提供了生物学前提。
亚组分析:无论BCLC分期(A/B期 vs C期)或是否存在门脉癌栓(无 vs Vp1~2 vs Vp3~4),试验组的获益趋势均保持一致,这为该联合方案在伴随高危特征患者中的应用提供了依据。
2. OS面临的现实挑战
尽管PFS优势巨大,但OS的获益却相对受限。试验组中位OS为24.0个月,对照组为21.5个月(HR 0.87,95% CI 0.57~1.32)。研究者指出,OS数据目前尚未成熟,且对照组在疾病进展后存在极高的交叉治疗率(75%交叉至试验组方案),可能掩盖了真实的OS差异。
同期社论对此敏锐提出,为何巨大的PFS优势难以转化为长期的OS效应?是否因为前期的强烈联合治疗导致了肝功能的不可逆恶化,从而降低了患者接受后续挽救治疗的机会?抑或肿瘤在联合治疗进展后变得更具侵袭性或耐药性?社论提示,临床医生在面对PFS的延长时,对于患者的最终生存获益仍需保持审慎的评估态度。
3. 安全性数据与生活质量(QoL)的考量
不良事件概况: 试验组≥3级治疗相关不良事件(TRAE)发生率为74.5%,对照组为22.3%,最常见的为天冬氨酸氨基转移酶(AST)升高(31% vs 13%)、丙氨酸氨基转移酶(ALT)升高(24% vs 14%)以及高血压(14% vs 0)。
致死性事件:试验组有3例患者死于TRAE(败血症、脑出血、消化道出血);对照组1例死于肝衰竭。
同期社论的安全性探讨:社论敏锐地指出,74.5%的重度TRAE发生率反映了三联方案的毒性负担,特别是在OS数据尚未成熟、PFS优势未能转化为明确生存获益的当下(LEAP-012研究已宣布因大概率无法达到OS预设终点而计划提前终止),这种负担对患者生活质量的侵蚀是必须审慎评估的平衡点。
讨论与临床启示
基于CHANCE2005/CARES-005研究的重磅结果及同期社论的深度评述,可提炼以下临床启示:
1. 疗效的确证性与靶点协同:该研究成功证明,在不可切除HCC患者中,TACE联合卡瑞利珠单抗与阿帕替尼能够带来统计学和临床意义上均高度显著的PFS和ORR改善,进一步巩固了“TACE+免疫+抗血管生成”三联疗法的可行性。
2. 人群的选择仍具争议:研究纳入了大量超出up-to-7标准及伴Vp3/4门静脉癌栓的高负荷患者。社论指出,单纯TACE在此类人群中PFS仅为3.2个月,这确证了单纯TACE不足以治疗高肿瘤负荷HCC。然而,这类高危人群的OS获益仍需长期随访数据支持,在此之前,系统性全身治疗是否应优先于此类强烈的局部+全身联合治疗,仍需个体化权衡。
3. 终点设定的反思:鉴于该三联疗法ORR极高,社论建议未来此类临床试验应将“获得根治性治疗机会的比例(降期后行手术切除、消融或肝移植)”作为预设的临床终点,这将比单纯讨论难以转化的OS更有实际的临床治愈价值。
4. MDT决策与CUSE框架:社论强调,在全球监管审批存在差异且高毒性负担的现实下,临床决策不应再单一依赖分期。临床医生可参考最新BCLC指南提出的CUSE框架(Complexity复杂性,Uncertainty不确定性,Subjectivity主观性,Emotion情感),由多学科团队(MDT)根据患者的基线肿瘤负荷、肝脏储备功能、后续耐受力及治疗意愿,审慎决策TACE与免疫靶向治疗的“联姻”。
总结
CHANCE2005/CARES-005研究是一项里程碑式的探索,它为高肿瘤负荷的不可切除HCC患者提供了极具价值的循证数据,也为“TACE+免疫+靶向”三联策略再添力证。但正如社论所提示的,在长期OS数据尚未成熟且面临毒性管理的挑战时,这种联合策略能否切实转化为患者的长生存与高质量获益,仍需更长时间的随访数据与更精细的人群筛选来验证。
[1] Zhu HD, Fan WJ, Zhao C, et al. Transarterial Chemoembolization Combined With Camrelizumab and Rivoceranib for Unresectable Hepatocellular Carcinoma (CHANCE2005/CARES-005): A Randomized Phase II Trial. J Clin Oncol. Published online February 24, 2026. doi:10.1200/JCO-25-01796.
[2] Chan LL, Chan SL. Transarterial Chemoembolization and Immunotherapy: Another Good Marriage?. J Clin Oncol. Published online March 2, 2026. doi:10.1200/JCO-26-00015.
排版编辑:肿瘤资讯-ZJN











 苏公网安备32059002004080号
苏公网安备32059002004080号


