骨髓增生异常综合征(MDS)作为起源于造血干细胞的异质性髓系肿瘤,其治疗长期面临靶向药物匮乏、高危患者预后恶劣的困境[1]。尤其异柠檬酸脱氢酶1(IDH1)突变MDS患者,不仅转白风险高、输血依赖率高,且传统治疗疗效有限,生存需求长期未被满足[2]。近期多项失败的3期临床研究进一步证实,MDS靶向治疗研发困难重重[3,4]。而IDH1抑制剂(如艾伏尼布[IVO])的临床探索,为此类人群带来了精准破局的希望,有望重新定义IDH1突变MDS的治疗格局。本期特邀江苏省人民医院的沈文怡教授,立足当前IDH1突变MDS精准治疗的快速发展,整合最新证据,厘清治疗现状与未来方向,以期为临床诊疗提供指引。
临床困局待解:MDS靶向治疗步履维艰
高危人群预后不佳,多线治疗疗效递减
MDS是一组高度异质性的克隆性造血干细胞疾病,其中高危患者的临床预后尤其严峻,据调查显示,超50%的亚洲MDS患者为较高危患者(HR,包括IPSS-R中危、高危和极高危组),且高危MDS发病率明显高于西方国家(IPSS-R高危患者比例:18.43% vs 12.37%,P<0.0001)[5]。这类高危患者较其他相对低危亚型向急性髓系白血病(AML)转化的风险更高(25% AML转化时间中位数 1.4年)、总生存期(OS)更短(中位OS 1.6年)[1]。既往,去甲基化药物(HMA)及异基因造血干细胞移植(allo-HSCT)是HR MDS的标准治疗方案,但HMA疗效有限、allo-HSCT受限于患者年龄、合并症及供体可及性,真实世界中的需求远未得到满足[6,7]。
2025年美国血液学会(ASH)年会公布的一项美国大规模回顾性研究清晰地揭示了这一现状。在1429例接受一线(1L)治疗的MDS患者中,高达74.2%的患者以HMA单药作为起始治疗[8]。然而,缓解率和生存结局随治疗线数增加而急剧恶化:1L治疗的中位OS为22.9个月、中位无进展生存期(PFS)为12.5个月、真实世界总缓解率(rwORR)为31.10%;但至4L+治疗时,中位OS、中位PFS和rwORR分别骤降至10.8个月、7.2个月、14.30%(图1、表1)[8]。
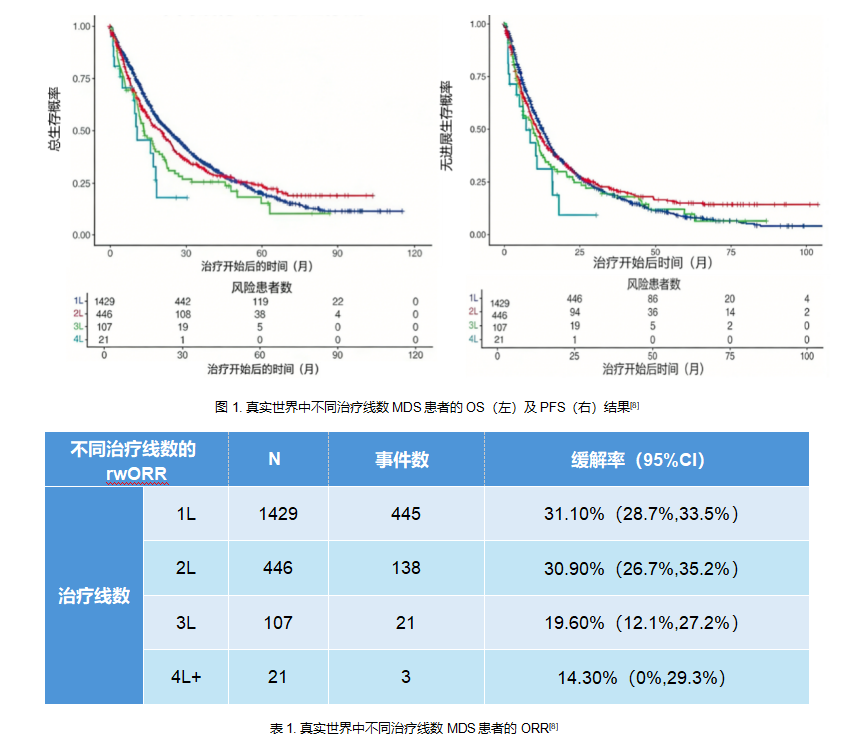
靶向药物研发受阻,联合治疗未改善生存困境
面对MDS传统治疗的失利,靶向药物被寄予厚望,但近年来,HR MDS靶向治疗领域却屡遭挫折,药物研发与临床转化进展缓慢。多项3期关键研究接连失利,如CD47抑制剂Magrolimab(ENHANCE研究)、TIM3抗体Sabatolimab(STIMULUS-MDS2研究)、NEDD8激活酶抑制剂Pevonedistat(PANTHER研究)等均未达到主要终点(图2)[3]。2025年美国血液肿瘤学会(SOHO)大会公布的VERONA 3期研究也显示,维奈克拉(VEN)+阿扎胞苷(AZA)方案未能为HR MDS患者带来OS获益(中位OS:VEN+AZA组22.18个月vs 安慰剂+AZA组21.68个月,HR 0.908,P=0.38),再次印证了MDS靶向药物开发的艰巨性[4]。此外,国际MDS联盟(icMDS)VALIDATE数据库的大规模研究也提供了佐证:在HR MDS患者中,相比HMA单药,HMA+VEN方案虽使复合完全缓解(CRc)率从27.7%升至48.8%(P<0.001),但中位OS无统计学差异(19.6个月 vs 17.4个月,P=0.33),缓解深度与长期生存之间的关联仍需深入探索[9]。
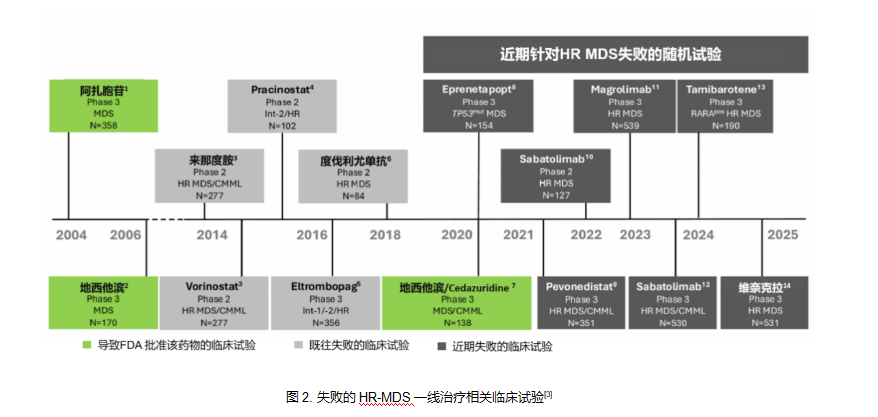
IDH1突变雪上加霜,预后劣势明确
在传统治疗难以突破生存瓶颈的当下,合并IDH1突变往往意味着患者预后更差。2025年ASH大会公布的一项研究数据显示,IDH1突变在MDS中的发生率约为3%,虽不算高发,但其不良预后因素地位十分明确:中性粒细胞绝对计数(ANC)显著低于IDH野生型(P<0.001),感染风险更高;原始细胞比例高于IDH野生型(P=0.003),疾病进展风险更高;同时IDH1突变的IPSS-M HR患者占比相较于IDH野生型也更高(57% vs 44.4%,P=0.02);自身免疫相关疾病发生率达28%,也明显高于IDH野生型及IDH2突变患者(P=0.036),临床管理负担更重;IDH1突变患者向AML转化的风险与IDH野生型相比(45.8% vs 29.1%,P<0.005)存在显著差异[2]。这些都意味着IDH1突变会加重患者的不良结局,让本就有限的治疗手段更难起效,也使其精准靶向治疗的临床需求变得更为迫切。
精准靶向破局:
艾伏尼布治疗IDH1突变MDS曙光初现
IVO疗效卓越,多人群获益明确
为打破预后不佳的僵局,IDH1抑制剂IVO的临床探索率先交出亮眼答卷,已披露的两项研究直接验证了其在不同人群中的多方案应用潜力[10-13]。
AG120-C-001 1期研究聚焦复发/难治(R/R)IDH1突变MDS患者,在18例疗效可评估患者中(IWG 2023疗效标准),ORR为72.2%,其中66.7%患者达到CRc;中位随访27.1个月,中位OS长达35.7个月,其中CRc患者的中位OS尚未达到,研究还观察到生存率与缓解率相关,且在IWG 2006和IWG 2023疗效标准之间显示出相似的趋势(图3)[10,11]。此外,AG120-C-001研究还评估了IVO对IDH1突变R/R MDS患者血液学的影响,结果显示,随治疗周期的增加,ANC、血红蛋白和血小板水平逐步改善并长期维持稳定(图4),60个月时所有血液学指标改善(HI)率均达到100%(IWG 2006疗效标准);83.3%的CRc患者获得或维持非输血依赖(TI),即使非CRc患者也有一半实现TI[11,12]。
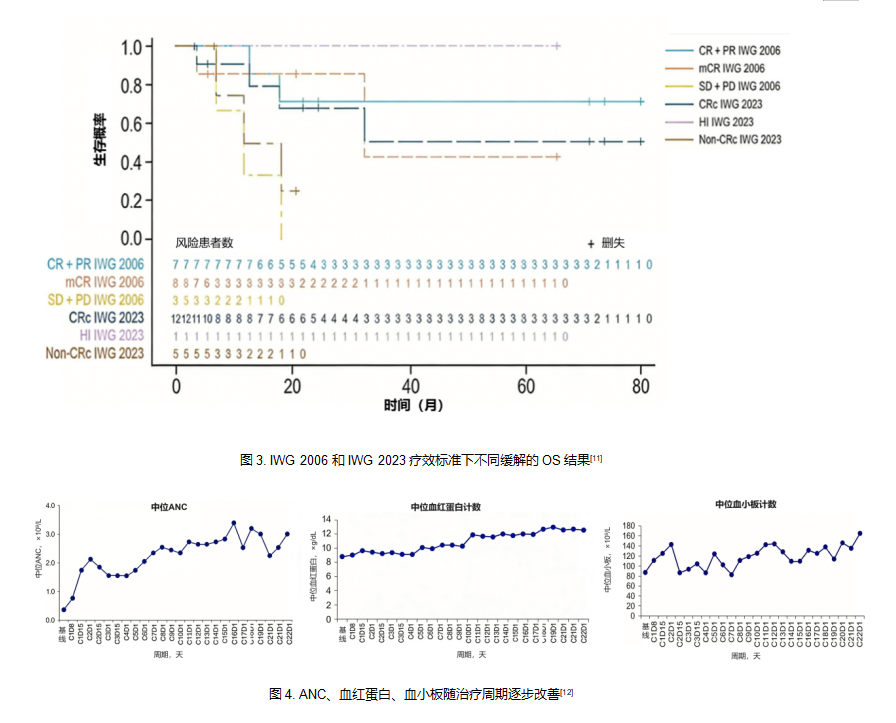
2024年EHA大会公布的IDIOME研究进一步拓展了IVO的适用边界,覆盖新诊断(ND)HR MDS、R/R HR MDS(AZA治疗失败)及R/R低危(LR)MDS(EPO治疗失败)患者,统一接受IVO单药治疗,其中ND HR MDS队列治疗3个周期后未达缓解者再联合AZA治疗[13]。结果显示,ND HR MDS队列中ORR达78%,48%患者实现完全缓解(CR)(图5),中位随访25.2个月时,中位OS与缓解持续时间(DOR)均未达到(图6);R/R HR MDS队列中,ORR 64%(图5),中位OS为8.9个月;即使是3例R/R LR MDS患者,也有2例实现CR,且陆续在治疗3-9周期后实现TI[13]。
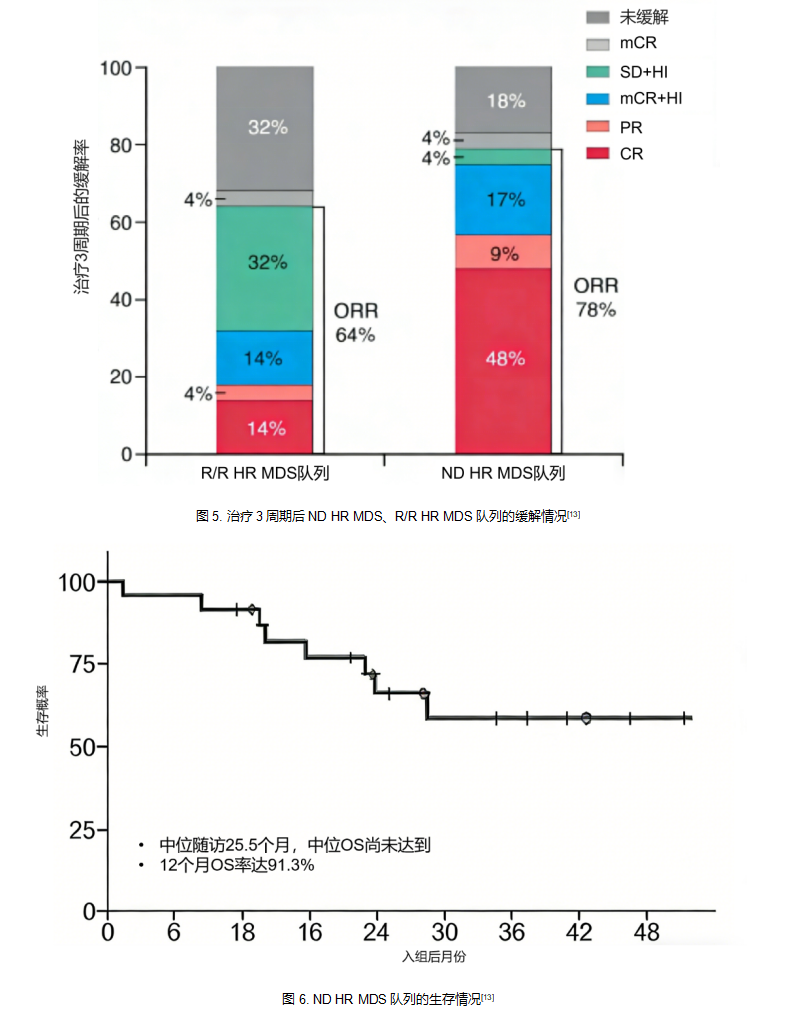
研究探索不止,扩展应用场景
针对IDH1突变髓系疾病的靶向治疗探索仍在不断深入,涉及前瞻性3期研究、联合方案及新药研发,推动IDH1抑制剂从后线向前线、从MDS向更广泛髓系肿瘤领域迈进。
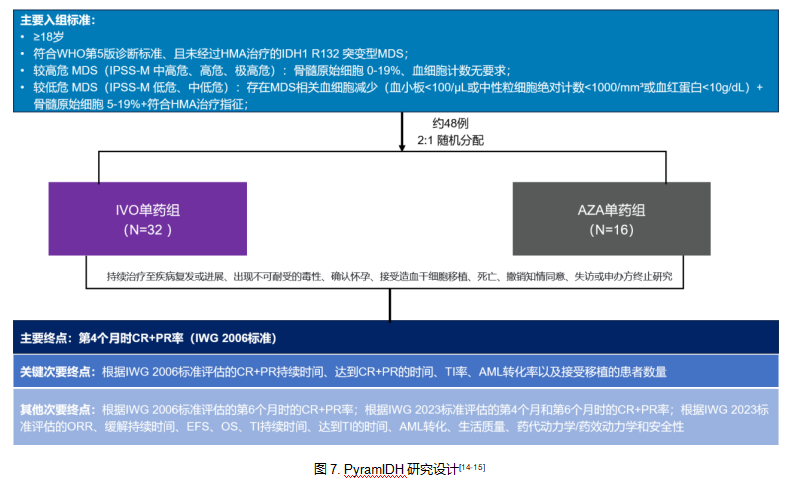
基于前期数据的优秀表现,IVO治疗IDH1突变MDS的3期PyramIDH研究正在进行中(NCT06465953),该研究为多中心、开放标签、随机非对照双臂临床试验,计划纳入48例未经HMA治疗的IDH1 R132突变MDS患者,按2:1比例随机分配至IVO单药组或AZA单药组,并根据IPSS-M精准分层(图7)[14,15]。研究以IWG 2006疗效标准的CR+部分缓解(PR)率为主要终点,预计2027年11月完成主要数据收集,结果将为IVO的标准治疗地位提供更坚实的循证证据[14,15]。
在联合方案的探索方面,2025年ASH大会公布了IVO联合芦可替尼治疗IDH1突变骨髓增殖性肿瘤(MPN)1b期研究(NCT06291987)的研究设计[16]。该研究创新性地将IDH1抑制剂与JAK抑制剂联用,评估IVO联合芦可替尼的安全性与初步疗效,有望为IDH1突变MPN患者提供全新治疗方向,填补此类髓系肿瘤精准治疗的空白[16]。
此外,新型IDH1抑制剂Olutasidenib也展现出明确的临床价值,其1/2期研究(NCT02719574)结果显示,在IDH1突变MDS患者中,Olutasidenib单药或联合AZA的ORR为59%,其中CR率27%、骨髓完全缓解(mCR)率32%;联合治疗组ORR更高(69%),所有ND患者均实现缓解[17]。中位缓解持续时间14.6个月,中位总生存期27.2个月[17]。该研究结果丰富了IDH1突变MDS的治疗格局,IDH1靶向治疗在MDS中的布局正加速推进。
总结
从治疗困局到精准突围,IDH1突变MDS的临床治疗正迎来靶向新纪元。IVO凭借AG120-C-001研究、IDIOME研究的坚实数据,证实其在R/R、ND HR MDS等多个人群中均可实现高缓解率、长期生存及显著的血液学改善,为IDH1突变MDS的精准靶向治疗带来了新的曙光[10-13]。未来,随着更多大型研究数据的披露、联合方案探索的深入及更多真实世界证据的积累,IDH1突变MDS患者有望走出传统治疗的阴霾,真正迈入更加个体化、精准化的治疗时代。
主任医师、副教授、硕士研究生导师
血液髓系肿瘤MDS/MPN亚专科负责人
COMPASS MDS/MPN规范诊疗示范中心负责人
带领团队成为MDS全球卓越中心(MDS center of Excellence)
中国血液病联盟骨髓增殖性肿瘤研究联盟副组长单位负责人
中华医学会血液学分会感染学组委员
中国抗癌协会第五届血液肿瘤专业委员会髓系学组委员
江苏省第十四批六大高峰人才
江苏省医学会血液学分会感染学组委员
江苏省卫计委科教强卫工程医学青年人才
江苏省免疫学会血液免疫专业委员会委员
[1]. 中国临床肿瘤学会(CSCO). 恶性血液病诊疗指南 2025.
[2]. Komrokji R, et al. 2025 ASH Poster 3851.
[3]. Stahl MF, et al. Blood. 2025 Nov 1:blood.2025029727.
[4]. GarciaManero, et al. 2025 SOHO MDS-1497.
[5]. Jiang Y, et al. Cancers (Basel). 2021 Jan 27;13(3):481.
[6]. 中华医学会血液学分会. 中华血液学杂志, 2019, 40(2) : 89-97.
[7]. Nikolopoulos T, et al. Mol Med. 2025 Feb 14;31(1):59.
[8]. Diego Andres Adrianzen Herrera, et al. 2025 ASH Oral 601.
[9]. Bewersdorf J, et al. 2025 ASH Oral 606.
[10]. DiNardo CD, et al. Blood Adv. 2024 Aug 13;8(15):4209-4220.
[11]. Madanat YF, et al. 2024 ASH Poster 1841.
[12]. Prince GT, et al. 2024 ASH Poster 3226.
[13]. Sebert M, et al. 2024 EHA Oral S182.
[14]. Santini V, et al. 2025 ASCO TPS6584.
[15]. https://clinicaltrials.gov/study/NCT06465953
[16]. Patel AA, et al. 2025 ASH Poster 5608.
[17]. Cortes JE, et al. Blood Adv. 2025 Oct 28;9(20):5293-5305.
免责声明:
本资料的内容仅作为科学信息参考,仅用于医疗卫生专业人士的学术交流,请勿用于任何其他用途。若您不是医疗卫生专业人士,请勿观看和/或传播此资料。
本资料可能会出现某些药品信息,但该药品/适应症可能尚未获得国家药品监督管理局的注册批准。医疗卫生专业人士做出的任何与治疗有关的决定应根据患者的具体情况并应参照国家药品监督管理局批准的药品说明书。对于本资料可能提到的相关诊断、治疗方法,请遵守国家卫生健康委员会以及相关部门批准使用的指南或规定。
审批号:M-TIBSO-CN-202603-00004











 苏公网安备32059002004080号
苏公网安备32059002004080号


