

晚期胃和胃食管结合部(G/GEJ)腺癌的治疗已从单一化疗迈向多靶点精准治疗时代。随着PD-(L)1抑制剂以及针对Claudin 18.2(CLDN18.2)的靶向抗体佐妥昔单抗相继获批一线使用,临床医生面临着在双生物标志物阳性患者中如何优化选择的难题。本文基于现有临床数据,从生物标志物判读的可靠性、生存获益的梯度效应、毒性特征的差异性、合并用药影响以及真实世界安全性等维度进行深度剖析。

一、研究背景:
晚期胃癌生存挑战与分子靶向突破
胃和胃食管结合部(G/GEJ)腺癌是全球范围内高发且致死率较高的恶性肿瘤,晚期阶段的5年生存率仅为5%至10% [1] 。长期以来,含铂化疗一直是治疗的基石,但获益十分有限。近年来,免疫检查点抑制剂(ICI)通过阻断PD-1/PD-L1通路,显著改善了PD-L1阳性患者的生存预后,成为标准治疗的重要组成部分。与此同时,CLDN18.2这一紧密连接蛋白因其在恶性转化过程中暴露于细胞表面并可被靶向,成为近年胃癌研究的热门靶点 [2-4] 。
佐妥昔单抗作为针对该靶点的首创IgG1单克隆抗体,通过SPOTLIGHT [5] 和GLOW研究 [6] 确立了其在一线治疗中的地位。然而, 当患者肿瘤同时表达CLDN18.2且PD-L1组合阳性评分(CPS)≥1时,如何在两种创新方案之间平衡选择,是当前肿瘤学界关注的临床议题 。

二、生物标志物检测:
精准决策的基石与挑战

CLDN 18.2
精准医疗的决策高度依赖于生物标志物检测的可信度与稳健性。 在佐妥昔单抗的临床应用中,CLDN18.2检测展现出较高的判读稳定性。 在相关的III期试验中,获益人群定义为:经验证的免疫组化(IHC)检测显示≥75%的肿瘤细胞呈现中至强度的胞膜染色 [5,6] 。流行病学数据显示,CLDN18.2在胃癌中的阳性率约为40% [7] 。此外,一项全球环评研究证实,CLDN18.2的测量在不同实验室间的准确性≥85% [8] ,为临床筛选获益人群提供了坚实的客观依据。

PD-L1
相比之下, PD-L1 CPS检测在实际应用中面临一定的判读一致性挑战,尤其是在低表达范围内。 数据显示,在CPS=1的阈值下,不同病理学家间的整体判读一致性仅为31% [9] ;即使在CPS=10的阈值下,一致性也仅提升至68% [9] 。此外,不同免疫药物对应不同的检测平台且不可互换,增加了临床检测的复杂性。在表达率分布上,PD-L1的表达呈现明显的层级特征:PD-L1 CPS≥10的患者约占总人群的16%,而约有50%~60%的患者处于CPS 1~9的区间,约30%的患者PD-L1 CPS<1 [10] 。
这种生物标志物检测特征的差异直接影响了临床路径的选择。在制定一线治疗方案时,生物标志物检测的可靠性已成为肿瘤科医生评估治疗方案确定性与风险收益比的重要参考依据。

CSCO胃癌诊疗指南(2025版)分子诊断推荐

ASCO晚期胃食管癌指南(2026版)生物标志物检测推荐

三、疗效深度解析:
关键临床试验数据
在缺乏直接头对头对比数据的情况下,通过对CheckMate-649 [11] 、KEYNOTE-859 [11] 与SPOTLIGHT [5] 、GLOW研究 [6] 的描述性评估,可以观察到两种方案各具特色的疗效图谱。
免疫治疗方案展现出明显的获益梯度效应,其生存改善程度与PD-L1表达水平呈正相关。



免疫治疗方案
在 CheckMate-649研究 中,纳武利尤单抗联合化疗相比于单用化疗的总生存期(OS)HR在CPS≥10、≥5和≥1的人群中分别为0.67、0.69和0.74,CPS<10和<1的人群仅为0.91和0.98,CPS≥1~<5、≥1~<10、≥5~<10的人群分别为0.93、0.88和0.80 [11] 。
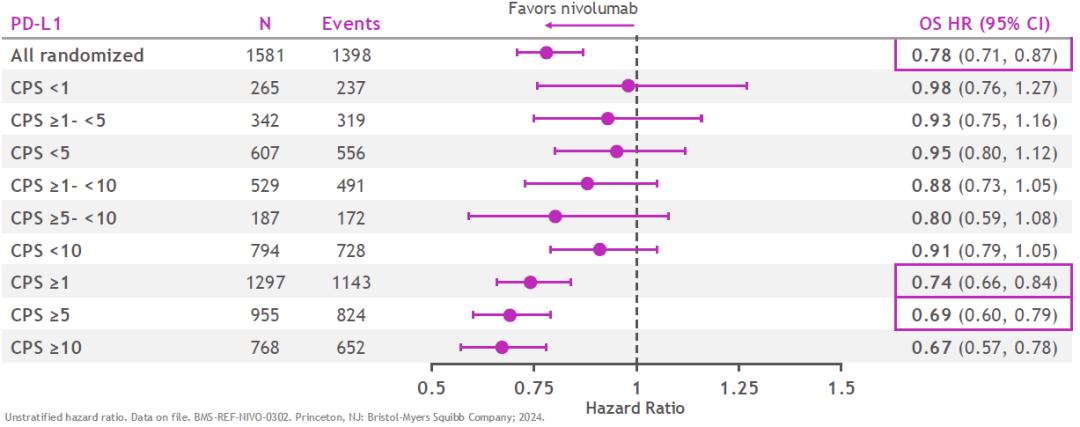
CheckMate 649研究中各PD-L1亚组的OS结果
KEYNOTE-859研究 也观察到类似趋势,帕博利珠单抗联合化疗相比于单用化疗的OS HR在CPS≥10、≥5和≥1的人群中分别为0.64、0.70和0.73,CPS<10和<1的人群仅为0.86和0.92,CPS≥1~<5、≥1~<10、≥5~<10的人群分别为0.78、0.83和0.93 [11] 。
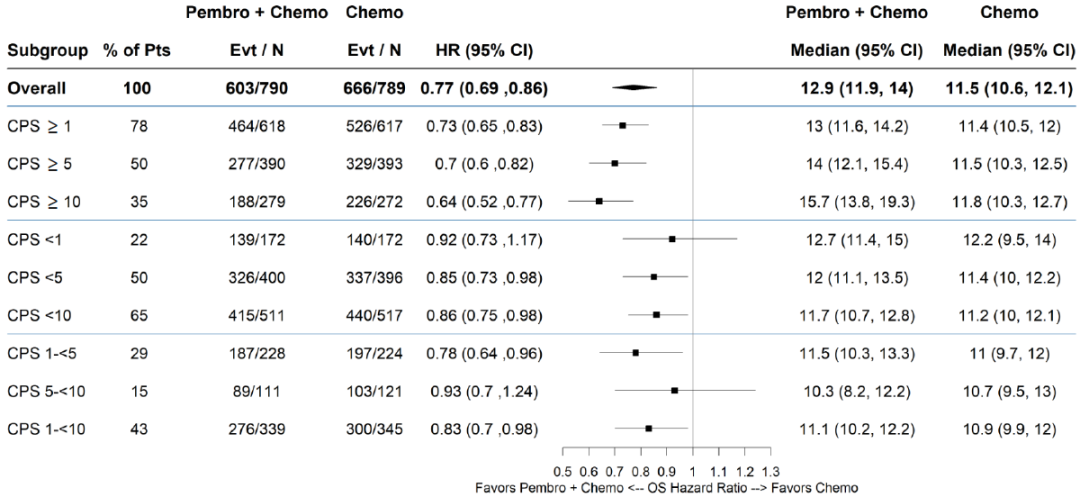
KEYNOTE-859研究中各PD-L1亚组的OS结果
综合上述数据分析, 免疫治疗在整体人群中所展现出的生存获益,很大程度上是由CPS≥10这一亚组人群的疗效所驱动的。而从CPS<10人群的OS HR来看,其临床获益并不明显。



靶向治疗方案
佐妥昔单抗在CLDN18.2阳性人群中展现出稳健且一致的疗效改善。
SPOTLIGHT研究中,佐妥昔单抗联合mFOLFOX6的中位无进展生存期(PFS)为10.61个月,中位OS为18.23个月 [5] 。
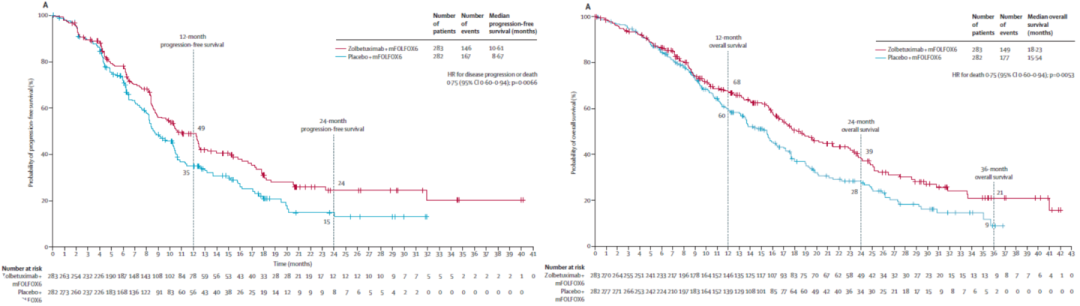
SPOTLIGHT研究的PFS和OS结果
GLOW研究中,佐妥昔单抗联合CAPOX的中位PFS和中位OS分别为8.21个月和14.39个月 [6] 。 尽管两项研究因地理分布及患者构成差异导致绝对生存值有所不同,但其风险比高度一致,PFS HR在0.75至0.77之间,OS HR在0.69至0.75之间 [5,6] 。值得注意的是,佐妥昔单抗的疗效并不受 PD-L1 表达水平的影响。
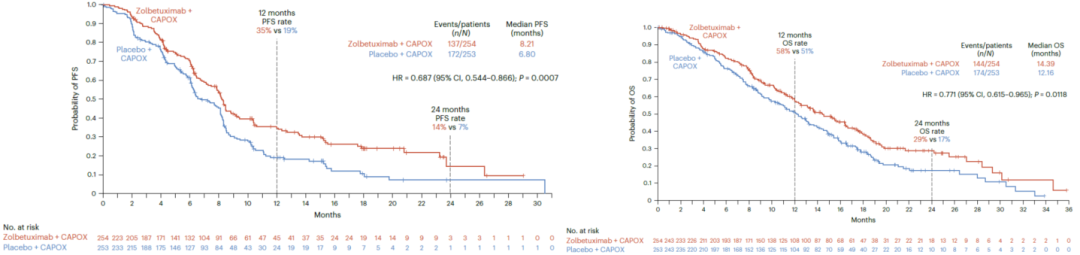
GLOW研究的PFS和OS结果

四、安全性Profile与管理:
短期不适与长期风险的权衡
两种方案的毒性特征各异,影响着临床管理重点。

靶向治疗方案
佐妥昔单抗主要副作用为消化道毒性,以恶心和呕吐最为显著。这些事件通常发生在首次输注的1小时内,但随治疗周期的推进而显著递减。通过实施包含5-HT3受体拮抗剂、NK-1受体拮抗剂、地塞米松及奥氮平的四联止吐方案,并适当减缓首次输注速度,可有效管理症状。真实世界研究数据显示,随着治疗周期的增加,恶心呕吐的频率显著下降,到第三周期时呕吐发生率已极低,输注完成率可达到100% [12] 。

免疫治疗方案
免疫治疗的总体耐受性良好,但需关注免疫相关不良事件(irAE)。irAE具有不可预测性和潜在的延迟性,中位发生时间约为40天。荟萃分析显示,胃癌ICI治疗相关的irAE总体发生率为16%,其中严重事件占3%,致死性事件占1%(主要死因为结肠炎和间质性肺病) [13] 。在获益梯度的低端人群(如CPS<10)中,临床医生需在预期的生存获益与潜在的毒性风险之间进行更为细致的权衡。

五、治疗建议:
个性化的决策路径
晚期G/GEJ腺癌的一线治疗决策正从单一标志物筛选转向更为综合的分子亚型评估。目前,针对CLDN18.2和PD-L1双阳性人群,探索 “靶向+免疫+化疗” 的联合模式已成为临床研究热点。
这种“靶免化”联合机制的核心在于利用协同效应:通过CLDN18.2靶向药物诱导的抗体依赖性细胞毒性(ADCC)作用,促进肿瘤抗原释放,改善肿瘤微环境的免疫原性(使“冷”肿瘤变“热”),进而增强PD-1抑制剂的免疫打击效力。
目前,旨在验证“靶免化联合”临床价值的III期研究正在全球范围内推进。这类研究通过不同机制的协同与碰撞,有望为患者构建更具优势的治疗模式。


在上述联合方案获得大规模III期临床确证数据并正式获批之前,基于现有临床研究证据,可形成如下相对清晰的治疗决策参考:
对于 HER2阴性且CLDN18.2阳性 的胃/胃食管结合部肿瘤患者,
• 当 PD-L1 CPS<1 时,佐妥昔单抗联合化疗是具有临床价值的治疗选择;
• 当 CPS≥10 时,免疫治疗已显示出较为明确的生存获益;
对于 CPS处于低表达区间(如1–<5) 的患者,考虑到该区间CPS判读一致性相对有限,且免疫治疗的总生存获益相对有限,可将佐妥昔单抗联合化疗作为一线治疗选择之一。
对于 CPS 5–<10 的中间区间患者,现有证据提示免疫治疗可能带来一定生存获益,但在这一双标志物共存 的人群中,CPS评分及其判读的可靠性仍是临床实践中 的重要考量因素。在此背景下,基于CLDN18.2这一明确靶点的治疗策略同样具有重要参考价值。
总体而言,在CLDN18.2阳性人群中,治疗决策需结合PD-L1表达水平、生物标志物判读稳定性以及患者具体情况进行综合判断,以实现更为合理的个体化治疗选择。
参考文献
[1] Casamayor M, Morlock R, Maeda H, Ajani J. Targeted literature review of the global burden of gastric cancer. Ecancermedicalscience. 2018 Nov 26;12:883.
[2] Rohde C, Yamaguchi R, Mukhina S, et al. Comparison of Claudin 18.2 expression in primary tumors and lymph node metastases in Japanese patients with gastric adenocarcinoma. Jpn J Clin Oncol. 2019 Sep 1;49(9):870-876.
[3] Hato SV, Khong A, de Vries IJ, et al. Molecular pathways: the immunogenic effects of platinum-based chemotherapeutics. Clin Cancer Res. 2014 Jun 1;20(11):2831-7.
[4] Türeci O, Sahin U, Schulze-Bergkamen H, et al. A multicentre, phase IIa study of zolbetuximab as a single agent in patients with recurrent or refractory advanced adenocarcinoma of the stomach or lower oesophagus: the MONO study. Ann Oncol. 2019;30(9):1487-1495.
[5] SHITARA K, LORDICK F, BANG YJ, et al. Zolbetuximab plus mFOLFOX6 in patients with CLDN18.2-positive, HER2-negative, untreated, locally advanced unresectable or metastatic gastric or gastro-oesophageal junction adenocarcinoma (SPOTLIGHT): a multicentre, randomised, double-blind, phase 3 trial. Lancet. 2023;401(10389):1655-1668.
[6] SHAH MA, SHITARA K, AJANI JA, et al. Zolbetuximab plus CAPOX in CLDN18.2-positive gastric or gastroesophageal junction adenocarcinoma: the randomized, phase 3 GLOW trial. Nat Med. 2023;29(8):2133-2141.
[7] Shitara K, Xu RH, Ajani JA, et al. Global prevalence of claudin 18 isoform 2 in tumors of patients with locally advanced unresectable or metastatic gastric or gastroesophageal junction adenocarcinoma. Gastric Cancer. 2024;27(5):1058-1068.
[8] Jasani B, Taniere P, Schildhaus HU, et al. Global Ring Study to Investigate the Comparability of Total Assay Performance of Commercial Claudin 18 Antibodies for Evaluation in Gastric Cancer. Lab Invest. 2024;104(1):100284.
[9] Fernandez AI, Robbins CJ, Gaule P, et al. Multi-Institutional Study of Pathologist Reading of the Programmed Cell Death Ligand-1 Combined Positive Score Immunohistochemistry Assay for Gastric or Gastroesophageal Junction Cancer. Mod Pathol. 2023;36(5):100128.
[10] Schoemig-Markiefka B, Eschbach J, Scheel AH, et al. Optimized PD-L1 scoring of gastric cancer. Gastric Cancer. 2021;24(5):1115-1122.
[11] September 26, 2024: Meeting of the Oncologic Drugs Advisory Committee Meeting Announcement - 09/26/2024 | FDA
[12] Kameishi S, Hirano H, Hirose T, et al. Safety and efficacy of zolbetuximab plus chemotherapy for CLDN18.2-positive gastric cancer: A single-center retrospective study. 2026 ASCO GI, abstr 308.
[13] Pei WG, Chen WZ, Wu YK, et al. Immune-related adverse events associated with immune checkpoint inhibitors for advanced gastric and gastroesophageal junction cancer: A meta-analysis. World J Gastrointest Oncol. 2023;15(2):352-367.
[14] Easaw JC, Lim HJ, Karachiwala H, Gill S, Zhu X, Bateman J. Zolbetuximab or Immunotherapy as the Initial Targeted Therapy in CLDN18.2-Positive, HER2-Negative Advanced Gastric Cancer: Weighing the Options. Curr Oncol. 2025;32(11):648.
审批编号:MAT-CN-VYL-2026-00054
审批时间:2026-3-18
材料有效期:2027-3-18












 苏公网安备32059002004080号
苏公网安备32059002004080号


