来源:肿瘤资讯
在血液肿瘤的治疗史上,从化疗到靶向治疗的转变堪称一场静默的革命。在这场革命中,布鲁顿酪氨酸激酶(BTK)抑制剂的问世,无疑是浓墨重彩的一笔。自首个BTK抑制剂伊布替尼获批用于慢性淋巴细胞白血病(CLL)以来,这类药物已深刻改变了多种B细胞恶性肿瘤及免疫介导性疾病的管理模式。它们不再仅仅是“化疗替代者”,而是演变为一种能够实现长期、甚至“无化疗”管理的多功能治疗平台。一篇近期发表于Biomolecules期刊的综述,系统梳理了BTK抑制剂的作用机制、临床证据、安全谱及其在血液病领域的广泛应用,为我们勾勒出一幅从“靶向”到“精准序贯”的治疗新图景。【肿瘤资讯】将提炼该综述的核心内容,带您一窥BTK抑制剂如何破局传统治疗,重塑当下的临床实践。

研究背景:BTK——B细胞信号通路的关键枢纽
BTK是B细胞受体(BCR)信号通路中的核心分子。在正常B细胞中,BCR信号对于细胞的生存、增殖和分化至关重要。然而,在多种成熟B细胞恶性肿瘤[如CLL、套细胞淋巴瘤(MCL)、边缘区淋巴瘤(MZL)等]中,这一信号通路常常被异常激活,成为肿瘤细胞赖以生存的“生命线”。BTK正是这条生命线上的关键节点。它不仅能传导来自BCR的“生长”信号,还参与肿瘤细胞与周围微环境的“对话”,促进其归巢、黏附和存活。
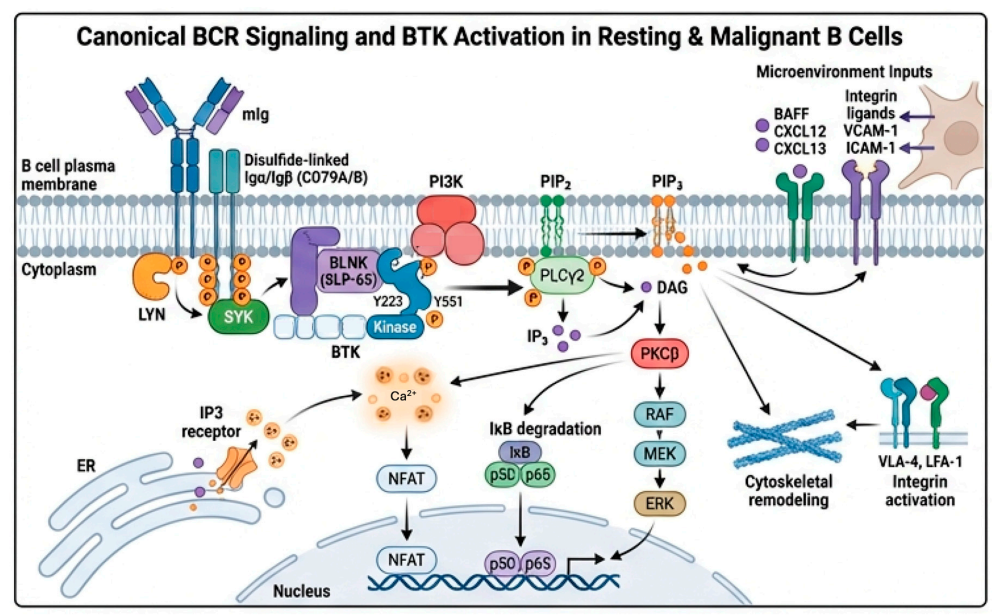
靶向抑制BTK,相当于切断了肿瘤细胞的多个关键生存途径。共价BTK抑制剂(如伊布替尼、阿可替尼、泽布替尼)通过与BTK蛋白上的C481位点不可逆结合,“锁死”其功能,从而强效抑制下游信号,导致肿瘤细胞从庇护所(如淋巴结)释放至外周血,并最终走向凋亡。然而,肿瘤细胞的狡猾之处在于,它会在治疗压力下发生基因突变,其中最常见的便是BTK的C481S突变,使得共价抑制剂无法有效结合,从而产生耐药。这一挑战催生了非共价BTK抑制剂(如匹妥布替尼)的诞生,它们不依赖C481位点,能够绕过经典的耐药机制,为后线治疗提供了新的“武器”。
临床证据:从一线到后线,从单药到联合
综述的核心部分详细梳理了BTK抑制剂在不同疾病、不同治疗线数中的关键临床试验证据,揭示了其治疗地位的不断演进。
表1.BTK抑制剂一线治疗相关临床试验证据
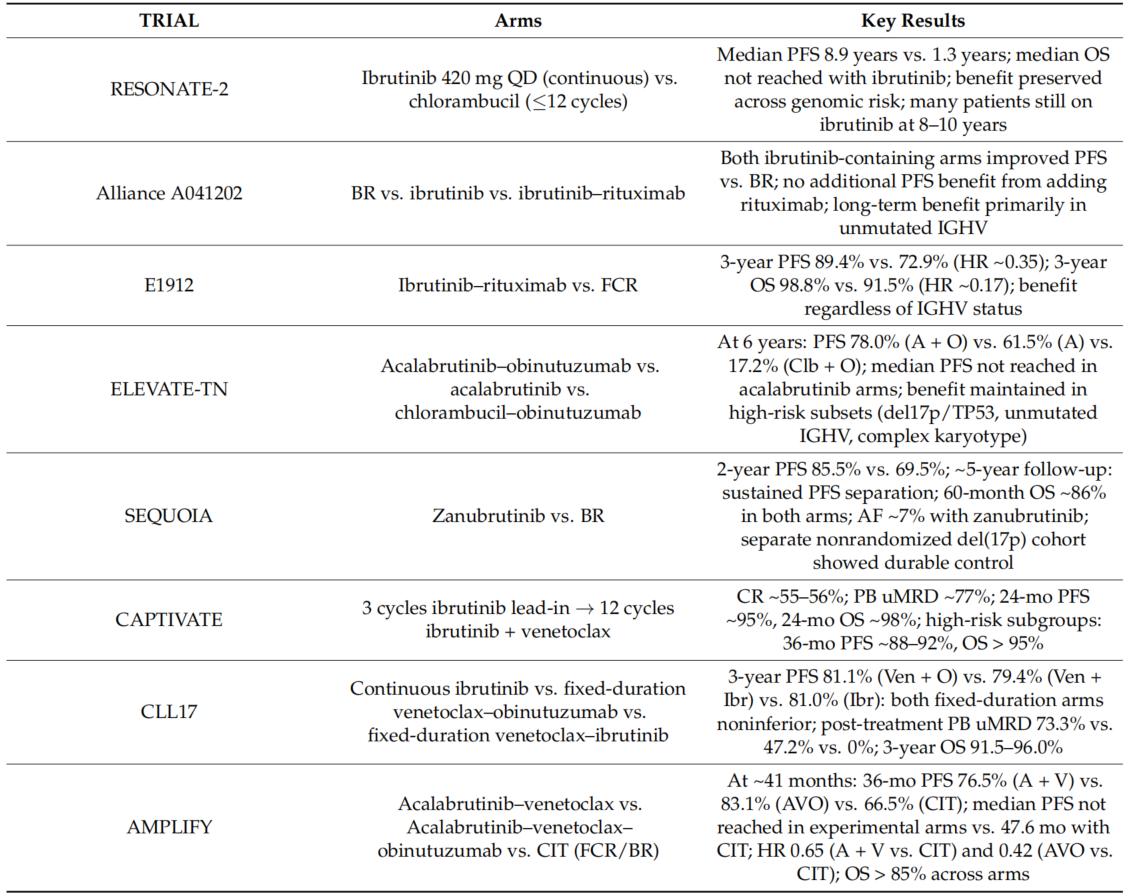
在CLL/SLL中的里程碑式突破:
一线治疗:确立“无化疗”标准。 早期的RESONATE-2研究首次证明,在老年、存在合并症的初治CLL患者中,单药伊布替尼相比传统化疗(苯丁酸氮芥),能将中位无进展生存期(PFS)从1.3年大幅延长至8.9年,且安全性可接受。随后的Alliance A041202和E1912研究进一步证实,伊布替尼为基础的治疗方案,无论是在老年还是年轻、体能状态好的患者中,其疗效均显著优于传统的化学免疫疗法(如BR、FCR)。
新一代BTK抑制剂的优效性。 随着第二代共价BTK抑制剂阿可替尼和泽布替尼的出现,治疗格局再次优化。ELEVATE-TN和SEQUOIA研究分别证实,阿可替尼联合奥妥珠单抗或泽布替尼单药,在一线治疗中均能带来持久PFS,且在高危患者(如伴del(17p)/TP53突变)中同样有效。ALPINE研究更是直接比较了泽布替尼与伊布替尼在复发/难治性CLL中的疗效,结果显示泽布替尼不仅在PFS上显示出优效性,其房颤、高血压等心血管不良事件的发生率也显著降低。
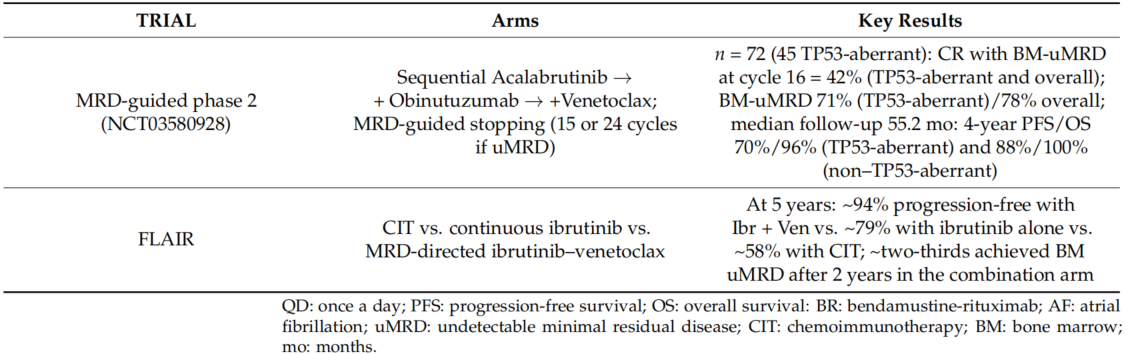
固定疗程与MRD驱动策略的兴起。 为了减少长期用药带来的毒性、耐药和经济负担,“有限期治疗”成为新的探索方向。CAPTIVATE研究显示,伊布替尼联合维奈克拉(BCL2抑制剂)固定疗程治疗,能在初治CLL中实现深度缓解和持久的治疗“假期”。CLL17和AMPLIFY研究则分别证实,固定疗程的维奈克拉联合奥妥珠单抗或伊布替尼/阿可替尼,其PFS非劣效于连续伊布替尼治疗,且能获得更高的微小残留病(MRD)阴性率。FLAIR和一项MRD指导的Ⅱ期研究更是将这一理念推向深入,实现了根据MRD状态个体化停药,在保证疗效的同时,显著降低了患者的治疗暴露。
后线治疗的迭代与序贯。 对于复发/难治性患者,ELEVATE-RR研究证实,阿可替尼的疗效不劣于伊布替尼,但安全性更优。ASCEND研究则确立了阿可替尼相比PI3K抑制剂或化疗联合方案的优效地位。当患者对共价BTK抑制剂耐药后,非共价抑制剂匹妥布替尼(BRUIN CLL-321研究)成为挽救治疗的有效选择,尤其适用于那些已经过BTK抑制剂和BCL2抑制剂“双重暴露”的患者。对于这类患者,CAR-T细胞疗法(如lisocabtagene maraleucel)也展现出有前景的疗效。
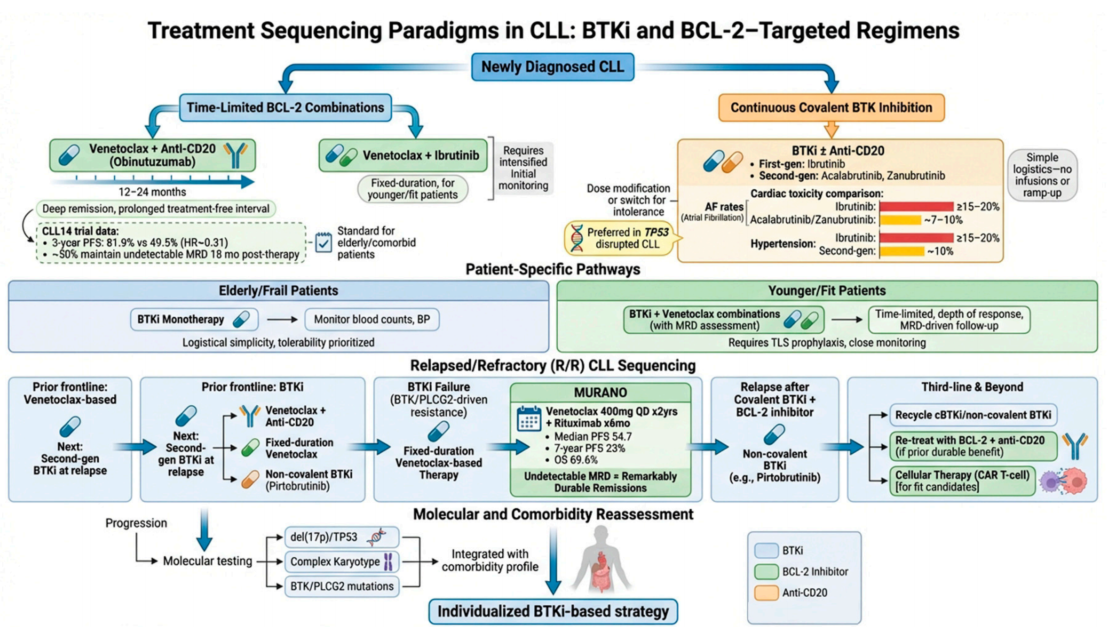
在其他B细胞淋巴瘤中的应用:
套细胞淋巴瘤(MCL): BTK抑制剂在MCL中同样成效显著。从最初在复发/难治性MCL中的单药有效,到RAY研究证实伊布替尼优于替西罗莫司,再到SHINE和TRIANGLE研究将BTK抑制剂推向一线和年轻患者的移植前诱导及维持治疗,其治疗地位不断提升。阿可替尼和泽布替尼在MCL中也显示出高缓解率和良好的耐受性,尤其是泽布替尼在多项研究中展现出极高的完全缓解率。
边缘区淋巴瘤(MZL)与华氏巨球蛋白血症(WM): BTK抑制剂已成为MZL和WM的标准治疗选择之一。泽布替尼在MZL的MAGNOLIA研究中取得了68%的客观缓解率。在WM中,INNOVATE研究确立了伊布替尼联合利妥昔单抗的优效性,而ASPEN研究则显示泽布替尼在疗效不劣于伊布替尼的同时,心血管毒性更低。
超越B细胞淋巴瘤的拓展:
慢性移植物抗宿主病(cGVHD): 伊布替尼因其同时抑制BTK和ITK(T细胞上的一个关键激酶)的双重作用,被成功应用于激素难治性cGVHD的治疗,可有效调节B细胞和T细胞的异常活化,恢复皮质类固醇敏感性。
免疫性血小板减少症(ITP): 新型口服可逆BTK抑制剂Rilzabrutinib在Ⅲ期LUNA3试验中,为既往治疗失败的慢性ITP患者带来了显著的持续血小板应答,展示了BTK抑制在自身免疫性疾病中的广阔前景。
安全性考量与临床管理
尽管BTK抑制剂开启了治疗新纪元,但伴随的毒性管理不容忽视。综述指出,不同BTK抑制剂的毒性谱差异主要源于其激酶选择性的不同。
心血管毒性: 这是最受关注的类效应。第一代伊布替尼因其对EGFR、TEC等激酶的脱靶抑制,房颤、高血压的发生率较高(约15-20%)。第二代共价抑制剂阿可替尼和泽布替尼,因更强的BTK选择性,将房颤发生率显著降低至约7-10%,高血压也控制在10%左右。
出血与感染: 出血(主要为1-2级瘀伤)和感染(尤其治疗初期)是另一类常见不良事件。临床管理强调术前暂停用药、避免合用强效抗血小板药物,以及常规进行疫苗接种和必要的抗感染预防。
药物相互作用: BTK抑制剂多经CYP3A酶系代谢,与质子泵抑制剂、强效CYP3A抑制剂/诱导剂存在相互作用,需在处方时仔细评估。
未来展望与待解之题
展望未来,综述指出了BTK抑制剂领域多个值得关注的发展方向和亟待填补的研究空白:
优化联合与序贯策略: 核心问题不再是“是否有效”,而是“如何最佳组合”。固定疗程的BTK抑制剂联合BCL2抑制剂(如维奈克拉)已在CLL中成熟,未来将在MCL、WM中进一步验证。如何合理安排共价与非共价BTK抑制剂的序贯使用,尤其是在“双耐药”患者中,是临床面临的现实挑战。
精准分层与生物标志物: 在弥漫大B细胞淋巴瘤(DLBCL)等异质性较强的疾病中,BTK抑制剂的疗效仅限于特定的分子亚型(如ABC型)。未来需要通过更精细的基因和转录组图谱分析,识别出真正能从BTK单药或联合治疗中获益的患者群体,避免“一刀切”式的无效治疗。
完善耐药监测: 随着BTK抑制剂的广泛应用,耐药问题日益突出。建立标准化的耐药监测体系,不仅检测经典的BTK C481S和PLCG2突变,更要关注非经典突变和旁路激活机制,是指导精准序贯治疗的关键。
拓展新适应症: 除了cGVHD和ITP,BTK抑制在自身免疫性疾病(如多发性硬化)、过敏性炎症甚至实体瘤中的应用潜力正在被积极探索,有望将BTK靶向治疗带入更广阔的医学领域。
下一代BTK靶向策略: 除了现有抑制剂,新型BTK蛋白降解剂(如NX-2127、BGB-16673)已进入临床早期探索阶段。这些药物能同时降解野生型和突变型BTK,有望克服现有药物的耐药问题,为“后BTK抑制剂”时代的患者带来新的希望。
总结
综上所述,从CLL/SLL的一线无化疗治疗,到MCL、MZL、WM的标准治疗,再到cGVHD和ITP的新兴应用,BTK靶向治疗深刻重塑了血液病的治疗范式。随着第二代、非共价抑制剂以及未来蛋白降解剂的问世,治疗的有效性与安全性得以不断优化。然而,面对耐药机制的复杂性、治疗方案的多样性和患者群体的异质性,临床医生和研究者仍需共同努力,通过精准的患者分层、优化的联合/序贯策略和创新的药物研发,将BTK抑制剂的应用推向一个新的高度,最终实现为每一位患者提供“个体化”、“最大化获益、最小化风险”的精准医疗目标。
Duminuco A, De Luca P, Stanzione G, et al. BTK Inhibition in Hematology: From CLL/SLL to Emerging Applications Across B-Cell and Immune Disorders[J]. Biomolecules, 2026, 16(1): 123.
排版编辑:Mathilda











 苏公网安备32059002004080号
苏公网安备32059002004080号


