自2007年Soda等首次在非小细胞肺癌中鉴定出具有转化活性的EML4-ALK融合基因以来,针对该靶点的治疗极大地改观了患者的生存预期。与ALK在结构上高度相似的ROS1基因,其重排同样能导致受体酪氨酸激酶(TKR)的持续激活,从而驱动肿瘤细胞的增殖与存活。尽管ROS1融合仅占所有NSCLC的1%-2%,但其在不吸烟的女性腺癌患者中具有显著代表性。
然而,在临床实践中,中枢神经系统(CNS)转移始终是此类患者治疗的巨大痛点。在ROS1阳性NSCLC中,CNS是极常见的初始疾病进展部位。约20%-40%的患者在诊断时即伴有CNS转移,而在疾病进展时,这一比例更是攀升至约47%。早期第一代(如克唑替尼)和部分第二代靶向药物面临着血脑屏障(BBB)的严峻挑战。血脑屏障中广泛存在的药物外排转运蛋白(如P-gp和BCRP)会通过主动外排机制将药物泵出,导致中枢神经系统内的药物暴露量不足。因此,大脑往往成为肿瘤生长的“庇护所”,导致患者在系统性疾病得到控制的情况下,依然面临致命的颅内进展。
一线治疗的代际演进与关键数据解析
过去十余年间,ALK与ROS1抑制剂(TKI)经历了从第一代到第三代的迅速演进,其核心驱动力在于提高靶点亲和力与突破血脑屏障。
ALK抑制剂的一线治疗演进
第一代(克唑替尼):PROFILE 1014研究奠定了其一线地位,客观缓解率(ORR)为74%,中位无进展生存期(PFS)为10.9个月。
第二代(阿来替尼、布格替尼、恩沙替尼等):这一代药物显著提升了CNS穿透性。
阿来替尼(Global ALEX 5年随访数据):中位PFS达到34.8个月(HR 0.43),整体ORR达83%,颅内ORR达81%。
布格替尼(ALTA-1L):中位PFS为30.8个月(HR 0.49),ORR 71%,颅内ORR达78%。
恩沙替尼(eXalt3):中位PFS为25.8个月(HR 0.51),ORR达74%,颅内ORR 63.6%。
第三代(洛拉替尼):CROWN研究的5年更新数据显示:中位PFS尚未达到,其相对于克唑替尼的进展或死亡风险大幅降低了81%(HR 0.19)。整体ORR为76%,颅内ORR 66%,在仅有可测量病灶的患者中颅内ORR达82%。
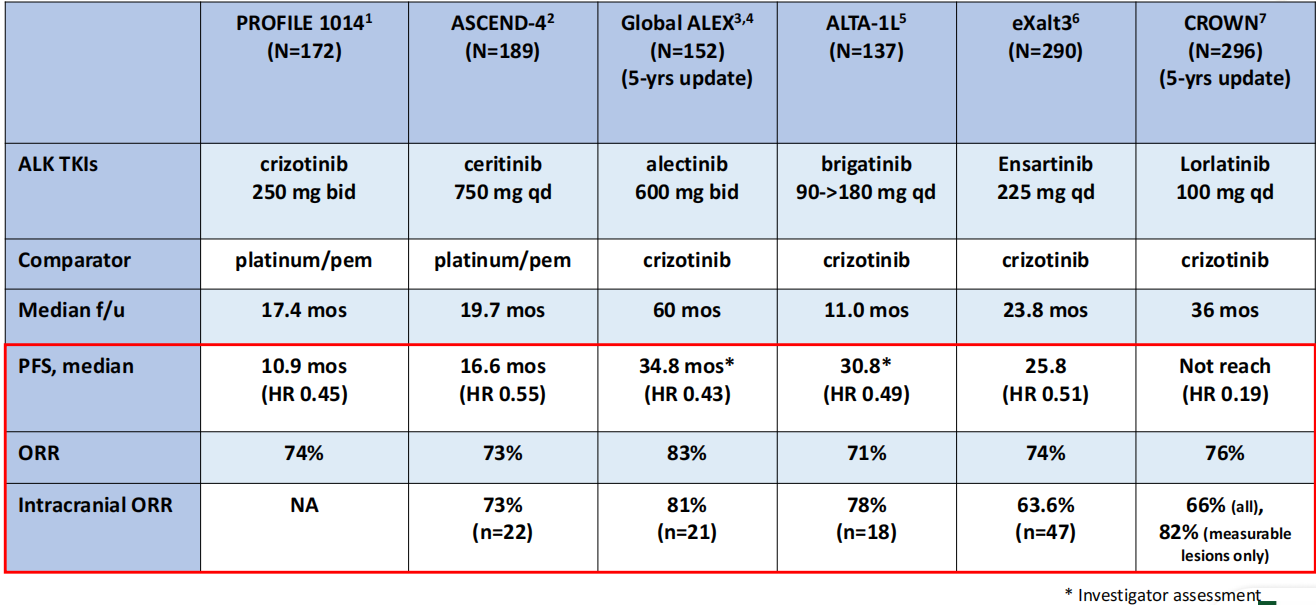
图1.ALK抑制剂一线治疗关键临床研究数据汇总
ROS1抑制剂的最新突破
TRIDENT-1研究:针对TKI初治患者,中位PFS达30.2个月,中位总生存期(mOS)达到了74.6个月。而在TKI经治患者中,mPFS和mOS分别为9.2个月和20.5个月。
TRUST-II研究:对于TKI初治患者中位PFS尚未达到,在经治患者中位PFS达到11.8个月。
深度剖析耐药机制与后线排兵布阵
随着患者生存期的延长,耐药问题成为不可回避的挑战。肿瘤的耐药机制呈现出高度的时空异质性,主要分为靶向耐药(On-target)和非靶向耐药(Off-target,又称旁路激活)。
1. 靶向耐药(On-target Resistance)与变异体的影响
靶点本身的二次突变是导致TKI失效的直接原因。不同EML4-ALK变体(Variant)在二代TKI进展后表现出截然不同的耐药图谱。例如,在二代ALKi进展后,Variant 3患者中G1202R突变发生率高达37.5%,而在Variant 1患者中未观察到此突变(0%),两者具有极显著统计学差异(P<0.001)。第三代药物(如洛拉替尼)能够有效抑制单点ALK突变(包含溶剂前沿突变)。然而,在洛拉替尼等三代药物耐药后,会涌现出极难处理的ALK复合突变(Compound mutations),如基于ALK G1202R或ALK I1171N/S的复合突变。
2. 第四代ALK TKI的崛起:对抗复合突变
为了克服包含双重顺式突变(Dual cis-mutations)在内的复杂突变,第四代ALK TKI正在加速走进临床。
NVL-655(Neladalkib):这种第四代新药在临床前和早期临床中均展现出克服多种耐药突变的潜力。在ALKove-01(1/2期)研究中,各剂量组的总体ORR为38%。在携带任何ALK突变的患者中,ORR提升至52%。在既往接受过洛拉替尼治疗且伴有任何ALK突变的患者中,ORR达到47%(伴有复合突变者为54%)。在洛拉替尼初治但伴有ALK突变的患者中,ORR更是高达88%。
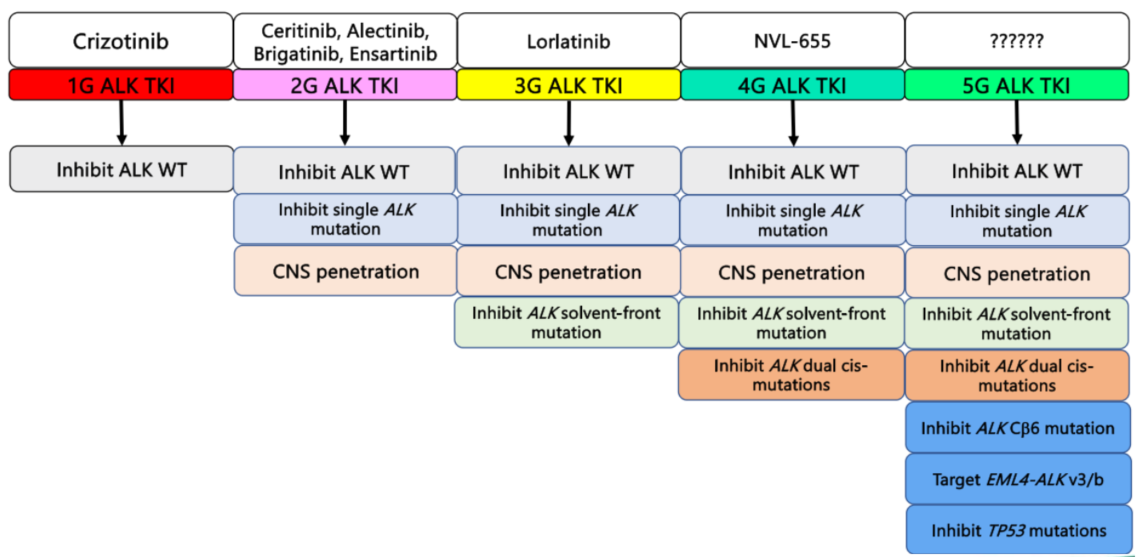
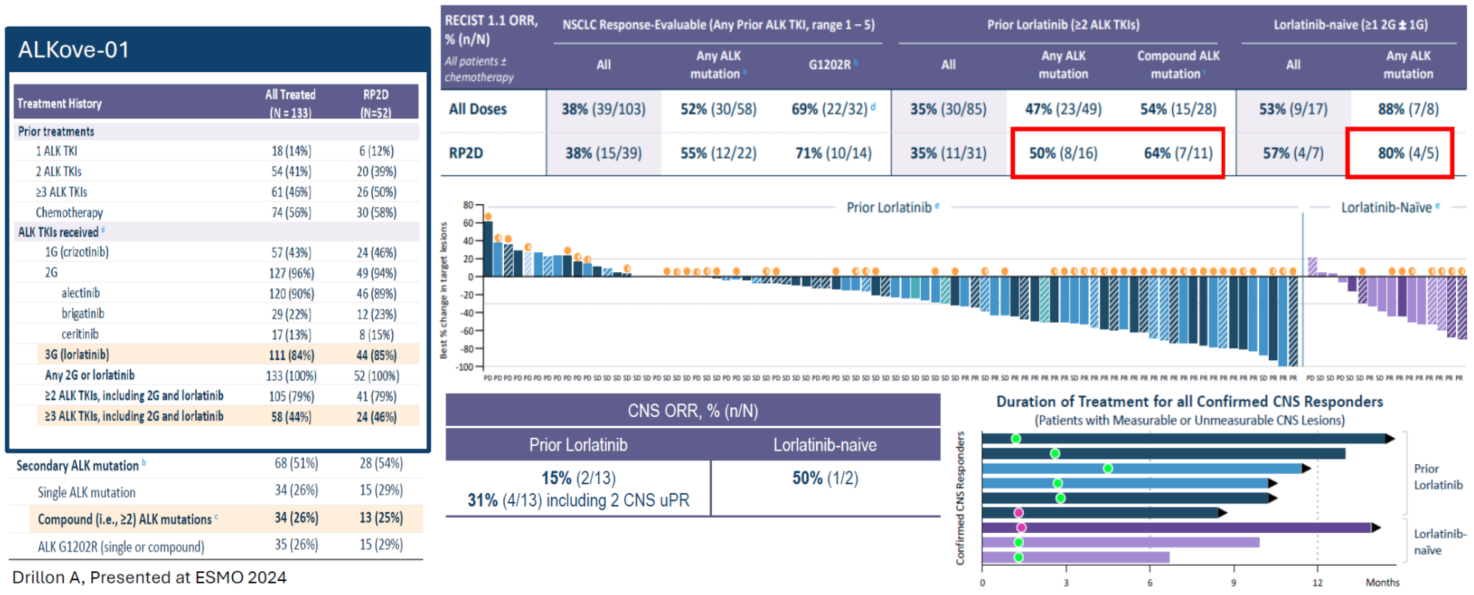
图3.ALKove-01临床试验数据,显示了NVL-655在伴有复合突变的难治性ALK阳性NSCLC中的显著疗效。
3. 非靶向耐药(Off-target Resistance)与旁路激活
当肿瘤细胞绕开ALK/ROS1信号通路时,单纯更换下一代同靶点TKI将无济于事。
在洛拉替尼耐药患者中,约35%出现了旁路激活机制(Bypass mechanism)。常见的旁路包括:MET扩增、HER2/EGFR激活、FGFR、以及下游的MAPK途径和PI3K/mTOR/PTEN途径异常。
此外,组织学转化(如向鳞状细胞癌或小细胞肺癌转化)也是重要的非靶向耐药途径。
面对脱靶耐药,现代肿瘤学正转向组合疗法(如ALK抑制剂+MET抑制剂或SHP2抑制剂)、抗体偶联药物(ADC,精准递送细胞毒性药物)以及免疫疗法。
未来洞察:从被动应战到早期拦截
未来的治疗焦点,正在从患者出现临床进展后再行干预,转向更早期的精准拦截与机制干预。
1. “药物耐受持久细胞”(DTP)
在靶向治疗初期,部分肿瘤细胞并未死亡,而是转入一种休眠或缓慢增殖的状态,成为药物耐受持久细胞(DTPs)。DTP细胞可以经历表观基因组学、转录组学以及代谢学上的重编程,从而逃避癌基因导向治疗的杀伤。
目前学术界正在探索的前沿策略包括:通过CDK4/6抑制剂诱导细胞周期停滞以维持细胞的耐受状态;使用组蛋白去乙酰化酶(HDAC)抑制剂或IGF-1R抑制剂靶向维持持久状态的关键因子;以及抑制调控转录的通路(如YAP-TEAD)。
2.正交治疗与PROTAC技术
为了根除微小残留病灶(MRD)并消除DTP群体,早期实施合理的联合治疗以预防多克隆耐药势在必行。
正交治疗(Orthogonal modalities):结合局部巩固治疗、靶向联合化疗,或采用免疫干预手段,对耐受细胞进行全方位打击。
靶向蛋白降解嵌合体(PROTACs):PROTAC是异双功能分子,它包含结合靶蛋白的配体、结合E3泛素连接酶的配体以及连接两者的Linker。它能够劫持细胞内源性的泛素-蛋白酶体系统,直接将靶蛋白(如致癌的ALK或ROS1融合蛋白)送入“垃圾处理站”进行降解。目前已有基于塞瑞替尼和布格替尼设计的至少6种ALK PROTAC分子进入临床前测试,并在时间与浓度依赖性上展现了强效的蛋白降解能力。
小结
对于临床医生而言,处理ALK/ROS1阳性NSCLC需要建立动态的、具有全局观的治疗策略:
1. 一线基石依然稳固,但需重视入脑能力:阿来替尼、布格替尼和洛拉替尼等新一代TKI已经成为ALK阳性NSCLC的一线优选,这不仅归功于其PFS数据,更在于其颅内病灶控制能力,极大延缓了由于血脑屏障导致的中枢神经系统避难所效应。
2.细化分子分型,Variant决定命运:不能仅仅停留在“ALK阳性”的粗略诊断。EML4-ALK的不同变异体(如Variant 3 vs Variant 1)直接影响患者在TKI耐药后的基因突变图谱(如G1202R的富集),这将深刻影响后续药物的选择。
3.四代药物破局复合突变:以NVL-655(Neladalkib)为代表的第四代ALK TKI正在改变游戏规则。对于经过三代药物(洛拉替尼)治疗后出现的复杂双重顺式突变,NVL-655展现出了极高的缓解率,填补了后线治疗的巨大空白。
4.警惕旁路激活与表型转化:耐药不可避免时,必须重新进行组织或液体活检。若证实为非靶向耐药(如MET扩增、PI3K异常或转化为小细胞肺癌),应果断切换策略,采用ADC药物、组合靶向疗法或化疗。
5.前置干预是未来治愈的关键:不要等临床复发才采取行动。关注药物耐受持久细胞(DTPs),利用CDK4/6抑制剂、PROTAC技术或早期的局部巩固治疗,将有望彻底消灭休眠的肿瘤细胞,最终将这部分晚期肺癌转变为可治愈或长期慢性控制的疾病。
排版编辑:肿瘤资讯-HYF











 苏公网安备32059002004080号
苏公网安备32059002004080号


