在前两期内容中,我们分别梳理了抗体偶联药物(ADC)的基本结构、作用机制,以及肺癌领域热门ADC靶点的临床布局,为大家呈现了这一精准治疗领域的核心框架。本文则聚焦“连接子”,其作为ADC“抗体-药物载荷”的关键桥梁,看似是中间环节,却直接决定了药物的治疗窗口、稳定性与抗肿瘤活性,堪称ADC发挥疗效的“隐形操盘手”。对于临床医生而言,深入理解连接子的设计逻辑与特性,能够更加精准地解读药物疗效差异、预判不良反应风险,为患者个体化治疗提供重要参考。
一、连接子的核心使命:平衡“稳”与“放”
ADC连接子的核心功能是帮助ADC药物在血液循环中保持稳定,避免药物载荷提前释放导致脱靶毒性;同时在到达肿瘤细胞后,高效释放细胞毒性载荷,确保杀伤效果。这一“稳中有放”的特性,是ADC药物区别于传统化疗的关键优势所在。
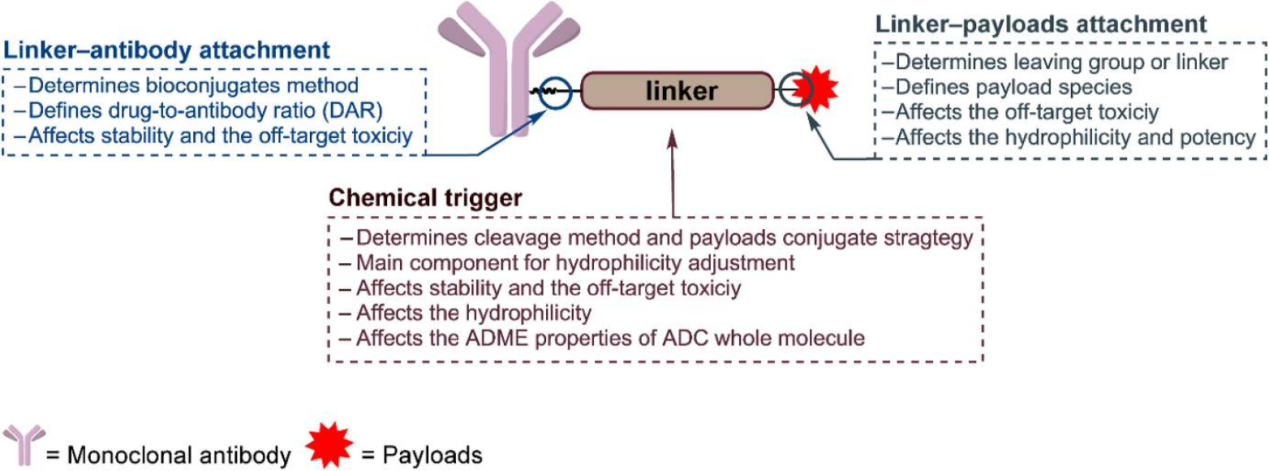
从结构来看,连接子主要由三部分构成:抗体结合位点、化学触发机制、载荷结合位点。其中化学触发机制是核心,直接决定了药物载荷的释放时机与方式;而连接子的稳定性则依赖于化学键的选择——既需要抵御血液中的酶解与化学攻击,又能在肿瘤细胞内的特定微环境(如酸性pH、高蛋白酶浓度)中快速断裂。
连接子的稳定性直接关联治疗安全性。例如,早期ADC因连接子稳定性不足,常出现药物载荷提前释放导致的严重骨髓抑制、胃肠道反应;而新一代连接子通过优化化学结构,显著降低了这类脱靶毒性,这也是近年来ADC药物耐受性提升的重要原因。
二、连接子的分类与临床应用场景
根据是否可断裂,连接子主要分为不可裂解型与可裂解型两大类,二者在设计逻辑、适用场景上各有侧重,也直接影响ADC药物的临床表现。
(一)不可裂解型连接子:经典设计,稳定为先
不可裂解型连接子多通过硫醚键等稳定化学键连接抗体与药物载荷,其释放依赖于ADC被肿瘤细胞内吞后,抗体在溶酶体中被完全降解,进而释放药物载荷。这类连接子的核心优势是血液循环中稳定性极高,脱靶毒性风险低,但缺点是药物载荷释放效率较低,且无法产生“旁观者效应”,对肿瘤异质性的适应能力有限。
在肺癌ADC中,较早期的ADC药物T-DM1即采用了不可裂解型硫醚连接子,将曲妥珠单抗与微管抑制剂DM1连接(药物抗体比DAR=3.1)[2]。临床数据显示,在一项纳入49例HER2过表达NSCLC患者的Ⅱ期试验中,T-DM1治疗的客观缓解率(ORR)仅20%,且仅见于IHC 3+亚组,中位无进展生存期(mPFS)仅2.7个月[3];另一项针对HER2突变NSCLC的Ⅱ期篮子试验中,其ORR虽提升至44%,但mPFS仍仅5个月[4]。这一结果很可能与不可裂解型连接子的药物载荷释放效率不足密切相关,也促使后续药物转向可裂解型设计。
(二)可裂解型连接子:精准触发,疗效升级
可裂解型连接子通过特定化学机制在肿瘤微环境中选择性断裂,目前已成为肺癌ADC的主流设计,肺癌领域ADC药物的连接子主要包括三类:
肽酶敏感型:依赖肿瘤细胞内高表达的溶酶体蛋白酶(如组织蛋白酶B)切割,是目前应用最广泛的类型。肺癌领域的德曲妥珠单抗(T-DXd)、瑞康曲妥珠单抗(SHR-A1811)、德达博妥单抗(Dato-DXd)等均采用肽酶/蛋白酶敏感型可裂解四肽连接子,在血液循环中稳定性优异,进入肿瘤细胞后能快速释放药物载荷[5, 6]。临床数据显示,T-DXd在HER2突变肺癌患者的Ⅱ期DESTINY-Lung01试验中,ORR达55%,mPFS为8.2个月,中位总生存期(mOS)17.8个月[7]。在HER2 IHC 2+或3+人群中,其ORR可达26.5%-34.1%[8],这与肽酶敏感型连接子带来的高效释放特性及旁观者效应密不可分。
酸敏感型:利用肿瘤内吞体pH降低(pH 5.0-6.0)触发连接子水解,适用于药物载荷对酸性环境耐受的ADC设计。这类连接子能在肿瘤细胞内快速响应微环境变化,但需平衡血液中(pH 7.4)的稳定性,避免过早释放。芦康沙妥珠单抗(sac-TMT)采用的CL2A碳酸酯连接子正是一种酸敏感型连接子,可通过pH敏感性机制降解,产生旁观者效应[9]。在II期OptiTROP-Lung03研究中,芦康沙妥珠单抗用于EGFR-TKI和含铂化疗耐药的EGFR突变NSCLC患者,芦康沙妥珠单抗组的ORR和mPFS均显著优于多西他赛组,分别达45%和6.9个月,总生存期(OS)数据亦展现出统计学优势,同样证实酸敏感型连接子策略在肺癌中的应用潜力[10]。
二硫键敏感型:依赖肿瘤细胞内高浓度的谷胱甘肽还原二硫键实现断裂,优点是触发条件特异性强,但在还原性较强的组织中可能存在脱靶风险。例如,针对CEACAM5的Tusamitamab ravtansine采用二硫键可裂解连接子(SPDB),在高表达CEACAM5的NSCLC患者中ORR达20.3%,但角膜炎等脱靶毒性发生率较高(29%)[11],限制了其临床应用。
值得关注的是,可裂解型连接子的“旁观者效应”——载荷释放后可穿透细胞膜,杀伤周围未表达靶抗原的肿瘤细胞——这一特性对解决肿瘤异质性问题至关重要。例如,Dato-DXd在TROP2阳性肺癌的Ⅲ期TROPION-Lung01试验中,即使在不同TROP2表达水平亚组中均观察到疗效,mPFS达4.4个月,显著优于化疗的3.7个月[12],正是得益于可裂解连接子带来的旁观者效应,扩大了治疗获益人群。
三、连接子的关键性能指标与临床解读
(一)稳定性:决定治疗安全性的核心
连接子的稳定性通常用“血浆半衰期”和“载荷泄露率”衡量。临床中,稳定性不足的连接子会导致载荷提前释放,引发骨髓抑制、消化道反应等不良反应。例如,早期采用酸敏感连接子的ADC(Mylotarg)由于连接子的不稳定性导致该ADC在到达目标位置前过早释放药物载荷,导致Mylotarg一度退市[13]。新一代连接子如T-DXd的四肽连接子,显著降低了血浆泄露率和脱靶毒性[7]。
(二)释放效率:影响抗肿瘤活性的关键
连接子的释放效率直接关联肿瘤细胞内载荷浓度。临床数据显示,采用高效可裂解连接子的ADC,其肿瘤细胞内载荷浓度可达不可裂解型ADC的5倍[14]。例如,采用肽酶敏感型连接子的TROP2 ADC(Dato-DXd)血浆泄露率低于6%[15],使得其在TROPION-Lung01试验中,ORR达26.4%,显著高于化疗组的12.8%[12];而HER3-DXd采用相同的四肽连接子,在EGFR-TKI耐药的EGFR突变NSCLC患者中,ORR达29.8%,mPFS 5.5个月[16],验证了该类连接子的高效释放特性。
(三)生物相容性:降低免疫原性风险
连接子的化学结构需避免引发免疫反应,同时不能影响抗体的靶向结合能力。适宜的亲水性或亲脂性可以增强ADC药物本身稳定性并降低免疫原性[17]。新一代连接子多采用小分子、低免疫原性设计,如四肽连接子、谷氨酰胺连接子等,临床中免疫机制导致的不良反应发生率显著降低,提升了患者耐受性。
四、肺癌ADC连接子的前沿进展与临床展望
连接子的结构优化与机制创新,是推动肺癌ADC药物向更高治疗窗、更广适用范围发展的核心动力。近年来,随着对肿瘤微环境特征的深度解析、化学合成技术的迭代升级以及定点偶联技术的成熟应用,肺癌ADC连接子的研发已从单一的“稳放平衡”设计,向多响应触发、亲疏水性调控、多功能协同的方向突破,为解决肺癌临床治疗中的肿瘤异质性、多药耐药、脱靶毒性等难题提供了新的技术方案。同时,连接子与抗体、载荷的协同设计理念逐渐成为研发主流,进一步提升了ADC药物在肺癌不同亚型、不同治疗线数中的临床价值。
从前沿研究方向来看,肺癌ADC连接子的创新主要集中在三大维度,且均已有基础研究或早期临床数据验证其可行性,为后续临床转化奠定了坚实基础。
其一,双响应/多响应可裂解连接子的开发,成为提升释药特异性的核心方向。传统单响应连接子仅依赖肿瘤细胞内单一微环境特征(如酸性、蛋白酶高表达)触发断裂,仍存在一定的脱靶风险,而双响应连接子需同时满足两种肿瘤特异性条件才能释放载荷,大幅提升了释药的精准性。例如,基于“酸敏感腙键+二硫键”的双响应连接子,需在肿瘤内吞体酸性环境(pH 5.0-6.0)与高谷胱甘肽浓度的双重作用下实现断裂,其血浆稳定性较单响应酸敏感连接子实现显著提升,脱靶毒性风险大幅降低[17]。此外,“肽酶敏感+磷酸酶敏感”的双响应连接子也已进入临床前研究,依托肺癌细胞内组织蛋白酶B与磷酸酶的双重高表达实现精准释药,在EGFR突变肺癌耐药细胞株中,展现出比单一肽酶敏感连接子更强的抗肿瘤活性,为解决肺癌靶向治疗耐药问题提供了新思路[18]。
其二,亲水性连接子的结构优化,有效改善了ADC药物的药代动力学特性与抗肿瘤效能。肺癌尤其是晚期NSCLC常存在肿瘤组织血管通透性低、药物渗透差的问题,而传统疏水性连接子易导致ADC药物聚集,降低肿瘤组织穿透性。新一代亲水性连接子通过引入PEG链、葡萄糖醛酸等亲水性基团,不仅提升了ADC的水溶性与血浆稳定性,还能增加药物在肿瘤组织中的渗透深度[19]。例如,基于β-葡萄糖醛酸的糖苷酶敏感型亲水性连接子,凭借糖基结构的高亲水性特征,可实现高DAR的稳定制备且无明显聚集,在低靶点表达肺癌模型中,能有效提升肿瘤内药物富集浓度,增强药物的肿瘤穿透性与旁观者效应。德达博妥单抗(Dato-DXd)的四肽连接子通过亲水性修饰优化了化学结构,血浆载荷泄露率维持在低水平,使其在不同TROP2表达水平的肺癌患者中均能实现疗效获益,这也直接验证了亲水性调控在肺癌ADC连接子设计中的核心价值[15]。
其三,连接子与定点偶联技术的协同应用,实现了ADC药物的均质化制备与疗效可控性提升。早期随机偶联技术导致ADC的DAR存在异质性,而连接子的化学结构与偶联位点的协同设计,可实现DAR的精准调控。例如,通过工程化改造抗体的半胱氨酸残基,结合马来酰亚胺类连接子的定点偶联技术,可制备出DAR=4的均质化ADC,这类均质化ADC在HER2靶向的肿瘤临床前研究中,抗肿瘤活性较随机偶联ADC实现显著提升,且脱靶毒性与血浆载荷泄露风险大幅降低[17, 20]。目前,该类连接子与定点偶联协同设计的ADC药物如瑞康曲妥珠单抗(SHR-A1811)已在HER2突变/阳性肺癌中开展Ⅲ期临床研究,其依托优化的可裂解连接子与精准偶联技术,在保持高效抗肿瘤活性的同时展现出更可控的安全性特征,3级以上药物相关不良反应发生率低,间质性肺病等特有毒性发生率低于同类药物[6]。
从临床应用展望来看,连接子的创新将进一步拓宽肺癌ADC药物的适用场景,推动肺癌精准治疗进入更精细化的阶段。一方面,针对肺癌不同亚型的微环境特征设计专属连接子,将实现“亚型定制化”ADC研发。例如,小细胞肺癌存在组织蛋白酶B高表达的微环境特征,靶向B7-H3的I-DXd采用第一三共DXd平台经典的组织蛋白酶B敏感型四肽可裂解连接子,该连接子可被肿瘤细胞内高表达的组织蛋白酶B特异性切割,二者的天然匹配让I-DXd在广泛期小细胞肺癌的Ⅱ期IDeate-Lung01试验中实现48.2%的客观缓解率,为小细胞肺癌的后线治疗提供了新选择[13, 21]。另一方面,连接子的创新将推动ADC药物与其他治疗手段的联合应用,如与免疫检查点抑制剂、抗血管生成药物联用。可裂解连接子释放的载荷在杀伤肿瘤细胞的同时,能诱导肿瘤细胞免疫原性死亡,而连接子的亲水性优化可提升ADC与免疫药物的协同作用效率,目前已有多项“ADC+PD-1/PD-L1”联合治疗肺癌的临床研究开展(NCT05555732、NCT05215340及NCT05609968等),连接子的设计成为提升联合疗效的关键变量。
此外,连接子的研发也将更加注重临床转化的实用性,针对肺癌临床治疗中的未满足需求进行定向设计。例如,针对脑转移肺癌患者,设计可穿透血脑屏障的亲脂性-亲水性平衡型连接子,提升ADC药物在脑转移灶中的浓度;针对多线化疗耐药的肺癌患者,开发可逆转耐药的连接子-载荷协同结构,通过连接子的化学修饰增强载荷对耐药靶点的抑制作用。这些定向设计思路,将使肺癌ADC药物从“靶点精准”向“临床需求精准”升级。
总体而言,连接子作为ADC药物的“核心枢纽”,其研发创新已成为肺癌精准治疗领域的重要突破点。从单一的化学桥梁,到与抗体、载荷协同设计的多功能模块,连接子的每一次升级都推动着肺癌ADC药物疗效与安全性的双重提升。未来,随着肿瘤微环境研究的不断深入、化学合成技术的持续创新以及临床研究的精准开展,连接子将朝着更精准、更高效、更适配肺癌临床需求的方向发展,为不同亚型、不同分期、不同治疗背景的肺癌患者提供个体化的治疗方案,也将推动ADC药物成为肺癌综合治疗中的核心药物之一。下一期,我们将聚焦ADC药物的“弹头”——药物载荷,解析不同细胞毒性分子的作用机制、结构特征及其在肺癌领域的临床应用差异,探讨载荷与连接子的协同设计如何影响ADC药物的临床疗效,敬请期待!
[1] Z. Su, D. Xiao, F. Xie, et al. Antibody-drug conjugates: Recent advances in linker chemistry[J]. Acta Pharm Sin B, 2021, 11(12): 3889-3907.
[2] A. Passaro, P. A. Jänne, S. Peters. Antibody-Drug Conjugates in Lung Cancer: Recent Advances and Implementing Strategies[J]. J Clin Oncol, 2023, 41(21): 3747-3761.
[3] S. Peters, R. Stahel, L. Bubendorf, et al. Trastuzumab Emtansine (T-DM1) in Patients with Previously Treated HER2-Overexpressing Metastatic Non-Small Cell Lung Cancer: Efficacy, Safety, and Biomarkers[J]. Clin Cancer Res, 2019, 25(1): 64-72.
[4] B. T. Li, R. Shen, D. Buonocore, et al. Ado-Trastuzumab Emtansine for Patients With HER2-Mutant Lung Cancers: Results From a Phase II Basket Trial[J]. J Clin Oncol, 2018, 36(24): 2532-2537.
[5] Y. Ogitani, T. Aida, K. Hagihara, et al. DS-8201a, A Novel HER2-Targeting ADC with a Novel DNA Topoisomerase I Inhibitor, Demonstrates a Promising Antitumor Efficacy with Differentiation from T-DM1[J]. Clin Cancer Res, 2016, 22(20): 5097-5108.
[6] T. Zhang, J. Xu, J. Yin, et al. SHR-A1811, a novel anti-HER2 antibody-drug conjugate with optimal drug-to-antibody ratio, efficient tumor killing potency, and favorable safety profiles[J]. PLoS One, 2025, 20(6): e0326691.
[7] B. T. Li, E. F. Smit, Y. Goto, et al. Trastuzumab Deruxtecan in HER2-Mutant Non-Small-Cell Lung Cancer[J]. N Engl J Med, 2022, 386(3): 241-251.
[8] E. F. Smit, E. Felip, D. Uprety, et al. Trastuzumab deruxtecan in patients with metastatic non-small-cell lung cancer (DESTINY-Lung01): primary results of the HER2-overexpressing cohorts from a single-arm, phase 2 trial[J]. Lancet Oncol, 2024, 25(4): 439-454.
[9] Q. Ouyang, J. Rodon, Y. Liang, et al. Results of a phase 1/2 study of sacituzumab tirumotecan in patients with unresectable locally advanced or metastatic solid tumors refractory to standard therapies[J]. J Hematol Oncol, 2025, 18(1): 61.
[10] W. Fang, X. Li, Q. Wang, et al. Sacituzumab tirumotecan versus docetaxel for previously treated EGFR-mutated advanced non-small cell lung cancer: multicentre, open label, randomised controlled trial[J]. Bmj, 2025, 389: e085680.
[11] A. Gazzah, C. Ricordel, A. Italiano, et al. Evaluation of the Safety, Pharmacokinetics, and Antitumor Activity of Tusamitamab Ravtansine in Patients With Nonsquamous NSCLC With High or Moderate Expression of Carcinoembryonic Antigen-Related Cell Adhesion Molecule 5[J]. JTO Clin Res Rep, 2025, 6(10): 100844.
[12] M. J. Ahn, K. Tanaka, L. Paz-Ares, et al. Datopotamab Deruxtecan Versus Docetaxel for Previously Treated Advanced or Metastatic Non-Small Cell Lung Cancer: The Randomized, Open-Label Phase III TROPION-Lung01 Study[J]. J Clin Oncol, 2025, 43(3): 260-272.
[13] R. Sheyi, B. G. de la Torre, F. Albericio. Linkers: An Assurance for Controlled Delivery of Antibody-Drug Conjugate[J]. Pharmaceutics, 2022, 14(2):
[14] F. Li, K. K. Emmerton, M. Jonas, et al. Intracellular Released Payload Influences Potency and Bystander-Killing Effects of Antibody-Drug Conjugates in Preclinical Models[J]. Cancer Res, 2016, 76(9): 2710-2719.
[15] D. Okajima, S. Yasuda, T. Maejima, et al. Datopotamab Deruxtecan, a Novel TROP2-directed Antibody-drug Conjugate, Demonstrates Potent Antitumor Activity by Efficient Drug Delivery to Tumor Cells[J]. Mol Cancer Ther, 2021, 20(12): 2329-2340.
[16] H. A. Yu, Y. Goto, H. Hayashi, et al. HERTHENA-Lung01, a Phase II Trial of Patritumab Deruxtecan (HER3-DXd) in Epidermal Growth Factor Receptor-Mutated Non-Small-Cell Lung Cancer After Epidermal Growth Factor Receptor Tyrosine Kinase Inhibitor Therapy and Platinum-Based Chemotherapy[J]. J Clin Oncol, 2023, 41(35): 5363-5375.
[17] K. Tsuchikama, Z. An. Antibody-drug conjugates: recent advances in conjugation and linker chemistries[J]. Protein Cell, 2018, 9(1): 33-46.
[18] S. Balamkundu, C. F. Liu. Lysosomal-Cleavable Peptide Linkers in Antibody-Drug Conjugates[J]. Biomedicines, 2023, 11(11):
[19] V. Kostova, P. Désos, J. B. Starck, et al. The Chemistry Behind ADCs[J]. Pharmaceuticals (Basel), 2021, 14(5):
[20] J. R. Junutula, H. Raab, S. Clark, et al. Site-specific conjugation of a cytotoxic drug to an antibody improves the therapeutic index[J]. Nat Biotechnol, 2008, 26(8): 925-932.
[21] C. M. Rudin, M. L. Johnson, L. Paz-Ares, et al. Ifinatamab Deruxtecan in Patients With Extensive-Stage Small Cell Lung Cancer: Primary Analysis of the Phase II IDeate-Lung01 Trial[J]. J Clin Oncol, 2026, 44(4): 261-273
往期链接:
肺癌ADC药物面面观(二):靶点选择与格局,临床管线的突破与展望
排版编辑:肿瘤资讯-HYF











 苏公网安备32059002004080号
苏公网安备32059002004080号


