胃肠化生(Intestinal Metaplasia, IM)是胃癌发生经典“Correa级联反应”中的关键癌前病变节点。然而,并非所有IM都会发展为胃癌,如何精准识别高危人群并进行有效干预,一直是消化系统肿瘤领域的重大临床挑战。
近日,美国癌症研究协会(AACR)旗下的顶级肿瘤学期刊Cancer Discovery(IF: 33.3)发表了题为“Mutational Signatures and Clonal Hematopoiesis in Intestinal Metaplasia across Countries with Varying Stomach Cancer Incidence”的重磅研究成果。该研究对来自6个不同胃癌发病率国家/地区的1500余例IM样本进行了深度基因组测序,不仅绘制了迄今最全面的IM驱动基因图谱,更首次揭示了“克隆性造血(CH)”与宿主-微生物黏膜免疫在驱动IM向胃癌进展中的核心作用。这一发现为胃癌的早期筛查、精准分层及靶向阻断提供了全新的转化医学视角。

研究背景与设计
胃癌的发病率在不同地理区域差异巨大(如东亚为高发区,北美为低发区)。除了幽门螺杆菌(Hp)感染,宿主遗传、环境及肠道微生物群的复杂相互作用在IM向胃癌演变中扮演着神秘角色。
本研究纳入了来自新加坡、韩国、中国香港、美国、日本和中国台湾的1582例IM样本及配对的正常样本,进行了高深度靶向测序(平均深度>1100×),并结合全基因组测序(WGS)、表观遗传学(EM-seq)、单细胞RNA测序(scRNA-seq)及微生物宏基因组学进行了多维度的全景分析。
研究结果
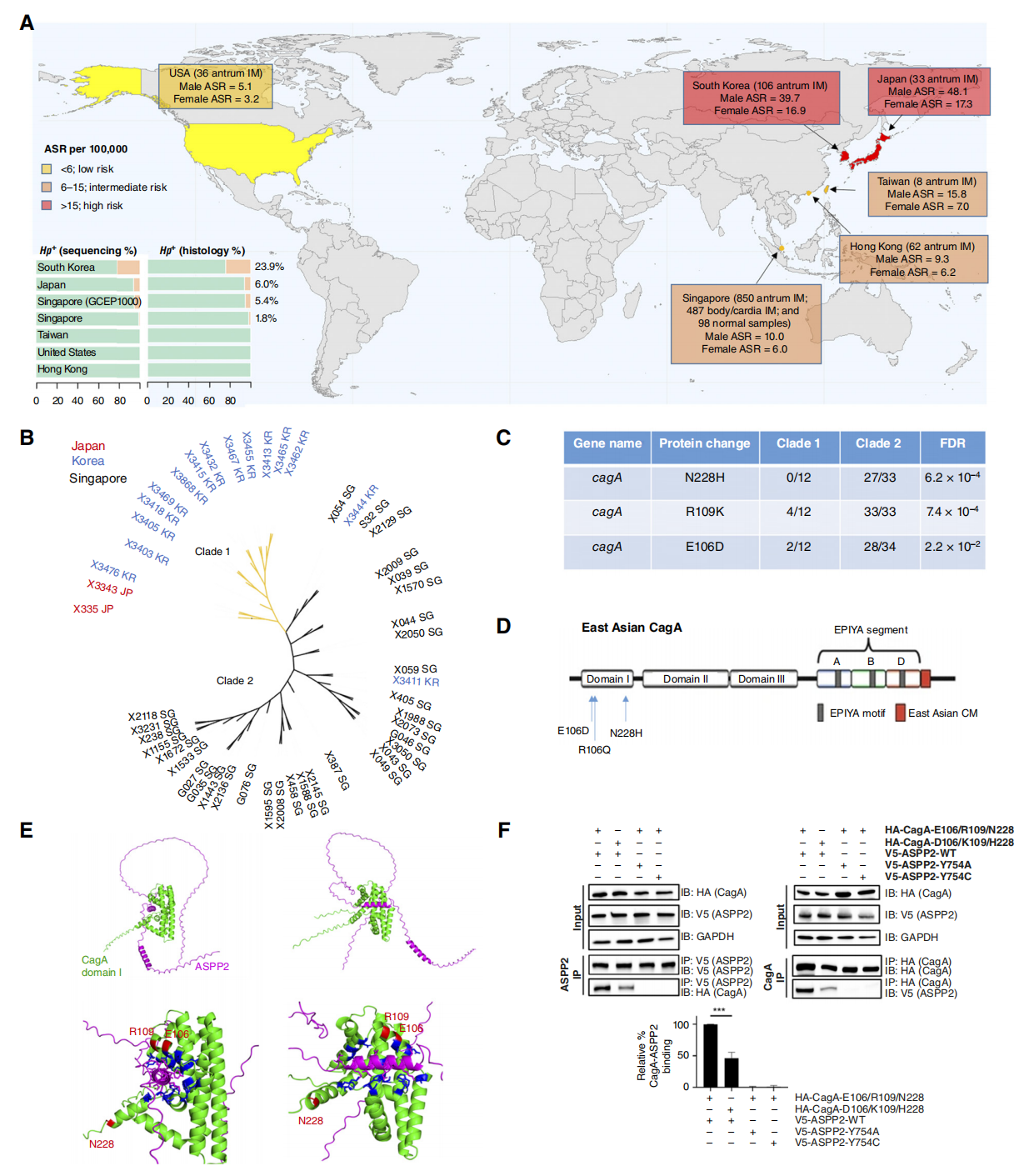
1. 探秘地域差异:高危区Hp携带更强致癌性的CagA变异
研究发现,胃癌高发国家(日本、韩国)的IM患者Hp感染率和丰度显著高于中等风险国家(如新加坡)。系统发育分析指出,中低危地区(如东南亚)的Hp菌株CagA蛋白常发生特异性氨基酸替换(E106D, R109K, N228H);而高危区(日韩)的Hp菌株则主要携带典型的高危序列(E106, R109, N228)。体外实验证实,高危区特有的CagA蛋白能更强效地与人类肿瘤抑制因子ASPP2结合,从而抑制后者的抑癌功能,这部分解释了东亚地区胃癌高发的病因学基础。
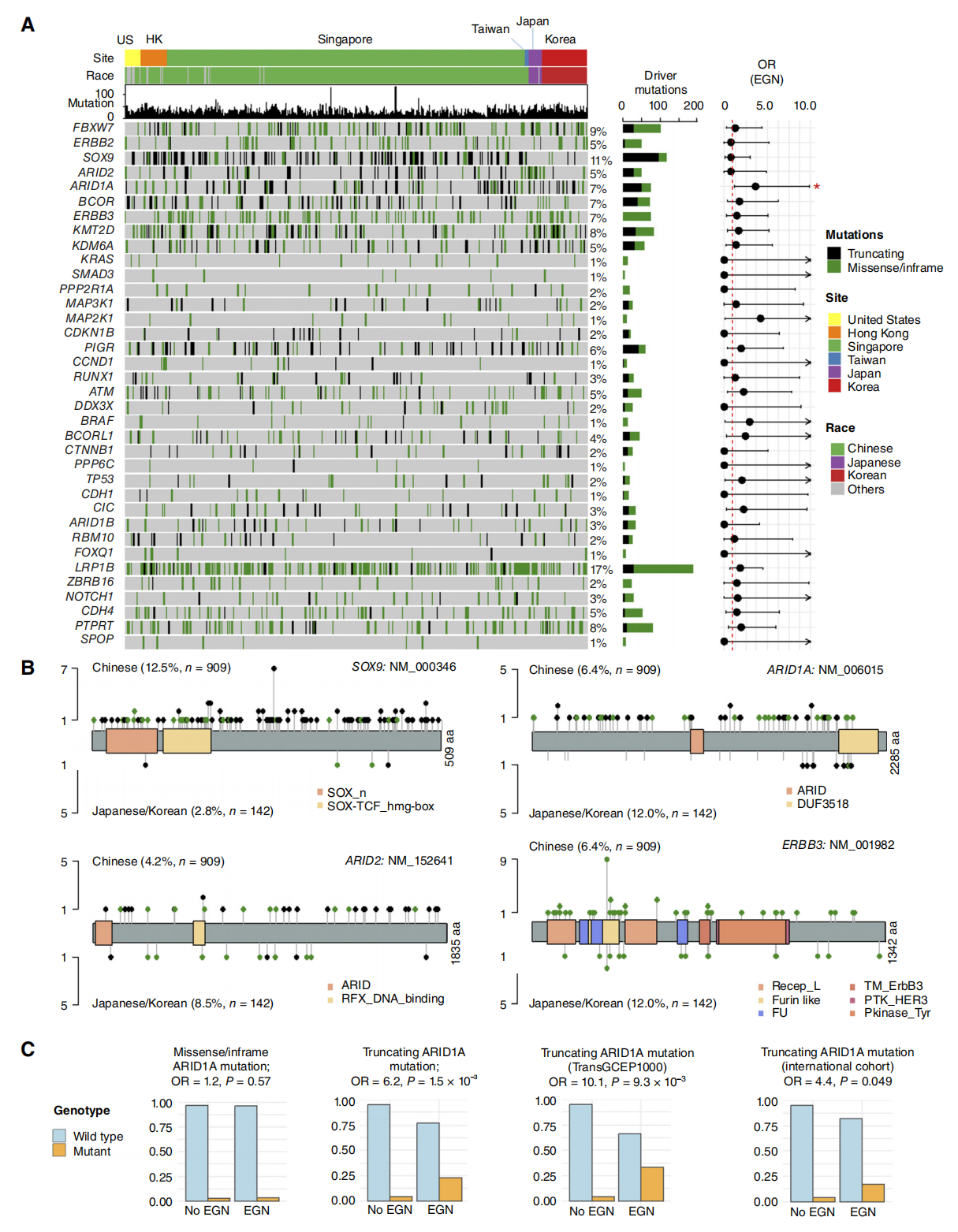
2. 绘制跨国IM驱动基因图谱,锁定KRAS/MAPK潜在干预靶点
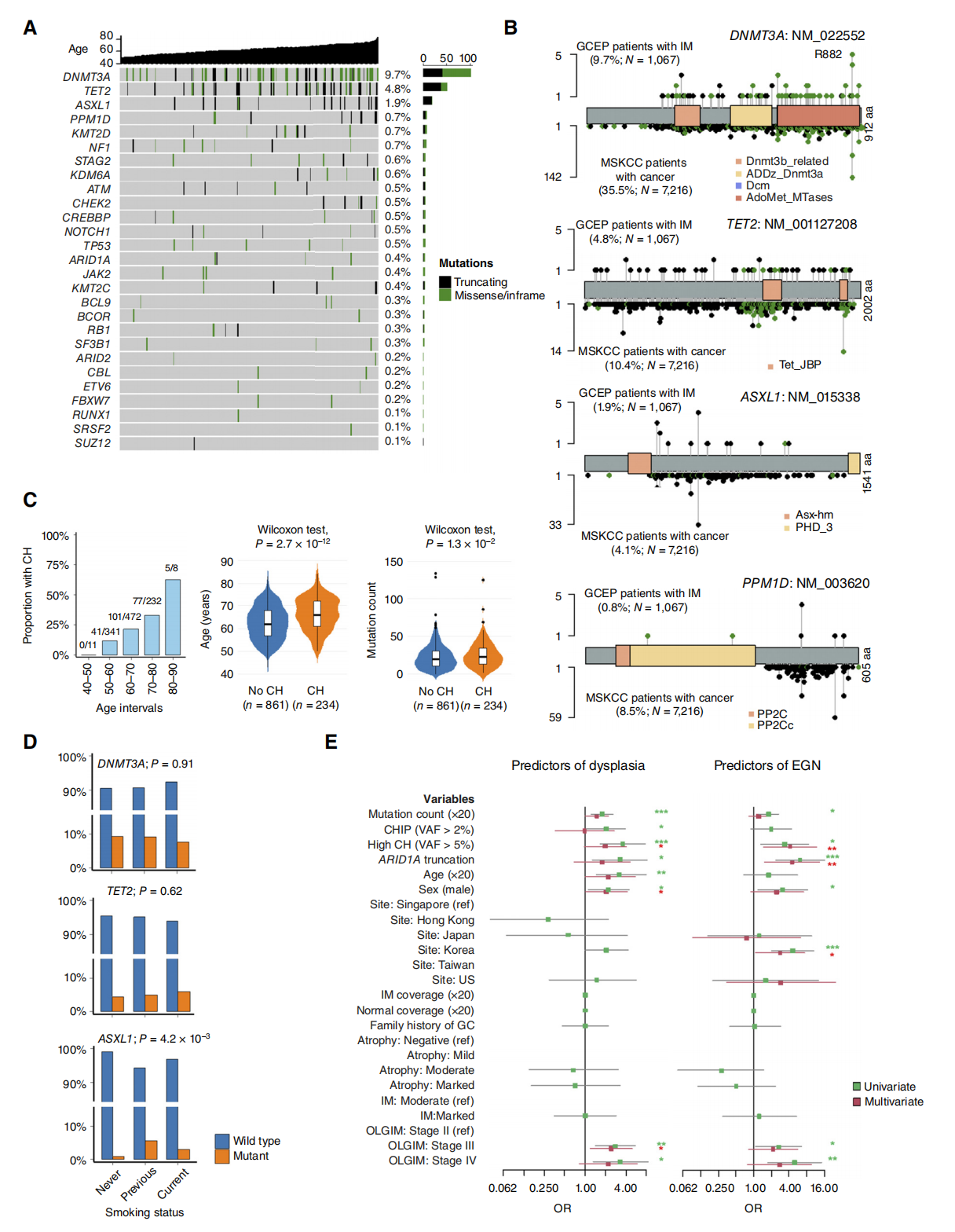
研究人员鉴定出47个显著突变的IM驱动基因(其中25个为首次发现)。不同地域的突变特征差异显著:
中国人群(含大陆、香港、台湾及新加坡华人)中,SOX9截短突变更为频发;
高危日韩人群中,染色质重塑基因ARID1A的截短突变显著富集,且该突变与IM进展为早期胃内瘤变(EGN)高度相关。
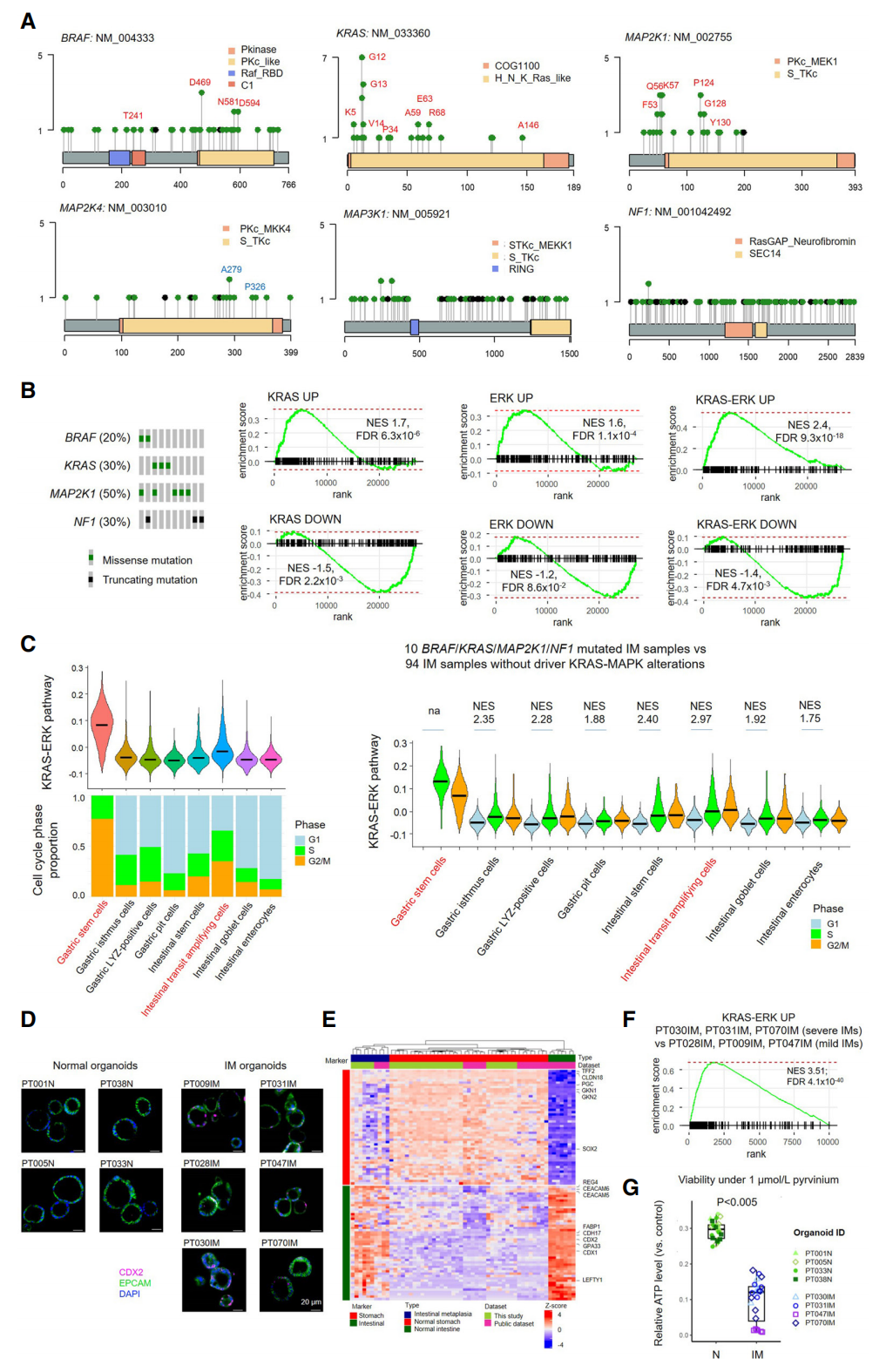
更具临床意义的是,研究发现许多IM病灶携带KRAS/MAPK信号通路的激活突变(如KRAS、BRAF)。在患者来源的IM类器官模型中,使用多通路靶向药物能够选择性地抑制IM细胞生长,而对正常胃类器官影响微弱。这提示,针对癌前病变寻找特定的多靶点“化学预防”不仅可行,且具有高度的靶向性。
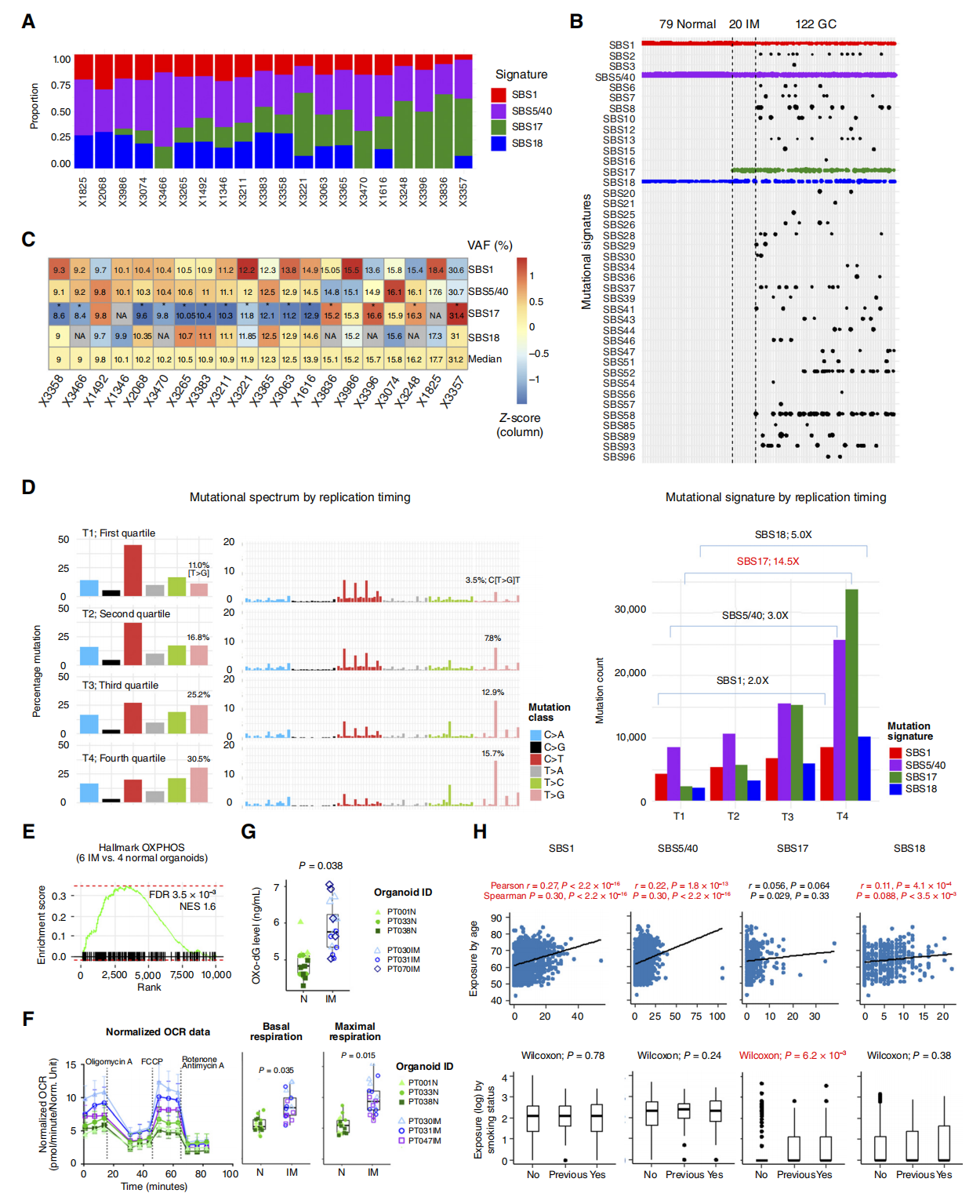
3. 发现IM专属突变指纹:SBS17
全基因组测序揭示了4种主要的单碱基替换(SBS)突变特征,其中SBS17(病因不明)是IM有别于正常胃组织的专属突变特征。
SBS17突变多表现为亚克隆形式,富集于DNA晚期复制区域和全基因组低甲基化区域,且与患者的吸烟史和氧化磷酸化(OXPHOS)水平升高导致的高氧化应激密切相关。
4. 跨界新突破:非上皮因素“克隆性造血(CH)”是胃癌进展的重要推手
研究团队将目光从胃上皮细胞转向了血液系统,发现IM患者中存在较高比例的克隆性造血(CH,即造血干细胞发生体细胞突变并克隆扩增,常见突变如DNMT3A, TET2)。
多因素回归分析证实:高克隆性造血(VAF > 5%)和ARID1A截短突变是IM进展为异常增生/早期胃癌的独立危险因素。当在传统的临床预测模型(年龄、性别、OLGIM分期)中加入基因组变量(CH和ARID1A)后,预测模型在长期随访队列中的AUC值从0.671大幅跃升至0.811。
5. 揭示机制:CH如何“隔山打牛”促进胃部癌变?
研究者构建了一个多组学互作模型,解释了血液中的CH如何影响胃壁黏膜:
具有高水平CH的IM患者,常伴发黏膜免疫受体基因PIGR的截短突变;
PIGR突变导致胃黏膜分泌IgA的能力受损,打破了黏膜微生态平衡;
免疫屏障的减弱导致口腔来源的致病菌(如链球菌)在胃壁大量定植;
致病菌的入侵进一步招募免疫细胞(如IgA+浆细胞和成熟T细胞),引发长期的慢性炎症,最终如同“催化剂”般加速了IM向胃癌的恶性转化。
临床意义与转化启示
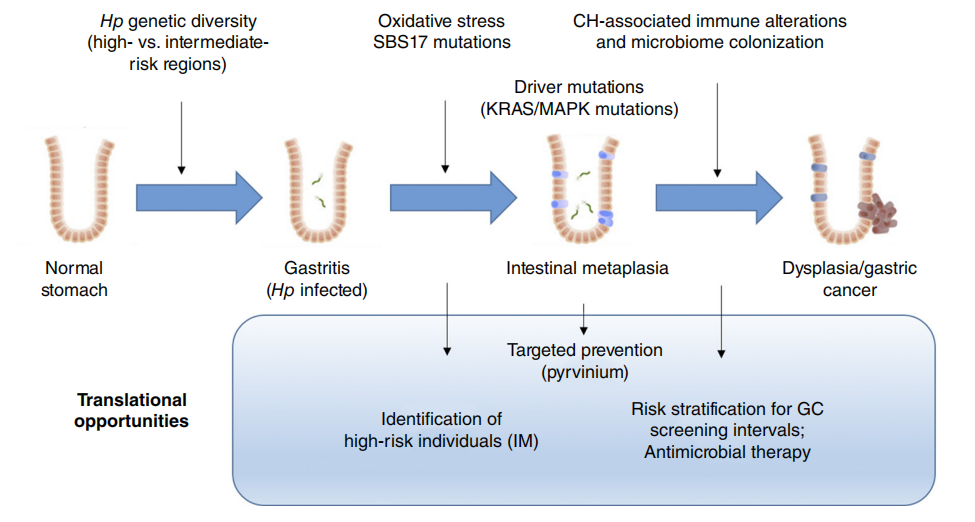
该研究不再局限于单一的癌细胞基因组,而是将病原体基因型、上皮细胞突变、非上皮系统改变(克隆性造血)以及黏膜微生物组进行了完美串联,描绘了一幅胃癌前病变演进的全景生态图。
对于临床实践而言,本研究带来了三大转化机遇:
更精准的高危人群分层:大多数IM患者终生不会得胃癌,普遍的内镜随访缺乏成本效益。未来通过检测外周血的CH状态和活检组织的ARID1A突变,可以将真正的高危患者筛选出来,进行更密集的内镜监测。
癌前病变的靶向“截断”治疗:KRAS/MAPK通路的激活突变提示,MEK/ERK抑制剂等靶向药物有望成为逆转或阻断IM进展的候选药物。
微生态干预的新思路:幽门螺杆菌根除后,部分患者仍有胃癌风险。针对伴有高CH水平的患者,探索靶向非Hp细菌(如口腔链球菌)的抗菌治疗,可能成为预防胃癌的另一把利器。
排版编辑:肿瘤资讯-as











 苏公网安备32059002004080号
苏公网安备32059002004080号


