弥漫大B细胞淋巴瘤(DLBCL)作为最常见的侵袭性非霍奇金淋巴瘤,占成人非霍奇金淋巴瘤病例的30%~40%,年发病率达5~7/10万人,其生物学异质性强、临床行为多样的特征给临床治疗带来诸多挑战。近日,发表于European Journal of Haematology杂志的一项重磅综述,系统梳理了DLBCL一线治疗的发展现状、生物学研究进展及未来方向,明确R-CHOP方案仍是基础治疗框架,而以抗体药物偶联物、双特异性抗体、CAR-T细胞疗法为代表的新型治疗手段,正推动DLBCL一线治疗向风险分层、生物标志物指导的精准化方向转型,为高危患者带来新的治疗希望。该研究综合了多项大型随机临床试验、真实世界研究及转化医学证据,为临床实践提供了全面且具指导性的参考。

研究背景:经典方案遇瓶颈,异质性成治疗关键障碍
自二十余年前R-CHOP方案(利妥昔单抗联合环磷酰胺、阿霉素、长春新碱、泼尼松)成为DLBCL一线治疗的金标准以来,该方案成功治愈了约三分之二的患者,大幅提升了患者的生存率。但临床实践中,仍有30%~40%的患者对一线治疗无效或出现复发,其中高危生物学特征、特殊基因亚型、不良临床指标的患者预后尤为恶劣,成为DLBCL治疗的核心痛点。
研究指出,DLBCL治疗失败的核心原因在于其显著的生物学异质性,活化B细胞样(ABC)亚型、MYC/BCL2/BCL6重排的双打击/三打击淋巴瘤、MYC和BCL2蛋白共表达的双表达淋巴瘤等分子亚型,对标准R-CHOP方案的缓解率显著偏低;同时,晚期病变、肿块体积大、IPI/NCCN-IPI评分高的高危临床特征,以及患者高龄、体能状态差、合并基础疾病等因素,也会进一步降低治疗效果,且复发/难治性患者的挽救治疗预后极差,历史数据显示原发性难治性患者的中位总生存期(OS)仅以月计。
此外,此前为优化R-CHOP方案开展的多项尝试均未取得理想效果:替换单克隆抗体为奥滨尤妥珠单抗的G-CHOP方案、化疗强化的DA-EPOCH-R方案、14天剂量密集型R-CHOP-14方案,均未显著改善患者的无进展生存期(PFS),反而增加了血液学毒性、神经毒性、发热性中性粒细胞减少等不良反应的发生风险。真实世界研究也证实,剂量密集型方案与标准21天方案的3年OS率无显著差异,且前者需要更多的生长因子支持,风险获益比不佳。这些结果表明,在未选择的DLBCL人群中,单纯对R-CHOP方案进行改良或强化难以突破治疗瓶颈,基于生物标志物的个体化治疗成为突破方向。
研究方法:多维度整合证据,梳理新型治疗策略的临床价值
该研究采用综述性研究方法,系统检索并整合了近年来DLBCL一线治疗领域的重要研究成果,包括大型随机对照临床试验(RCT)、真实世界研究、转化医学研究、荟萃分析等,研究范围覆盖抗体药物偶联物、免疫调节药物、BTK抑制剂、双特异性抗体、CAR-T细胞疗法等多种新型治疗手段。
研究以生物学机制-临床证据-实践考量为核心逻辑,将治疗策略分为三类:一是在R-CHOP基础上联合靶向免疫通路的药物(来那度胺、BTK 抑制剂);二是针对高危患者的抗体药物偶联物(维泊妥珠单抗)方案;三是处于临床研究阶段的双特异性抗体和一线CAR-T细胞疗法。同时,研究重点分析了肿瘤微环境(TME)、分子分型、高危生物标志物在治疗决策中的作用,并梳理了不同方案在不同亚组患者中的疗效、毒性及适用场景,为临床风险分层治疗提供依据。
表1. 改善DLBCL一线R-CHOP方案的主要初步尝试
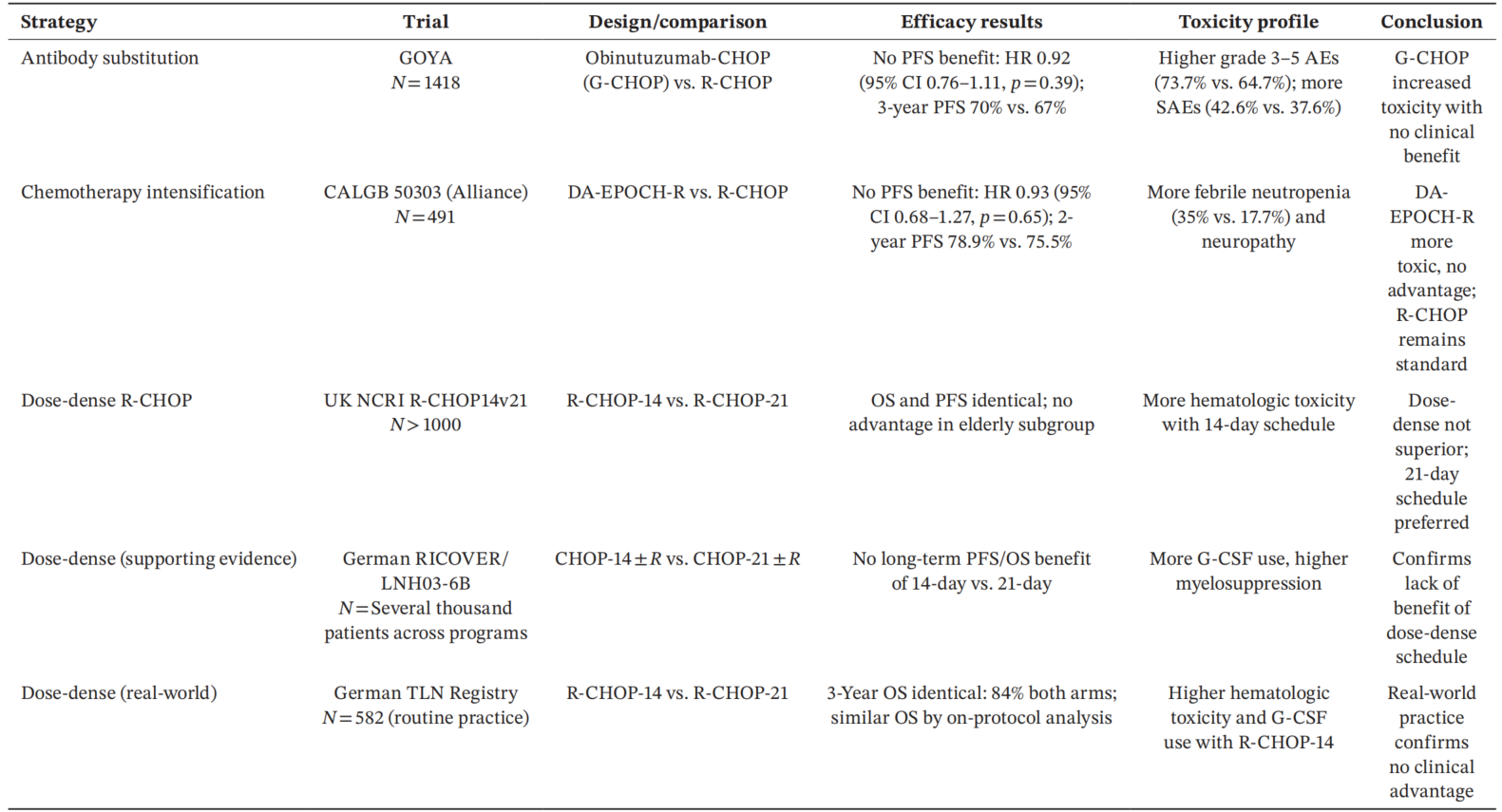
研究结果:新型疗法各展所长,高危患者治疗取得突破性进展
靶向免疫通路药物:亚组获益显著,整体疗效未达预期
基于DLBCL的分子机制,研究人员探索了在R-CHOP基础上联合免疫调节药物来那度胺和BTK抑制剂伊布替尼的治疗策略,二者均针对ABC亚型DLBCL的BCR-NF-κB信号通路异常激活的核心特征。
Ⅱ期E1412试验显示,R²-CHOP方案(来那度胺联合R-CHOP)使患者的疾病进展或死亡风险降低34%,3年PFS率达73%,优于标准R-CHOP的61%。但针对ABC亚型的Ⅲ期ROBUST试验却未证实其显著获益,二者结果的差异与试验设计、患者风险分层、来那度胺剂量及依从性相关。目前,来那度胺仍不推荐作为DLBCL一线标准治疗,仅可在老年、体弱等精选患者中谨慎使用。
BTK抑制剂伊布替尼的Ⅲ期PHOENIX试验显示,在非GCB亚型DLBCL人群中,伊布替尼联合R-CHOP未改善整体疗效,但亚组分析发现,60岁以下、携带MYD88/CD79B突变的MCD/N1基因型患者的无事件生存期(EFS)显著提升。这表明BTK抑制剂的治疗价值仅局限于分子水平精筛的亚组人群,而非广泛的非GCB亚型患者。
维泊妥珠单抗方案:高危患者的优选,成为首个验证有效的R-CHOP改良方案
CD79b作为B细胞受体复合物的关键组分,在成熟B细胞恶性肿瘤中广泛表达,是理想的治疗靶点。维泊妥珠单抗(抗CD79b抗体药物偶联物)通过将细胞毒性载荷MMAE靶向递送至恶性B细胞,实现精准杀伤,且可绕过蒽环类药物的耐药机制。
Ⅲ期POLARIX试验是该领域的里程碑研究,该试验将R-CHOP方案中的长春新碱替换为维泊妥珠单抗,形成Pola-R-CHP方案,在中高危初治DLBCL患者中取得了显著疗效:中位随访28个月时,患者2年PFS率达76.7%,显著高于标准R-CHOP的70.2%,且3级及以上不良反应未显著增加,风险获益比优异。亚组分析显示,ABC亚型、IPI评分高、肿瘤增殖活性强的患者获益更为明显,同时该方案避免了长春新碱的神经毒性,更适合老年或合并基础疾病的患者。
真实世界研究进一步验证了Pola-R-CHP方案的有效性和安全性:中国多中心研究显示,该方案的12个月PFS率和完全缓解(CR)率均高于R-CHOP,且在晚期、ECOG评分≥2、结外受累≥2处、非GCB亚型等高危亚组中均观察到获益;针对80岁以上老年患者的研究显示,减量Pola-R-CHP方案的12个月OS率达86.2%,PFS率达78.5%,且无神经毒性相关剂量调整,耐受性良好。荟萃分析也证实,在ABC亚型 DLBCL 中,Pola-R-CHP方案的PFS和OS均优于其他新型一线治疗方案,成为目前唯一经大型RCT验证、可用于高危DLBCL一线治疗的方案。
双特异性抗体:早期临床数据优异,Ⅲ期试验亟待验证
CD20×CD3双特异性抗体通过同时结合B细胞的CD20和T细胞的CD3,重定向T细胞杀伤恶性B细胞,可绕过肿瘤微环境的免疫抑制,为免疫“冷”肿瘤患者带来治疗机会。研究指出,肿瘤微环境是影响DLBCL预后的重要因素:CD8+T细胞浸润高、抑制性髓系细胞少的免疫 “热” 肿瘤预后良好,而T细胞密度低、抑制性巨噬细胞富集、成纤维细胞占优的免疫“冷”肿瘤则易发生免疫逃逸,对标准治疗响应差,双特异性抗体正是针对这一痛点的重要策略。
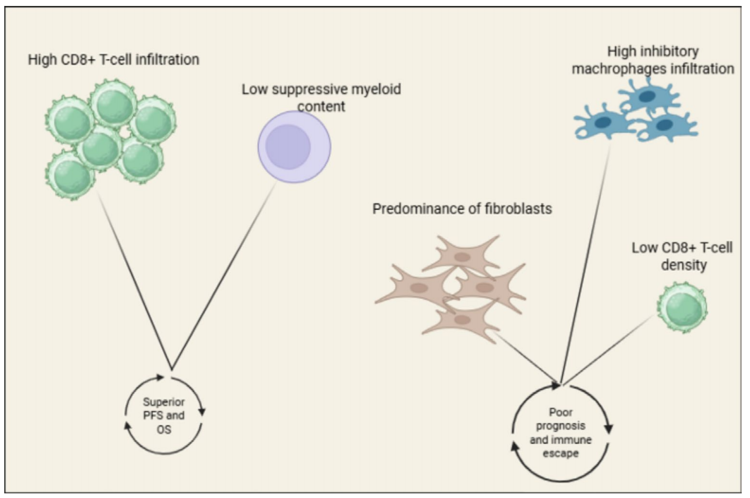
目前,多款CD20×CD3双特异性抗体的一线临床研究取得了积极结果:EPCORE NHL-2试验中,epcoritamab联合R-CHOP在IPI≥3的高危初治患者中实现了高CR率,细胞因子释放综合征(CRS)以低级别为主,无治疗中断;GO40515试验中,莫妥珠单抗联合CHOP的客观缓解率(ORR)达87.5%,CR率达85%,毒性以中性粒细胞减少为主,CRS和神经系统事件均为低级别;格菲妥单抗联合Pola-R-CHP的COALITION试验在65岁以下高危患者中实现了持久的高响应率,且安全性可控。
现阶段,epcoritamab、格菲妥单抗的Ⅲ期随机对照试验正在开展,分别对比其联合标准方案与单纯标准方案的疗效,这两项试验将成为双特异性抗体能否进入DLBCL一线标准治疗的关键依据。目前,双特异性抗体联合方案仍处于临床试验阶段,尚未推荐用于常规临床实践。
表2.已完成(A)和正在进行(B)的DLBCL一线CD20×CD3双特异性抗体试验
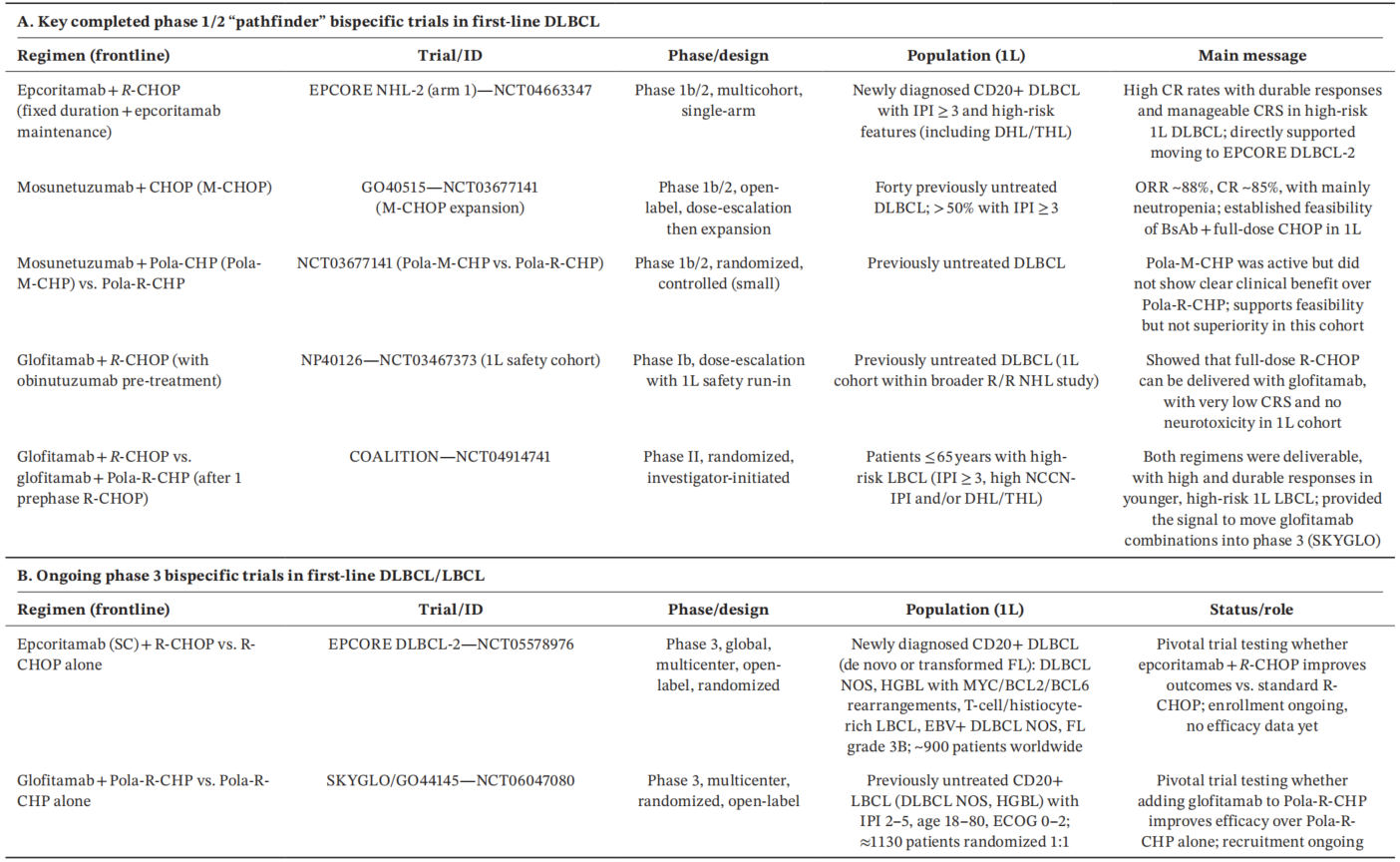
一线CAR-T细胞疗法:高危难治亚组显优势,尚处研究探索期
嵌合抗原受体T细胞(CAR-T)疗法是目前血液肿瘤治疗的重要手段,该研究聚焦于阿基仑赛在DLBCL一线治疗中的应用,其核心针对经一线诱导治疗后早期治疗失败的高危患者。
Ⅱ期ZUMA-12试验显示,对于经2周期R-CHOP诱导治疗后PET-CT阳性(Deauville 4~5)、且合并双打击/三打击或IPI≥3的高危患者,阿基仑赛治疗的ORR达89%,CR率达78%,73%的患者维持持续缓解,且毒性与复发/难治性患者中的表现一致,CRS和免疫效应细胞相关神经毒性综合征(ICANS)均可控,无治疗相关死亡。真实世界对照分析显示,此类患者若接受标准治疗,预后显著劣于阿基仑赛治疗组,证实了早期CAR-T治疗对高危难治患者的价值。
目前,Ⅲ期ZUMA-23试验正在开展,这是首个将CAR-T疗法作为初治高危DLBCL一线治疗的随机对照试验,对比阿基仑赛与标准化疗的疗效,其结果将明确CAR-T疗法在DLBCL一线治疗中的定位。现阶段,一线CAR-T细胞疗法仅推荐在临床试验中用于超高危DLBCL患者,常规临床实践中仍以挽救治疗为主。
研究总结:R-CHOP仍是基础,风险分层精准化成未来核心
该综述明确,DLBCL一线治疗正处于转型期,但R-CHOP方案仍是不可替代的基础治疗框架,单纯的经验性强化或改良均无法在未选择人群中改善疗效,而以生物标志物为指导的风险分层、精准化治疗,成为突破治疗瓶颈的核心方向。
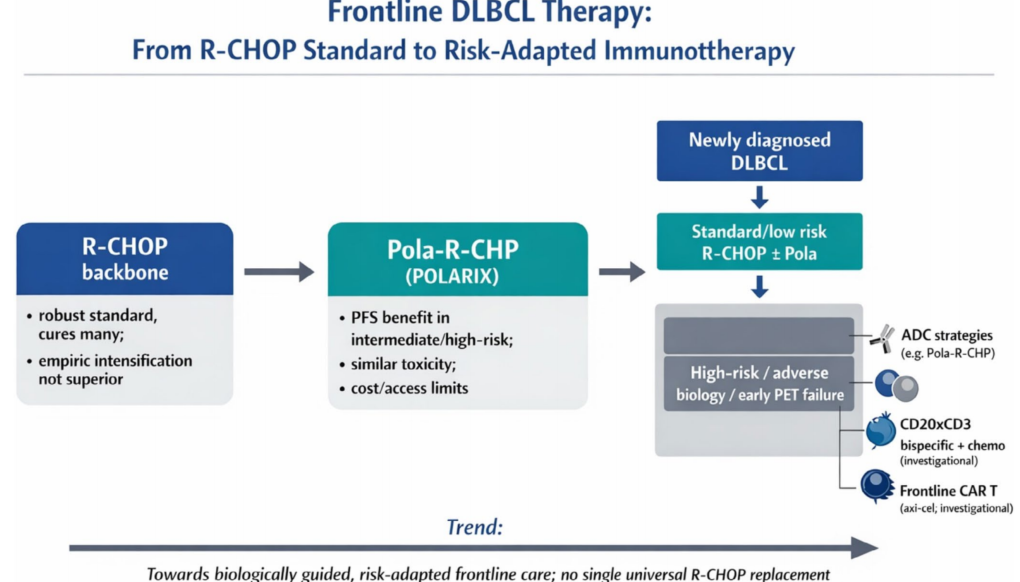
从目前的临床证据来看,Pola-R-CHP方案是首个经大型RCT和真实世界研究验证的、可用于中高危DLBCL一线治疗的方案,在ABC亚型、高IPI评分、老年/体弱患者中具有明确的获益,可作为此类患者的优选方案;对于标准低危患者,R-CHOP方案仍为最优选择,兼顾疗效和安全性。双特异性抗体和CAR-T细胞疗法虽早期临床数据优异,展现出对高危、免疫抑制微环境患者的治疗潜力,但尚未完成Ⅲ期验证,目前仍处于临床试验阶段,未来有望成为超高危或早期治疗失败患者的一线治疗选择。
总体而言,DLBCL的一线治疗已告别“一刀切”的时代,进入“R-CHOP为基础,新型疗法分层应用”的精准化阶段。未来,随着更多Ⅲ期临床试验的完成、生物标志物研究的深入和新型治疗手段的研发,DLBCL的一线治疗格局将进一步优化,有望实现更高的治愈率,同时最大限度降低治疗毒性,改善患者的生存质量。
Eur J Haematol . 2026 Feb 3. doi: 10.1111/ejh.70129
排版编辑:Mathilda











 苏公网安备32059002004080号
苏公网安备32059002004080号


