随着分子分型在急性髓系白血病(AML)中的深入应用,异柠檬酸脱氢酶 1(IDH1)突变患者的靶向治疗已是研究热点,这类患者在传统治疗模式下预后不佳,生存需求长期未被满足,而以艾伏尼布(IVO)为代表的IDH1抑制剂的出现,正扭转治疗困境,这一特定亚型逐渐走向“主动干预”。在2025年ASH年会上,多项围绕IDH1抑制剂的研究被集中披露,为该人群治疗策略的升级提供了新的循证依据。本期特邀河南省肿瘤医院的尹青松教授,结合近年的最新进展,系统梳理IDH1突变AML从传统治疗到IVO靶向联合的精准化革新历程。
往昔困境:前IDH抑制剂时代,IDH1突变AML预后不佳
在IDH抑制剂尚不可及的时代,IDH1突变AML患者主要接受以阿糖胞苷(Ara-C)为基础的强化疗或维奈克拉(VEN)联合去甲基化药物(HMA)治疗,但整体疗效与长期生存仍存在明显局限[1,2]。中国人群的真实世界数据为此提供了证据——安徽血液病合作学组(ACHG)开展的一项多中心回顾性研究,系统分析了726例接受以阿糖胞苷为基础的强化疗或VEN+HMA治疗的中国AML患者生存情况[1]。IDH野生型、IDH1突变和IDH2突变患者的中位年龄分别为52岁、59.5岁和59.5岁,中位随访时间25.2个月[1]。结果显示,IDH1突变患者的缓解率与生存获益均稍显不足:完全缓解(CR)率为51.1%,IDH野生型和IDH2突变患者则分别为64.9%和56.2%;中位总生存期(mOS)为13.2个月,不及IDH野生型患者的19.1个月,也低于IDH2突变患者的48.9个月(图1)[1]。
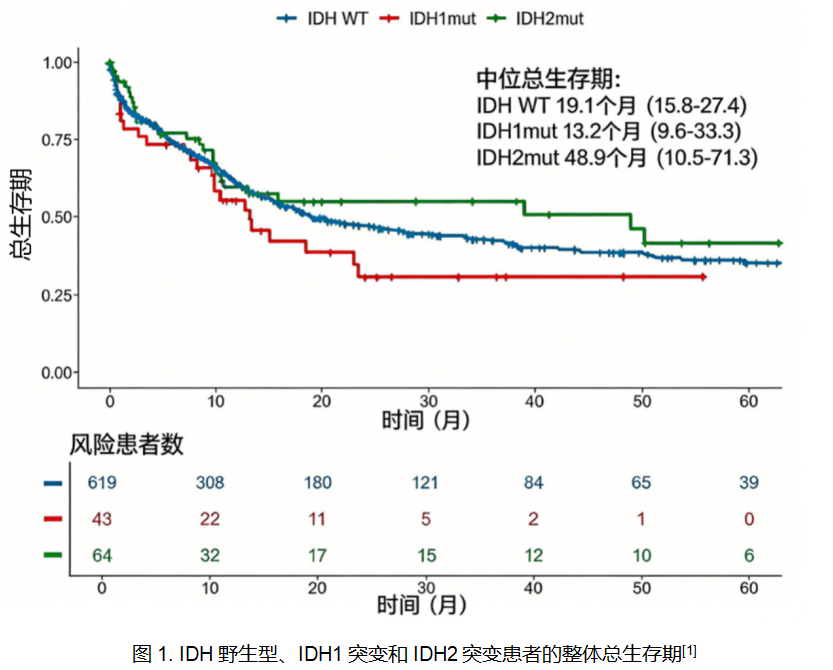
在全球多中心研究中同样观察到这一现象。VIALE-A研究的长期随访数据显示,在接受VEN+阿扎胞苷(AZA)治疗不适合强化疗(unfit)新诊断(ND)AML人群中,IDH1突变患者的mOS为10.2个月,而IDH2突变患者的mOS可延长至27.5个月[2]。
以上研究结果均一致证实:前IDH抑制剂时代,IDH1突变AML患者在强化疗、低强度治疗(含VEN+HMA)等传统治疗模式下,均面临生存劣势,亟需通过早期基因筛查与精准靶向干预,打破生存瓶颈[1,2]。
双证加持:IVO+AZA方案确立标准治疗地位
在此背景下,IDH1抑制剂联合方案的探索成为破解临床困局的关键方向之一。近年来,FDA已先后批准IVO和Olutasidenib(OLU)两款IDH1抑制剂治疗IDH1突变AML成人患者[3,4]。一项来自美国、澳大利亚和西班牙的1/2期、开放标签临床研究结果显示,OLU+AZA方案治疗ND AML患者的复合完全缓解(CRc)率 54%,ORR 77%,mOS 未达到(NR),12个月的OS率为75%[5]。一项前瞻性、随机、安慰剂对照试验(RCT,即AGILE研究)与多项真实世界研究(RWS)双重验证,IVO+AZA方案是改善IDH1突变unfit ND AML患者生存的核心选择[6-11]。
前瞻性RCT研究与真实世界数据高度契合
AGILE研究已充分证实IVO+AZA方案治疗IDH1突变unfit ND AML患者的显著优势[6]。该研究长期随访数据(中位随访28.6个月)显示,IVO+AZA组患者的mOS长达29.3个月,明显优于安慰剂(PBO)+AZA组的7.9个月(p<0.0001),且随时间推移,IVO+AZA组的长期生存优势持续存在(两组12个月、24个月和36个月OS率分别为62.9% vs 38.3%、53.1% vs 17.4%、41.0% vs 11.9%)[7]。
此外,2025年ASH大会公布的多项RWS从不同临床场景验证了IVO+AZA方案治疗IDH1突变ND AML的临床转化价值。这些RWS(包括法国IVOOBS研究、美国TriNetX数据库研究和上市后ALIDHE研究)纳入的患者基线特征更为复杂,但其观察到的结果与AGILE研究高度一致(表1)[6-10],且上市后ALIDHE研究也提供了IVO+AZA方案在真实世界的安全性数据,且与AGILE研究的安全性特征相似[10]。
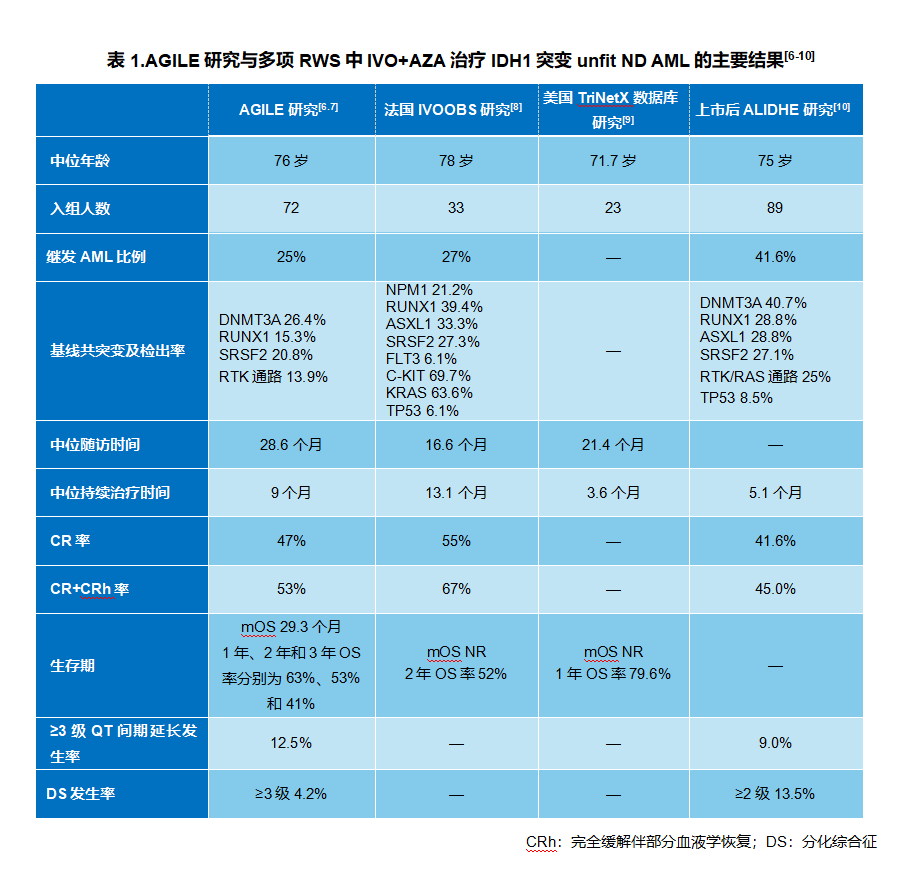
总体而言,无论是在严格设计的RCT,还是在患者构成更加复杂的RWS中,IVO+AZA方案均能稳定实现深度缓解和延长OS[6-10]。RCT与RWS的高度一致性充分表明,IVO+AZA治疗IDH1突变unfit ND AML患者的临床试验结果具备良好的可转化性,为其在真实临床实践中的广泛应用提供了坚实的循证基础。
合并共突变患者同样获益,适用人群广泛
在总体生存优势确立的基础上,AGILE研究进一步对基线共突变进行了亚组分析,结果显示,IVO+AZA方案的疗效不受常见共突变影响:对于合并DNMT3A突变、SRSF2突变、RUNX1突变以及RTK通路基因突变的患者,与PBO+AZA组相比,IVO+AZA方案均能显著改善缓解率与生存期(图2),充分体现了该方案的广泛适用性[11]。
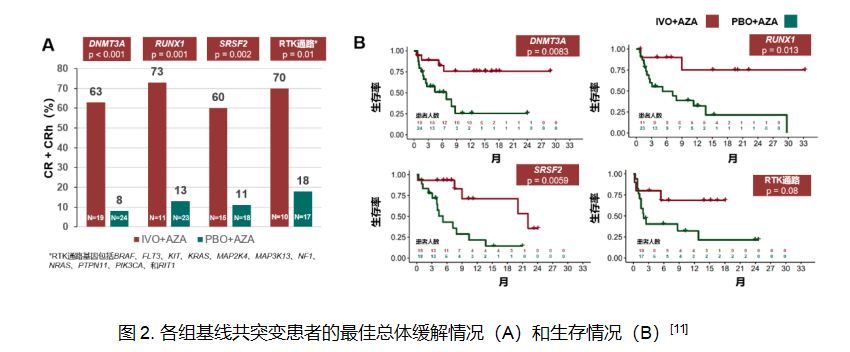
ELN 2024风险重塑,预后层级跃升
随着AGILE研究和真实世界证据的持续积累,IDH1抑制剂对IDH1突变AML预后的影响已体现在风险分类更新中。欧洲白血病网络(ELN)2024风险分类明确将接受IVO+AZA治疗的IDH1突变(TP53野生型)AML患者归为预后良好组,且不论患者是否携带激活信号基因突变(表2)[12]。这一权威认定,不仅是对前IDH抑制剂时代IDH1突变患者预后中等/不良定位的颠覆,更从指南层面确立了IVO+AZA方案在IDH1突变unfit ND AML患者中的标准治疗地位。
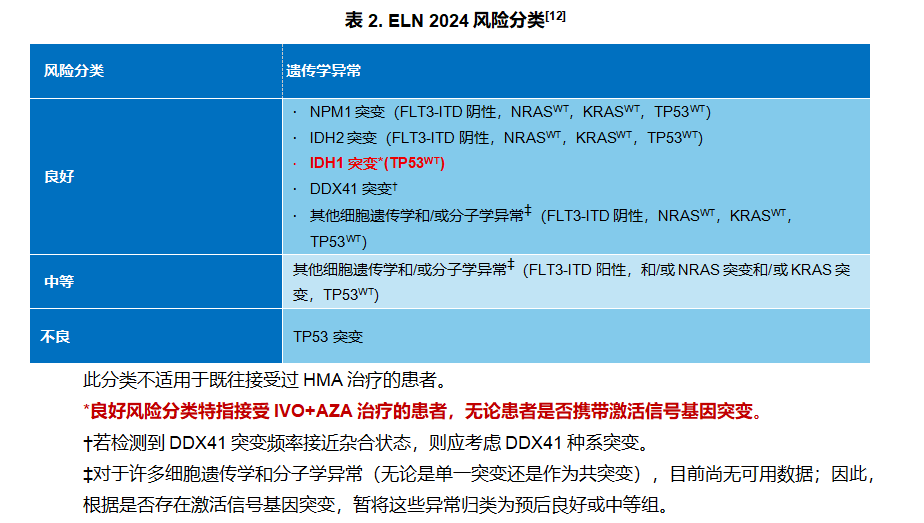
三联进阶:fit与unfit ND AML患者全面覆盖
在IVO+AZA方案奠定标准地位的同时,以IVO为基础的三联方案正持续拓展潜在适应症边界,以更深缓解为导向,以期为适合强化疗(fit)和unfit ND AML患者提供更具潜力的治疗选择。
IVO+VEN+HMA:unfit患者的高效选择
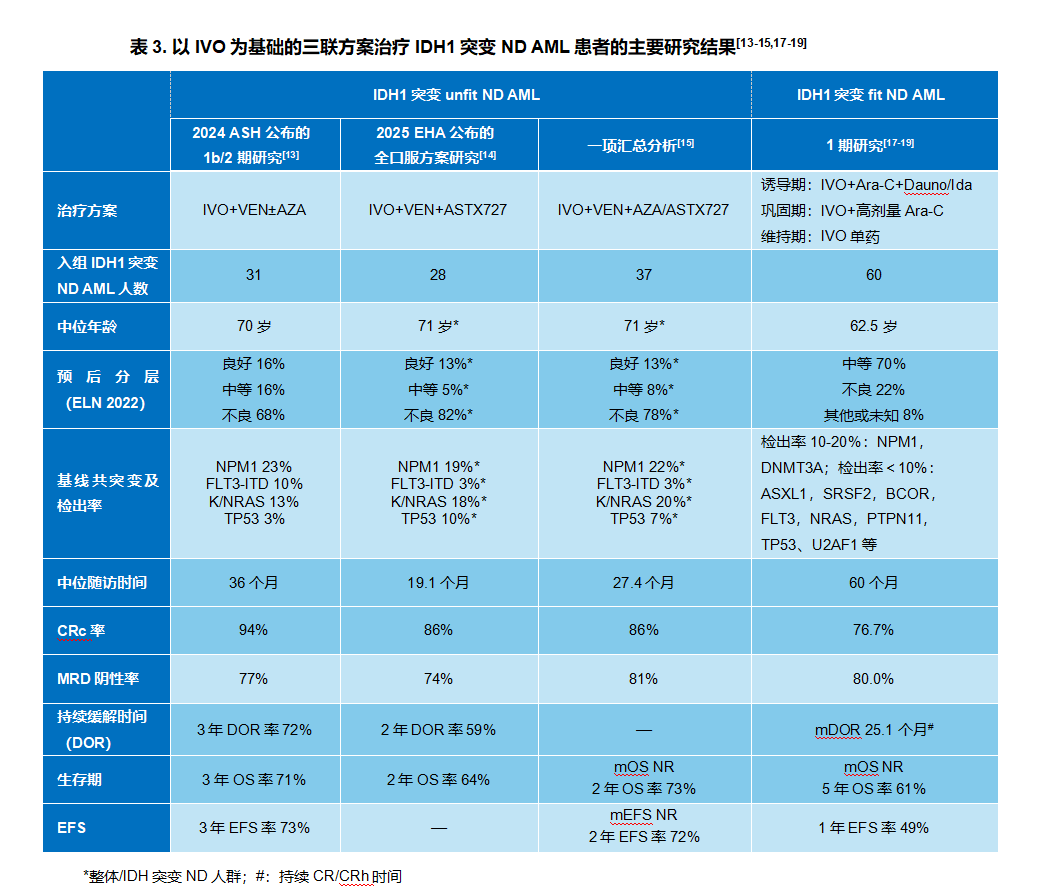
针对unfit ND AML患者,美国MD安德森癌症中心已有多项早期研究发现IVO、VEN与HMA(如AZA、ASTX727)之间的协同作用,该三联方案可实现较高比例的深度缓解(CRc率86%-94%,可测量残留病[MRD]阴性率74%-81%,表3),并呈现出持久的生存获益(mOS均未达到,表3)[13-15]。
目前正在开展一项为前瞻性、多中心、随机、双盲、安慰剂对照3期试验(EVOLVE-1研究),将进一步验证IVO+AZA±VEN在该人群中的疗效与安全性[16]。研究计划纳入230例IDH1突变unfit ND AML或MDS/AML患者,以无事件生存(EFS)为主要终点,旨在明确在IVO+AZA方案基础上增加VEN,能否为IDH1突变unfit ND AML患者带来更多获益[16]。该研究结果有望进一步巩固三联方案在unfit ND AML患者中的治疗地位。
IVO+标准强化疗:fit患者的生存革新方案
在fit ND AML患者中,IVO联合标准强化疗的早期探索同样取得积极信号。一项1期多中心、开放标签研究(NCT02632708)对IDH突变fit ND AML患者采用IDH抑制剂联合强化疗方案(Ara-C+柔红霉素[Dauno]或伊达比星[Ida])的结果进行了探索[17]。研究包括60例IDH1突变患者,2025 ASH大会公布了该人群的长期随访结果,中位随访60个月,mOS NR,5年OS率高达61%,多数患者实现深度且持久的缓解(表3);此外,48%患者成功桥接异基因造血干细胞移植,接受IVO维持治疗的患者血细胞计数趋于正常且稳定,为fit ND AML患者提供了超越传统化疗的多方获益[17-19]。
目前一项前瞻性、多中心、随机、双盲、安慰剂对照的3期临床试验(HOVON150AML研究)也正在进行中,其中计划入组484例IDH1突变fit ND AML患者,采用“诱导(Ara-C+蒽环类+IVO)+巩固(中剂量Ara-C+IVO)+维持(IVO)”的全周期方案,致力于为IDH1突变fit ND AML的治疗策略提供更高级的循证支持[20]。
总结
IDH1突变AML的治疗已迈入“精准靶向主导”的新时代:前IDH抑制剂时代的预后困境,推动了IDH1抑制剂联合方案的持续探索[1,2]。从早期基因筛查到分层治疗,IDH1突变AML的精准诊疗路径已逐渐清晰。IVO+AZA方案凭借RCT与RWS的双重验证,获ELN 2024预后良好归类,成为IDH1突变unfit ND AML患者的标准治疗[6-12];IVO+VEN+HMA与IVO+标准强化疗的联合方案,则分别为unfit和fit ND AML患者提供了更具潜力的治疗选择,相关3期临床研究将进一步完善证据链,静待其最新结果揭晓,为精准诊疗奠定更坚实的循证力量[13-20],持续刷新IDH1突变 ND AML的疗效高度。
博士、主任医师、博士生导师
河南省肿瘤医院血液科副主任、白血病病区主任
国务院政府特殊津贴专家中原科技创新领军人才
美国MD安德森癌症中心 博士后
中国临床肿瘤学会(CSCO)白血病专委会 常务委员
中国抗癌协会血液病转化专委会 委员
中国实验血液学会血液免疫学组 委员
河南省生命关怀协会急性白血病专业委员会 主任委员
河南省医学会血液学分会 常务委员
河南省抗癌协会血液肿瘤专业委员会 副主任委员
河南省生命关怀协会慢淋专业委员会 副主任委员
主持国家自然科学基金项目、河南省自然科学基金和省部共建项目等课题
中华血液学杂志、白血病淋巴瘤等杂志审稿专家
[1]. Chen E, et al. 2025 ASH. Poster 3389.
[2]. Pratz KW, et al. Am J Hematol. 2024 Apr;99(4):615-624.
[3].https://www.accessdata.fda.gov/scripts/cder/daf/index.cfm?event=BasicSearch.process
[4].https://www.accessdata.fda.gov/scripts/cder/daf/index.cfm?event=BasicSearch.process
[5]. Watts JM, et al. Lancet Haematol. 2023 Jan;10(1):e46-e58.
[6]. Montesinos P, et al. N Engl J Med. 2022 Apr 21;386(16):1519-1531.
[7]. Montesinos P, et al. Blood Adv. 2025 Oct 28;9(20):5177-5189.
[8]. Peterlin P, et al. 2025 ASH. Poster 1658.
[9]. Zeidner JF, et al. 2025 ASH. Poster 3401.
[10]. Vyas P, et al. 2025 ASH. Poster 3443.
[11]. de Botton S, et al. 2022 ASCO. Poster P250.
[12]. Döhner H, et al. Blood. 2024 Nov 21;144(21):2169-2173.
[13]. Marvin-Peek J, et al. 2024 ASH. Oral 219.
[14]. Marvin-Peek J, et al. 2025 EHA. Poster PS1471.
[15]. DiNardo CD, et al. J Clin Oncol. 2025 Aug 20;43(24):2692-2699.
[16]. Döhner H, et al. 2025 ASH. Poster 5192.
[17]. Stein EM, et al. Blood. 2021 Apr 1;137(13):1792-1803.
[18]. Stein EM, et al. 2025 ASH. Oral 992.
[19]. Stein EM, et al. 2021 ASH. Poster 1276.
[20].https://clinicaltrials.gov/study/NCT03839771?cond=AML&intr=ivosidenib%20%5C(AG-120%5C)&rank=7
免责声明:
本资料的内容仅作为科学信息参考,仅用于医疗卫生专业人士的学术交流,请勿用于任何其他用途。若您不是医疗卫生专业人士,请勿观看和/或传播此资料。
本资料可能会出现某些药品信息,但该药品/适应症可能尚未获得国家药品监督管理局的注册批准。医疗卫生专业人士做出的任何与治疗有关的决定应根据患者的具体情况并应参照国家药品监督管理局批准的药品说明书。对于本资料可能提到的相关诊断、治疗方法,请遵守国家卫生健康委员会以及相关部门批准使用的指南或规定。
审批号:M-TIBSO-CN-202602-00006











 苏公网安备32059002004080号
苏公网安备32059002004080号


